История открытия
- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Водород, нахождение в природе. Получение водорода и его физические свойства презентация
Содержание
- 1. Водород, нахождение в природе. Получение водорода и его физические свойства
- 2. История открытия
- 3. Л. Гитон де Морво (1737—1816) барон,
- 5. План урока Общая характеристика водорода Нахождение водорода
- 6. Задание: I общая характеристика водорода. II нахождение водорода в природе.
- 7. Общая характеристика водорода 1. Химический знак -
- 8. Нахождение водорода в природе Составная часть
- 9. Получение водорода Если бы перед
- 10. Получение в промышленности Электролиз воды
- 11. Получение в лаборатории 1) взаимодействие металлов с
- 12. Получение водорода
- 13. Аппарат Киппа
- 14. Назовите металл и кислоту, которые
- 15. Физические свойства Простое
- 16. Сравнение Кислород Водород
- 17. Способы собирания
- 18. Способы собирания
- 19. Способы собирания
- 20. Физические свойства
- 21. Физические свойства
- 22. Физические свойства
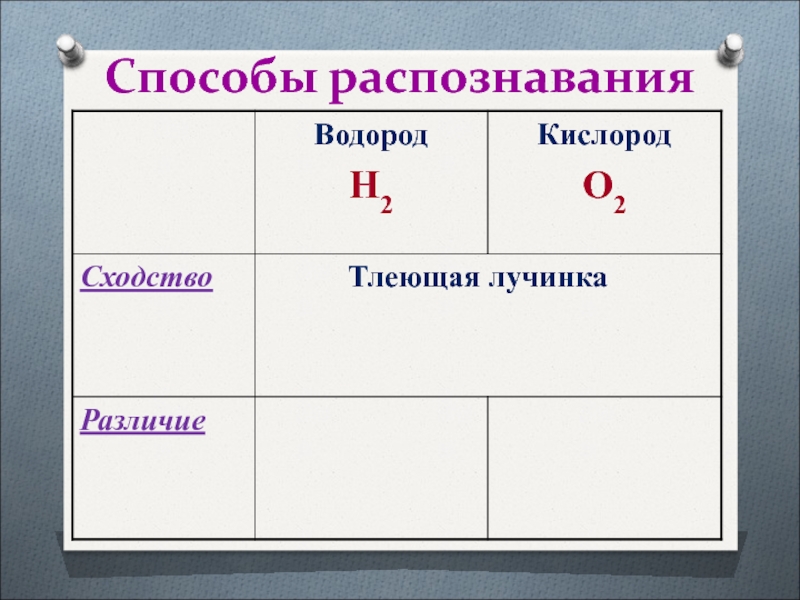
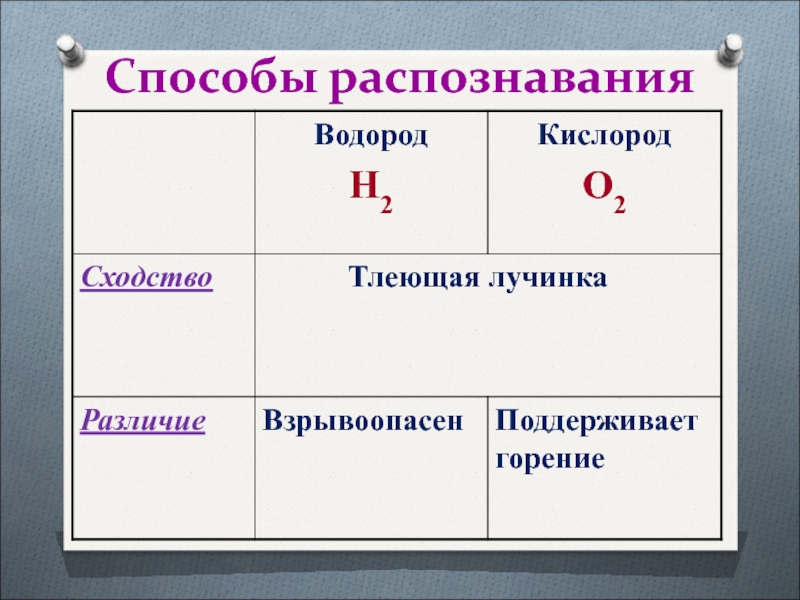
- 23. Способы распознавания
- 24. Способы распознавания
- 25. Способы распознавания
- 26. Задание 1. Мыльные пузыри, наполненные водородом, поднимаются вверх. Объясните это явление.
- 27. Задание 2. Подберите коэффициенты в уравнениях реакций
- 28. Задание 3. Вставьте пропущенные формулы в уравнениях
- 29. Задание 4. Выберите реакции, в результате которых
- 30. Задание 5. Рассчитайте, какую массу водорода можно
- 31. Домашнее задание §25 , §26. Ответить на вопросы № 2, 3, 5.
- 32. Подумайте и закончите предложения: – Сегодня
- 33. Использованная литература: 1. Г.Е.Рудзитис, Ф.Г. Фельдман
Слайд 1 Генри Кавендиш
(1731-1810) английский физик и химик
Получил
водород в 1766г. И дал ему название «горючий воздух».
Слайд 2 История открытия
Антуан Лавуазье
(1743-1794) французский химик, один
из создателей современной химии
В 1783-1784 совместно с
Жаном Мёнье осуществили
термическое разложение воды и установили, что она состоит из кислорода и водорода.
В 1783-1784 совместно с
Жаном Мёнье осуществили
термическое разложение воды и установили, что она состоит из кислорода и водорода.
Слайд 3Л. Гитон де Морво
(1737—1816)
барон, французский химик. В 1787г. дал современное
название водороду. Он предложил латинское название гидрогениум, означающее «рождающий воду».
Слайд 5План урока
Общая характеристика водорода
Нахождение водорода в природе
Получение водорода
Физические свойства водорода
Слайд 7Общая характеристика водорода
1. Химический знак -
2. Порядковый номер –
3. Относительная атомная
масса Ar -
4. Химическая формула -
5. Относительная молекулярная масса Мr (Н2) -
6. Молярная масса М
7. Валентность - .
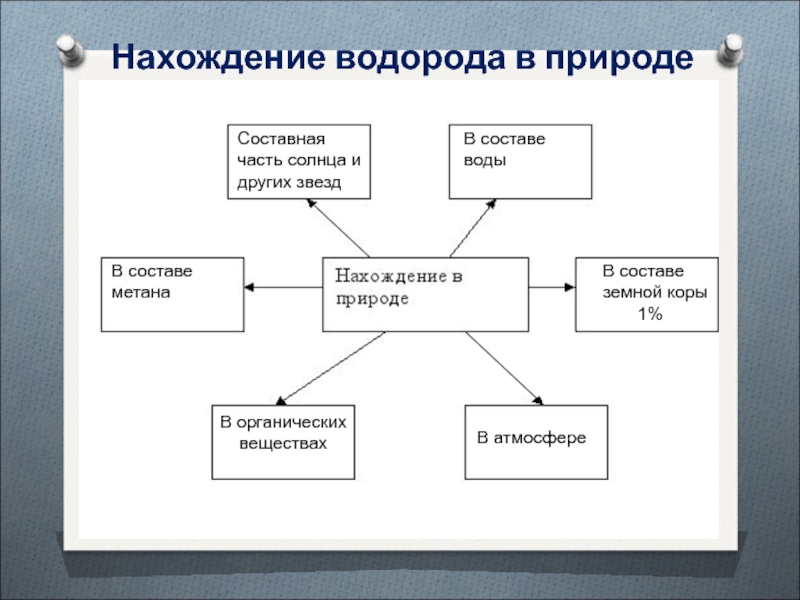
Слайд 8Нахождение водорода в природе
Составная часть солнца и других звезд
В составе
воды
В составе земной коры
1%
В составе метана
В органических веществах
В атмосфере
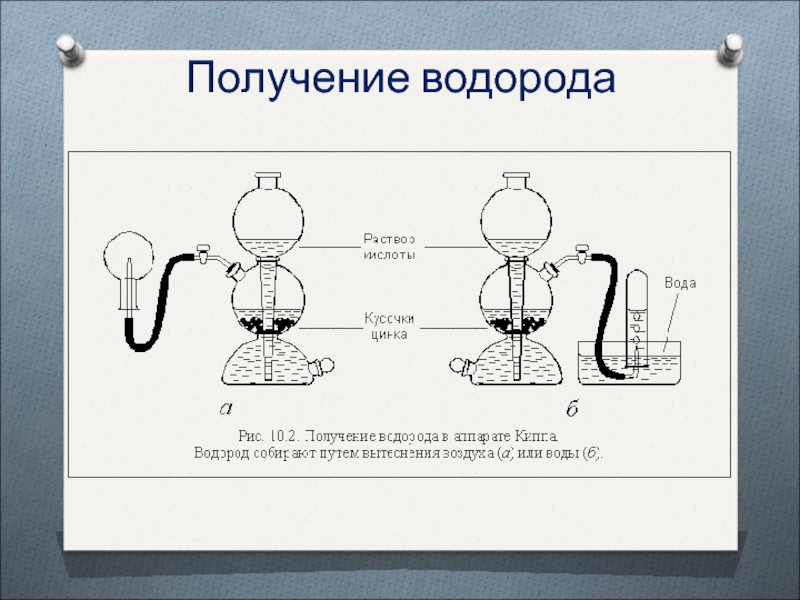
Слайд 9Получение водорода
Если бы перед вами стояла задача: получить большое количество
водорода, - какое сырье вы бы выбрали и почему?
2Н2О электрический ток 2Н2 + О2
Слайд 10Получение в промышленности
Электролиз воды
2H2O = 2H2↑ +
O2↑
Конверсия метана
t
CH4 + 2H2O = 4H2 + CO2
Термическое разложение метана
t
CH4 = 2H2 + C
Конверсия метана
t
CH4 + 2H2O = 4H2 + CO2
Термическое разложение метана
t
CH4 = 2H2 + C
Слайд 11Получение в лаборатории
1) взаимодействие металлов с кислотами
Zn + 2HCl = ZnCl2 + H2↑
Zn + H2SO4 = ZnSO4 + H2↑
2) взаимодействие активных металлов (Li, Na, K, Ca, Ba) с водой
2Na + 2H2O = 2NaOH + H2↑
Ca + 2H2O = Ca(OH)₂ + H2↑
Zn + H2SO4 = ZnSO4 + H2↑
2) взаимодействие активных металлов (Li, Na, K, Ca, Ba) с водой
2Na + 2H2O = 2NaOH + H2↑
Ca + 2H2O = Ca(OH)₂ + H2↑
Слайд 14 Назовите металл и кислоту, которые использовались для получения водорода?
Как можно собрать водород?
Определите отличие: горящая лучина вносится в пробирку с кислородом,
горящая лучина вносится в пробирку с водородом?
Определите отличие: горящая лучина вносится в пробирку с кислородом,
горящая лучина вносится в пробирку с водородом?
Получение водорода
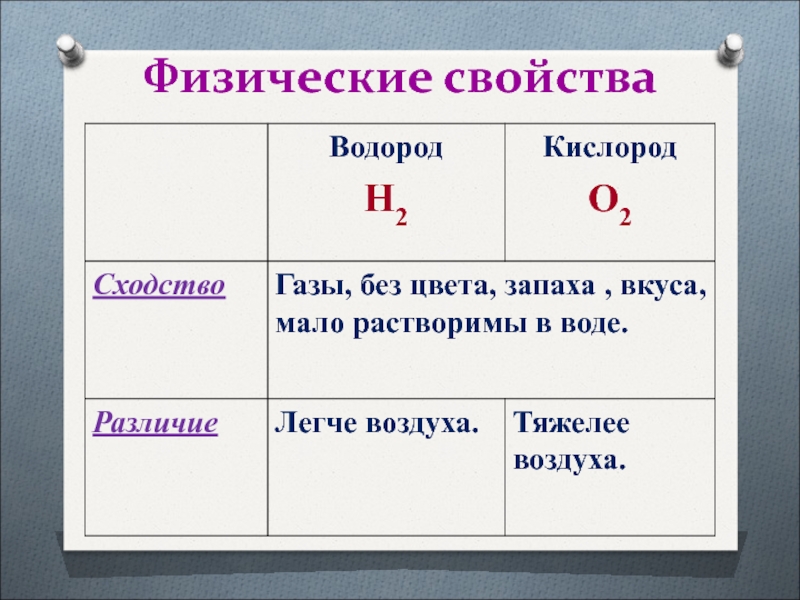
Слайд 15Физические свойства
Простое вещество водород – это газ,
легче воздуха, без цвета, без запаха, без вкуса, tкип = – 2530С, малорастворим в воде. Собирать водород можно путем вытеснения воздуха из пробирки или воды. При это пробирку нужно перевернуть вверх дном.
Слайд 27Задание 2.
Подберите коэффициенты в уравнениях реакций получения водорода:
а) Mg + HCl
→ MgCl2 + H2↑
б) K + H2O → KOH + H2↑
в) C + H2O → CO2↑ + H2↑
г) H2O → H2↑ + O2↑
б) K + H2O → KOH + H2↑
в) C + H2O → CO2↑ + H2↑
г) H2O → H2↑ + O2↑
Слайд 28Задание 3.
Вставьте пропущенные формулы в уравнениях реакций:
а) … + 2HCl →
FeCl2 + …↑
б) 2… + 2H2O → 2LiOH + H2↑
в) CH4 + H2O → CO↑ + …
б) 2… + 2H2O → 2LiOH + H2↑
в) CH4 + H2O → CO↑ + …
Слайд 29Задание 4.
Выберите реакции, в результате которых образуется водород:
а) Al + H2SO4
→
б) Na + H2O →
в) CO2 + H2O →
г) H2O →
д) CaO + HCl →
е) Na + HCl →
б) Na + H2O →
в) CO2 + H2O →
г) H2O →
д) CaO + HCl →
е) Na + HCl →
Слайд 30Задание 5.
Рассчитайте, какую массу водорода можно получить при растворении 13 г
цинка в соляной кислоте.
Слайд 32Подумайте и закончите предложения:
– Сегодня на уроке я узнал…
–
На уроке я понял…
– Теперь я знаю как…
– Теперь я знаю как…
Слайд 33Использованная литература:
1. Г.Е.Рудзитис, Ф.Г. Фельдман « Химия 8», Москва, Просвещение,
2008
2. Н.Л.Глинка « Общая химия»
3.http://www.krugosvet.ru/enc/nauka_i_tehnika/himiya/VODOROD.html
4. http://www.chem.msu.su/rus/history/element/H.html
5.http://yandex.ru/yandsearch?lr=213&text=%D0%BF%D0%B0%D1%80%D0%B0%D1%86%D0%B5%D0%BB%D1%8C%D1%81+%D1%84%D0%BE%D1%82%D0%BE
6.http://yandex.ru/yandsearch?text=%D0%BA%D0%B0%D0%B2%D0%B5%D0%BD%D0%B4%D0%B8%D1%88%20%D1%84%D0%BE%D1%82%D0%BE&lr=213
7.http://yandex.ru/yandsearch?text=%D0%B0%D0%BD%D1%82%D1%83%D0%B0%D0%BD%20%D0%BB%D0%BE%D1%80%D0%B0%D0%BD%20%D0%BB%D0%B0%D0%B2%D1%83%D0%B0%D0%B7%D1%8C%D0%B5%20%D1%84%D0%BE%D1%82%D0%BE&lr=213
8. 8. http://www.vtx-club.org/forum/viewtopic.php?t=3623&p=74777
2. Н.Л.Глинка « Общая химия»
3.http://www.krugosvet.ru/enc/nauka_i_tehnika/himiya/VODOROD.html
4. http://www.chem.msu.su/rus/history/element/H.html
5.http://yandex.ru/yandsearch?lr=213&text=%D0%BF%D0%B0%D1%80%D0%B0%D1%86%D0%B5%D0%BB%D1%8C%D1%81+%D1%84%D0%BE%D1%82%D0%BE
6.http://yandex.ru/yandsearch?text=%D0%BA%D0%B0%D0%B2%D0%B5%D0%BD%D0%B4%D0%B8%D1%88%20%D1%84%D0%BE%D1%82%D0%BE&lr=213
7.http://yandex.ru/yandsearch?text=%D0%B0%D0%BD%D1%82%D1%83%D0%B0%D0%BD%20%D0%BB%D0%BE%D1%80%D0%B0%D0%BD%20%D0%BB%D0%B0%D0%B2%D1%83%D0%B0%D0%B7%D1%8C%D0%B5%20%D1%84%D0%BE%D1%82%D0%BE&lr=213
8. 8. http://www.vtx-club.org/forum/viewtopic.php?t=3623&p=74777