- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Валентные состояния атома углерода. Гибридизация презентация
Содержание
- 1. Валентные состояния атома углерода. Гибридизация
- 2. 1s 2px 2py 1s 2px 2py 2pz
- 3. Процессы выравнивания орбиталей по форме и энергии называют гибридизацией.
- 4. Первое валентное состояние углерода sр3-Гибридизация -
- 5. 1s 2s 2px 2py 2pz 1s 2px
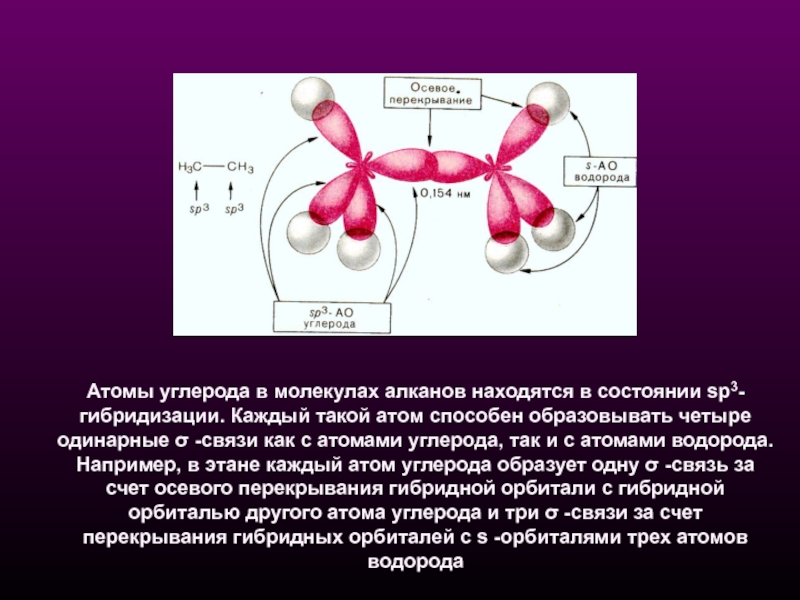
- 6. Атомы углерода в молекулах алканов находятся
- 7. Молекулярная структура алканов СХЕМА ОБРАЗОВАНИЯ
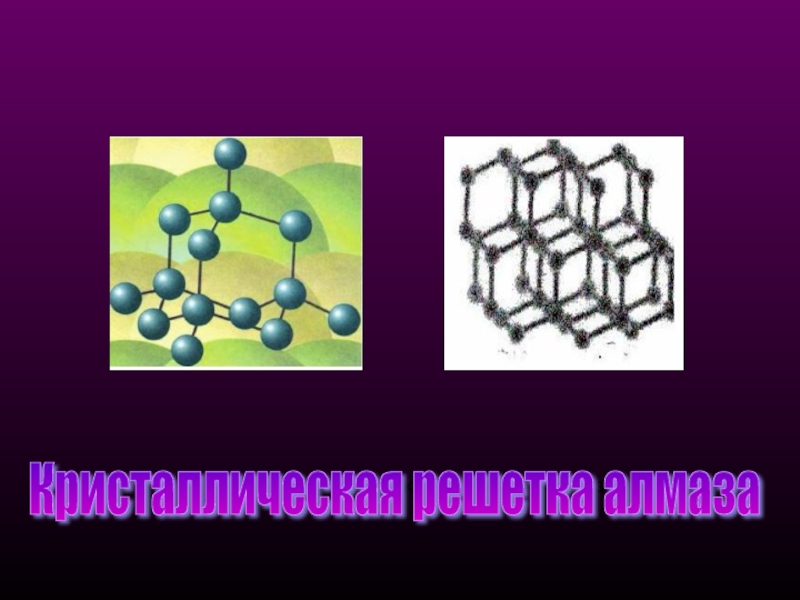
- 8. Кристаллическая структура алмаза Кристаллическая решетка алмаза
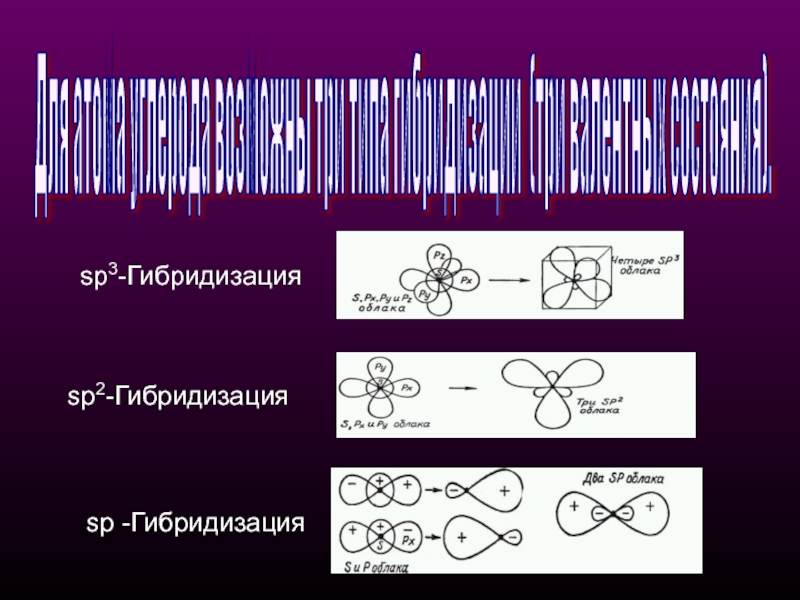
- 9. Для атома углерода возможны три типа гибридизации
- 10. sр2-Гибридизация - смешение одной 2s- и двух
- 11. sp2– ГИБРИДИЗАЦИЯ 1s 2s 2px
- 12. sр2-Гибридизация
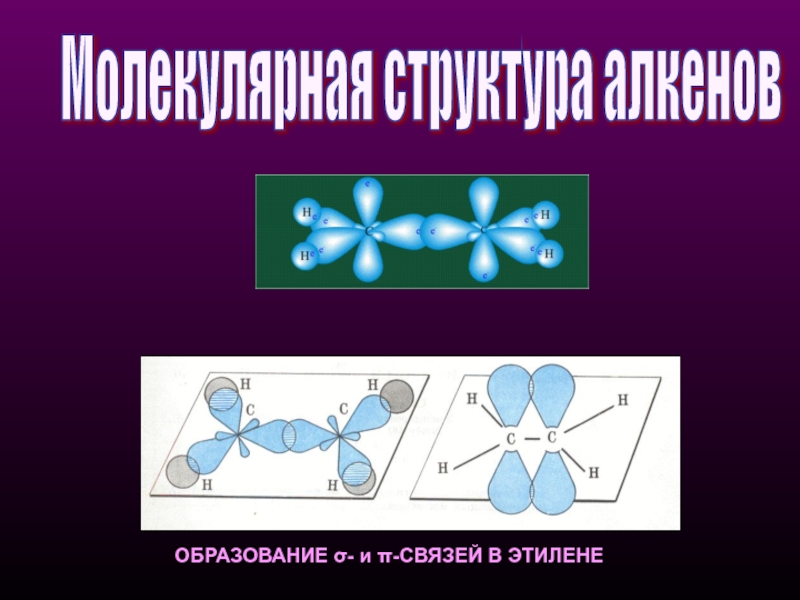
- 13. ОБРАЗОВАНИЕ σ- и π-СВЯЗЕЙ В ЭТИЛЕНЕ Молекулярная структура алкенов
- 14. Третье валентное состояние углерода sр-Гибридизация -
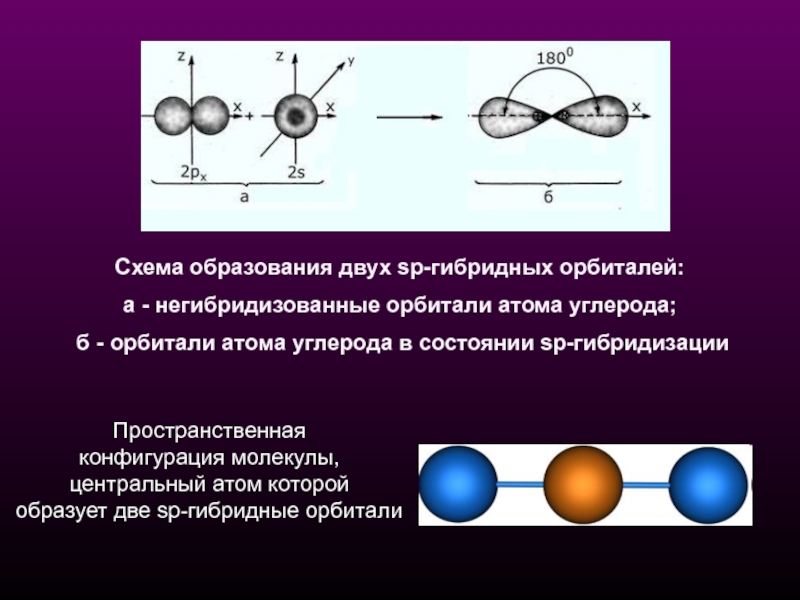
- 15. Схема образования двух sp-гибридных орбиталей: а
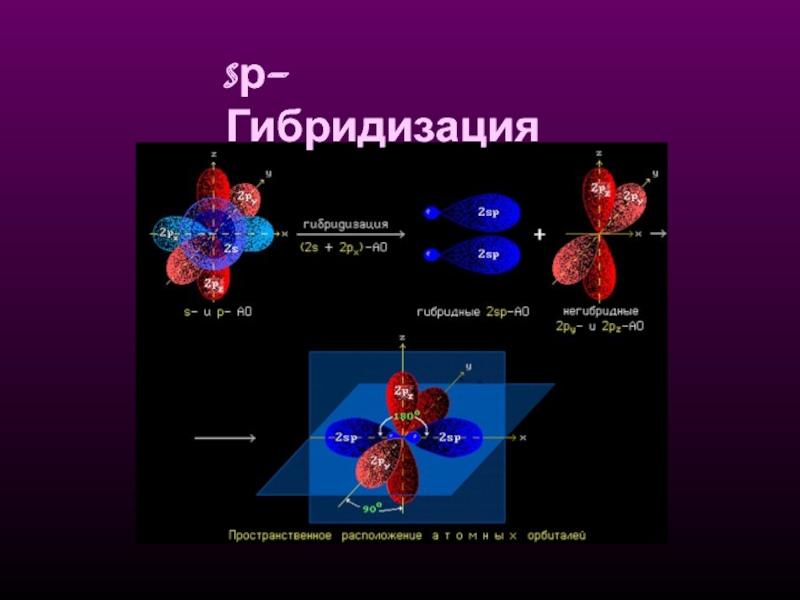
- 16. sр-Гибридизация
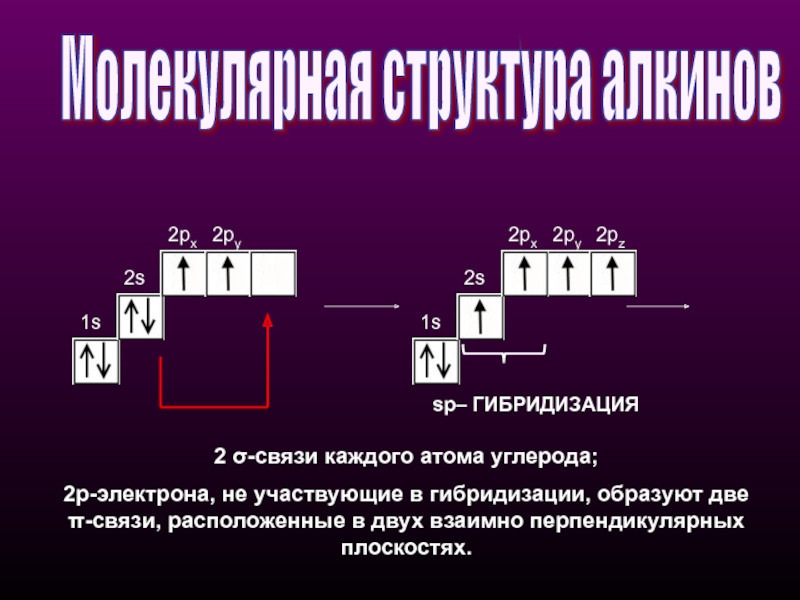
- 17. Молекулярная структура алкинов 1s 2s 2px
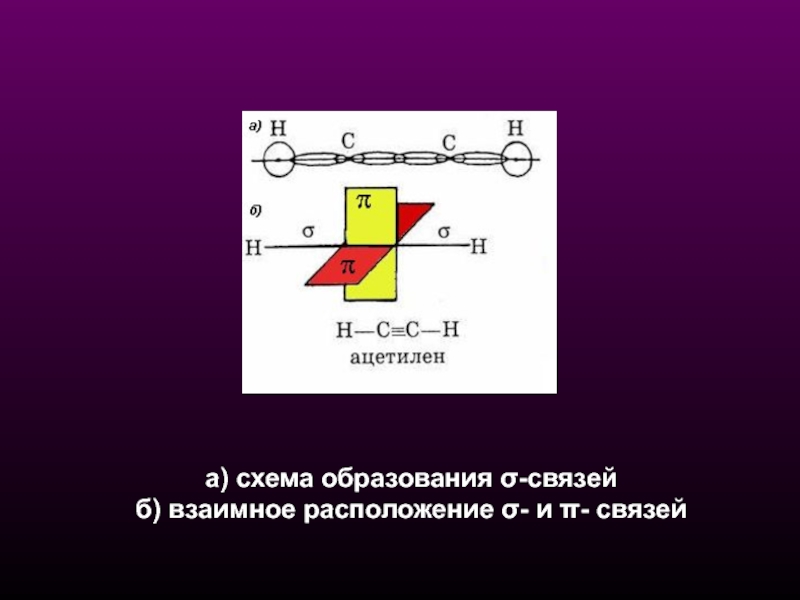
- 18. а) схема образования σ-связей б) взаимное расположение σ- и π- связей
- 19. Молекулярная структура алкинов СХЕМА ОБРАЗОВАНИЯ σ-СВЯЗЕЙ В АЦЕТИЛЕНЕ ОБРАЗОВАНИЯ π- СВЯЗЕЙ в АЦЕТИЛЕНЕ
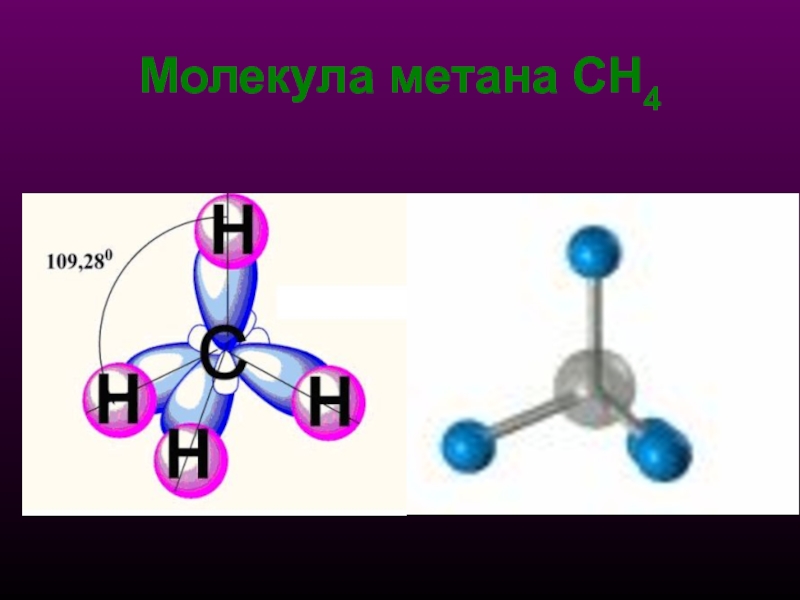
- 20. Молекула метана СН4
- 21. Пример 3. Образование
- 22. Пример 3. Образование молекулы СН4 (продолжение) 4.
- 23. Типы гибридизации
Слайд 21s
2px
2py
1s
2px
2py
2pz
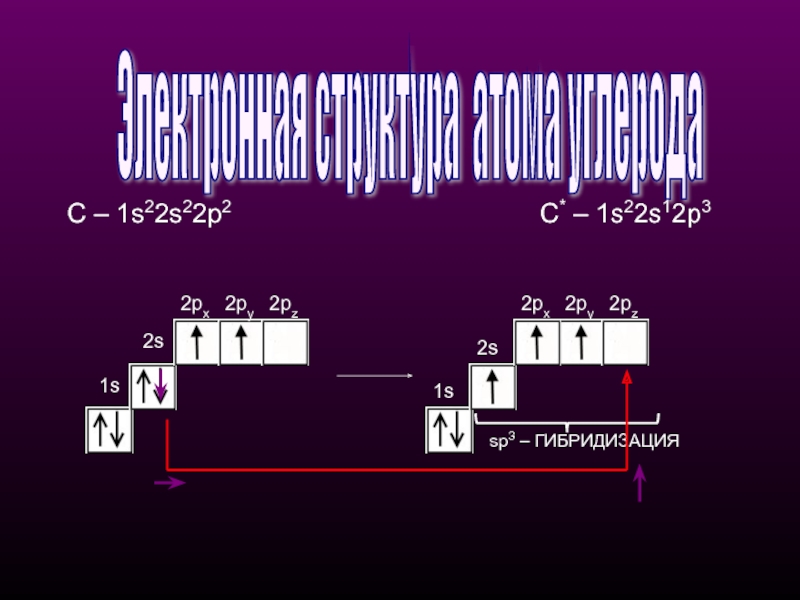
sp3 – ГИБРИДИЗАЦИЯ
Электронная структура атома углерода
2s
2pz
С – 1s22s22p2
С* –
Слайд 4Первое валентное состояние углерода
sр3-Гибридизация - смешение одной 2s- и трех
Поэтому sp3-гибридизованный атом углерода часто называют "тетраэдрическим".
Состояние углеродного атома с sp3-гибридными орбиталями (первое валентное состояние) характерно для предельных углеводородов - алканов.
sp3 - тетраэдрическое
строение
sр3-Гибридизация
Слайд 51s
2s
2px
2py
2pz
1s
2px
2py
2pz
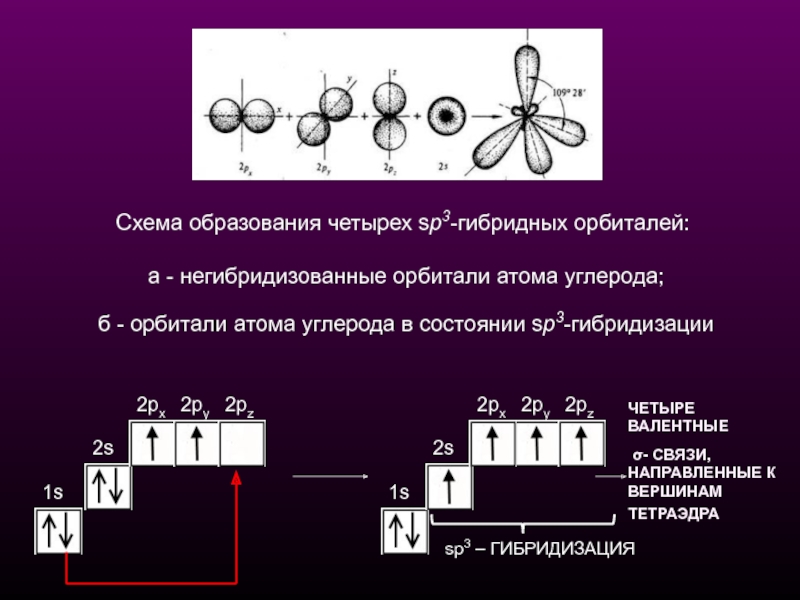
ЧЕТЫРЕ ВАЛЕНТНЫЕ
σ- СВЯЗИ, НАПРАВЛЕННЫЕ К ВЕРШИНАМ ТЕТРАЭДРА
sp3 – ГИБРИДИЗАЦИЯ
Схема
Слайд 6
Атомы углерода в молекулах алканов находятся в состоянии sp3-гибридизации. Каждый такой
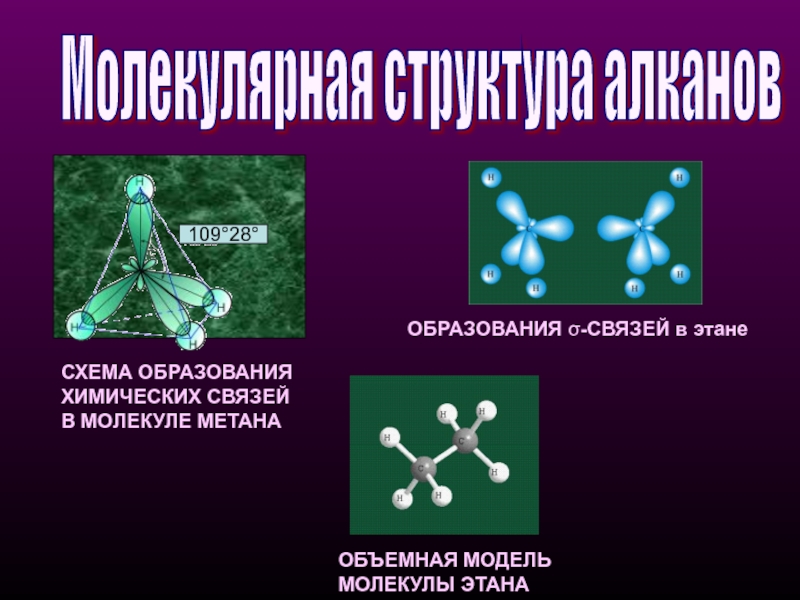
Слайд 7Молекулярная структура алканов
СХЕМА ОБРАЗОВАНИЯ
ХИМИЧЕСКИХ СВЯЗЕЙ
В МОЛЕКУЛЕ МЕТАНА
ОБЪЕМНАЯ МОДЕЛЬ
ОБРАЗОВАНИЯ σ-СВЯЗЕЙ в этане
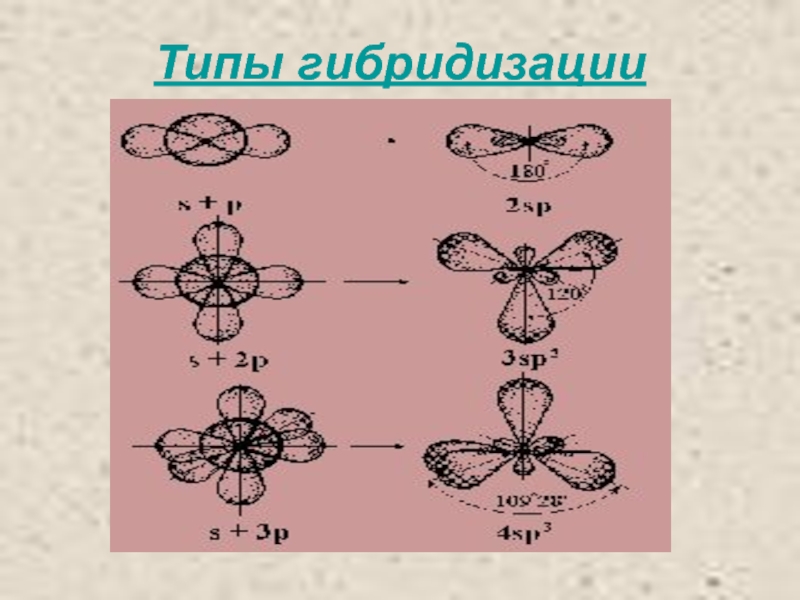
Слайд 9Для атома углерода возможны три типа гибридизации (три валентных состояния).
sр3-Гибридизация
sр2-Гибридизация
sр -Гибридизация
Слайд 10sр2-Гибридизация - смешение одной 2s- и двух 2р-орбиталей, одна 2p не
Состояние атома углерода с sp2-гибридными орбиталями (второе валентное состояние) характерно для непредельных углеводородов ряда этилена - алкенов
Второе валентное состояние углерода
sp2 - плоскостное
строение
sр2-Гибридизация
Слайд 11
sp2– ГИБРИДИЗАЦИЯ
1s
2s
2px
2py
2pz
1s
2s
2px
2py
2pz
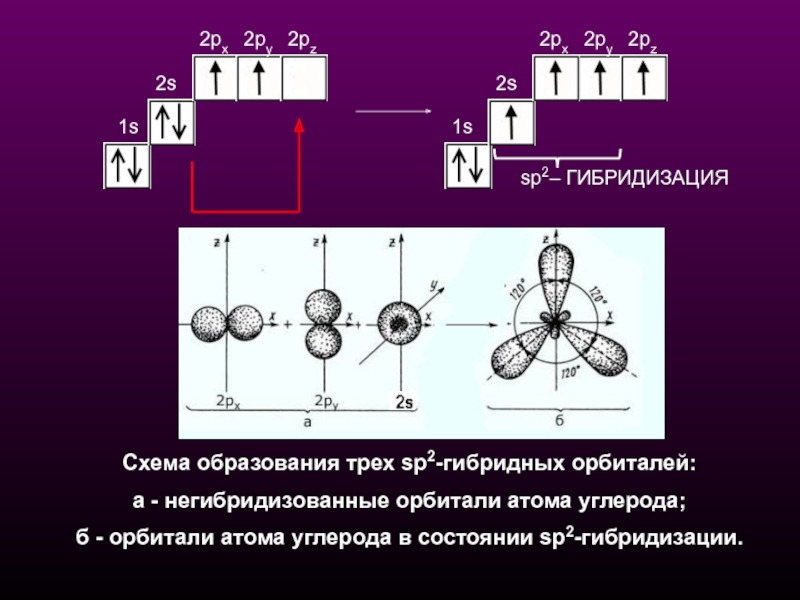
Схема образования трех sр2-гибридных орбиталей:
a - негибридизованные орбитали атома
б - орбитали атома углерода в состоянии sp2-гибридизации.
Слайд 14Третье валентное состояние углерода
sр-Гибридизация - смешение одной 2s- и одной
Состояние атома углерода с sp-гибридными орбиталями (третье валентное состояние) характерно для непредельных углеводородов ацетиленового ряда - алкинов.
sp - линейное
строение
sр-Гибридизация
Слайд 15Схема образования двух sp-гибридных орбиталей:
а - негибридизованные орбитали атома углерода;
Пространственная
конфигурация молекулы,
центральный атом которой
образует две sp-гибридные орбитали
Слайд 17Молекулярная структура алкинов
1s
2s
2px
2py
1s
2s
2px
2py
2pz
sp– ГИБРИДИЗАЦИЯ
2 σ-связи каждого атома углерода;
2p-электрона, не
Слайд 19Молекулярная структура алкинов
СХЕМА ОБРАЗОВАНИЯ σ-СВЯЗЕЙ В АЦЕТИЛЕНЕ
ОБРАЗОВАНИЯ π- СВЯЗЕЙ в
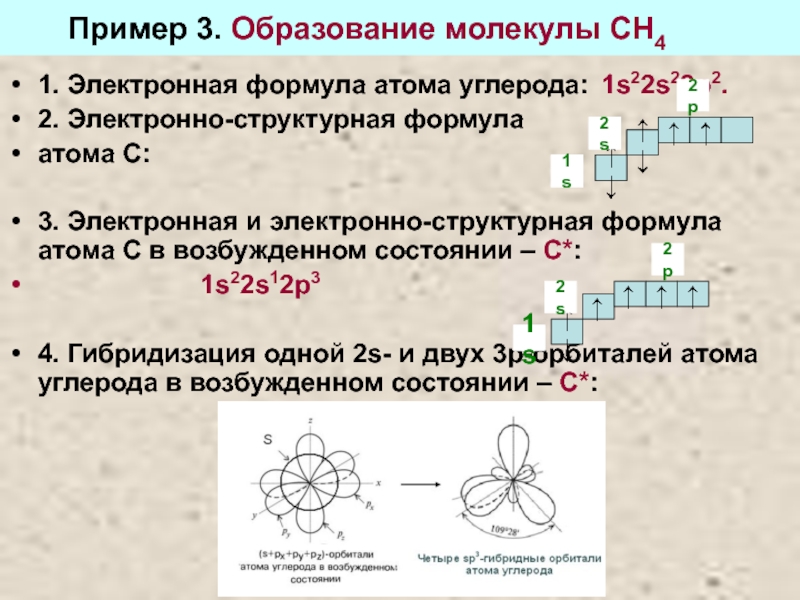
Слайд 21 Пример 3. Образование молекулы СН4
1. Электронная формула
2. Электронно-структурная формула
атома С:
3. Электронная и электронно-структурная формула атома С в возбужденном состоянии – С*:
1s22s12p3
4. Гибридизация одной 2s- и двух 3р-орбиталей атома углерода в возбужденном состоянии – С*:
2p
2s
1s
2p
2s
1s
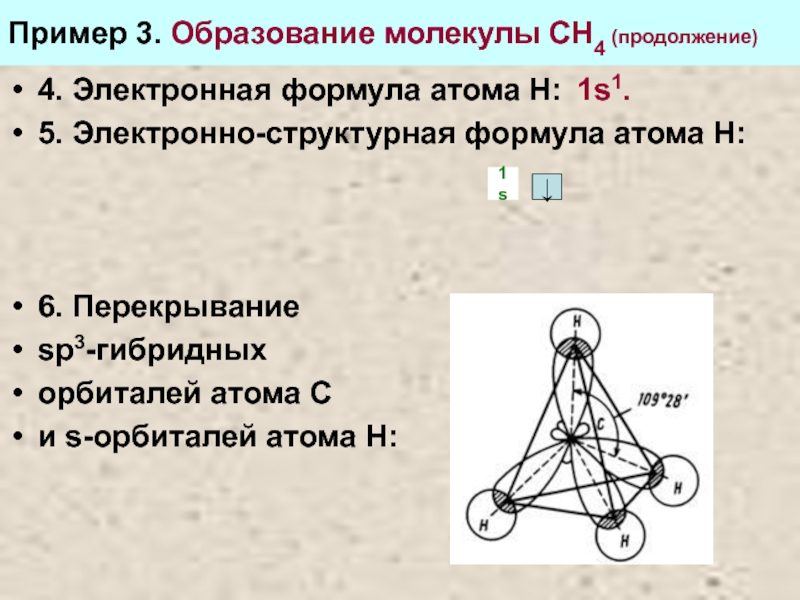
Слайд 22Пример 3. Образование молекулы СН4 (продолжение)
4. Электронная формула атома Н: 1s1.
5.
6. Перекрывание
sp3-гибридных
орбиталей атома С
и s-орбиталей атома Н:
↓
1s