Лекции №19 - 20:
Тема: «IV и III группы периодической системы элементов Д.И. Менделеева»
План:
1. Общая характеристика IV группы ПСХЭ.
2. Натрия гидрокарбонат.
3. Общая характеристика III группы ПСХЭ.
4. Кислота борная.
5. Натрия тетраборат.
- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
V и III группы периодической системы элементов Д.И. Менделеева презентация
Содержание
- 1. V и III группы периодической системы элементов Д.И. Менделеева
- 2. Натрия гидрокарбонат Natrii hydrocarbonas NaHCO3
- 4. Белый кристаллический порошок без запаха, солено-щелочного
- 5. Хорошо растворяется в воде, нерастворим
- 6. 1) Na+ - пирохимическая реакция
- 7. - прозрачность и цветность раствора
- 8. Метод нейтрализации, ацидиметрия Рабочий раствор-
- 9. в хорошо укупоренной таре Ф
- 10. Кислота борная Acidum boricum H3BO3
- 11. В промышленности борную кислоту получают из
- 12. Жирные на ощупь, бесцветные, прозрачные чешуйчатые
- 13. В холодной воде растворяется плохо, в
- 14. 1) с этанолом в присутствии конц.
- 15. 2) с куркумовой бумажкой, одновременно
- 16. - прозрачность и цветность; - допускается присутствие
- 17. Метод нейтрализации в присутствии глицерина,
- 18. - как антисептическое средство в виде 2-3%
- 19. В хорошо укупоренной таре
- 20. Натрия тетроборат. Бура Natrii tetraboras Borax
- 21. В природе встречается в свободном
- 22. бесцветные прозрачные легковыветривающиеся кристаллы или белый
- 23. Хорошо растворяется в воде, лучше в
- 24. а) Na+: пирохимическая реакция -окрашивание пламени
- 25. - не должно быть примесей карбонатов; -
- 26. Метод нейтрализации (ацидиметрия) Рабочий раствор – 0,1N
- 27. Ф а
- 28. в хорошо укупоренной таре в
Слайд 1Ф а р м а ц е в т и ч
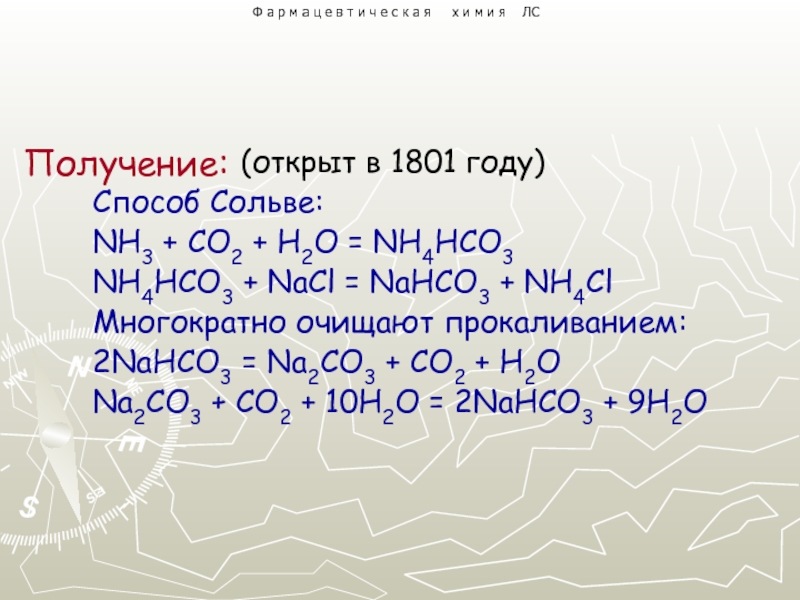
Слайд 3 (открыт в 1801
Способ Сольве:
NH3 + CO2 + H2O = NH4HCO3
NH4HCO3 + NaCl = NaHCO3 + NH4Cl
Многократно очищают прокаливанием:
2NaHCO3 = Na2CO3 + CO2 + H2O
Na2CO3 + CO2 + 10H2O = 2NaHCO3 + 9H2O
Ф а р м а ц е в т и ч е с к а я х и м и я ЛС
Получение:
Слайд 4 Белый кристаллический порошок без запаха, солено-щелочного вкуса, устойчив в сухом
Ф а р м а ц е в т и ч е с к а я х и м и я ЛС
Описание:
Слайд 5 Хорошо растворяется в воде, нерастворим в 95% спирте.
пользоваться свежепрокипяченной и охлажденной очищенной водой
растворять соль без встряхивания
Ф а р м а ц е в т и ч е с к а я х и м и я ЛС
Растворимость:
Слайд 6 1) Na+ - пирохимическая реакция
2) на карбонат - ион
NaHCO3
NaHCO3 + MgSO4 -> Mg(HCO3)2 + Na2SO4
Ф а р м а ц е в т и ч е с к а я х и м и я ЛС
Подлинность:
Слайд 7 - прозрачность и цветность раствора
- не допускается
- допустимое предельное содержание Cl-, SO42-, Fe, Ca2+, As
- потеря в весе при прокаливании не меньше 36,6%
Ф а р м а ц е в т и ч е с к а я х и м и я ЛС
Чистота:
Слайд 8 Метод нейтрализации, ацидиметрия
Рабочий раствор- 0,1н HCl
Ind - м/о
NaHCO3
C% = T*K*V*100% = не менее 99%
q
Ф а р м а ц е в т и ч е с к а я х и м и я ЛС
Количественное определение:
Слайд 11 В промышленности борную кислоту получают из борсодержащих минералов (ашарита Mg2OB2O5*H2O)
Ф а р м а ц е в т и ч е с к а я х и м и я ЛС
Получение:
Слайд 12 Жирные на ощупь, бесцветные, прозрачные чешуйчатые кристаллы или мелкий белый
Ф а р м а ц е в т и ч е с к а я х и м и я ЛС
Описание:
Слайд 13 В холодной воде растворяется плохо, в горячей – хорошо. Растворима
Ф а р м а ц е в т и ч е с к а я х и м и я ЛС
Растворимость:
Слайд 14 1) с этанолом в присутствии конц. H2SO4, при этом образуется
Ф а р м а ц е в т и ч е с к а я х и м и я ЛС
Подлинность:
Слайд 15 2) с куркумовой бумажкой, одновременно добавляя несколько капель HCl
Ф а р м а ц е в т и ч е с к а я х и м и я ЛС
Слайд 16- прозрачность и цветность;
- допускается присутствие примесей: кальция, железа, тяжелых металлов,
Чистая борная кислота должна полностью растворяться в горячей воде и спирте.
Ф а р м а ц е в т и ч е с к а я х и м и я ЛС
Чистота:
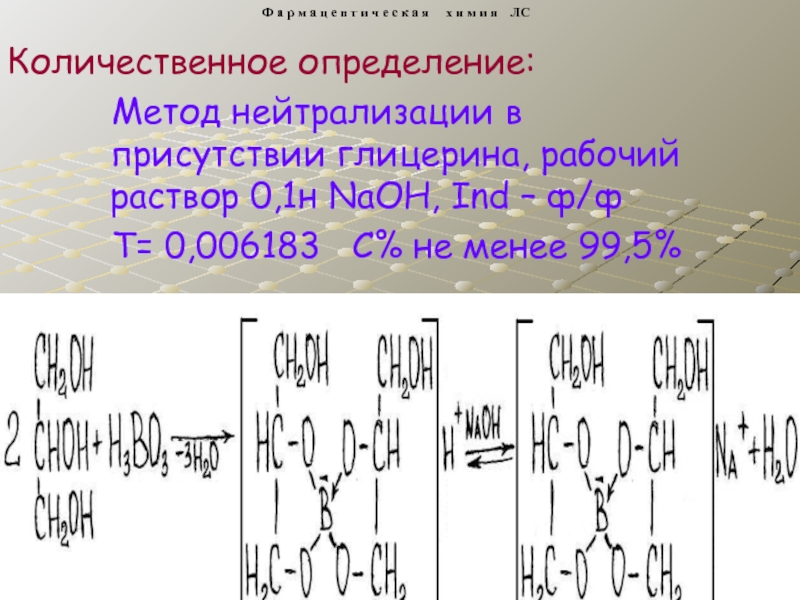
Слайд 17 Метод нейтрализации в присутствии глицерина, рабочий раствор 0,1н NaOH,
Т= 0,006183 С% не менее 99,5%
Ф а р м а ц е в т и ч е с к а я х и м и я ЛС
Количественное определение:
Слайд 18- как антисептическое средство в виде 2-3% растворов для полоскания горла,
- 1-2% водные растворы применяются в глазной практике
Ф а р м а ц е в т и ч е с к а я х и м и я ЛС
Применение:
Слайд 20
Натрия тетроборат. Бура
Natrii tetraboras Borax
Na2B4O7*10H2O М.м. 381,37
Ф а р м а
Слайд 21 В природе встречается в свободном состоянии. В промышленности получают
Ф а р м а ц е в т и ч е с к а я х и м и я ЛС
Получение:
Слайд 22 бесцветные прозрачные легковыветривающиеся кристаллы или белый кристаллический порошок
Ф а р
Описание:
Слайд 23 Хорошо растворяется в воде, лучше в горячей. Легко в глицерине,
Ф а р м а ц е в т и ч е с к а я х и м и я ЛС
Растворимость:
Слайд 24а) Na+:
пирохимическая реакция -окрашивание пламени в желтый цвет
б) бура дает
Ф а р м а ц е в т и ч е с к а я х и м и я ЛС
Подлинность:
Слайд 25- не должно быть примесей карбонатов;
- допускаются примеси мышьяка, хлоридов, сульфатов,
Ф а р м а ц е в т и ч е с к а я х и м и я ЛС
Чистота:
Слайд 26Метод нейтрализации (ацидиметрия)
Рабочий раствор – 0,1N HCL
Ind – м/о
Na2B4O7 * 10H2O
C% 99,5– 103%
Ф а р м а ц е в т и ч е с к а я х и м и я ЛС
Количественное определение:
Слайд 27
Ф а р м а ц е в т
Применение:
как антисептик в виде 1-2% растворов
Слайд 28 в хорошо укупоренной таре в прохладном месте
Ф а р
Хранение: