- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Углерод. Аллотропные модификации презентация
Содержание
- 1. Углерод. Аллотропные модификации
- 2. Положение в таблице Менделеева Углерод Carbogenium -
- 3. Нахождение в природе В настоящее время известно
- 4. Нахождение в природе Углерод занимает 17-е место
- 5. Нахождение в природе Углерод входит в состав
- 6. Свободный углерод В свободном виде углерод встречается
- 7. Алмаз
- 8. Графит
- 9. Модель фуллерена С60 Модель фуллерена С60
- 10. Все это - чистый углерод
- 11. Алмаз Алмаз – бесцветное, прозрачное, сильно преломляющее
- 12. Алмаз Плотность алмаза – 3,5 г/см3, tплав=3730С,
- 13. Алмаз Непрерывная трехмерная сетка ковалентных связей, которая
- 14. Графит Графит – устойчивая при нормальных условиях
- 15. Графит Атомы углерода в графите расположены отдельными
- 16. Графит Графит характеризуется меньшей плотностью и твердостью,
- 17. Карбин Карбин был получен в начале 60-х
- 18. Карбин Он имеет вид черного мелкокристаллического порошка,
- 19. Карбин За счет существования различных типов связи
- 20. Другие формы углерода Известны и другие формы
- 21. Фуллерены Фуллерены – класс химических соединений, молекулы
- 22. Фуллерены Происхождение термина "фуллерен" связано с именем
- 23. Фуллерены В начале 70-х годов физхимик–органик Е.Осава
- 24. Фуллерены В противоположность первым двум, графиту и
- 25. Фуллерены В фуллерене плоская сетка шестиугольников (графитовая
- 26. Фуллерены Молекулы фуллеренов, в которых атомы углерода
- 27. Фуллерены Кристалл фуллерита имеет плотность 1,7 г/см3,
- 28. Фуллерены Наиболее эффективный способ получения фуллеренов основан
- 29. Фуллерены Регулируя натяжение пружины, можно добиться, чтобы
- 30. Нанотрубки Наряду со сфероидальными углеродными структурами, могут
- 31. Нанотрубки На рисунке представлена идеализированная модель однослойной
- 32. Нанотрубки Многослойные нанотрубки отличаются от однослойных значительно
- 33. Нанотрубки Нанотрубка может быть получена из протяжённых
- 34. Нанотрубки В основе многих технологических применений нанотрубок
- 35. Наночастицы В процессе образования фуллеренов из графита
- 36. Заключение Хотя фуллерены имеют короткую историю, это
Слайд 2Положение в таблице Менделеева
Углерод Carbogenium - 6ой элемент в таблице Менделеева.
Слайд 3Нахождение в природе
В настоящее время известно более миллиона соединений углерода с
Слайд 4Нахождение в природе
Углерод занимает 17-е место по распространенности в земной коре
Слайд 5Нахождение в природе
Углерод входит в состав органических веществ в растительных и
Слайд 6Свободный углерод
В свободном виде углерод встречается в нескольких аллотропных модификациях –
Слайд 11Алмаз
Алмаз – бесцветное, прозрачное, сильно преломляющее свет вещество. Алмаз тверже всех
Структура алмаза
Слайд 12Алмаз
Плотность алмаза – 3,5 г/см3, tплав=3730С, tкип=4830оС. Алмаз можно получить из
Слайд 13Алмаз
Непрерывная трехмерная сетка ковалентных связей, которая характеризуется большой прочностью, определяет многие
Знаменитый бриллиант «Кохинор»
Слайд 14Графит
Графит – устойчивая при нормальных условиях аллотропная модификация углерода, имеет серо-черный
Структура графита
Слайд 15Графит
Атомы углерода в графите расположены отдельными слоями, образованными из плоских шестиугольников.
Слайд 16Графит
Графит характеризуется меньшей плотностью и твердостью, а также графит может расщепляться
Графитовый электрод
Слайд 17Карбин
Карбин был получен в начале 60-х годов В.В. Коршаком, А.М. Сладковым,
Строение карбина
Слайд 18Карбин
Он имеет вид черного мелкокристаллического порошка, однако может существовать в виде
Слайд 19Карбин
За счет существования различных типов связи и разных способов укладки цепей
Метеорит содержащий вкрапления карбина
Слайд 20Другие формы углерода
Известны и другие формы углерода, такие как уголь, кокс
Сажа
Слайд 21Фуллерены
Фуллерены – класс химических соединений, молекулы которых состоят только из углерода,
Фуллерен С70
Слайд 22Фуллерены
Происхождение термина "фуллерен" связано с именем американского архитектора Ричарда Букминстера Фуллера,
Купол Фуллера
Слайд 23Фуллерены
В начале 70-х годов физхимик–органик Е.Осава предположил существование полой, высокосимметричной молекулыС60,
Первый способ получения и выделения твердого кристаллического фуллерена был предложен в 1990 г. В.Кречмером и Д.Хафманом с коллегами в институте ядерной физики в г. Гейдельберге (Германия).
Слайд 24Фуллерены
В противоположность первым двум, графиту и алмазу, структура которых представляет собой
Модель фуллерена С60
Слайд 25Фуллерены
В фуллерене плоская сетка шестиугольников (графитовая сетка) свернута и сшита в
Фуллерены с n< 60 оказались неустойчивыми, хотя из чисто топологических соображений наименьшим возможным фуллереном является правильный додекаэдр С20.
Слайд 26Фуллерены
Молекулы фуллеренов, в которых атомы углерода связаны между собой как одинарными,
Слайд 27Фуллерены
Кристалл фуллерита имеет плотность 1,7 г/см3, что значительно меньше плотности графита
Слайд 28Фуллерены
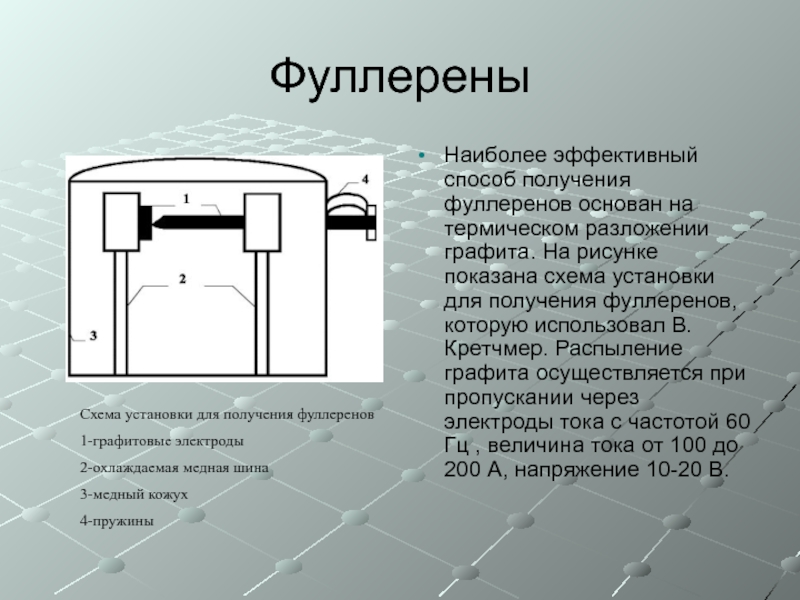
Наиболее эффективный способ получения фуллеренов основан на термическом разложении графита. На
Схема установки для получения фуллеренов
1-графитовые электроды
2-охлаждаемая медная шина
3-медный кожух
4-пружины
Слайд 29Фуллерены
Регулируя натяжение пружины, можно добиться, чтобы основная часть подводимой мощности выделялась
Если получаемый порошок соскоблить и выдержать в течение нескольких часов в кипящем толуоле, то получается темно-бурая жидкость. При выпаривании ее во вращающемся испарителе получается мелкодисперсный порошок, в нем содержится до 10% фуллеренов С60 (90%) и С70 (10%).
Слайд 30Нанотрубки
Наряду со сфероидальными углеродными структурами, могут образовываться также и протяженные цилиндрические
Идеальная нанотрубка представляет собой свернутую в цилиндр графитовую плоскость, выложенную правильными шестиугольниками, в вершинах которых расположены атомы углерода.
Строение нанотрубки
Слайд 31Нанотрубки
На рисунке представлена идеализированная модель однослойной нанотрубки. Такая трубка заканчивается полусферическими
Слайд 32Нанотрубки
Многослойные нанотрубки отличаются от однослойных значительно более широким разнообразием форм и
Слайд 33Нанотрубки
Нанотрубка может быть получена из протяжённых фрагментов графита, которые далее скручиваются
Слайд 34Нанотрубки
В основе многих технологических применений нанотрубок лежит такое их свойство, как
Слайд 35Наночастицы
В процессе образования фуллеренов из графита образуются также наночастицы. Это замкнутые
Слайд 36Заключение
Хотя фуллерены имеют короткую историю, это направление науки быстро развивается, привлекая
Физика фуллеренов занимается исследованием структурных, механических, магнитных, оптических свойств фуллеренов и их соединений. Сюда относится также изучение характера взаимодействия между атомами углерода в этих соединениях, свойства и структура систем, состоящих из молекул фуллеренов. Физика фуллеренов является наиболее продвинутой ветвью в области фуллеренов.
Химия фуллеренов связана с созданием и изучением новых химических соединений, основу которых составляютфуллерены, а также изучает химические процессы, в которых они участвуют. Следует отметить, что по концепциям и методам исследования это направление химии во многом принципиально отличается от традиционной химии.
Технология фуллеренов включает в себя как методы производства фуллеренов, так и различные их приложения.