- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Углекислый газ, угольная кислота и её соли презентация
Содержание
- 1. Углекислый газ, угольная кислота и её соли
- 2. Физические свойства СО2 СО2 – бесцветный газ, без
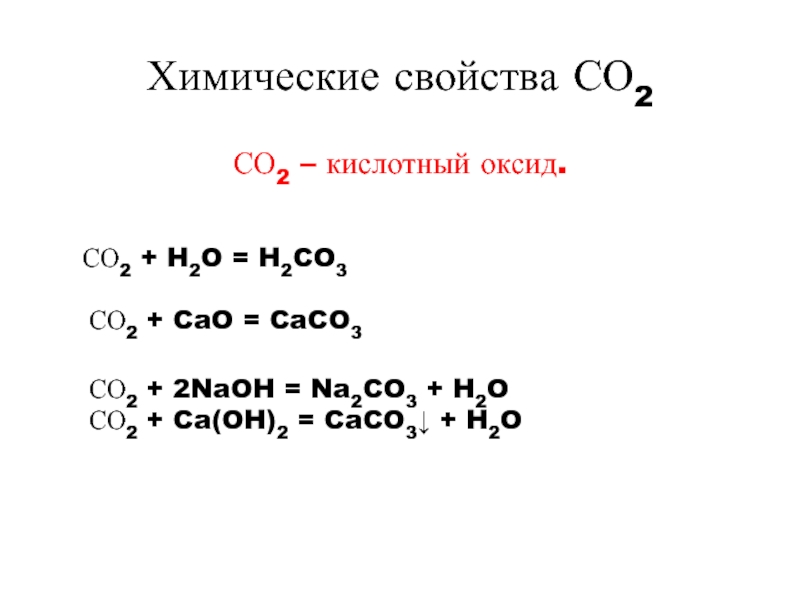
- 3. Химические свойства СО2 СО2 – кислотный оксид. СО2 +
- 4. Немного истории Английский химик Дж. Пристли в 1767 году сделал первую бутылку газировки.
- 5. При взаимодействии углекислого газа образуется нестойкое соединение
- 6. Сталактиты и сталагмиты Вода, проникающая в
- 7. При достаточном количестве карбоната кальция в растворе
- 8. Сливаясь со временем, сталактит со сталагмитом образуют колонну — сталагнат.
- 9. CaCO3 –мел, мрамор, известняк Na2CO3 –
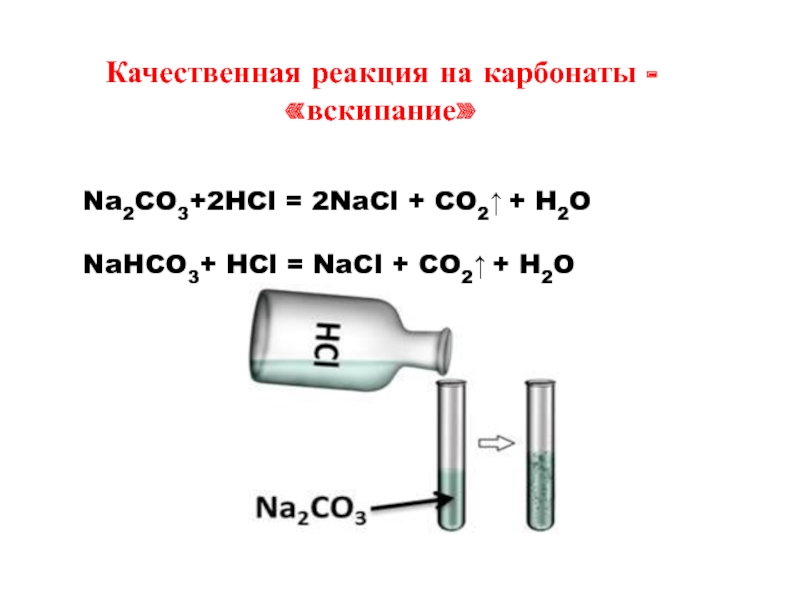
- 10. Качественная реакция на карбонаты - «вскипание»
Слайд 2Физические свойства СО2
СО2 – бесцветный газ, без запаха, в 1,5 раза тяжелее
СО2– «сухой лёд» - для хранения пищевых продуктов.
Слайд 3Химические свойства СО2
СО2 – кислотный оксид.
СО2 + 2NaOH = Na2CO3 + H2O
СО2 + Ca(OH)2 = CaCO3↓
СО2 + CaO = CaCO3
СО2 + H2O = H2CO3
Слайд 5При взаимодействии углекислого газа образуется нестойкое соединение – угольная кислота.
Угольная кислота H2CO3 –
Угольная кислота H2CO3 – двухосновная кислота => 2 ряда солей:
1) средние – карбонаты (MgCO3)
2) кислые – гидрокарбонаты (Сa(HCO3)2
Слайд 6Сталактиты и сталагмиты
Вода, проникающая в пещеру, растворяет известняк в химической реакции:
CaCO3 + H2O
При определённых условиях (разница в парциальном давлении углекислого газа в растворе и воздухе) реакция идёт в обратную сторону, и происходит отложение карбоната кальция — растут сталактиты.