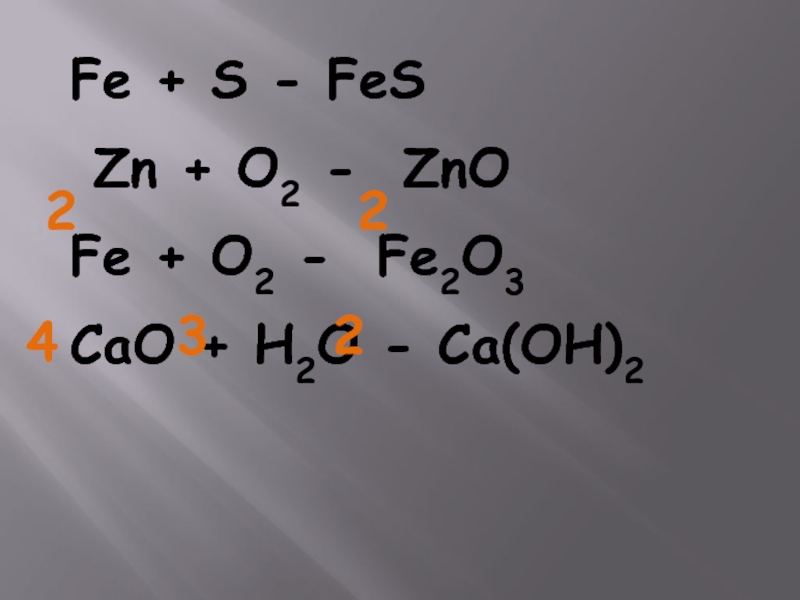- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Типы химических реакций презентация
Содержание
- 1. Типы химических реакций
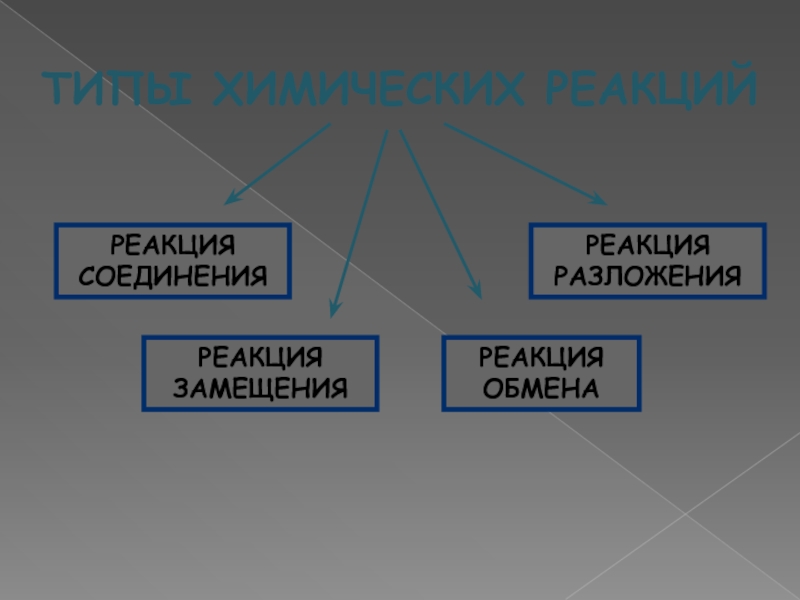
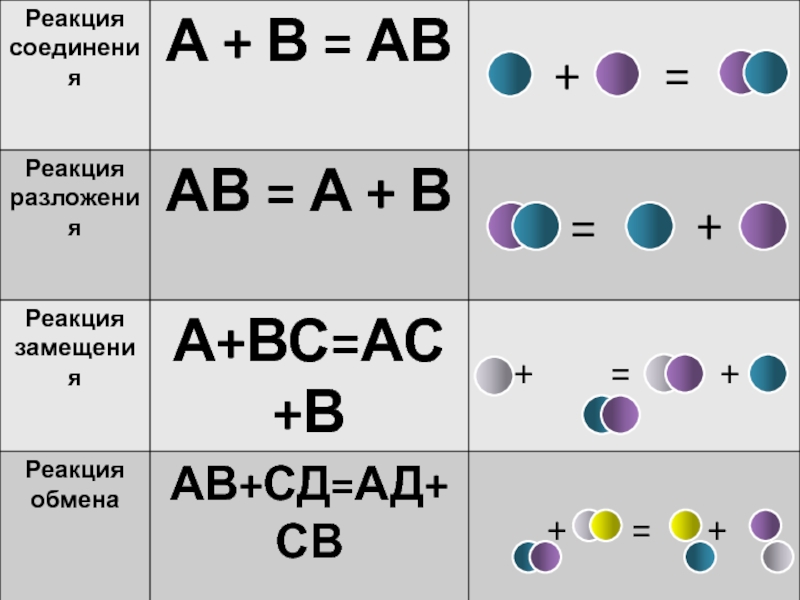
- 2. ТИПЫ ХИМИЧЕСКИХ РЕАКЦИЙ РЕАКЦИЯ СОЕДИНЕНИЯ РЕАКЦИЯ РАЗЛОЖЕНИЯ РЕАКЦИЯ ЗАМЕЩЕНИЯ РЕАКЦИЯ ОБМЕНА
- 3. П.П. Бажов «Малахитовая шкатулка»
- 4. Реакция разложения малахита: оксид меди (II)
- 5. – это реакции, в результате которых сложное
- 7. 1) CaO + CO2 = CaCO3 2)
- 8. – это реакции, в которых из нескольких
- 9. Fe + S - FeS
- 10. 1) 2HgO = 2Hg + O2 2)
- 11. Реакции между простым и сложным веществом, в
- 12. Zn + HCl – ZnCl2 + H2
- 13. Реакции между двумя сложными веществами, в результате
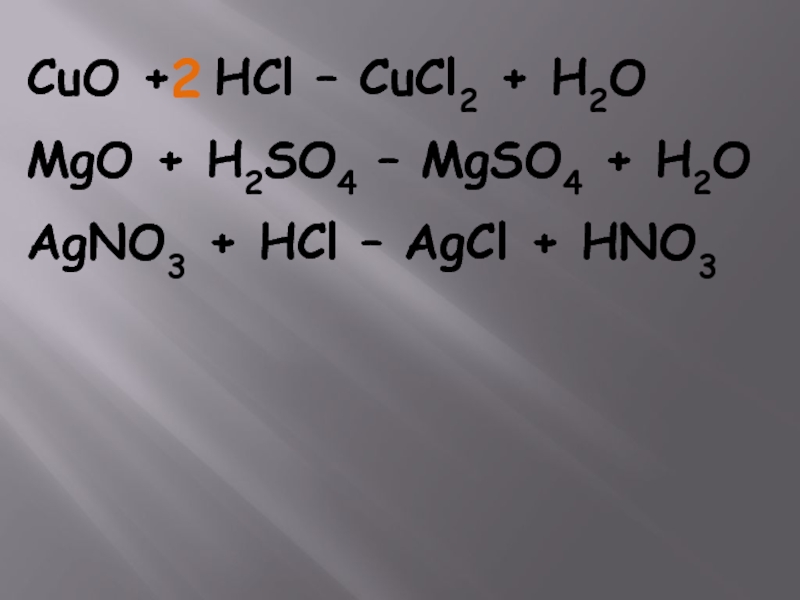
- 14. CuO + HCl – CuCl2 + H2O
- 15. + =
- 20. Список литературы http://prosto-o-slognom.ru/chimia/18_chim_reak.html 2. http://www.kristallikov.net/page19.html
Слайд 4Реакция разложения малахита:
оксид меди
(II)
(CuOH)2CO3 = 2CuO + H2O + CO2
малахит
вода
оксид
(IV)
Слайд 5– это реакции, в результате которых сложное вещество разлагается на несколько
Реакции разложения -
+
=
Слайд 71) CaO + CO2 = CaCO3
2) CO2 + 2NaOH = Na2CO3
3) Fe + S = FeS
4) 2H2O = 2H2 + O2↑
5) CuO + H2 = Cu + H2O
6) Zn + 2HCl = ZnCl2 + H2↑
7) ZnO + H2SO4 = ZnSO4 + H2O
8) Cu(OH)2 = CuO + H2O
Слайд 8– это реакции, в которых из нескольких простых или сложных веществ
Реакции соединения -
+
=
Подавляющее большинство реакций соединения экзотермичны.
Слайд 101) 2HgO = 2Hg + O2
2) CaCO3 = CaO + CO2
3)
4) CuO + H2 = Cu + H2O
5) 2H2 + O2 = 2H2O
6) H2SO4 + 2KOH = K2SO4 + 2H2O
7) BaO + SO2 = BaSO3
Слайд 11Реакции между простым и сложным веществом, в результате которых атомы простого
Реакции замещения -
+
+
=
Слайд 13Реакции между двумя сложными веществами, в результате которых они обмениваются своими
Реакции обмена -
+
+
=