- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Свойства растворов ВМС: особенности растворения, реологические свойства, осмос. Устойчивость растворов ВМС презентация
Содержание
- 1. Свойства растворов ВМС: особенности растворения, реологические свойства, осмос. Устойчивость растворов ВМС
- 2. Высокомолекулярные соединения… … вещества, молекулярная масса которых,
- 3. Сходства и различия растворов ВМС и коллоидных растворов
- 4. Растворы ВМС … … лиофильные коллоидные системы,
- 5. Строение (структура) ВМС линейная разветвлённая
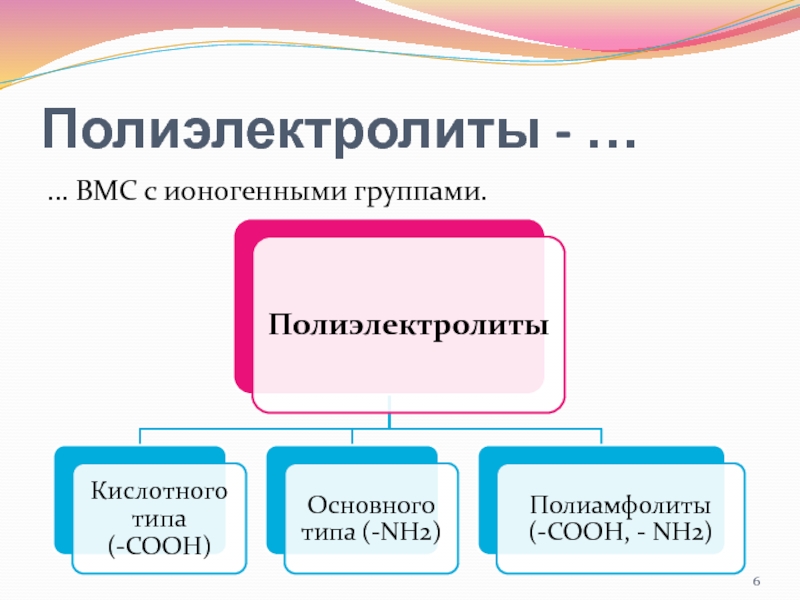
- 6. Полиэлектролиты - … … ВМС с ионогенными группами.
- 7. В растворе полиамфолита устанавливается равновесие
- 8. Особенности растворения ВМС Взаимодействие ВМС с водой
- 9. Ограниченное набухание Сопровождается образованием студня. Студень
- 10. Неограниченное набухание Ведёт к растворению ВМС.
- 11. Количественная оценка набухания Степень набухания
- 12. Свойства растворов ВМС Факторы устойчивости ВМС
- 13. Пути коагуляции растворов ВМС К коагуляции растворов
- 14. Коацервация… … расслаивание концентрированного раствора ВМС при
- 15. Высаливание… …нарушение устойчивости растворов ВМС при действии
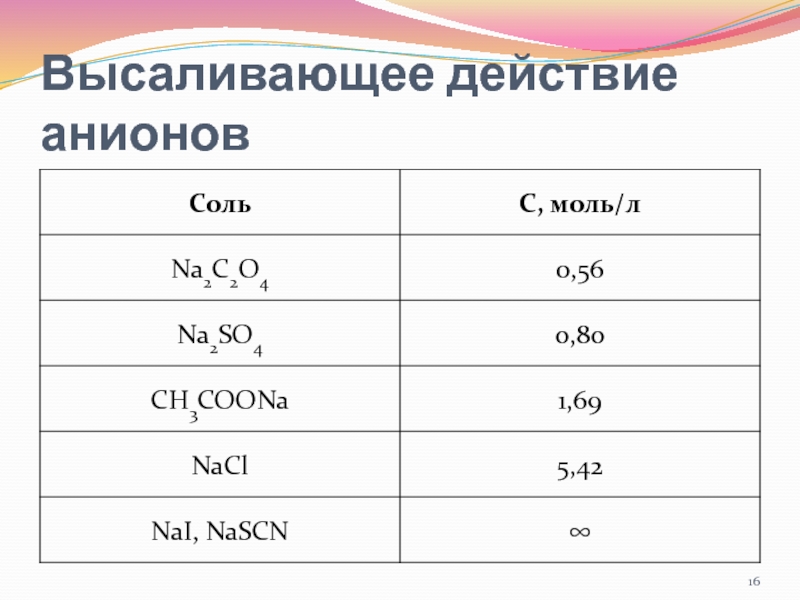
- 16. Высаливающее действие анионов
- 17. Ряды Гофмейстера C2O42- > SO42- > CH3COO-
- 18. Застудневание растворов ВМС - … … переход
- 19. Основу студня составляет пространственная сетка из цепей
- 20. Старение студней… Синерезис – уплотнение пространственной сетки
- 21. Вязкость растворов ВМС (η) … … внутреннее
- 22. Уравнение Эйнштейна η=η0(1+αϕ) η - вязкость раствора
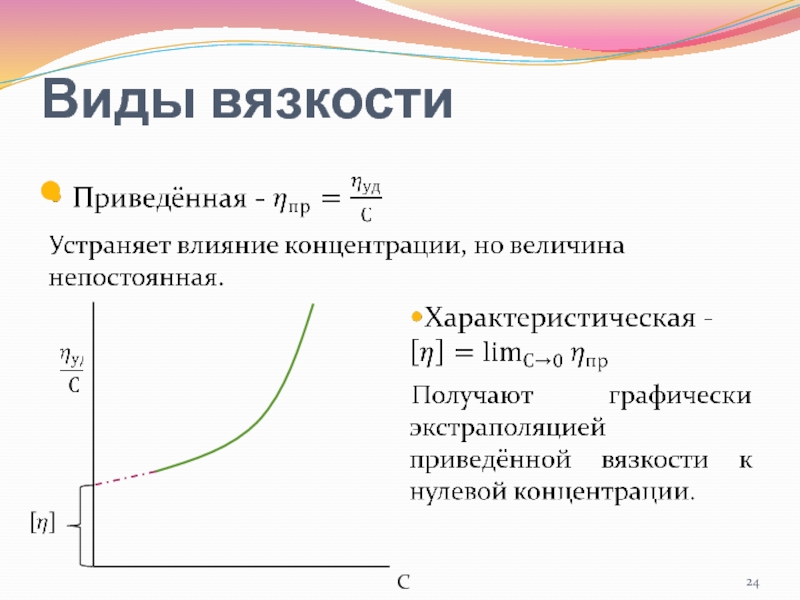
- 23. Виды вязкости
- 24. Виды вязкости С
- 25. Модифицированное уравнение Штаудингера
- 26. Вязкость крови… … очень важный показатель крови,
- 27. Вязкость крови В норме для плазмы крови
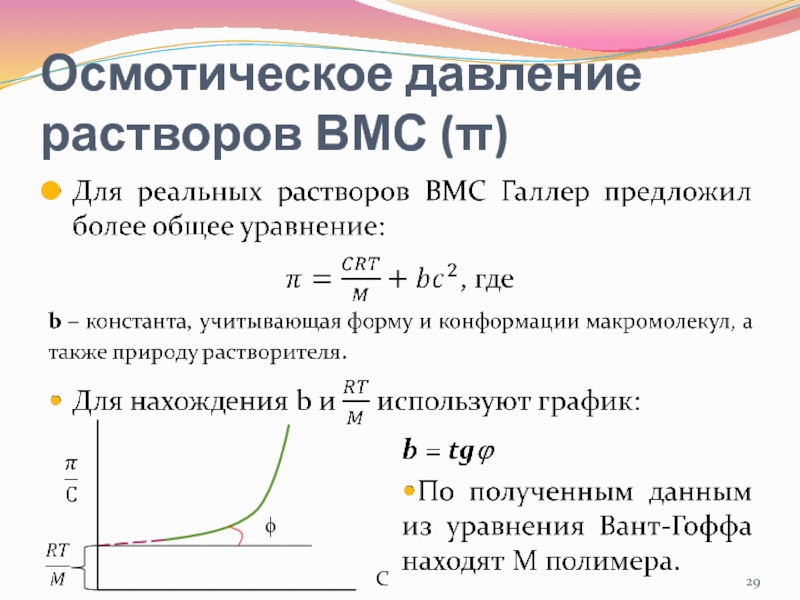
- 28. Осмотическое давление растворов ВМС (π)…
- 29. Осмотическое давление растворов ВМС (π) ϕ C
- 30. Онкотическое давление(πонк) … …часть осмотического давления крови,
- 31. Понижение πонк, вызванное гипопротеинемией, ведёт к развитию
- 32. Мембранное равновесие Доннана Описывает распределение электролитов по
- 33. Анализ уравнения Доннана Возможны 3 варианта распределения
- 34. Причина мембранного равновесия избирательная проницаемость клеточных мембран,
- 35. Спасибо за внимание!
Слайд 1Свойства растворов ВМС: особенности растворения, реологические свойства, осмос. Устойчивость растворов ВМС.
Лекции
Лектор:
канд. хим. наук, доцент
Иванова Надежда Семёновна
Слайд 2Высокомолекулярные соединения…
… вещества, молекулярная масса которых, по данным одних авторов составляет
К числу природных ВМС, играющих важную роль в жизнедеятельности человека, следует отнести белки, НК, полисахариды.
Слайд 4Растворы ВМС …
… лиофильные коллоидные системы, термодинамически устойчивые и обратимые;
… молекулярнодисперсные
Слайд 5Строение (структура) ВМС
линейная
разветвлённая
пространственная
Специфические свойства ВМС обусловлены их способностью принимать различные конформации
Конформации – энергетически неравноценные формы макромолекул, возникающие при простом повороте звеньев без разрыва химической связи.
Слайд 7В растворе полиамфолита устанавливается равновесие
Заряд белка зависит от:
количества и способности
рН среды.
ИЭТ – значение рН, при котором белок не заряжен за счёт равного числа кислотных и основных групп. В ИЭТ белок имеет вид: NH3+ - R – COO--
ОН-
Н+
Слайд 8Особенности растворения ВМС
Взаимодействие ВМС с водой начинается с процесса набухания.
Набухание –
Причина набухания – различия в размерах и подвижности молекул: молекулы ВМС велики и малоподвижны, молекулы НМС малы и очень подвижны.
Различают 2 вида набухания: ограниченное и неограниченное.
Слайд 9Ограниченное набухание
Сопровождается образованием студня.
Студень – пространственная сетка из цепей макромолекул,
Слайд 11Количественная оценка набухания
Степень набухания
где m0, V0 – масса и объём ВМС
m, V – масса и объём после набухания.
Факторы, влияющие на набухание:
Температура
Электролиты
рН
Обращённый ряд Гофмейстера
SCN->I- >NO3- >Cl- >CH3COO- >SO42- >C2O42-
Слайд 12
Свойства растворов ВМС
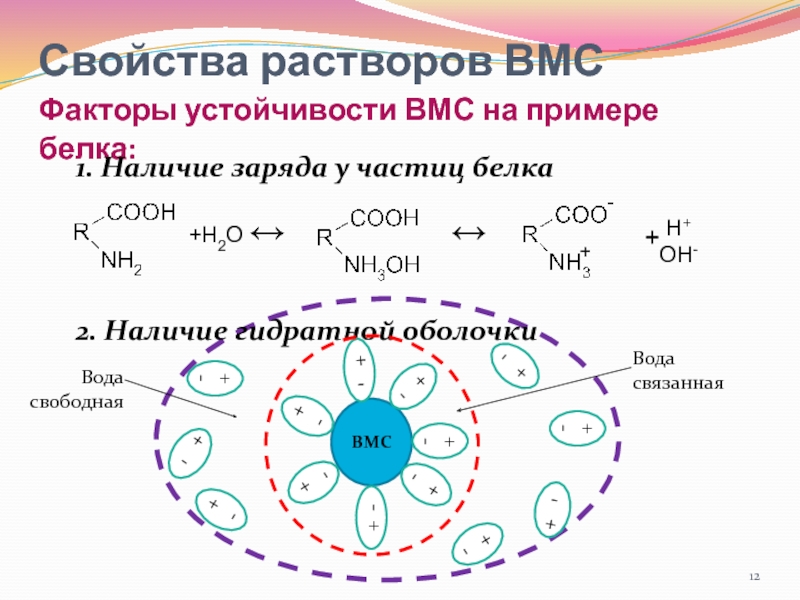
Факторы устойчивости ВМС на примере белка:
1. Наличие заряда у
2. Наличие гидратной оболочки
+Н2О ↔
↔
-
+
Н+
ОН-
+
ВМС
+ -
+ -
+ -
+-
+ -
+ -
+ -
+ -
+ -
- +
- +
+ -
+ -
+ -
Вода связанная
Вода свободная
Слайд 13Пути коагуляции растворов ВМС
К коагуляции растворов приводит:
одновременная нейтрализация заряда частицы ВМС
Электролитом нейтрализовать заряд и добавить дегидратирующее вещество (спирт, ацетон, танин и др.).
В начале провести дегидратацию, а затем нейтрализовать заряд частицы ВМС.
Данные схемы предложены учёным Кройтом.
Слайд 14Коацервация…
… расслаивание концентрированного раствора ВМС при действии дегидратирующих веществ на 2
Причина: слияние свободной воды у частиц ВМС; связанная вода не затрагивается. Считать коагуляцией коацервацию нельзя, т.к. у частицы сохранилась часть гидратной оболочки.
Слайд 15Высаливание…
…нарушение устойчивости растворов ВМС при действии неорганических солей.
Высаливающее действие соли заключается
Слайд 17Ряды Гофмейстера
C2O42- > SO42- > CH3COO- > Cl- > NO3- >
высаливающее действие повышают устойчивость коллоидов ВМС
Большое влияние на процесс высаливания оказывает длина макромолекулы и молекулярная масса ВМС: чем они больше, тем легче идёт высаливание. На этом принципе основано фракционное высаливание, сущность которого заключается в том, что добавляя к растворам ВМС возрастающие концентрации соли можно выделить отдельные фракции белков.
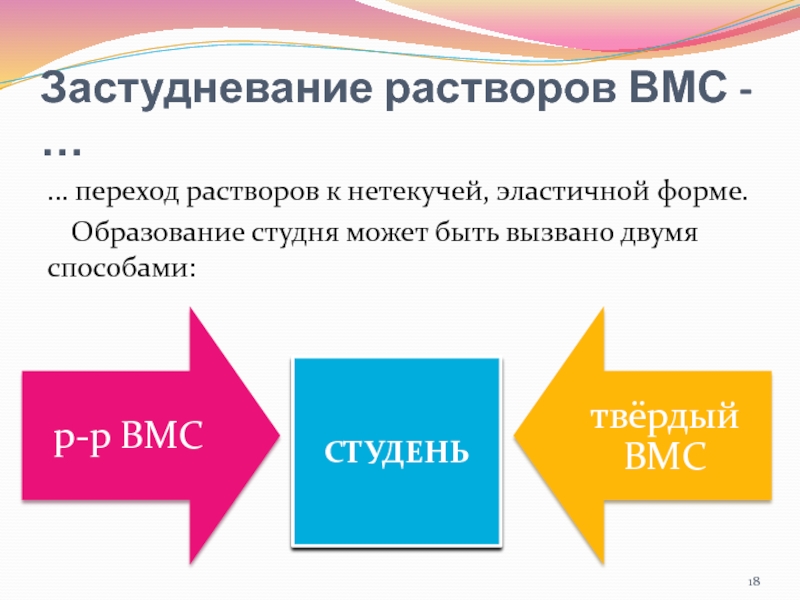
Слайд 18Застудневание растворов ВМС - …
… переход растворов к нетекучей, эластичной форме.
Образование
СТУДЕНЬ
Слайд 19Основу студня составляет пространственная сетка из цепей полимера, заполненная молекулами НМС.
Студни
Студни с сильными связями (химическими) достаточно прочные.
Слайд 20Старение студней…
Синерезис – уплотнение пространственной сетки студня за счёт выдавливания части
Синерезис в живых тканях указывает на старение организма: потеря воды приводит к утоньшению костей, сухости кожи, уменьшению эластичности тканей.
Слайд 21Вязкость растворов ВМС (η) …
… внутреннее трение между слоями ВМС, движущимися
Величина вязкости определяется силами молекулярного притяжения, поэтому
↑ в растворах полярных веществ;
↑ в растворах с размерами частиц, превышающими размеры частиц растворителя;
на величину вязкости оказывает влияние форма частиц (?, ಟ, ಯ, Ο и др);
↑ с увеличением молекулярной массы растворённого вещества;
↑ с увеличением концентрации частиц вещества.
Слайд 22Уравнение Эйнштейна
η=η0(1+αϕ)
η - вязкость раствора
η0 – вязкость растворителя
α – коэффициент, зависящий
ϕ - объёмная доля частиц
Недостаток: не учитывает наличие различных слоёв у частиц (сольватных, адсорбционных, электрических), создающих дополнительные вязкостные эффекты.
14.III 1879 — 18.IV 1955
Эйнштейн Альберт
Слайд 26Вязкость крови…
… очень важный показатель крови, определяющий максимальный срок службы сердца
Что дает Вам анализ крови на вязкость? Ответ очень прост. Проснетесь Вы завтра или нет. Вязкость крови изменяется в очень широких пределах. При этом на состояние крови влияет очень много факторов. Критическое увеличение вязкости крови ставит всю сердечно-сосудистую систему и ее хозяина на грань выживаемости. Т.е. увеличение вязкости крови повышает кардиологический риск либо риск внезапной сердечной смерти.
Слайд 27Вязкость крови
В норме для плазмы крови и лимфы η=1,4∙10-3Па∙С (t=37°С).
↑ концентрации
На η влияет и состояние мембран эритроцитов (до 45% объёма крови): в норме высокая эластичность, потеря или снижение которой ведёт к ↑η крови.
Слайд 30Онкотическое давление(πонк) …
…часть осмотического давления крови, обусловленная наличием белков и их
В норме ~ 3,1 кПа. Отклонение этой величины от нормы приводит к серьёзным нарушениям функционирования организма.
Причина: на кровь в капилляре действуют гидростатическое давление (ргидр.) ~ 4,5 кПа и онкотическое давление. Стенка капилляра представляет собой мембрану, непроницаемую для белка, но проницаемую для воды и безбелковой части плазмы.
ргидр способствут выдавливанию воды и безбелковой части плазмы в межклеточную жидкость. πонк способствует всасыванию воды из ткани в капилляр.
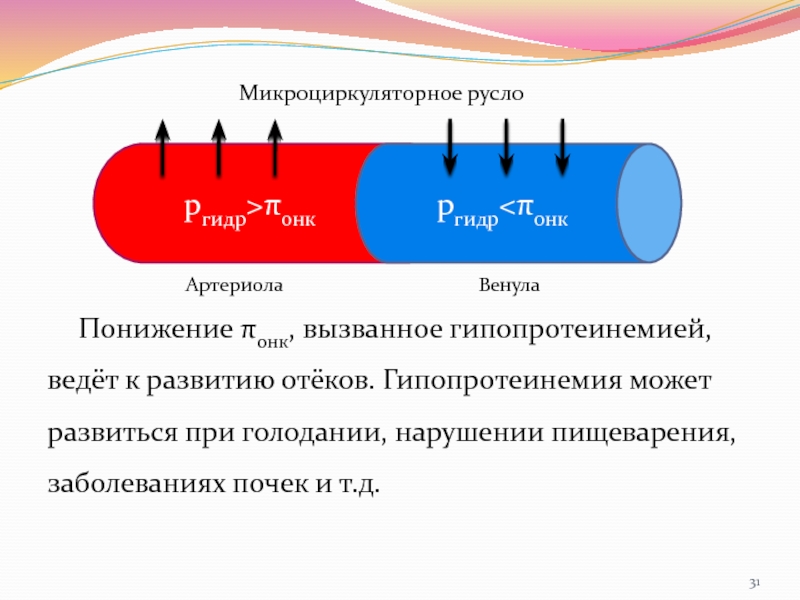
Слайд 31Понижение πонк, вызванное гипопротеинемией, ведёт к развитию отёков. Гипопротеинемия может развиться
ргидр>πонк
ргидр<πонк
Микроциркуляторное русло
Артериола
Венула
Слайд 32Мембранное равновесие Доннана
Описывает распределение электролитов по обе стороны клеточной мембраны.
сout –
сin – концентрация ионов внутри клетки;
х – количество ионов, перешедших в клетку из межклеточной жидкости.
Слайд 33Анализ уравнения Доннана
Возможны 3 варианта распределения ионов:
1) cout > cin ⇒
2)
3) cin = cout ⇒
Вывод: концентрация ионов в клетке будет всегда выше, чем в межклеточной жидкости.
Слайд 34Причина мембранного равновесия
избирательная проницаемость клеточных мембран, из-за которой соли белка всегда
Значение равновесия Доннана в жизнедеятельности: πin > πout ⇒ поддержание тургора клеток даже в изотонических растворах.