- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Substancje chemiczne презентация
Содержание
- 1. Substancje chemiczne
- 2. Substancje chemiczne Krystyna Sitko
- 3. Wszystko co nas otacza uczeni nazwali materią.
- 4. Piktogramy Substancja wybuchowa Substancja łatwopalna
- 5. Substancja a ciało fizyczne Ciała fizyczne to
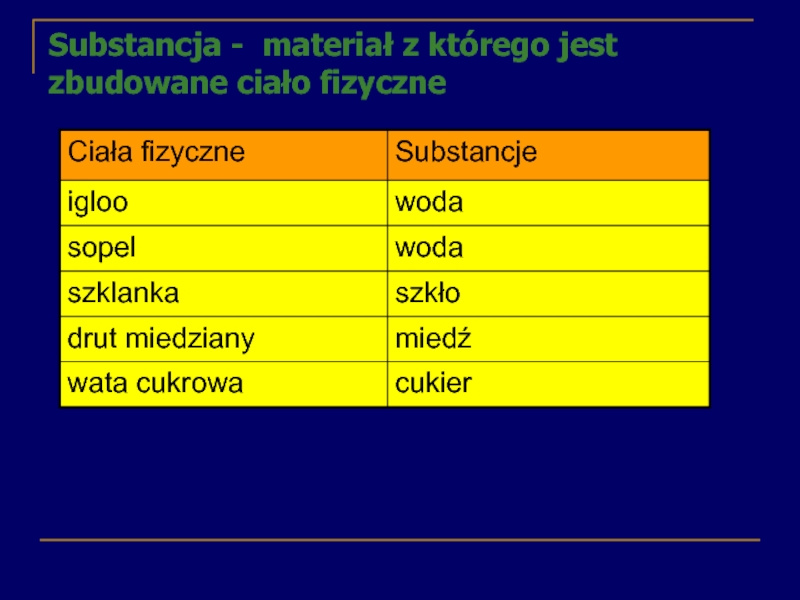
- 6. Substancja - materiał z którego jest zbudowane ciało fizyczne
- 7. Właściwość fizyczna stan skupienia temperatura
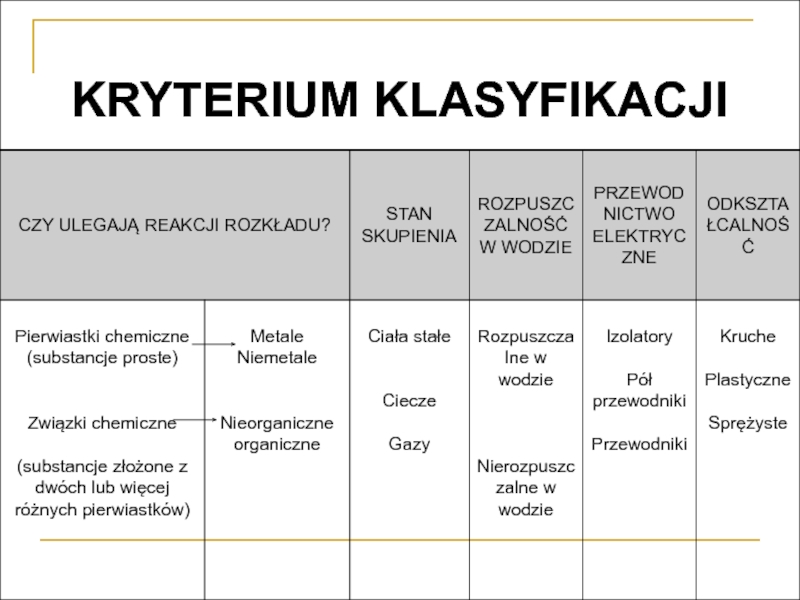
- 8. Podział substancji Substancje dzielą się
- 9. Substancja złożona- tlenek żelaza (III) Substancja prosta
- 10. Pierwiastek chemiczny Pojęcie pierwiastka chemicznego wprowadził w
- 11. Nazwy pierwiastków Nazwy pierwiastków pochodzą między innymi
- 12. Symbole pierwiastków Obecnie stosowaną symbolikę wprowadził w
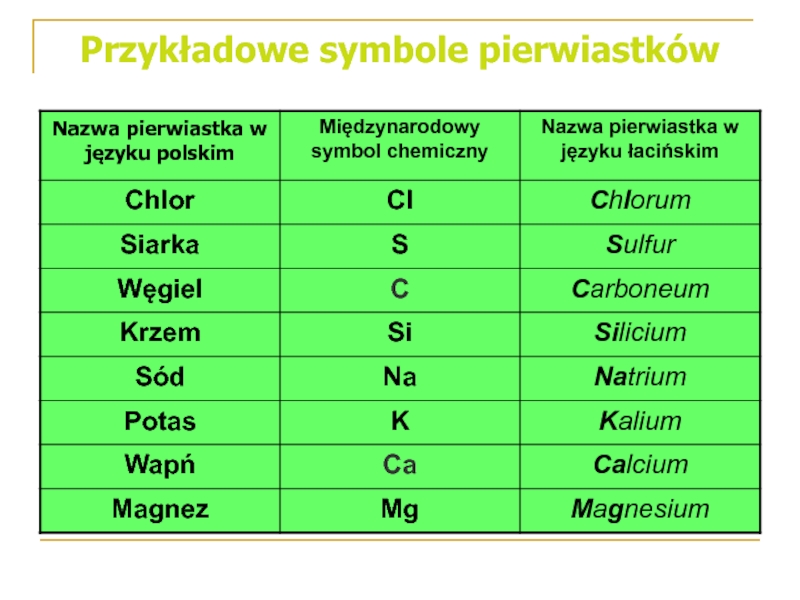
- 13. Przykładowe symbole pierwiastków
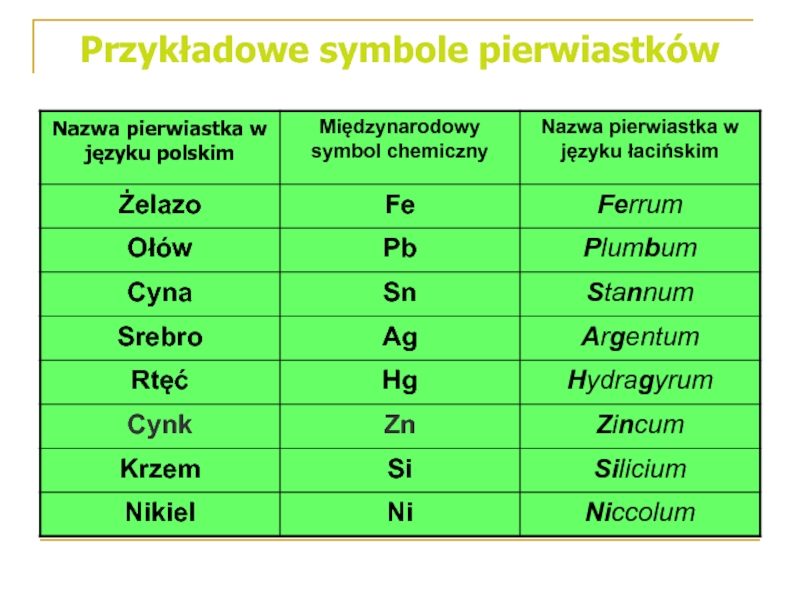
- 14. Przykładowe symbole pierwiastków
- 15. Przykładowe symbole pierwiastków
- 16. Stan skupienia substancji chemicznej Substancje chemiczne mogą
- 17. Przemiany chemiczne substancje mogą zmieniać tylko niektóre
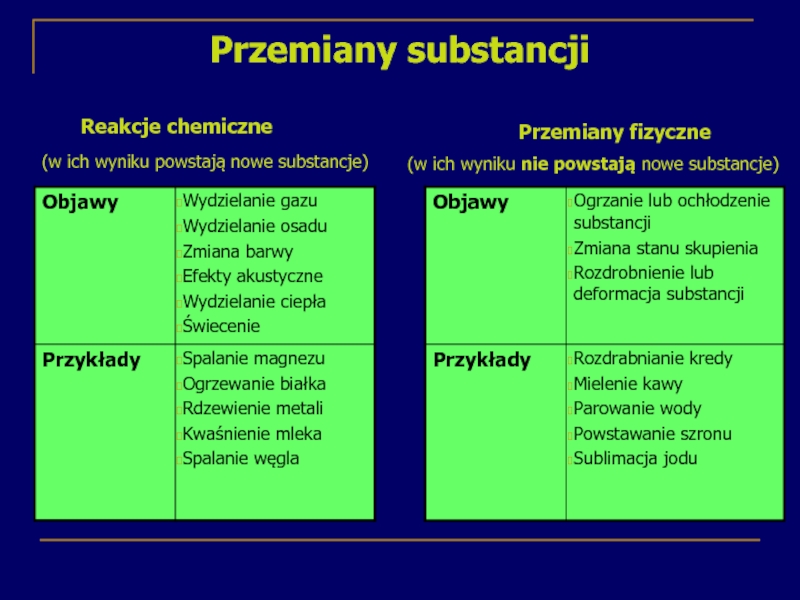
- 18. Przemiany substancji
- 19. Doświadczenie Obserwacja zmian zachodzących na przedmiotach
- 21. Substancja chemiczna w określonych warunkach (temperatura, ciśnienie)
- 22. W praktyce rzadko spotykamy się z substancjami
- 23. Wybrane substancje chemiczne i ich właściwości: Ciało
- 24. Ciecz – Alkohol (etanol) Właściwości fizyczne i
- 25. Gaz ziemny Gaz ziemny - to mieszanka
Слайд 1Materiały pochodzą z Platformy Edukacyjnej Portalu www.szkolnictwo.pl
Wszelkie treści i zasoby edukacyjne
Слайд 3Wszystko co nas otacza uczeni nazwali materią. Na przykład szpilka i
Elementy materii, które mają ten sam skład i charakterystyczne cechy, nazywamy substancjami
celuloza
żelazo
Слайд 4Piktogramy
Substancja wybuchowa
Substancja łatwopalna
Substancja toksyczna
Substancja żrąca
Substancja szkodliwa
Substancja drażniąca
Substancje chemiczne,
Слайд 5Substancja a ciało fizyczne
Ciała fizyczne to otaczające nas przedmioty
Igloo
Sopel
Szklanka
Drut
Wata cukrowa
Przykłady ciał fizycznych:
Слайд 7Właściwość fizyczna
stan skupienia
temperatura topnienia
temperatura wrzenia
barwa
rozpuszczalność w wodzie i innych rozpuszczalnikach
wytrzymałość na
gęstość
przewodnictwo elektryczne i cieplne
zachowanie się w polu magnetycznym
kowalność
połysk
Właściwością fizyczną jest:
Charakterystyczne cechy danej substancji, za pomocą których można ją opisać, nazywamy właściwościami fizycznymi
Слайд 8 Podział substancji
Substancje dzielą się na:
proste
-takie których nie można
złożone
-takie które można rozłożyć na substancje prostsze
Слайд 9Substancja złożona- tlenek żelaza (III)
Substancja prosta - jod
Substancje proste to pierwiastki
a substancje złożone to związki chemiczne
Слайд 10Pierwiastek chemiczny
Pojęcie pierwiastka chemicznego wprowadził w II połowie XVII wieku angielski
Robert Boyle
Znane dziś pierwiastki występujące w przyrodzie zostały odkryte do 1925 roku. W miarę postępu nauki otrzymywano nowe pierwiastki.
Слайд 11Nazwy pierwiastków
Nazwy pierwiastków pochodzą między innymi od:
nazw państw: na przykład
nazw ciał niebieskich: na przykład hel ( z greckiego helios – słońce)
imion bogów i postaci mitologicznych: na przykład niob
nazwisk wybitnych uczonych: na przykład kiur – nazwa nadana na cześć odkryć Marii Skłodowskiej-Courie i jej męża Piotra.
Właściwości pierwiastków: na przykład fosfor zawdzięcza swoją nazwę temu, że jedna z jego odmian świeci w ciemności ( phosphorus oznacza „niosący światło”)
Слайд 12Symbole pierwiastków
Obecnie stosowaną symbolikę wprowadził w 1815 roku Jacob Berzelius.
Jacob Berzelius
Symbol
Слайд 16Stan skupienia substancji chemicznej
Substancje chemiczne mogą występować w stanie:
gazowym (np.para
ciekłym (np.kwas siarkowy VI)
stałym (np.tlenek wapnia)
Слайд 17Przemiany chemiczne
substancje mogą zmieniać tylko niektóre swoje właściwości fizyczne i wtedy
mogą powstawać nowe substancje chemiczne i wtedy zachodzi reakcja chemiczna
substancje mogą się ze sobą mieszać w dowolnym stosunku masowym- powstają mieszaniny substancji
z jąder jednych atomów mogą powstawać jądra innych atomów- są to przemiany promieniotwórcze
Substancje ulegają ciągłym przemianom. Podczas tych przemian:
Слайд 18Przemiany substancji
Reakcje chemiczne
(w ich wyniku
Przemiany fizyczne
(w ich wyniku nie powstają nowe substancje)
Слайд 19Doświadczenie
Obserwacja zmian zachodzących na przedmiotach
Określ jakim zmianom uległy przedmioty przedstawione
Co zaobserwowałeś?
Zmieniła się barwa. Powstała substancja jest krucha. Przedmioty zniszczone w wyniku korozji mają inne właściwości fizyczne niż przedmioty niezniszczone.
Слайд 21Substancja chemiczna w określonych warunkach (temperatura, ciśnienie) występuje w danym stanie
Слайд 22 W praktyce rzadko spotykamy się z substancjami chemicznymi, częściej są to
Слайд 23Wybrane substancje chemiczne i ich właściwości: Ciało stałe - Złoto
Ogólne informacje:
Symbol
Liczba atomowa -79
Stopień utleniania - -I, +I, +III, +V
Właściwości metaliczne – metal przejściowy
Właściwości tlenków – amfoteryczne
Masa atomowa -196,966569(5)[a][4]u
Stan skupienia – stały
Gęstość -19300 kg/m³
Temperatura topnienia - 1064,18 °C
Temperatura wrzenia -2856 °C
Слайд 24Ciecz – Alkohol (etanol)
Właściwości fizyczne i chemiczne etanolu;
-ciecz bezbarwna
-lżejsza od wody
-dobrze
Zastosowanie Etanolu -produkcja napojów alkoholowych -wykorzystywany do preparatów chemicznych i farmaceutycznych -jako paliwo w silnikach spalinowych -do produkcji leków
Слайд 25Gaz ziemny
Gaz ziemny - to mieszanka węglowodorów gazowych (etan, metan, propan),
Właściwości gazu ziemnego:
Ciężar – lżejszy od powietrza
Stan skupienia – gazowy
Zapach – bezwonny
Działanie duszące
Kolor – bezbarwny
Gaz palny
Wybuchowy – przy stężeniu z tlenem - granice wybuchowości 5 % - 15 %
wartość opałowa 35200-62800 kJ/m3,