элемент главной подгруппы второй группы, пятого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 38. Обозначается символом Sr (лат. Strontium). Простое вещество стронций — мягкий, ковкий и пластичный щёлочноземельный металл серебристо-белого цвета.
- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Стронций презентация
Содержание
- 1. Стронций
- 2. Новый элемент обнаружили в минерале стронцианите, найденном
- 3. Стронций. Основные сведения об элементе. Основные физические
- 4. При комнатной температуре решетка Стронция кубическая гранецентрированная
- 5. Стронций. Основные сведения об элементе. Химические свойства.
- 6. Металлический стронций быстро окисляется на воздухе, образуя
- 7. Распространённость стронция в природе. Среднее содержание Стронция
- 8. Основные минералы носители SrAl3(AsO4)SO4(OH)6 — кеммлицит; Sr2Al(CO3)F5
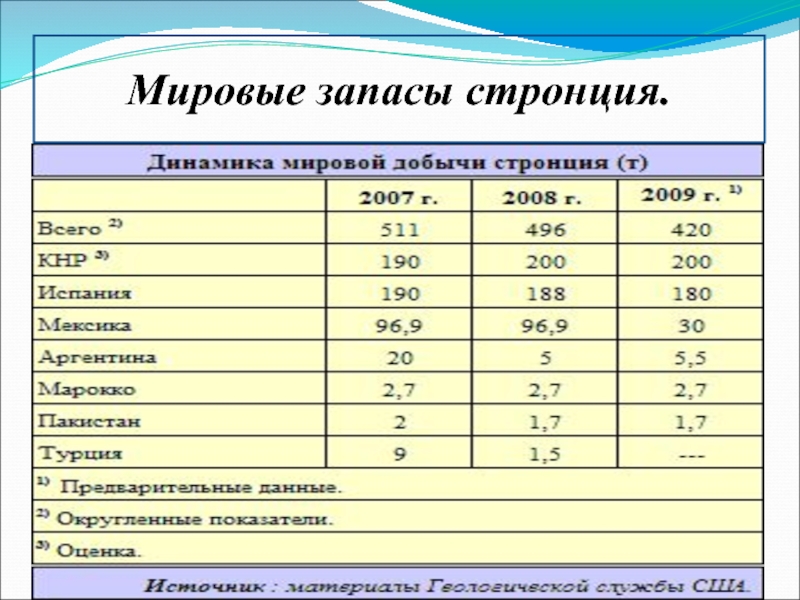
- 9. Мировые запасы стронция.
- 10. Основные месторождения по добычи стронция. Известны месторождения
- 11. Области применения Металлургия Металлотермия Магнитные материалы Пиротехника Атомноводородная энергетика Медицина
Слайд 2Новый элемент обнаружили в минерале стронцианите, найденном в 1764 году в
свинцовом руднике близ шотландской деревни Строншиан, давшей впоследствии название новому элементу. Присутствие в этом минерале оксида нового металла было установлено в 1787 году Уильямом Крюйкшенком и Адером Кроуфордом. Выделен в чистом виде сэром Хемфри Дэви в 1808 году.
Слайд 3Стронций. Основные сведения об элементе. Основные физические характеристики.
Относительная электроотрицательность : 1.0
Температура
плавления: 768°C
Атомная масса: 81,62 а.е.м.
Электродный потенциал: -2,89
Теплопроводность: 0,737
Плотность: 2,6 г/см3
Цвет в твёрдом состоянии: Серебристо-белый
Тип: Щелочно-земельный металл
Атомная масса: 81,62 а.е.м.
Электродный потенциал: -2,89
Теплопроводность: 0,737
Плотность: 2,6 г/см3
Цвет в твёрдом состоянии: Серебристо-белый
Тип: Щелочно-земельный металл
Орбитали: 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s2
1ый потенциал ионизации: 5,569 В
Ковалентный радиус: 1,91 Å
Слайд 4При комнатной температуре решетка Стронция кубическая гранецентрированная (α-Sr) с периодом а
= 6,0848Å; при температуре выше 248 °С превращается в гексагональную модификацию (β-Sr) с периодами решетки а = 4,32Å и с = 7,06 Å; при 614 °C переходит в кубическую объемноцентрированную модификацию (γ-Sr) с периодом а = 4,85Å. Атомный радиус 2,15Å, ионный радиус Sr2+ 1,20Å. Плотность α-формы 2,63 г/см3 (20 °C); tпл 770 °С, tкип 1383 °C; удельная теплоемкость 737,4 кдж/(кг·К) [0,176 кал/(г·°С)]; удельное электросопротивление 22,76·10-6 ом·см-1. Стронций парамагнитен, атомная магнитная восприимчивость при комнатной температуре 91,2·10-6. Стронций - мягкий пластичный металл, легко режется ножом. Изотоп - стронций 90
Слайд 5Стронций. Основные сведения об элементе. Химические свойства.
Стронций в своих соединениях всегда
проявляет валентность +2. По свойствам стронций близок к кальцию и барию, занимая промежуточное положение между ними.
В электрохимическом ряду напряжений стронций находится среди наиболее активных металлов (его нормальный электродный потенциал равен −2,89 В). Энергично реагирует с водой, образуя гидроксид:
Sr+2H2O Sr(OH)2+H2
Взаимодействует с кислотами, вытесняет тяжёлые металлы из их солей. С концентрированными кислотами (H2SO4, HNO3) реагирует слабо.
В электрохимическом ряду напряжений стронций находится среди наиболее активных металлов (его нормальный электродный потенциал равен −2,89 В). Энергично реагирует с водой, образуя гидроксид:
Sr+2H2O Sr(OH)2+H2
Взаимодействует с кислотами, вытесняет тяжёлые металлы из их солей. С концентрированными кислотами (H2SO4, HNO3) реагирует слабо.
Слайд 6Металлический стронций быстро окисляется на воздухе, образуя желтоватую плёнку, в которой
помимо оксида SrO всегда присутствуют пероксид SrO2 и нитрид Sr3N2. При нагревании на воздухе загорается, порошкообразный стронций на воздухе склонен к самовоспламенению.
Энергично реагирует с неметаллами — серой, фосфором, галогенами. Взаимодействует с водородом (выше 200оС), азотом (выше 400оС). Практически не реагирует с щелочами.
Энергично реагирует с неметаллами — серой, фосфором, галогенами. Взаимодействует с водородом (выше 200оС), азотом (выше 400оС). Практически не реагирует с щелочами.
Слайд 7Распространённость стронция в природе.
Среднее содержание Стронция в земной коре (кларк) 3,4·10-2%
по массе, в геохимических процессах он является спутником кальция. Известно около 30 минералов Стронция; важнейшие - целестин SrSO4 и стронцианит SrCO3. В магматических породах Стронций находится преимущественно в рассеянном виде и входит в виде изоморфной примеси в кристаллическую решетку кальциевых, калиевых и бариевых минералов. В биосфере Стронций накапливается в карбонатных породах и особенно в осадках соленых озер и лагун (месторождения целестина).
Слайд 8Основные минералы носители
SrAl3(AsO4)SO4(OH)6 — кеммлицит;
Sr2Al(CO3)F5 — стенонит;
SrAl2(CO3)2(OH)4•Н2О — стронциодрессерит;
SrAl3(PO4)2(OH)5•Н2О — гойясит;
Sr2Al(PO4)2OH
— гудкенит;
SrAl3(PO4)SO4(OH)6 — сванбергит;
Sr(AlSiO4)2 — слосонит;
Sr(AlSi3O8)2•5Н2О — брюстерит;
Sr5(AsO4)3F — ферморит;
Sr2(B14O23)•8Н2О — стронциоджинорит;
Sr2(B5O9)Cl•Н2О — стронциохильгардит;
SrFe3(PO4)2(OH)5•Н2О — люсуньит;
SrMn2(VO4)2•4Н2О — сантафеит;
Sr5(PO4)3OH — беловит;
SrV(Si2O7) — харадаит.
SrAl3(PO4)SO4(OH)6 — сванбергит;
Sr(AlSiO4)2 — слосонит;
Sr(AlSi3O8)2•5Н2О — брюстерит;
Sr5(AsO4)3F — ферморит;
Sr2(B14O23)•8Н2О — стронциоджинорит;
Sr2(B5O9)Cl•Н2О — стронциохильгардит;
SrFe3(PO4)2(OH)5•Н2О — люсуньит;
SrMn2(VO4)2•4Н2О — сантафеит;
Sr5(PO4)3OH — беловит;
SrV(Si2O7) — харадаит.
Слайд 10Основные месторождения по добычи стронция.
Известны месторождения стронция в Калифорнии, Аризоне (США);
России(Пермский край), Китай и других странах