- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Строение и свойства комплексных соединений презентация
Содержание
- 1. Строение и свойства комплексных соединений
- 2. Основные вопросы темы: Современные представления о строении
- 3. Реагенты в химии Катализаторы Лекарственные препараты Витамины Хлорофилл Гемоглобин И др.
- 4. КС– это такие соединения, в узлах кристаллической
- 5. Примеры реакций комплексообразования HgI2 + 2KI =
- 6. Кристаллогидраты: CuSO4•5H2O [Cu(H2O)4]SO4 ∙ Н2О
- 7. Альфред Вернер Швейцарский химик, 1893г
- 8. Составные части комплексных соединений [Co+3 (NH3)
- 9. Характеристика центрального атома Комплексообразующая способность
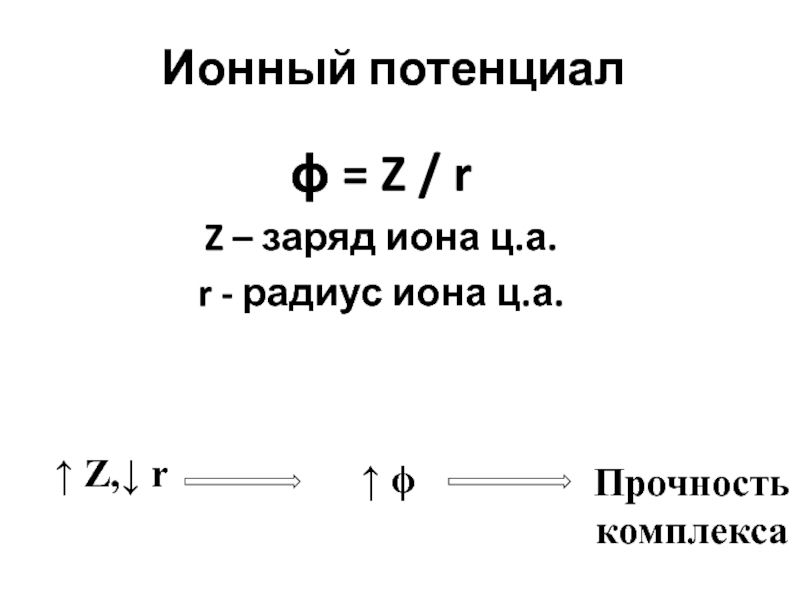
- 10. Важнейшие характеристики центрального атома : Степень окисления Координационное число Ионный потенциал
- 11. Степень окисления Положительная K3[Fe3+(CN)6],
- 12. Координационное число (КЧ) Это число атомов или групп атомов, непосредственно связанных с центральным атомом
- 13. - от размеров центрального атома
- 14. Na[BF4]
- 15. Na3[AlF6]
- 16. - от степени окисления центрального атома:
- 17. чаще всего кч устойчивого комплекса в два
- 18. Al(OH)3 + NaOH= Na[Al(OH)4] Al(OH)3 +3
- 19. Ионный потенциал ϕ = Z / r
- 20. Характеристика лигандов
- 21. Лиганды NH3, H2O, CO, NO, N2,
- 22. -монодентатные лиганды, содержат 1 донорный атом
- 23. -бидентатные лиганды, содержат 2 донорных атома и
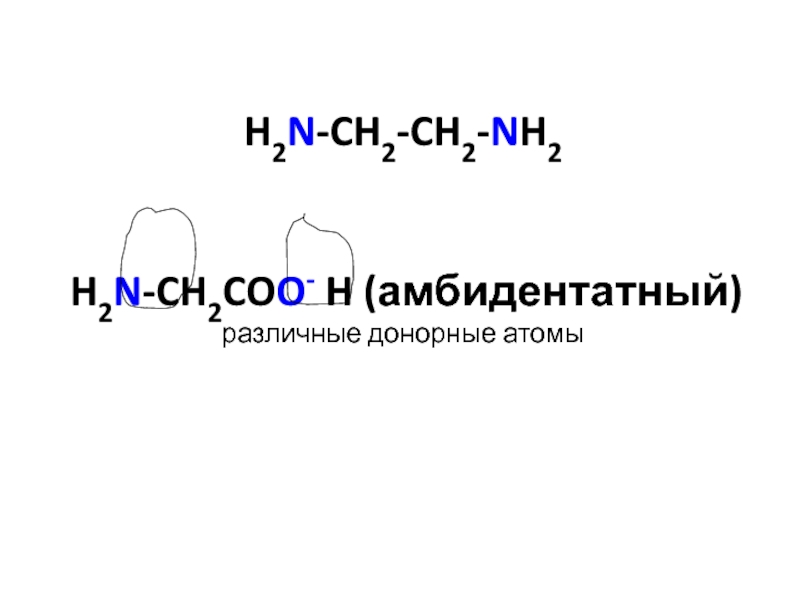
- 24. H2N-CH2-CH2-NH2 H2N-CH2COO- H (амбидентатный) различные донорные атомы
- 25. -полидентатные лиганды: СН2 - СH – CH2
- 26. ЭДТА (этилендиаминтетраацетат –анион) -OOCH2C
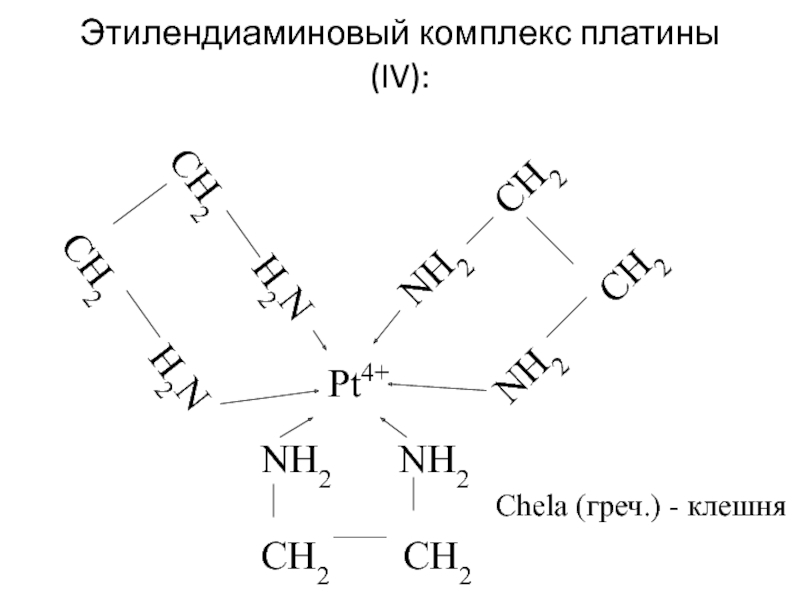
- 27. Этилендиаминовый комплекс платины(IV): Chela (греч.) - клешня
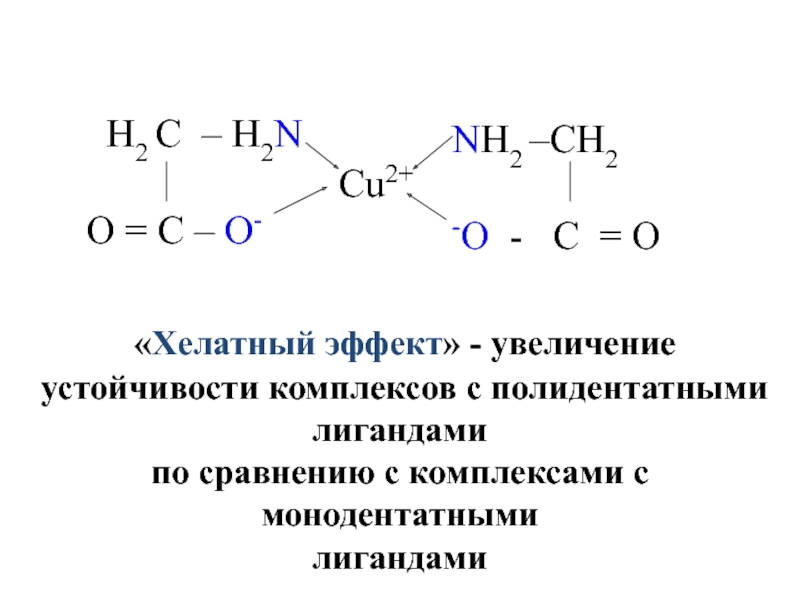
- 28. «Хелатный эффект» - увеличение
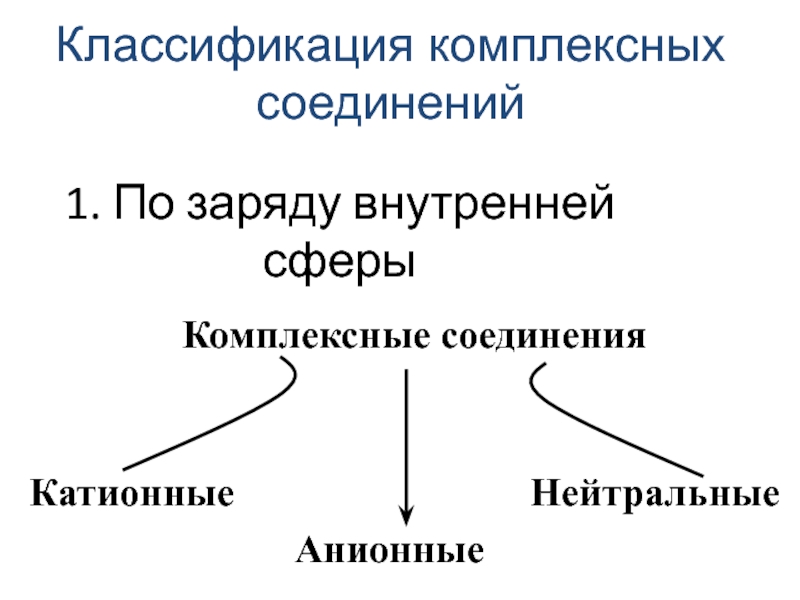
- 29. 1. По заряду внутренней сферы Классификация комплексных соединений
- 30. [Cu(NH3)4]SO4 Na3[Co(NO2)6]
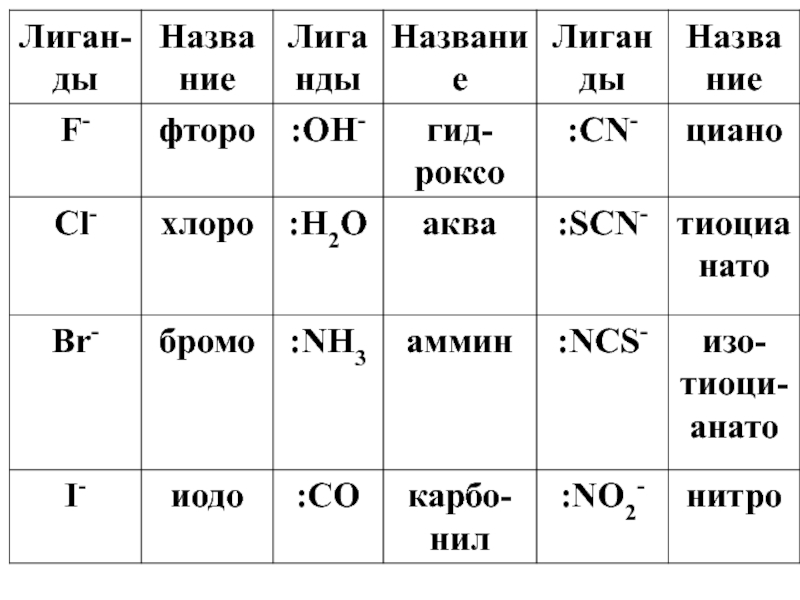
- 31. 2. По природе лиганда: Гидроксокомплексы ( ОН-)
- 32. Классификация КС по природе лигандов
- 33. 3. По способности ионизировать: Электролиты [Cu(NH3)4]SO4 Неэлектролиты
- 34. Номенклатура комплексных соединений
- 36. [Cu(NH3)4]SO4 [Cr (NH3)3(H2O)2 Cl]Br2 Бромид хлородиакватриамминхрома (III)
- 37. Природа химической связи в комплексных соединениях
- 38. Метод валентных связей: связь – ковалентная, лиганд
- 39. Zn2+ + 4 NH3 → [Zn(NH3)4]2+
- 40. Zn2+ •• ••
- 41. Zn0:1s22s22p63s23p64s23d104p0 Zn2+:1s22s22p63s23p64s03d104p0
- 43. Для атомов комплексообразователей: E(n−1)d ≈ Ens ≈
- 44. Ni+II [Ni(CN)4]2– уст., диамагн., квадрат КЧ
- 45. Fe+II [FeF6]4– уст., парамагн., октаэдр КЧ
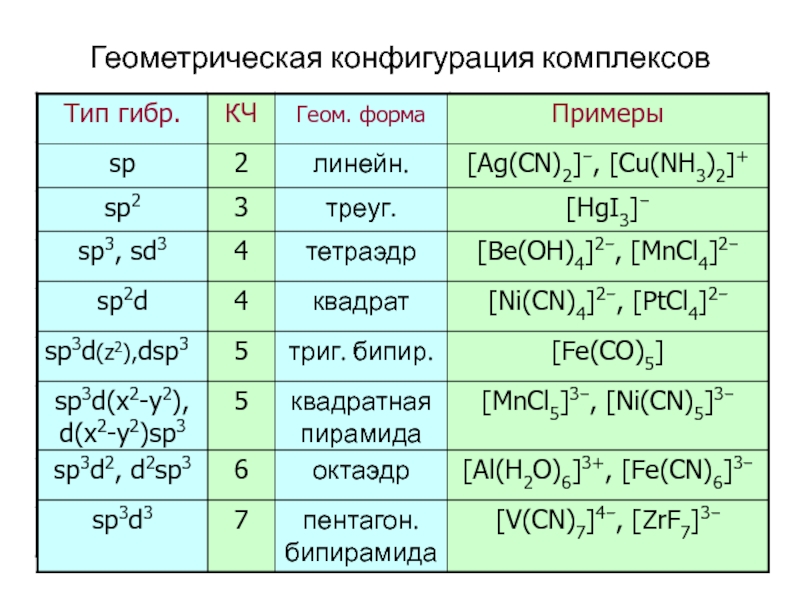
- 46. Геометрическая конфигурация комплексов
- 47. Спектрохимический ряд СO > CN– >
- 48. ТЕОРИЯ КРИСТАЛЛИЧЕСКОГО ПОЛЯ Лиганды – точечные заряды
- 49. В случае [ML6]ν±,0 : октаэдрическое поле лигандов
- 50. ТКП-октаэдрическое поле Сильное поле лигандов Δmax: переход
- 51. Сильное поле
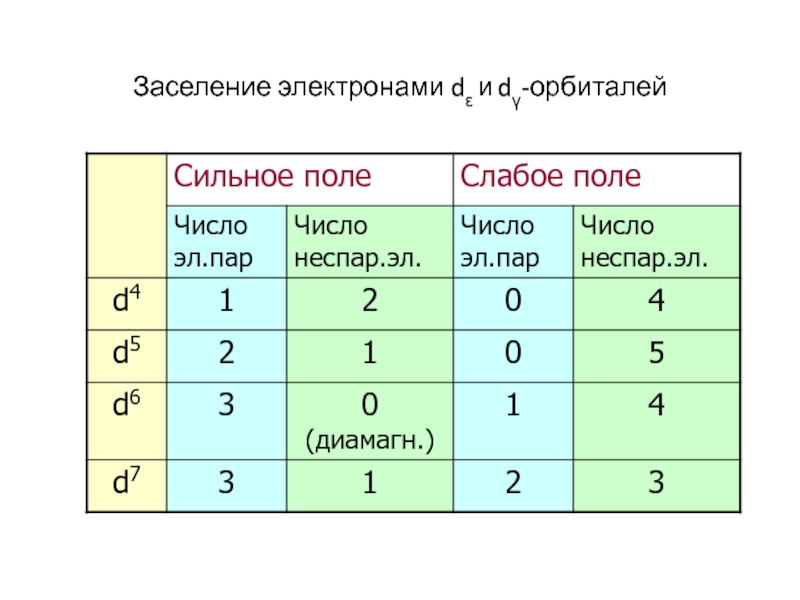
- 52. Заселение электронами dε и dγ-орбиталей
- 53. Лиганды сильного и слабого поля Спектрохимический ряд
- 54. [Co(H2O)6]2+
- 55. Цветность комплексных соединений При облучении образца в-ва
- 56. Цветность комплексов Комплексы Sc(III), Cu(I), Zn(II), Cd(II)
- 59. Изомерия комплексных соединений Изомерия – явление существования
- 60. Изомерия лигандов Связевая —NO2– и
- 61. Изомерия внутренней сферы: геометрическая Геометрическая изомерия вызвана
- 62. Геометрическая изомерия Плоскоквадратные комплексы при наличии двух
- 63. Геометрическая изомерия [ML′5L′′]: изомеров нет цис- и транс-изомеры дигидроксотетраамминкобальта(II)
- 64. Изомерия внутр. сферы: оптическая Оптическая (зеркальная)
- 65. Оптическая изомерия Оптические изомеры способны вращать плоскость
- 66. Междусферная изомерия: 1) сольватная (гидратная); 2) ионная
- 67. Междусферная изомерия Ионные (ионизационные) изомеры [Pt(NH3)4Cl2]Br2
- 68. Диссоциация комплексных соединений
- 69. K4 [Fe(CN)6]
- 70. K4 [Fe(CN)6]→ 4 K+ + [Fe(CN)6 ] 4- первичная диссоциация
- 71. [Fe(CN)6 ] 4- ↔ Fe2+ +6(CN)- вторичная
- 72. [Ni(NH3)6]2+ Кн = 2·10-9 (непрочный комплекс) Куст.=1/ Кн
- 73. Кн и Ку (β)относятся только к комплексному иону! Не забывайте !
- 74. Правило циклов Чугаева Наибольшей устойчивостью обладают пяти-
- 75. Реакция Чугаева Ni2+ + 2 NH3·H2O
- 76. Разрушение комплексных соединений Труднорастворимый осадок Слабый электролит
- 77. [Ag (NH3)2]+↔ Ag+ + 2 NH3 Кн = 9,3 ·10-8
- 78. [Ag (NH3)2]++ KI =AgI↓+
- 79. [Ag (NH3)2]+↔ Ag+ + 2 NH3
- 80. Использование реакций комплексообразования в фармацевтическом анализе: Для
- 81. Для маскировки мешающих ионов. Например, при обнаружении
- 82. Для изменения окислительно-восстановительных свойств ионов. Например,
- 83. Биологическая роль комплексных соединений
- 84. Порфирин:
- 85. Простейший порфирин — порфин Порфирины — природные
- 86. Активный центр миоглобина (кислород-связывающий белок скелетных мышц и мышцы сердца)– макроциклическое соединение – гем:
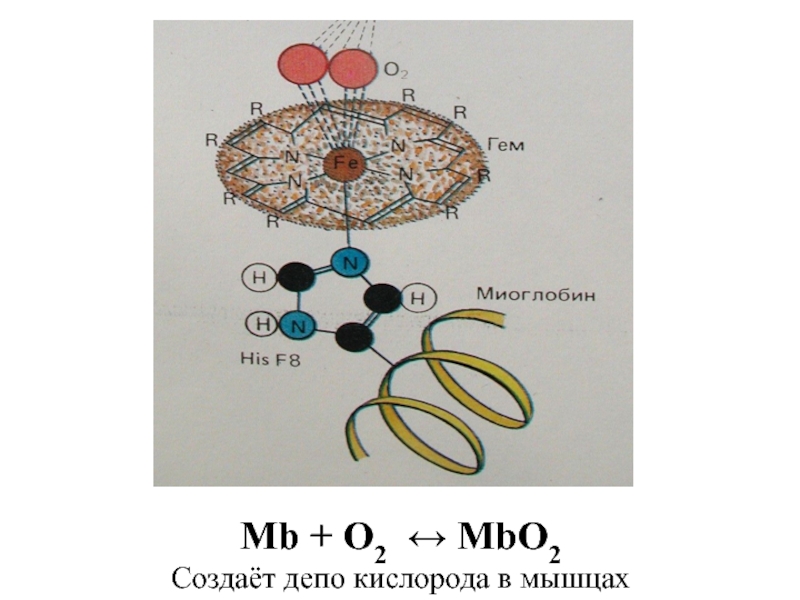
- 87. Mb + O2 ↔ MbO2 Создаёт депо кислорода в мышцах
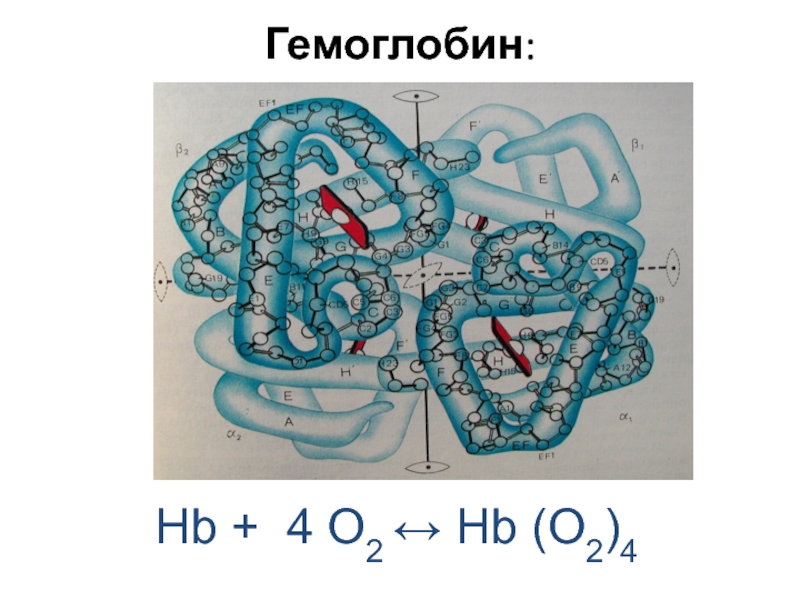
- 88. Гемоглобин: Hb + 4 O2 ↔ Hb (O2)4
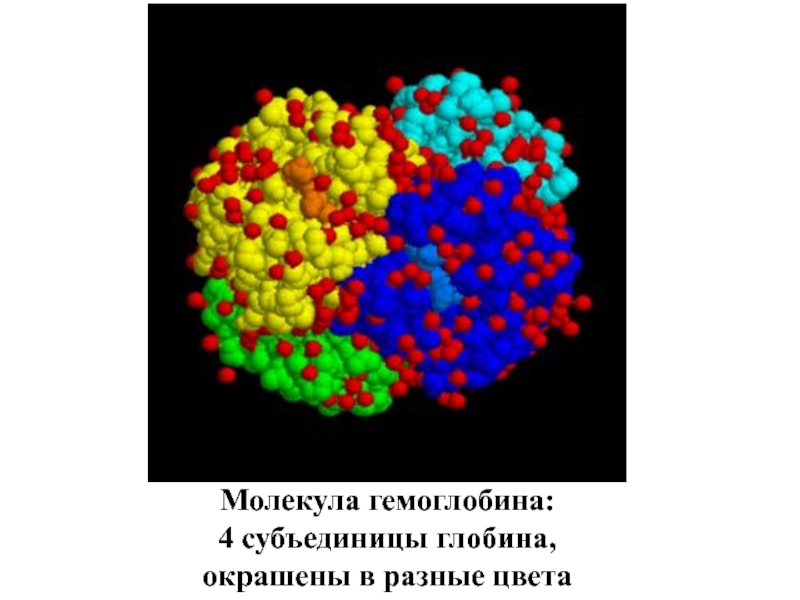
- 89. Молекула гемоглобина: 4 субъединицы глобина, окрашены в разные цвета
- 90. Гемоглоби́н (от др.-греч. αἷμα — кровь и
- 91. Зеленый пигмент растений–хлорофилл (от греч. χλωρός, «зелёный»
- 92. Применение комплексных соединений в медицине
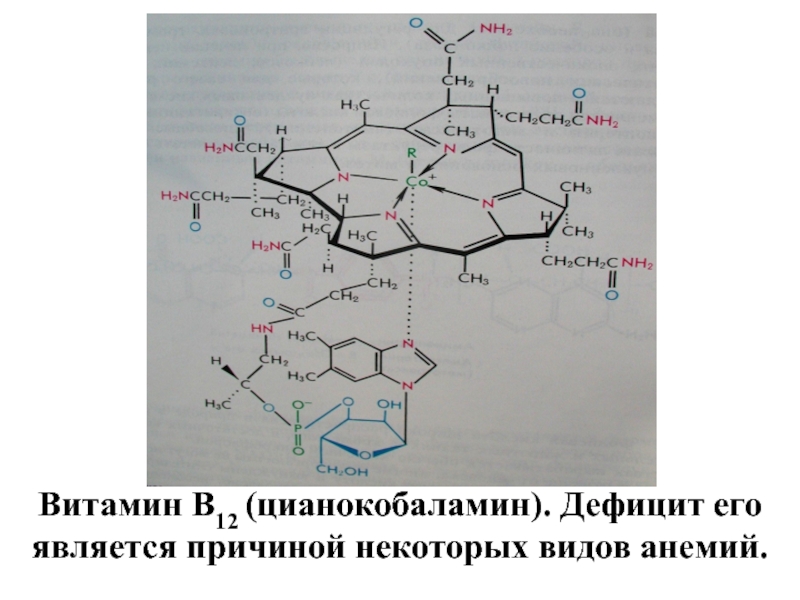
- 93. Витамин В12 (цианокобаламин). Дефицит его является причиной некоторых видов анемий.
- 94. Унитиол - антидот при отравлениях соединениями мышьяка,
- 95. Комплексоны (ЭДТА, Na2ЭДТА, Na2CaЭДТА): тетацин -OOCH2C
- 96. Противоопухолевый препарат: цис-изомер дихлородиамминплатины ЦИСПЛАТИН — цитотоксический
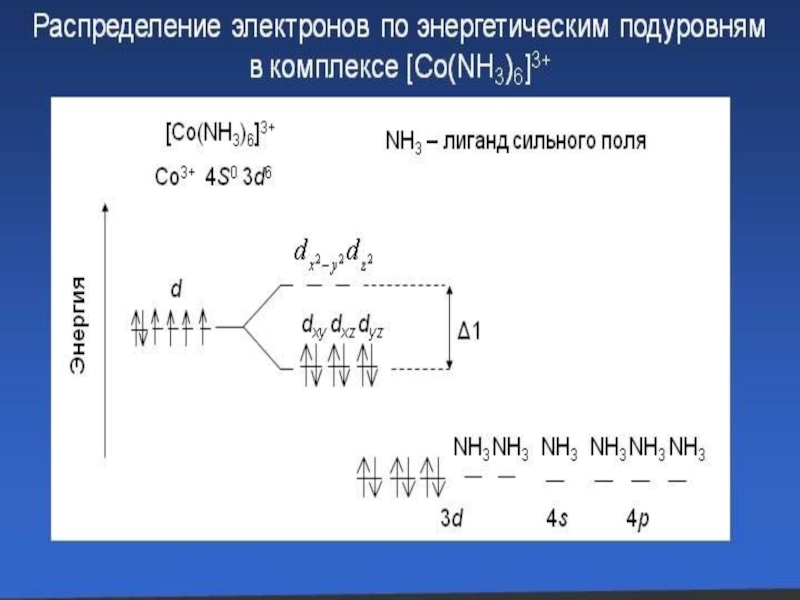
Слайд 2Основные вопросы темы:
Современные представления о строении и свойствах комплексных соединений.
Биологическая роль
Слайд 4КС– это такие соединения, в узлах кристаллической решётки которых находятся комплексы
Чугаев Л.А.
Комплексные соединения (КС) – это продукт
сочетания простых соединений, способных
к самостоятельному существованию
Слайд 5Примеры реакций комплексообразования
HgI2 + 2KI = K2[HgI4]
KF + BF3 = K[BF4]
Al(OH)3+
AgCl + 2NH3=[Ag(NH3)2]Cl
Слайд 8Составные части комплексных соединений
[Co+3 (NH3) 6]3+Cl3
Центральный
атом
Лиганды
Ион внешней
сферы
Внутреняя сфера
Внешняя
сфера
Координационное
число
Слайд 9Характеристика центрального атома
Комплексообразующая способность
элементов
f > d > p >
Инертные газы также могут выступать в качестве комплексообразователя:
Cs [XeF7]
Слайд 10Важнейшие характеристики центрального атома :
Степень окисления
Координационное число
Ионный потенциал
Слайд 11Степень окисления
Положительная
K3[Fe3+(CN)6], K4[Fe2+(CN)6],
Cs[Xe+6F7],
Отрицательная
[N -3H4 ] Cl
Нулевая
[Cl2(H2O)4]
Слайд 12Координационное число (КЧ)
Это число атомов или групп атомов, непосредственно связанных
Слайд 13
- от размеров центрального атома и лигандов.
Лат. liganda -то,
КЧ зависит:
Слайд 17чаще всего кч устойчивого комплекса в два раза больше степени окисления
КЧ = 2Z
Эмпирическое правило:
Слайд 18Al(OH)3 + NaOH= Na[Al(OH)4]
Al(OH)3 +3 NaOH= Na3[Al(OH)6]
- концентрации исходных компонентов
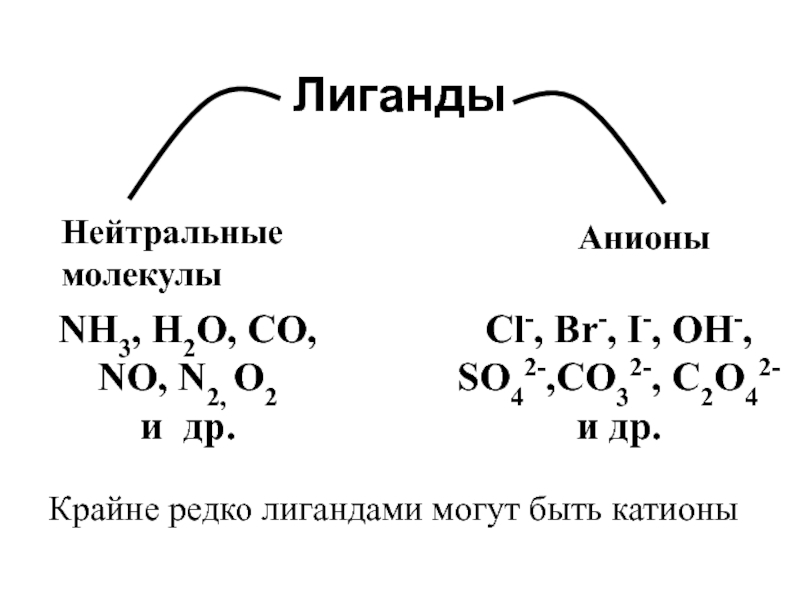
Слайд 21Лиганды
NH3, H2O, CO,
NO, N2, O2
и др.
Cl-, Br-, I-, OH-,
SO42-,CO32-, C2O42-
и др.
Крайне редко лигандами могут быть катионы
Слайд 22-монодентатные лиганды, содержат 1 донорный атом (H2 O, NH3, OH-, Cl-,
Число донорных атомов в лиганде характеризует его координационную ёмкость – дентатность
Лат. dentalus – имеющий зубы
Слайд 23-бидентатные лиганды, содержат 2 донорных атома и занимают два координационных места:
О
O O - S O O -
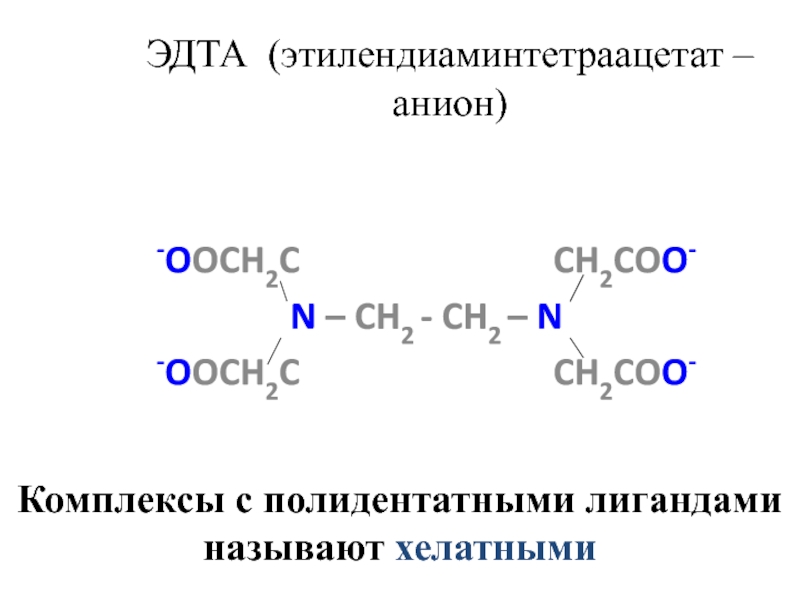
Слайд 26ЭДТА (этилендиаминтетраацетат –анион)
-OOCH2C
N – CH2 - CH2 – N
-OOCH2C CH2COO-
Комплексы с полидентатными лигандами
называют хелатными
Слайд 28
«Хелатный эффект» - увеличение
устойчивости комплексов с полидентатными лигандами
по
лигандами
Слайд 312. По природе лиганда:
Гидроксокомплексы ( ОН-)
Аквакомплексы (Н2О)
Аммиакатные комплексы (NH3)
Ацидокомплексы ( CN-
Карбонильные (СО)
И др.
Слайд 333. По способности ионизировать:
Электролиты [Cu(NH3)4]SO4
Неэлектролиты [Pt(NH3)2Cl2]
4. По свойствам электролита:
Кислоты Н[AuCl4]
Основания [Cu(Н2О)4](ОН)2
Соли
Слайд 36[Cu(NH3)4]SO4
[Cr (NH3)3(H2O)2 Cl]Br2
Бромид хлородиакватриамминхрома (III)
Na3[Co(NO2)6]
ГГексанитрокобальтат (III) натрия
[Pt(NH3)2Cl2]
Сульфат тетраамминмеди (II)
Гексанитрокобальтат
Дихлородиамминплатина
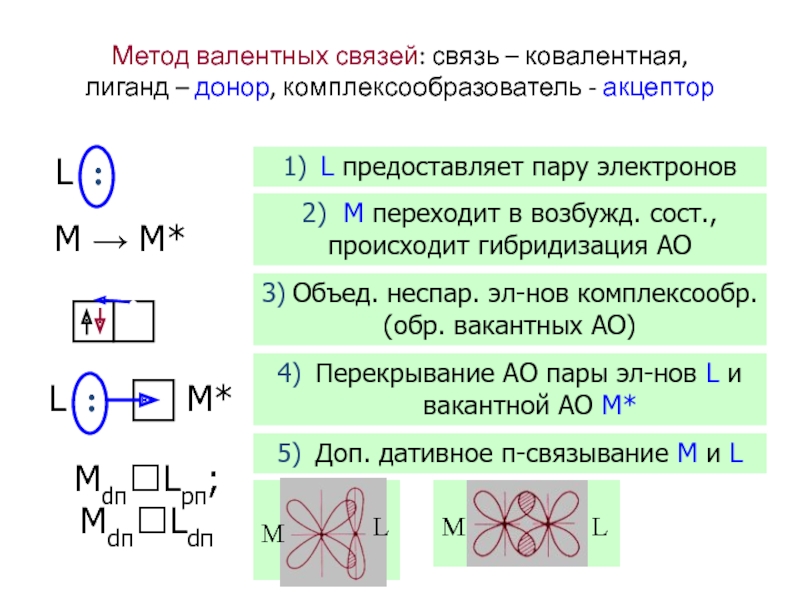
Слайд 38Метод валентных связей: связь – ковалентная, лиганд – донор, комплексообразователь -
L :
M → M*
L :
Mdπ?Lpπ; Mdπ?Ldπ
1) L предоставляет пару электронов
2) M переходит в возбужд. сост., происходит гибридизация АО
3) Объед. неспар. эл-нов комплексообр. (обр. вакантных АО)
4) Перекрывание АО пары эл-нов L и вакантной АО M*
5) Доп. дативное π-связывание M и L
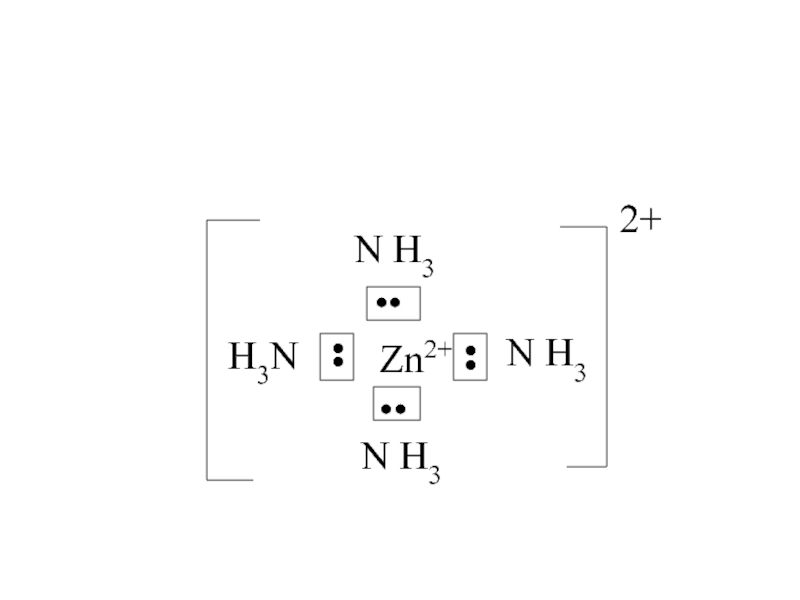
Слайд 41Zn0:1s22s22p63s23p64s23d104p0
Zn2+:1s22s22p63s23p64s03d104p0
3d
4s
4p
Zn2+:
••
••
••
••
[ Zn (NH3)4]2+
sp3 гибридизация АО
тетраэдрическая структура
Слайд 43Для атомов комплексообразователей: E(n−1)d ≈ Ens ≈ Enp ≈ End
Пример:
Атом Ni0 парамагнитен
Ni0
Ni*
[Ni(CO)4] уст., диамагнитный, тетраэдрич.
Ni+II
[NiBr4]2– неуст., парамагн., тетраэдрич.
КЧ 4
КЧ 4
Слайд 44Ni+II
[Ni(CN)4]2– уст., диамагн., квадрат
КЧ 4
[Ni(CN)5]3– уст., диамагн., квадратная пирамида
КЧ 5
[Ni(H2O)6]2+, [Ni(NO2)6]4–
КЧ 6
Ni+II
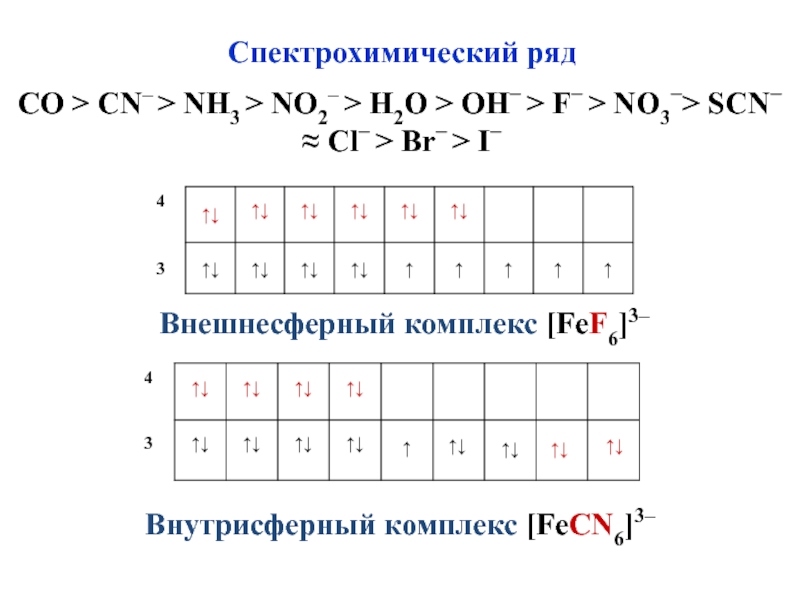
Слайд 47Спектрохимический ряд
СO > CN– > NH3 > NO2– > H2O >
≈ Cl− > Br− > I−
Внешнесферный комплекс [FeF6]3–
Внутрисферный комплекс [FeCN6]3–
Слайд 48ТЕОРИЯ КРИСТАЛЛИЧЕСКОГО ПОЛЯ
Лиганды – точечные заряды (кристаллическое поле).
Связь между лиогандами и
Вырожденный d-подуровень центрального атома под действием поля лигандов расщепляется в соответствии с симметрией окружения.
Слайд 49В случае [ML6]ν±,0 : октаэдрическое поле лигандов
Поле слабо влияет (энергия падает)
Поле сильно влияет (энергия растет) в случае АО d(z2) и d(x2–y2), располож. вдоль осей координат (ближе всего к лигандам)
Eо
|Eγ–Eо| = 3/5 Δ ; |Eε–Eо| = 2/5 Δ
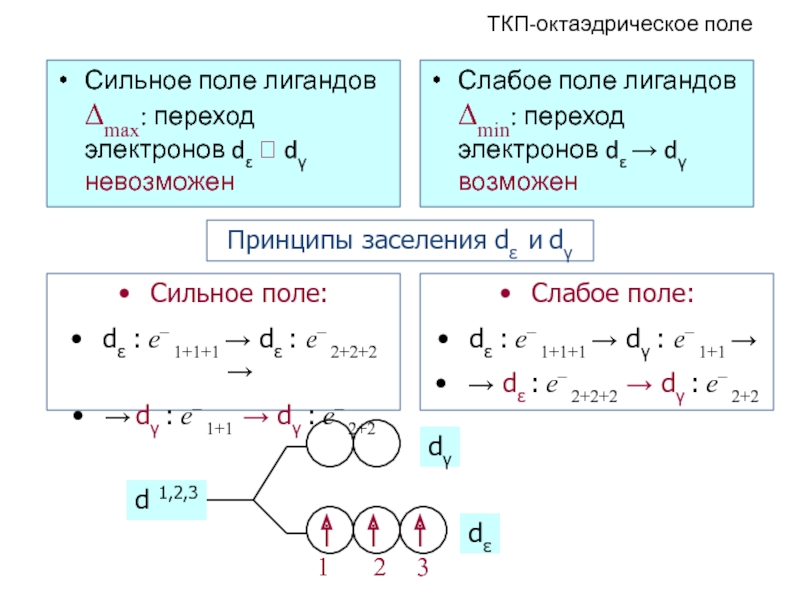
Слайд 50ТКП-октаэдрическое поле
Сильное поле лигандов Δmax: переход электронов dε ⭲ dγ невозможен
Слабое
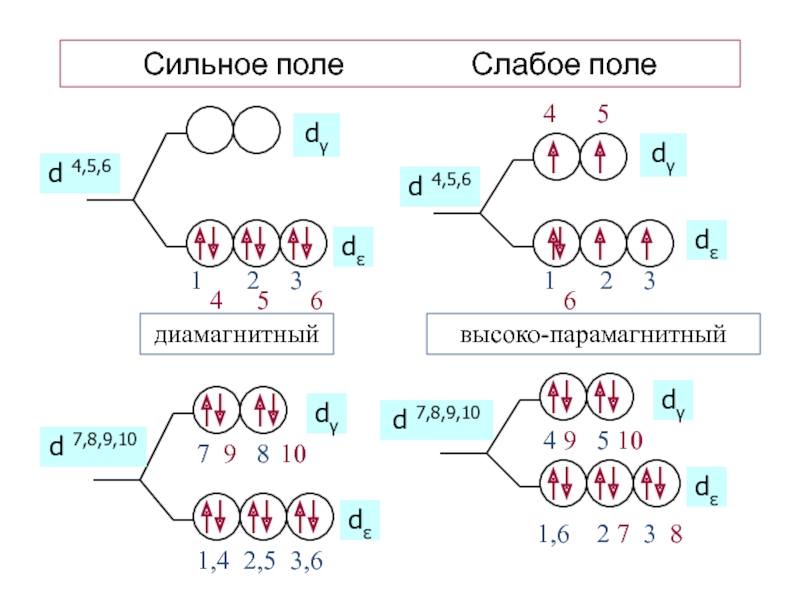
Принципы заселения dε и dγ
Сильное поле:
dε : e– 1+1+1 → dε : e– 2+2+2 →
→ dγ : e– 1+1 → dγ : e– 2+2
Слабое поле:
dε : e– 1+1+1 → dγ : e– 1+1 →
→ dε : e– 2+2+2 → dγ : e– 2+2
d 1,2,3
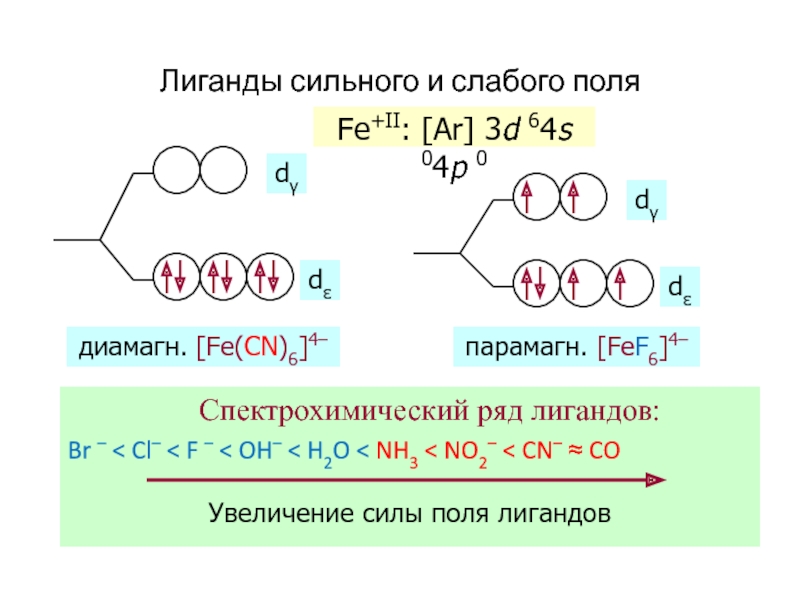
Слайд 53Лиганды сильного и слабого поля
Спектрохимический ряд лигандов:
Br – < Cl–
Fe+II: [Ar] 3d 64s 04p 0
диамагн. [Fe(CN)6]4–
парамагн. [FeF6]4–
Слайд 54
[Co(H2O)6]2+ розовый
[Co(CH3COO)2] ярко-розовый
[Co(NO2)6]4-
[Co(NH3)6]2+ буро-розовый
Усиление поля лигандов
Влияние поля лигандов на окраску комплексов
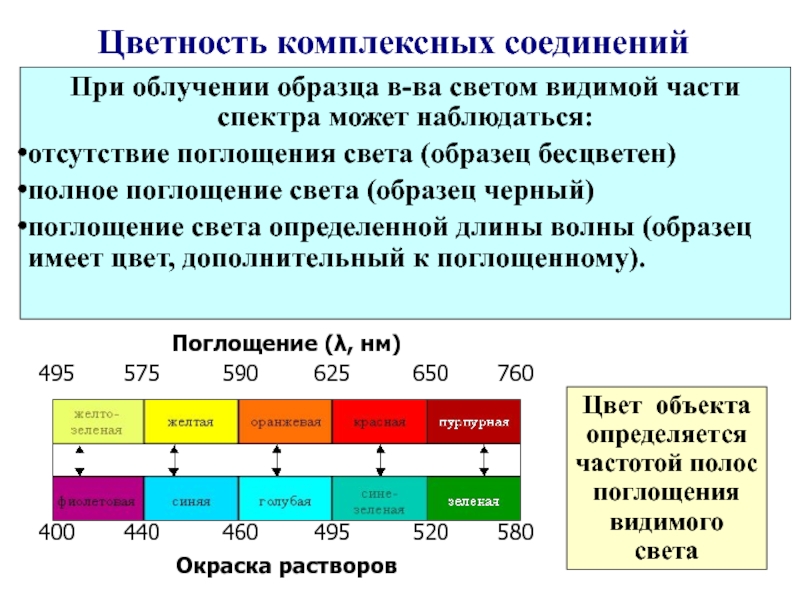
Слайд 55Цветность комплексных соединений
При облучении образца в-ва светом видимой части спектра может
отсутствие поглощения света (образец бесцветен)
полное поглощение света (образец черный)
поглощение света определенной длины волны (образец имеет цвет, дополнительный к поглощенному).
Цвет объекта определяется частотой полос поглощения видимого света
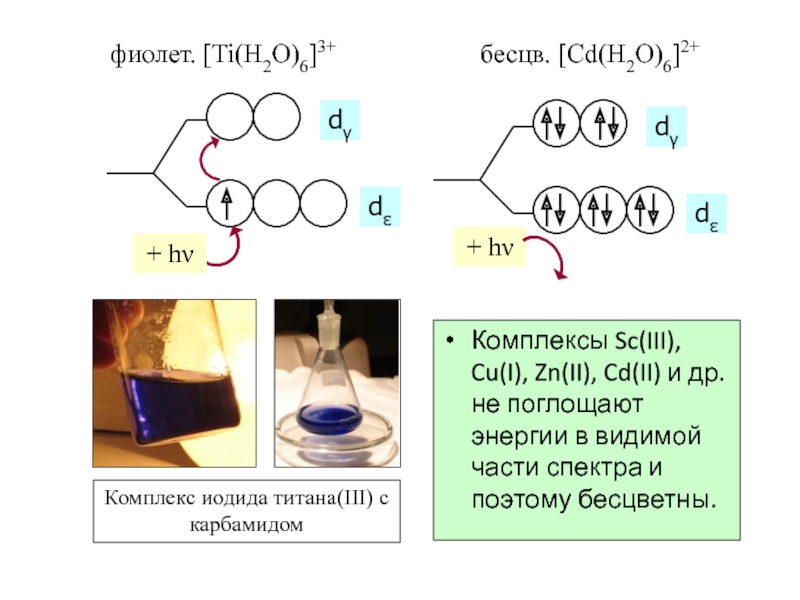
Слайд 56Цветность комплексов
Комплексы Sc(III), Cu(I), Zn(II), Cd(II) и др. не поглощают энергии
фиолет. [Ti(H2O)6]3+
бесцв. [Cd(H2O)6]2+
Слайд 59Изомерия комплексных соединений
Изомерия – явление существования соединений, одинаковых по составу и
В случае комплексных соединений изомерия обусловлена:
различием в строении и координации лигандов
различием в строении внутренней координационной сферы
различным распределением частиц между внутренней и внешней сферой
Слайд 60Изомерия лигандов
Связевая
—NO2– и —ONO–
нитро-
[Co(NH3)5NO2]2+ (желто-коричн.р-р)
[Co(NH3)5ONO]2+ (розов.р-р)
—NCS– и —SCN–
тиоцианато-N тиоцианато-S
[Cr(H2O)5(NCS)]2+
[Cr(H2O)5(SCN)]2+
Изомерия лигандов
Лиганды сложного строения (напр., аминокислоты) образуют изомеры, координация которых ведет к получению комплексов с разными свойствами.
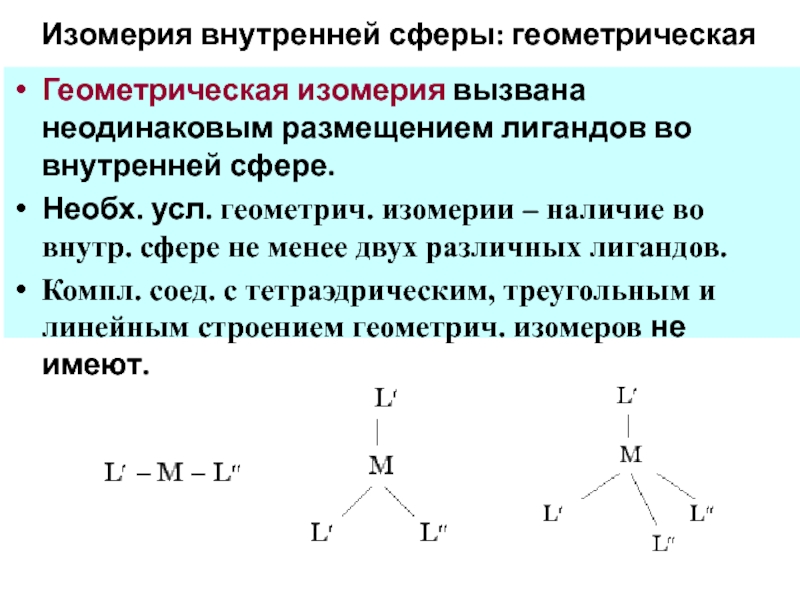
Слайд 61Изомерия внутренней сферы: геометрическая
Геометрическая изомерия вызвана неодинаковым размещением лигандов во внутренней
Необх. усл. геометрич. изомерии – наличие во внутр. сфере не менее двух различных лигандов.
Компл. соед. с тетраэдрическим, треугольным и линейным строением геометрич. изомеров не имеют.
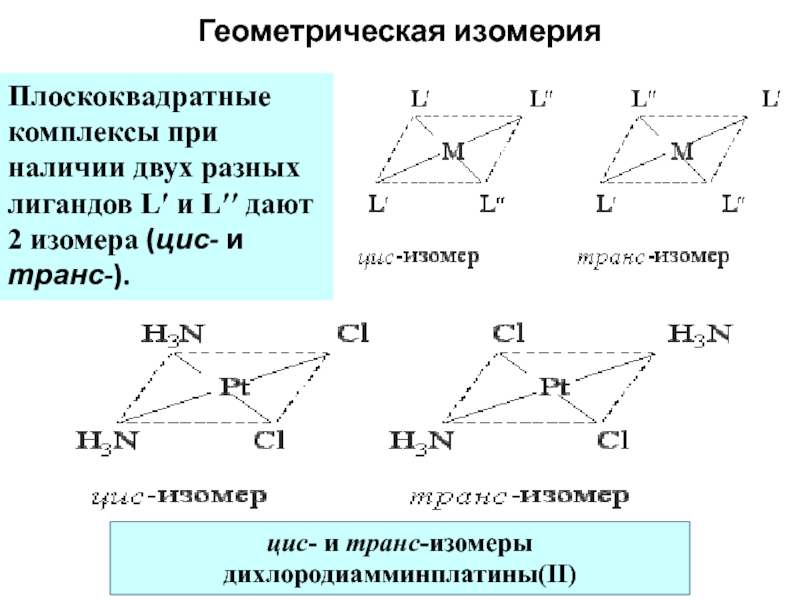
Слайд 62Геометрическая изомерия
Плоскоквадратные комплексы при наличии двух разных лигандов L′ и L′′
Слайд 63Геометрическая изомерия
[ML′5L′′]: изомеров нет
цис- и транс-изомеры дигидроксотетраамминкобальта(II)
Слайд 64Изомерия внутр. сферы: оптическая
Оптическая (зеркальная) изомерия: способность комплексов существовать в
Триоксалатокобальтат(III)-
-ион [Co(С2O4)3]3–
Слайд 65Оптическая изомерия
Оптические изомеры способны вращать плоскость поляризации светового луча (влево, L-изомер,
Световой луч (а) пропускают через поляризатор, и он становится плоскополяризованным (б).
После пропускания через р-ры оптич. изомеров (в, г).
Угол вращения плоскости поляризации α (определяется анализатором).
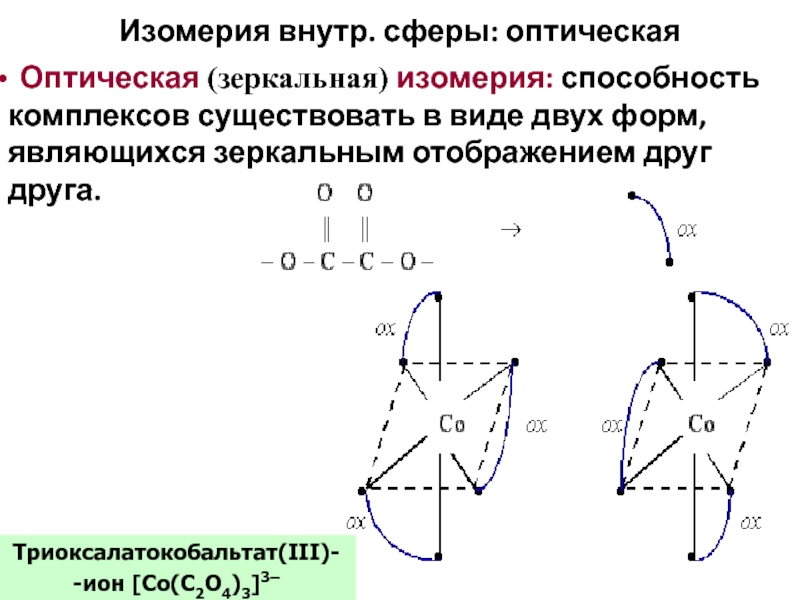
Слайд 66Междусферная изомерия:
1) сольватная (гидратная); 2) ионная изомерия
[Co(en)2Cl2]Cl · H2O
[Co(H2O)(en)2Cl]Cl2
[Co(NH3)5I]SO4
[Co(NH3)5SO4]I
1 Cl–;
2 Cl– (2 AgCl↓)
SO42– (BaSO4↓)
I– (AgI↓)
Слайд 67Междусферная изомерия
Ионные (ионизационные) изомеры
[Pt(NH3)4Cl2]Br2 и [Pt(NH3)4Br2]Cl2
[Pt(NH3)4SO4](OH)2 и [Pt(NH3)4(OH)2]SO4
Координационные изомеры
[Cr(NH3)4(NCS)2] [Cr(NH3)2(NCS)4]
[Cr(NH3)6] [Cr(NCS)6]
Слайд 71[Fe(CN)6 ] 4- ↔ Fe2+ +6(CN)-
вторичная диссоциация
Константа нестойкости (Кн):
Kн = 1ּ10-31
(очень
Слайд 74Правило циклов Чугаева
Наибольшей устойчивостью обладают пяти- и шестичленные металлоциклы. Соединения с
Слайд 75Реакция Чугаева
Ni2+ + 2 NH3·H2O + 2H2L =
= [Ni(HL)2](т)
бис(диметилглиоксимато)никель(II)
Слайд 76Разрушение комплексных соединений
Труднорастворимый осадок
Слабый электролит
Окислить или восстановить
Выделить в виде газа
Связать в
Слайд 78
[Ag (NH3)2]++ KI =AgI↓+ NH3 +K+
Кs(AgI) = 1,5·10 -16
[Ag (NH3)2]++2CN- =
Кн = 8·10-22
Слайд 80Использование реакций комплексообразования в фармацевтическом анализе:
Для обнаружения ионов. Например, ионы кобальта
H2N – C – C–NH2 ↔ HN = C – C = NH + Co2+ ↔ HN = C – C = NH↓ + H+
|| || | | | |
S S HS SH S S
Co
Для разделения ионов. Так, если надо ионы Cu2+ и Мg2+ отделить друг от друга, то в раствор, содержащий их, добавляют избыток NН4ОН. При этом ионы меди (II) переходят в раствор в виде тетраамминмеди (II), а катионы Мg2+ осаждаются в гидроксид магния Мg(ОН)2.
Слайд 81Для маскировки мешающих ионов. Например, при обнаружении ионов Ni2+ в присутствии
Fe3+ + 6 F- ↔ [FeF6]3-
После маскировки Fе3+ проводят аналитические реакции на ионы никеля (II).
Для растворения осадков. Так, при добавлении к хлориду серебра концентрированной хлороводородной кислоты осадок АgСl растворяется :
AgCl + 2 HCl → H2[ AgCl3 ]
Слайд 82
Для изменения окислительно-восстановительных свойств ионов. Например, молибден (VI) в виде МоО3⋅Н2О
[P( Mo2O7)6]7- по отношению к нему является окислителем.
В экстракционном концентрировании и разделении веществ получают нейтральные комплексы, способные переходить из воды в органический растворитель, не смешивающийся с ней.
Для количественного определения различных химических соединений в том числе и лекарственных веществ, в состав которых входят анионы, способные образовывать с титрантом комплексные соединения. Для этой цели применяют такие методы, как комплексонометрия, куприметрия и другие.
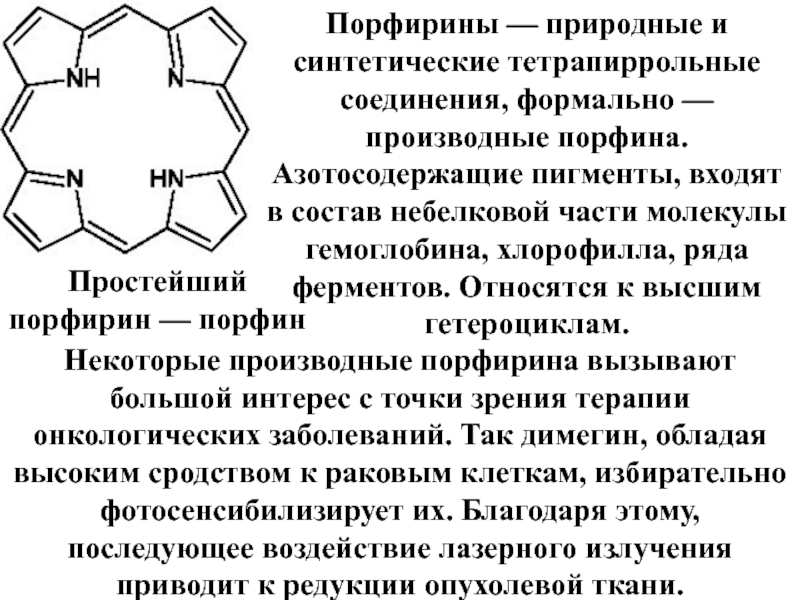
Слайд 85Простейший порфирин — порфин
Порфирины — природные и синтетические тетрапиррольные соединения, формально
Некоторые производные порфирина вызывают большой интерес с точки зрения терапии онкологических заболеваний. Так димегин, обладая высоким сродством к раковым клеткам, избирательно фотосенсибилизирует их. Благодаря этому, последующее воздействие лазерного излучения приводит к редукции опухолевой ткани.
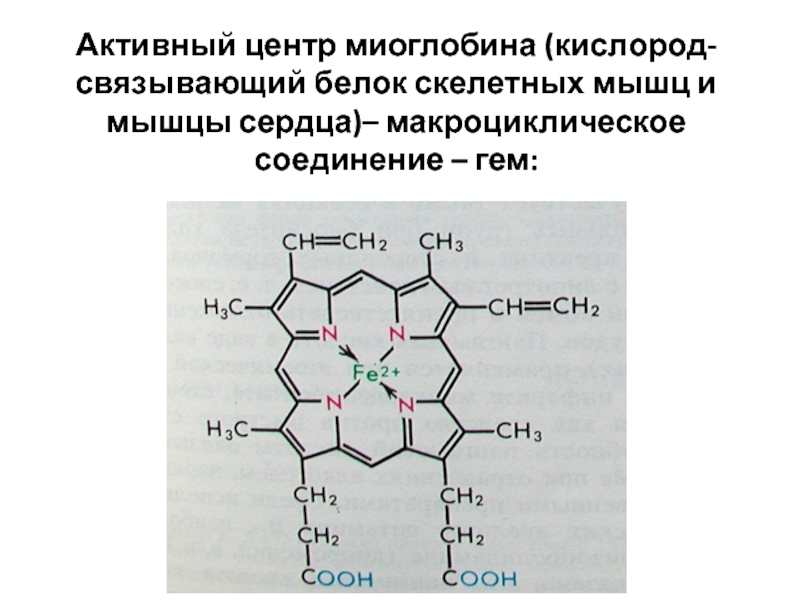
Слайд 86 Активный центр миоглобина (кислород-связывающий белок скелетных мышц и мышцы сердца)– макроциклическое
Слайд 90Гемоглоби́н (от др.-греч. αἷμα — кровь и лат. globus — шар)
Главная функция гемоглобина заключается в трех этапах, определяющих три его свойства. 1-ый этап - присоединение O2 к гемоглобину. 2-ой - образование сложных взаимоотношений между гемом и O2, а именно превращение O2 в синглетный кислород. Данный этап является этапом трансформации O2 в его реакционно-способную форму, необходимую для дальнейшего взаимодействия с клетками и является главной функцией гемоглобина. 3-ий этап - отдача синглетного кислорода в ткани. У человека в капиллярах лёгких в условиях избытка кислорода последний соединяется с гемоглобином. Током крови эритроциты, содержащие молекулы гемоглобина со связанным кислородом, доставляются к органам и тканям, где O2 мало; здесь необходимый для протекания окислительных процессов кислород освобождается из связи с гемоглобином.
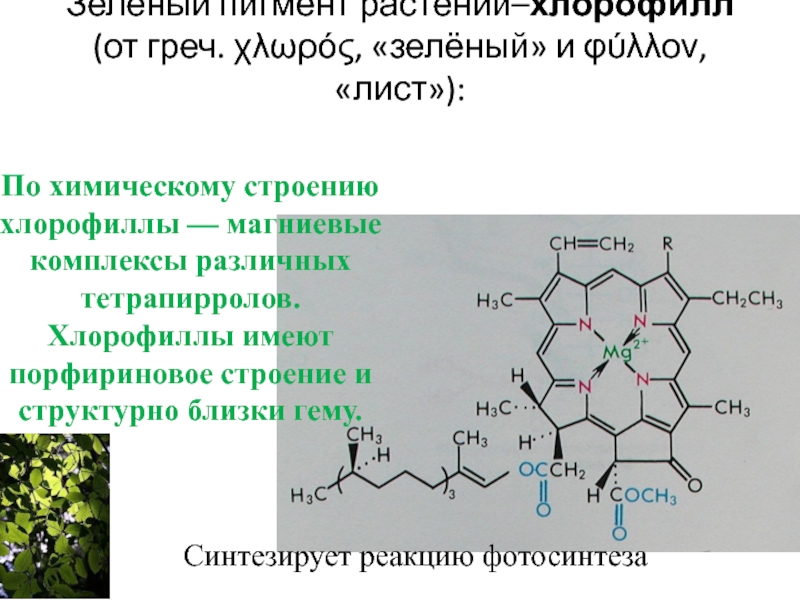
Слайд 91Зеленый пигмент растений–хлорофилл (от греч. χλωρός, «зелёный» и φύλλον, «лист»):
Синтезирует реакцию
По химическому строению хлорофиллы — магниевые комплексы различных тетрапирролов. Хлорофиллы имеют порфириновое строение и структурно близки гему.
Слайд 94Унитиол - антидот при отравлениях соединениями мышьяка, ртути и солями тяжелых
Меркаптидная связь
Слайд 95Комплексоны (ЭДТА, Na2ЭДТА, Na2CaЭДТА): тетацин
-OOCH2C
N – CH2 - CH2 – N
-OOCH2C CH2COO-
Сa2+
Hg2+
Hg2+ + ЭДТА · Ca2+→ Ca2+ + ЭДТА · Hg2+




![Примеры реакций комплексообразованияHgI2 + 2KI = K2[HgI4]KF + BF3 = K[BF4]Al(OH)3+ NaOH = Na[Al(OH)4]AgCl + 2NH3=[Ag(NH3)2]Cl](/img/tmb/1/37010/af90afcf751fa54f943948196c2caa17-800x.jpg)
![Кристаллогидраты: CuSO4•5H2O [Cu(H2O)4]SO4 ∙ Н2О Н -](/img/tmb/1/37010/e7704555c9e02e7dddac5d9ee4dd2d07-800x.jpg)

![Составные части комплексных соединений [Co+3 (NH3) 6]3+Cl3ЦентральныйатомЛигандыИон внешнейсферыВнутреняя сфера Внешняя сфера Координационное число](/img/tmb/1/37010/96dac73bed54273a39e314764dbe3cd5-800x.jpg)


![Степень окисленияПоложительнаяK3[Fe3+(CN)6], K4[Fe2+(CN)6], Cs[Xe+6F7], К[BF4]Отрицательная [N -3H4 ] ClНулевая [Cl2(H2O)4]](/img/tmb/1/37010/6cc7d9c130c6d990d865897f15ae2941-800x.jpg)


![Na[BF4] Na3[AlF6]rB3+ = 0,02 нмrAl3+ = 0,057 нм](/img/tmb/1/37010/ef9fe61e7b74319b6b24278a0eb7afc7-800x.jpg)
![Na3[AlF6] Na [AlCl4] Al3+rF_ = 0,133 нмrCl- = 0,181 нм](/img/tmb/1/37010/69664228faf223807bbdc2c739f5a5f8-800x.jpg)


![Al(OH)3 + NaOH= Na[Al(OH)4] Al(OH)3 +3 NaOH= Na3[Al(OH)6]- концентрации исходных компонентов :](/img/tmb/1/37010/58a55f6c5d7a620a8dfb7c161718e412-800x.jpg)




![[Cu(NH3)4]SO4 Na3[Co(NO2)6] [Co(NH3)4Cl2]Cl [Pt(NH3)2Cl2] [Fe(CO)5]](/img/tmb/1/37010/a50f05f347b686e263e10a610a38a594-800x.jpg)


![3. По способности ионизировать:Электролиты [Cu(NH3)4]SO4Неэлектролиты [Pt(NH3)2Cl2]4. По свойствам электролита:Кислоты Н[AuCl4]Основания [Cu(Н2О)4](ОН)2Соли [Ag(NH3)2]Cl](/img/tmb/1/37010/dd769bf45c9b317441b5d8627174a5e7-800x.jpg)

![[Cu(NH3)4]SO4[Cr (NH3)3(H2O)2 Cl]Br2Бромид хлородиакватриамминхрома (III)Na3[Co(NO2)6] ГГексанитрокобальтат (III) натрия[Pt(NH3)2Cl2] Сульфат тетраамминмеди (II)Гексанитрокобальтат (Ш) натрияДихлородиамминплатина](/img/tmb/1/37010/37e56d8afa5d23146e1df84d8a462263-800x.jpg)

![Zn2+ + 4 NH3 → [Zn(NH3)4]2+](/img/tmb/1/37010/1e8c5531cf653a4b840662ba2604225a-800x.jpg)
![Zn0:1s22s22p63s23p64s23d104p0 Zn2+:1s22s22p63s23p64s03d104p03d4s4pZn2+:••••••••[ Zn (NH3)4]2+sp3 гибридизация АОтетраэдрическая структура](/img/tmb/1/37010/c0b4da5a19d81444958bb3366ff79f3a-800x.jpg)
![3d4s4pCr3+:••••••••[Cr(H2O)6 ]3+••••d2sp3 гибридизация АОоктаэдрическая структура](/img/tmb/1/37010/39154f5b4fa08add94a31f6e76da883b-800x.jpg)
![Для атомов комплексообразователей: E(n−1)d ≈ Ens ≈ Enp ≈ End Пример: комплексы никеля. Ni0 [Ar]](/img/tmb/1/37010/ce5d7bdb80014c38775ae954f169c966-800x.jpg)
![Ni+II[Ni(CN)4]2– уст., диамагн., квадратКЧ 4[Ni(CN)5]3– уст., диамагн., квадратная пирамидаКЧ 5[Ni(H2O)6]2+, [Ni(NO2)6]4– : уст., парамагн., октаэдрКЧ 6Ni+II](/img/tmb/1/37010/5c8d4ced6a9c929566895e06efa6782a-800x.jpg)
![Fe+II[FeF6]4– уст., парамагн., октаэдрКЧ 6Fe+II[Fe(CN)6]4– уст., диамагн., октаэдрКЧ 6](/img/tmb/1/37010/0ab3ffbfb8fd4fe395b6a698feae8d49-800x.jpg)

![В случае [ML6]ν±,0 : октаэдрическое поле лигандовПоле слабо влияет (энергия падает) в случае АО d(xy),](/img/tmb/1/37010/7beeee892f150355f6276b1601638546-800x.jpg)
![[Co(H2O)6]2+ розовый[Co(CH3COO)2] ярко-розовый [Co(NO2)6]4- оранжевый[Co(NH3)6]2+ буро-розовыйУсиление поля лигандовВлияние](/img/tmb/1/37010/c6efbbd55b047abaad604e4893d529ef-800x.jpg)


![Изомерия лигандовСвязевая —NO2– и —ONO– нитро- нитрито-[Co(NH3)5NO2]2+ (желто-коричн.р-р)[Co(NH3)5ONO]2+ (розов.р-р)—NCS– и —SCN–тиоцианато-N](/img/tmb/1/37010/ec288820defb865a8b9ec6a145d3e7a4-800x.jpg)
![Геометрическая изомерия[ML′5L′′]: изомеров нетцис- и транс-изомеры дигидроксотетраамминкобальта(II)](/img/tmb/1/37010/5864b520e206b34bec9639784208544a-800x.jpg)

![Междусферная изомерия: 1) сольватная (гидратная); 2) ионная изомерия [Co(en)2Cl2]Cl · H2O[Co(H2O)(en)2Cl]Cl2[Co(NH3)5I]SO4[Co(NH3)5SO4]I1 Cl–; H2O (AgCl↓)2 Cl–](/img/tmb/1/37010/1a38329b644a131535eac3016ff02c2a-800x.jpg)
![Междусферная изомерияИонные (ионизационные) изомеры [Pt(NH3)4Cl2]Br2 и [Pt(NH3)4Br2]Cl2[Pt(NH3)4SO4](OH)2 и [Pt(NH3)4(OH)2]SO4 pH >> 7](/img/tmb/1/37010/6026fa3a086420c3bc1d101ebc2cbdc0-800x.jpg)

![K4 [Fe(CN)6]](/img/tmb/1/37010/45a422b74ade3d2f73a39ddb9f237bf1-800x.jpg)
![K4 [Fe(CN)6]→ 4 K+ + [Fe(CN)6 ] 4- первичная диссоциация](/img/tmb/1/37010/55795ad08473470c19a9c1f69f630506-800x.jpg)
![[Fe(CN)6 ] 4- ↔ Fe2+ +6(CN)- вторичная диссоциацияКонстанта нестойкости (Кн):Kн = 1ּ10-31 (очень прочный комплекс)](/img/tmb/1/37010/f0abc4a8e0a2fece353220df0a0380e9-800x.jpg)
![[Ni(NH3)6]2+ Кн = 2·10-9 (непрочный комплекс)Куст.=1/ Кн](/img/tmb/1/37010/0d764a8194730f6408c5bc55009f54f4-800x.jpg)


 + 2NH4+ + 2H2Oбис(диметилглиоксимато)никель(II)](/img/tmb/1/37010/6c5de70baf40343c5f449ec690ab95da-800x.jpg)
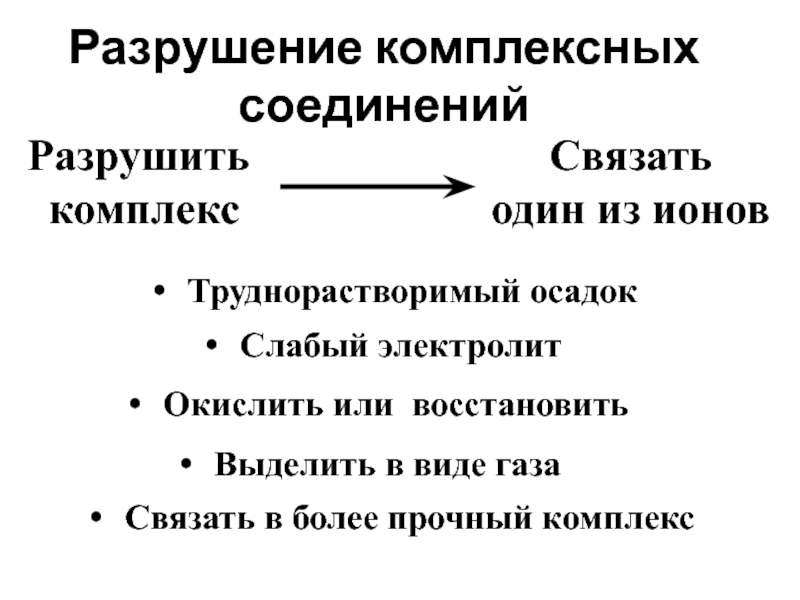
![[Ag (NH3)2]+↔ Ag+ + 2 NH3 Кн = 9,3 ·10-8](/img/tmb/1/37010/961ca707642d368e2f4050eccf21f5f5-800x.jpg)
![[Ag (NH3)2]++ KI =AgI↓+ NH3 +K+ Кs(AgI) = 1,5·10 -16 [Ag (NH3)2]++2CN- =](/img/tmb/1/37010/95765447871a6852a56be05b640bd17b-800x.jpg)
![[Ag (NH3)2]+↔ Ag+ + 2 NH3](/img/tmb/1/37010/1934a4123a6219f7633a7998a141524b-800x.jpg)




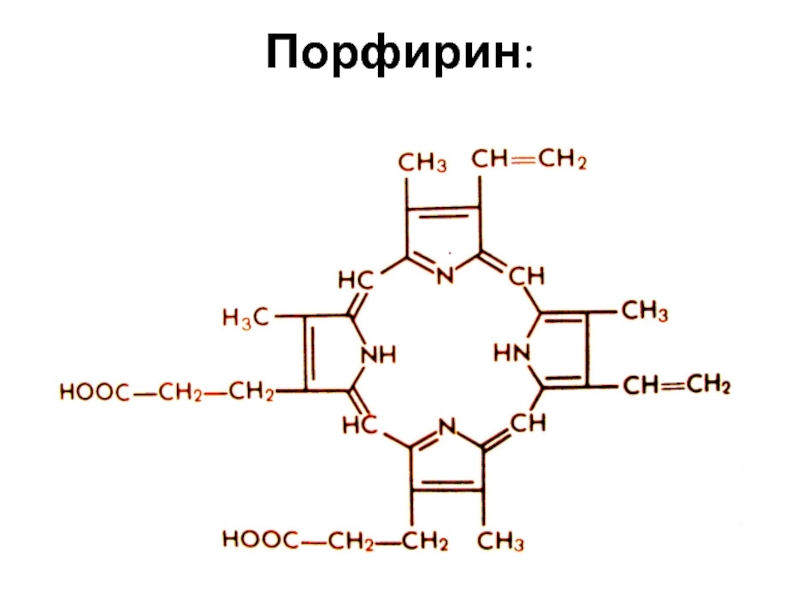




![Противоопухолевый препарат: цис-изомер дихлородиамминплатины ЦИСПЛАТИН — цитотоксический препарат алкилирующего действия [Pt(NH3)2Cl2]](/img/tmb/1/37010/3d776cd8e50537effbe1451d56379952-800x.jpg)






