- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Строение атома презентация
Содержание
- 1. Строение атома
- 2. Разделы лекционного курса
- 3. В V веке до нашей эры Левкипп
- 4. Изучая атмосферу и движение воздуха, Дальтон пришел
- 5. М. Фарадей установил, что ток в растворе
- 6. Испускаемый атомами водорода свет, пройдя через призму,
- 7. Опыты Рентгена и Беккереля За открытие естественной
- 8. Опыты Крукса и Томсона Вращение вертушки с
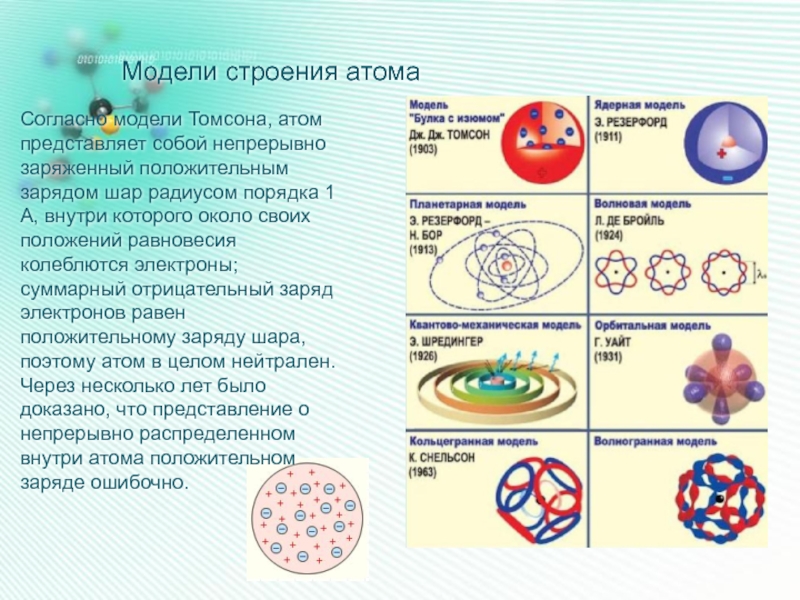
- 9. Модели строения атома Согласно модели Томсона, атом
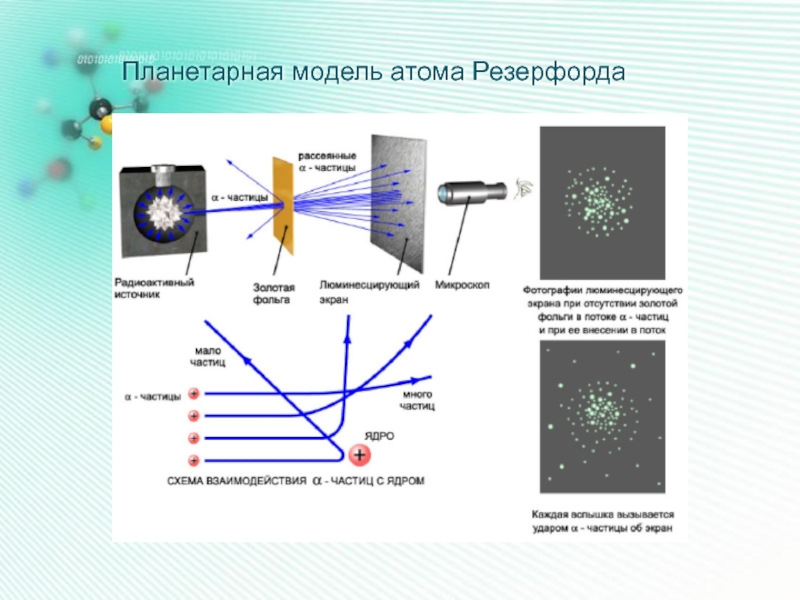
- 10. Планетарная модель атома Резерфорда
- 11. Постулаты Н. Бора
- 12. Квантово-механические принципы строения вещества
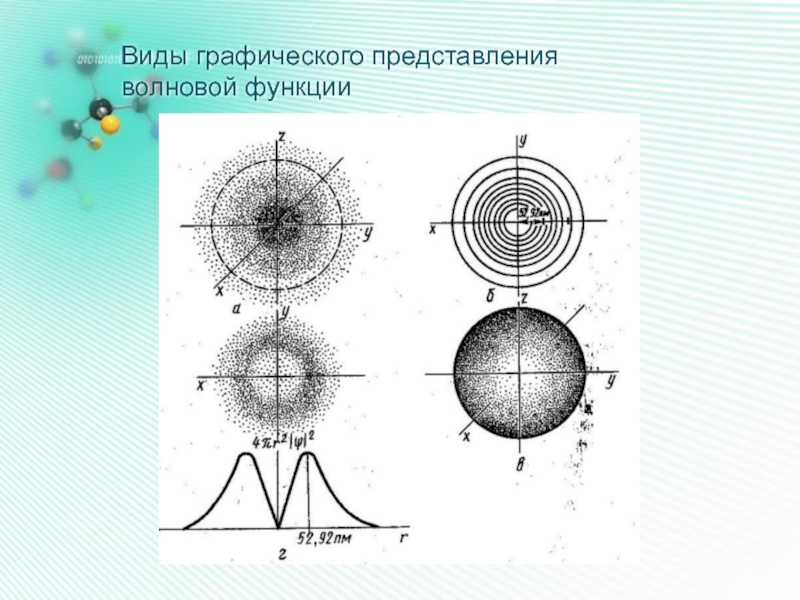
- 13. Виды графического представления волновой функции
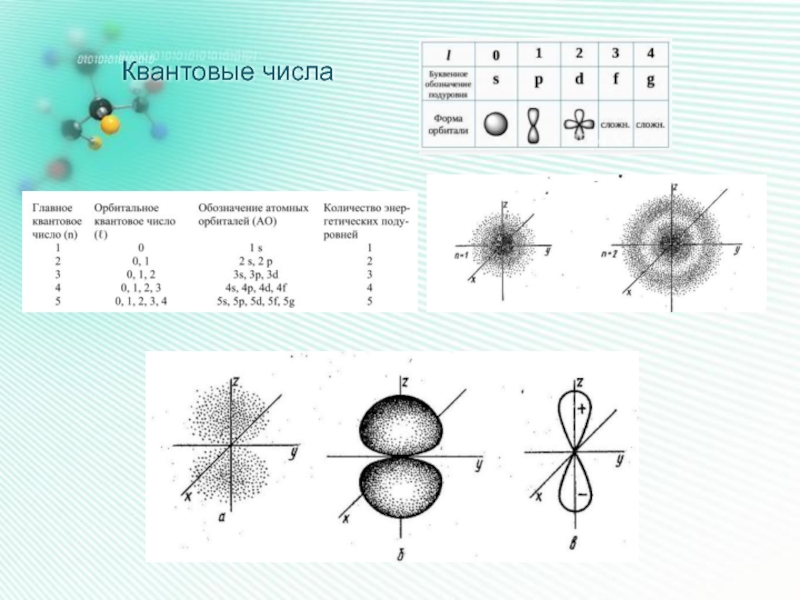
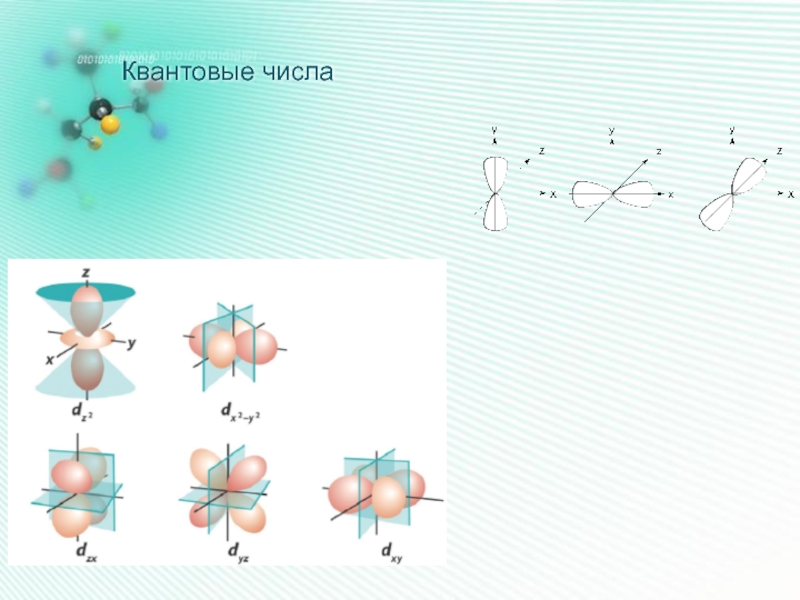
- 14. Квантовые числа
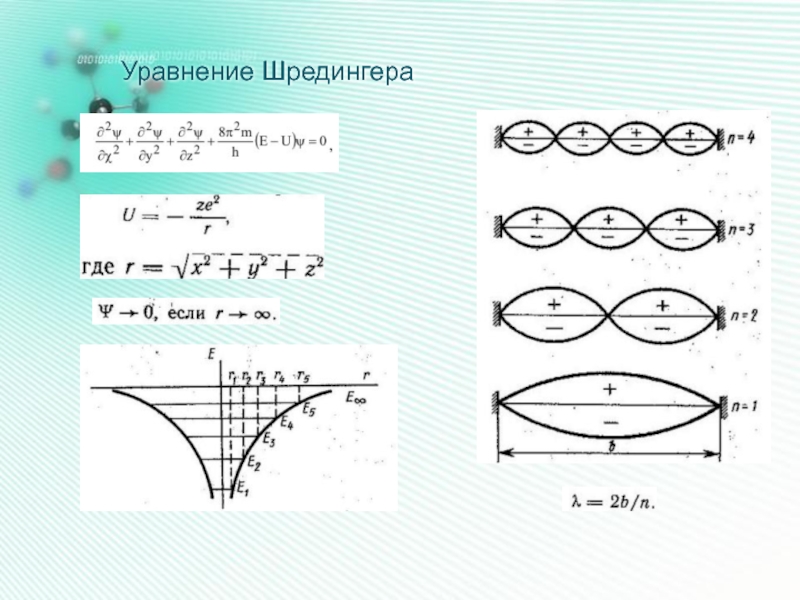
- 15. Уравнение Шредингера
- 16. Квантовые числа
- 17. Квантовые числа
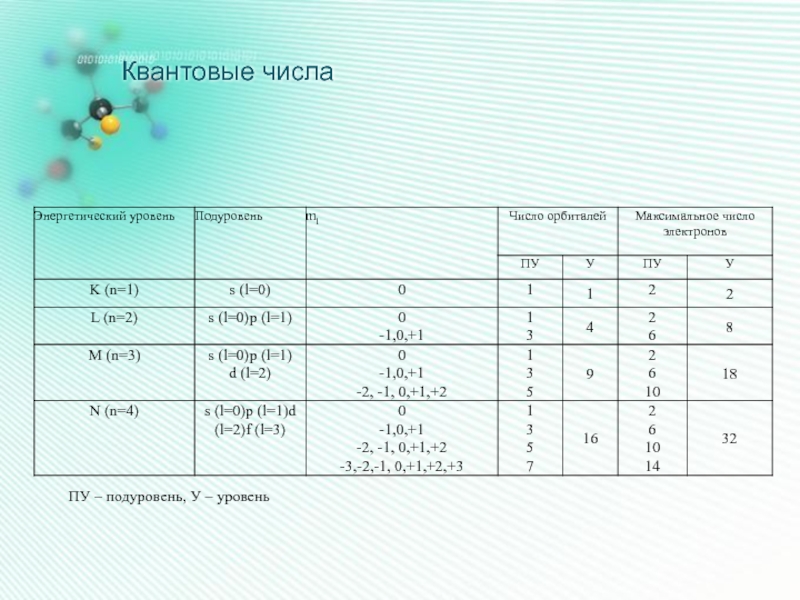
- 18. Квантовые числа ПУ – подуровень, У – уровень
Слайд 1ХИМИЯ
Модуль 1
Строение вещества
лекция 1
Строение атома
Лектор к.х.н., доцент
Черняк Михаил Юрьевич
Слайд 3В V веке до нашей эры Левкипп и Демокрит первыми употребили
"Если бы я хотел
читать, не зная букв - бессмысленное дело.
Если бы я хотел
рассуждать о
естественных вещах, не имея представления о
началах их, это было бы столь же
бессмысленно".
М. В. Ломоносов
Слайд 4Изучая атмосферу и движение воздуха, Дальтон пришел к выводу, противоречащему убеждениям
Слайд 5М. Фарадей установил, что ток в растворе электролита это упорядоченное движение
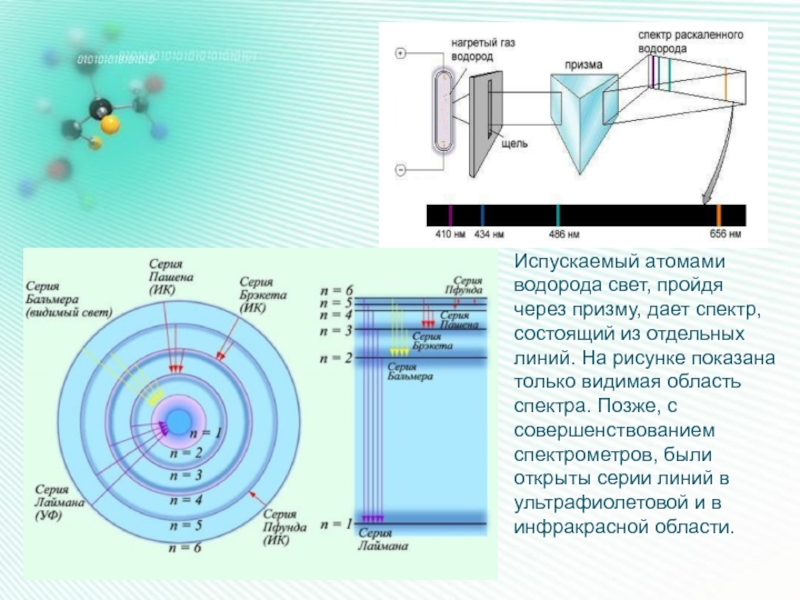
Слайд 6Испускаемый атомами водорода свет, пройдя через призму, дает спектр, состоящий из
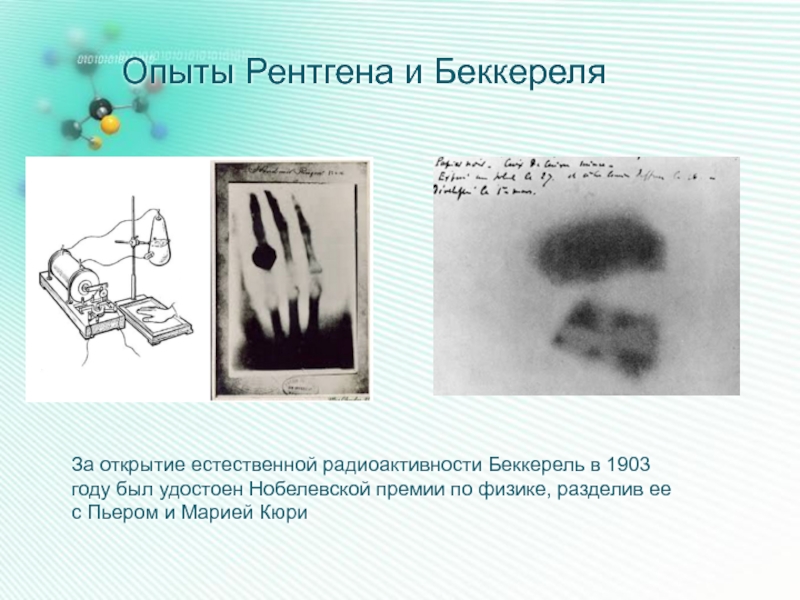
Слайд 7Опыты Рентгена и Беккереля
За открытие естественной радиоактивности Беккерель в 1903 году
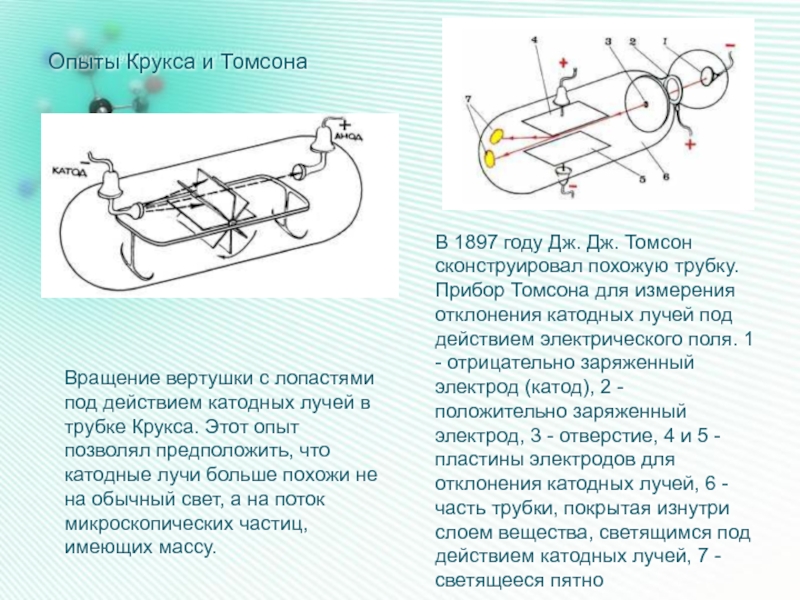
Слайд 8Опыты Крукса и Томсона
Вращение вертушки с лопастями под действием катодных лучей
В 1897 году Дж. Дж. Томсон сконструировал похожую трубку. Прибор Томсона для измерения отклонения катодных лучей под действием электрического поля. 1 - отрицательно заряженный электрод (катод), 2 - положительно заряженный электрод, 3 - отверстие, 4 и 5 - пластины электродов для отклонения катодных лучей, 6 - часть трубки, покрытая изнутри слоем вещества, светящимся под действием катодных лучей, 7 - светящееся пятно