План урока
- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Строение атома презентация
Содержание
- 2. 1. История изучения атома. 2.
- 3. Люди всегда задумывались о строении микромира, но
- 4. В 1879 году английский ученый
- 5. В 1895г. немецкий ученый
- 6. В 1896 году французский ученый
- 7. Главным итогом совершенных открытий было,
- 8. Первой экспериментально обоснованной моделью
- 9. Когда на их пути помещали
- 10. Основываясь на эксперименте. Резерфорд предположил, что в
- 11. Современная модель строения атома. Состав
- 12. Нуклоны имеют следующие характеристики:
- 13. Вокруг ярда движутся электроны (e-),
- 14. Число протонов определяет заряд ядра (Z) Число
- 15. Химический элемент – это определенный вид атомов с одинаковым зарядом ядра
- 16. Домашнее задание § 6 РТ: стр. Задания №
Слайд 2
1. История изучения атома.
2. Открытия, доказавшие сложность строения атома.
3. Модели атома.
4.
Состав атома.
Слайд 3Люди всегда задумывались о строении микромира, но на пороге новой эры
так и не пришли к единой точке зрения.
Э. Резерфорд
Н. Бор
А. Беккерель
Слайд 4 В 1879 году английский ученый Уильям Крукс открыл катодные
лучи - поток быстролетящих отрицательно заряженных частиц, размеры которых были меньше самого маленького атома водорода, по вызываемой ими люминесценции.
В 1891г. Д. Стонэй предложил назвать эти открытые частицы электронами.
В 1891г. Д. Стонэй предложил назвать эти открытые частицы электронами.
Слайд 5 В 1895г. немецкий ученый Уильям Конрад Рентген обнаружил
новый вид излучения, обладающего большой проникающей способностью, и назвал их X - лучами. Таинственные лучи засвечивали фотопленку, завернутую в черную бумагу.
В настоящее время рентгеновские лучи широко используются в различных областях науки и техники.
В настоящее время рентгеновские лучи широко используются в различных областях науки и техники.
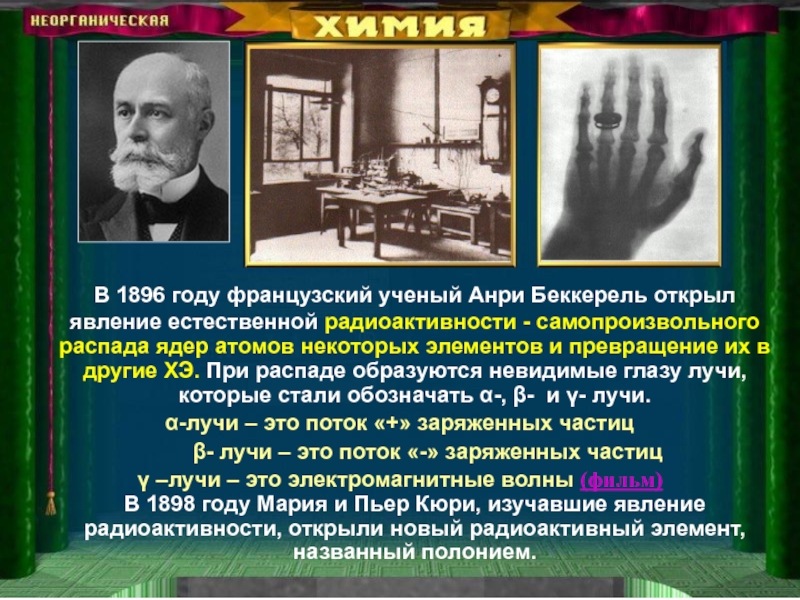
Слайд 6 В 1896 году французский ученый Анри Беккерель открыл явление
естественной радиоактивности - самопроизвольного распада ядер атомов некоторых элементов и превращение их в другие ХЭ. При распаде образуются невидимые глазу лучи, которые стали обозначать α-, β- и γ- лучи.
α-лучи – это поток «+» заряженных частиц
β- лучи – это поток «-» заряженных частиц
γ –лучи – это электромагнитные волны (фильм) В 1898 году Мария и Пьер Кюри, изучавшие явление радиоактивности, открыли новый радиоактивный элемент, названный полонием.
α-лучи – это поток «+» заряженных частиц
β- лучи – это поток «-» заряженных частиц
γ –лучи – это электромагнитные волны (фильм) В 1898 году Мария и Пьер Кюри, изучавшие явление радиоактивности, открыли новый радиоактивный элемент, названный полонием.
Слайд 7 Главным итогом совершенных открытий было, ясное осознание того, что
атом не является мельчайшей частицей вещества, он имеет сложное строение. Было предложено несколько гипотез - моделей строения атома.
Большинство из них основывалось на предположениях, что атом, оставаясь в целом электронейтральным, представляет собой совокупность положительно и отрицательно заряженных частиц.
Большинство из них основывалось на предположениях, что атом, оставаясь в целом электронейтральным, представляет собой совокупность положительно и отрицательно заряженных частиц.
Слайд 8 Первой экспериментально обоснованной моделью строения атома была планетарная
модель Эрнеста Резерфорда, создать которую ему помог специально проведенный опыт.
Поток α - частиц, излучаемых радиоактивным источником через узкую щель направляется на тонкую золотую фольгу. Регистрация α - частиц проводилась при помощи флюоресцирующего экрана. В отсутствии фольги α - частицы двигались узким пучком, вызывая на экране яркую вспышку.
Поток α - частиц, излучаемых радиоактивным источником через узкую щель направляется на тонкую золотую фольгу. Регистрация α - частиц проводилась при помощи флюоресцирующего экрана. В отсутствии фольги α - частицы двигались узким пучком, вызывая на экране яркую вспышку.
Слайд 9 Когда на их пути помещали золотую фольгу, то происходило
в основном их слабое рассеивание. Однако, было обнаружено, что отдельные α - частицы могут отскакивать от фольги, вызывая свечение дополнительных экранов, помещенных в различных участках пространства до основного экрана.
Слайд 10Основываясь на эксперименте. Резерфорд предположил, что в центре атома находится массивное
«+» заряженное ядро, вокруг которого движутся электроны. Эта модель получила название планетарной.
Слайд 11Современная модель строения атома.
Состав ядра
Ядро - это центральная часть
атома, в котором сосредоточена практически вся его масса.
Ядро состоит из нуклонов - протонов и нейтронов.
Ядро имеет положительный заряд, равный количеству протонов находящихся в нем.
В ядре также находятся нейтроны - частицы, имеющие массу, но не обладающие зарядом.
Ядро состоит из нуклонов - протонов и нейтронов.
Ядро имеет положительный заряд, равный количеству протонов находящихся в нем.
В ядре также находятся нейтроны - частицы, имеющие массу, но не обладающие зарядом.
Слайд 12
Нуклоны имеют следующие характеристики:
масса
заряд
p+ 1 +1
n0 1 0
Mасса атома (массовое число) складывается из суммы масс протонов и нейтронов.
p+ 1 +1
n0 1 0
Mасса атома (массовое число) складывается из суммы масс протонов и нейтронов.
Ar = m p+ + m n
Слайд 13
Вокруг ярда движутся электроны (e-), образующие электронную оболочку, размеры которой определяют
размеры самого атома.
Заряд e- по величине равен заряду p+, но противоположен по знаку.
Масса e- в 2000раз меньше массы протона
Заряд e- по величине равен заряду p+, но противоположен по знаку.
Масса e- в 2000раз меньше массы протона
Слайд 14Число протонов определяет заряд ядра (Z)
Число протонов равно числу электронов: атом
– электронейтральная частица
Число протонов и электронов совпадает с порядковым номером ХЭ
Число нейтронов = Аr - Z
Число протонов и электронов совпадает с порядковым номером ХЭ
Число нейтронов = Аr - Z