- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Сложные эфиры презентация
Содержание
- 1. Сложные эфиры
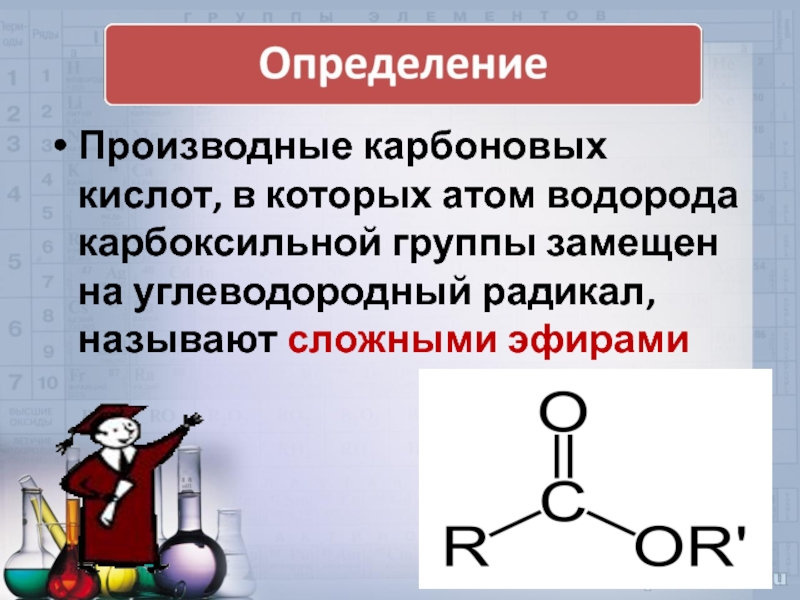
- 2. Производные карбоновых кислот, в которых атом водорода
- 3. В общей формуле сложных эфиров можно
- 4. CH3 метиловый эфир уксусной кислоты C3H7 пропиловый
- 5. CH3 метил ацетат C3H7 пропил формиат Названия
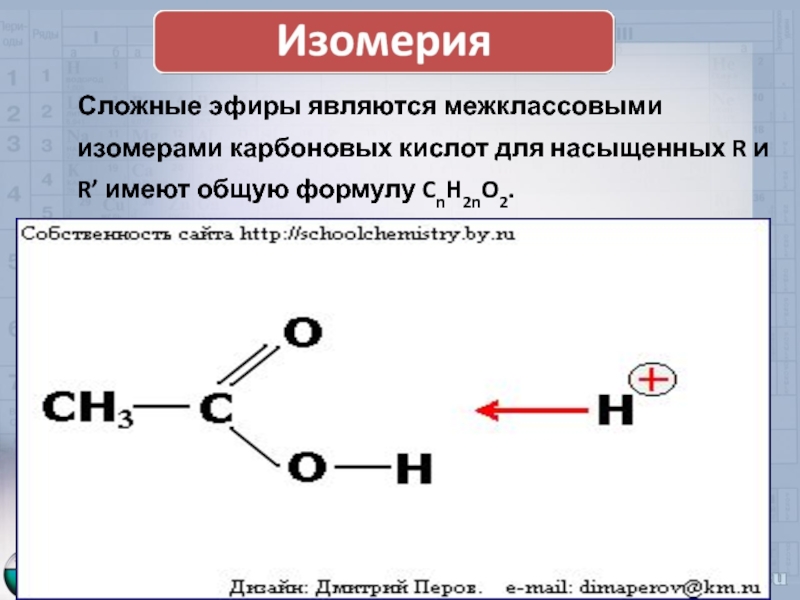
- 6. Сложные эфиры являются межклассовыми изомерами карбоновых кислот
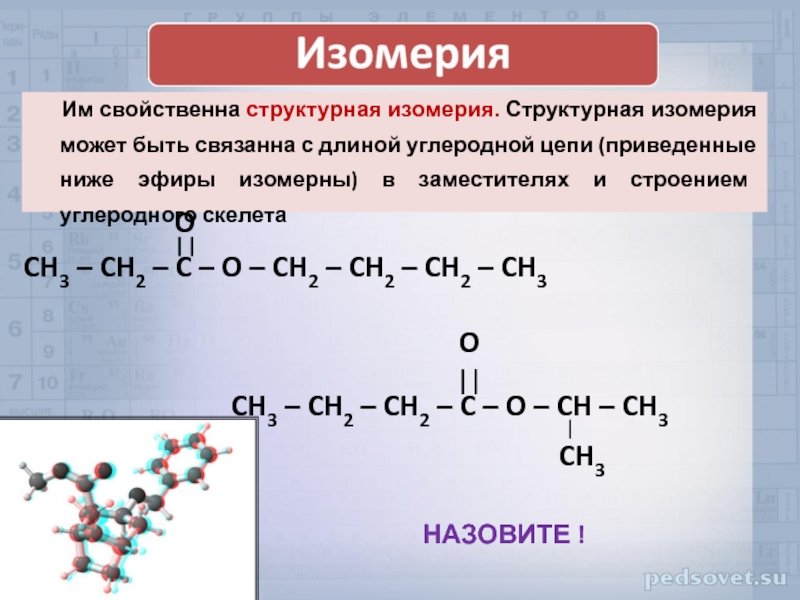
- 7. Им свойственна структурная изомерия. Структурная изомерия может
- 8. Сложные эфиры с относительно небольшой молекулярной массой
- 9. Когда число атомов С в исходных карбоновой
- 10. При увеличении размеров органических групп, входящих в
- 11. Воска - сложные эфиры одиночных жирных кислот
- 12. Третья группа – жиры. В отличие от
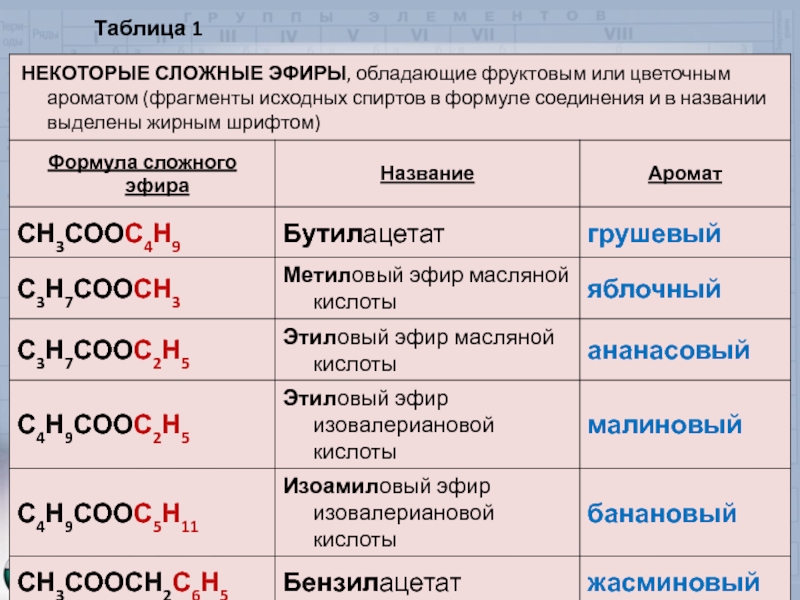
- 13. Таблица 1
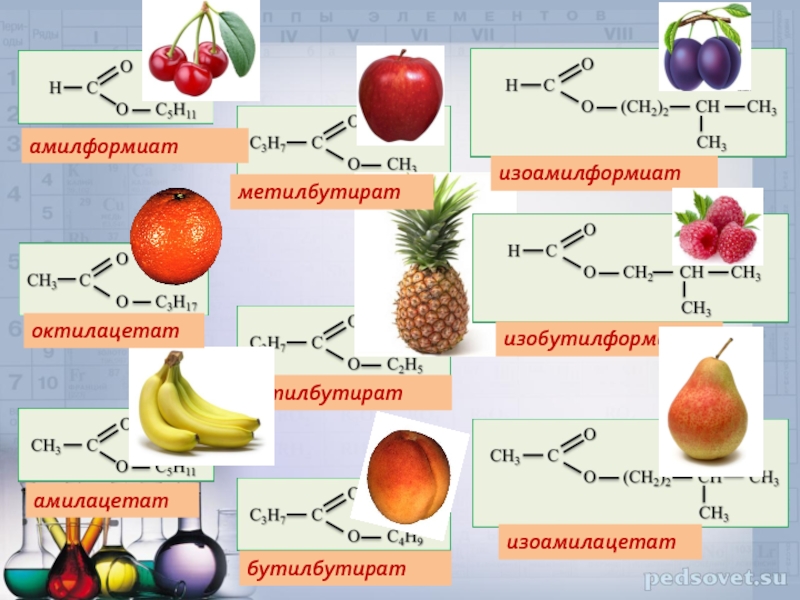
- 14. амилацетат этилбутират изоамилацетат изоамилформиат изобутилформиат бутилбутират октилацетат амилформиат метилбутират
- 15. "Одежда украшает внешность, а духи
- 16. Сложные эфиры могут быть получены при
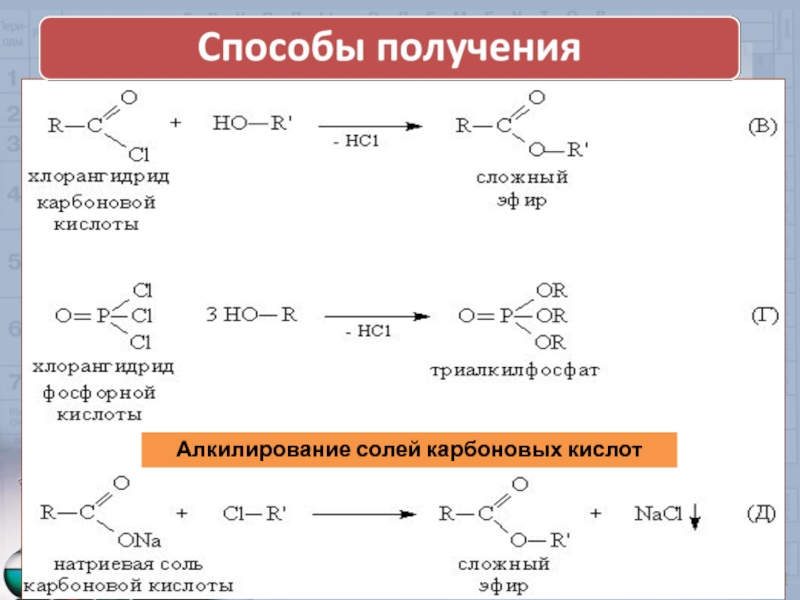
- 17. Алкилирование солей карбоновых кислот
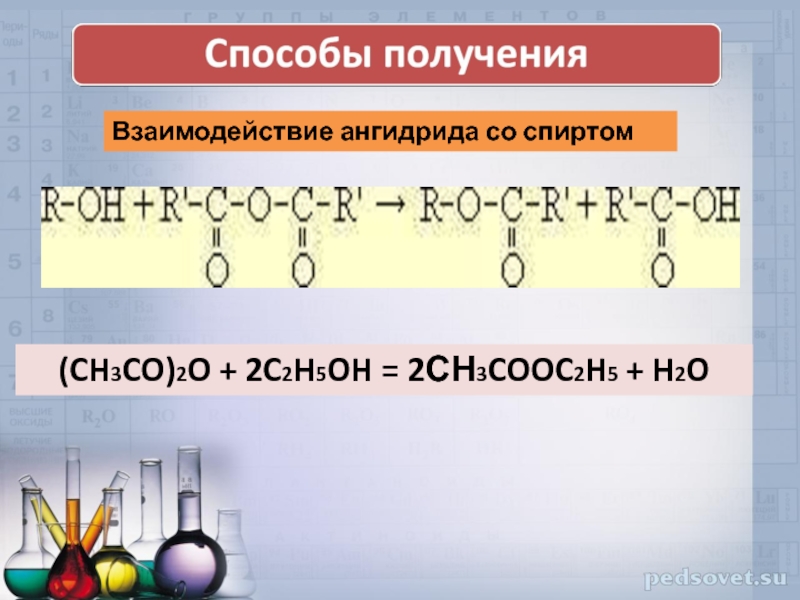
- 18. (CH3CO)2O + 2C2H5OH = 2СН3COOC2H5 + H2O Взаимодействие ангидрида со спиртом
- 19. 2CH3 – COOCH3 + 7O2 Реакция горения
- 20. Процесс - расщепление сложного эфира
- 21. Кислотный гидролиз сложных эфиров является обратимым
- 22. лекарственные средства синтетические и искусственные волокна лаки производство напитков и кондитерских изделий парфюмерия и косметика
- 23. Полиметилметакрилат – органическое стекло (плексиглас) – получается
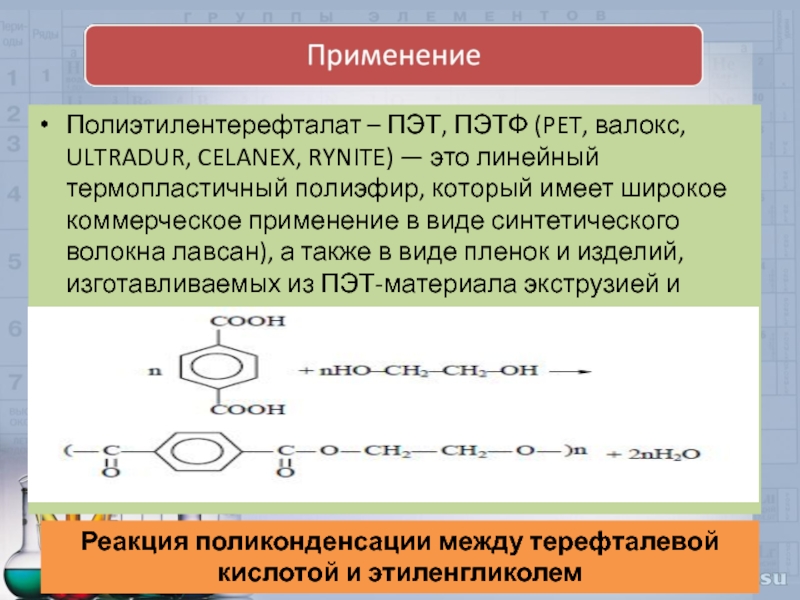
- 24. Полиэтилентерефталат – ПЭТ, ПЭТФ (PET, валокс, ULTRADUR,
- 25. Параграф 21, №1-3, 8, 12
- 26. СПАСИБО ЗА ВНИМАНИЕ!
Слайд 2Производные карбоновых кислот, в которых атом водорода карбоксильной группы замещен на
Слайд 3
В общей формуле сложных эфиров можно R и R’ – углеводородные
Слайд 4CH3
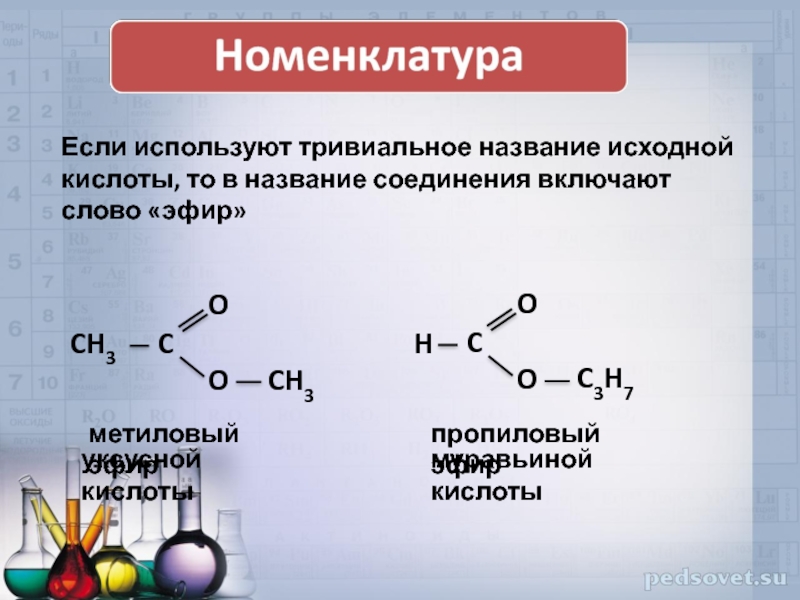
метиловый эфир
уксусной кислоты
C3H7
пропиловый эфир
Если используют тривиальное название исходной кислоты, то в
муравьиной кислоты
Слайд 5CH3
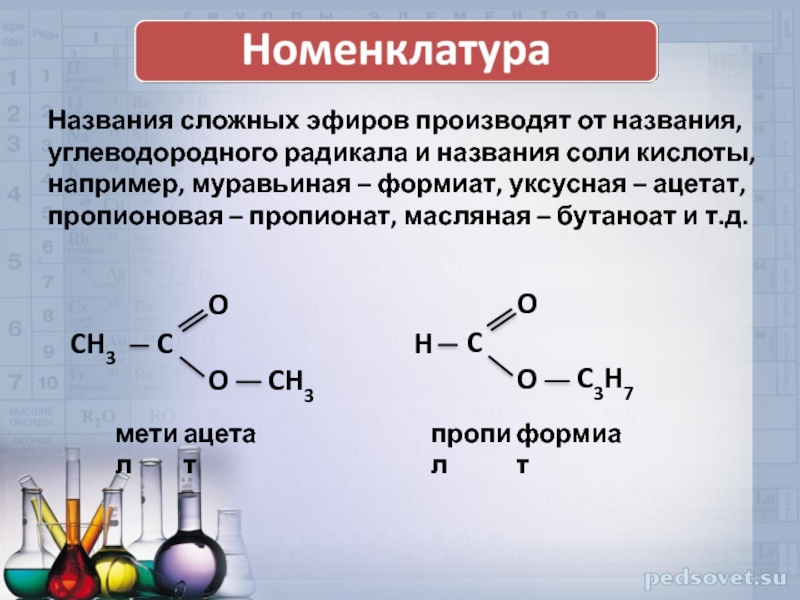
метил
ацетат
C3H7
пропил
формиат
Названия сложных эфиров производят от названия, углеводородного радикала и названия соли
Слайд 6Сложные эфиры являются межклассовыми изомерами карбоновых кислот для насыщенных R и
Слайд 7Им свойственна структурная изомерия. Структурная изомерия может быть связанна с длиной
НАЗОВИТЕ !
Слайд 8Сложные эфиры с относительно небольшой молекулярной массой представляют собой легковоспламеняющиеся жидкости
цветы
фрукты
воск
Слайд 9Когда число атомов С в исходных карбоновой кислоте и спирте не
Слайд 10При увеличении размеров органических групп, входящих в состав сложных эфиров, до
Искусственный воск
Пчелиный воск
CH3(CH2)14–CO–OCH2(CH2)29CH3
Слайд 11Воска - сложные эфиры одиночных жирных кислот и одноатомных спиртов с
Пчелиный воск содержит смесь различных сложных эфиров, один из компонентов воска, который удалось выделить и определить его состав, представляет собой мирициловый эфир пальмитиновой кислоты C15H31COOC31H63. Китайский воск (продукт выделения кошенили – насекомых Восточной Азии) содержит цериловый эфир церотиновой кислоты C25H51COOC26H53. Кроме того, воски содержат и свободные карбоновые кислоты и спирты, включающие большие органические группы. Воски не смачиваются водой, растворимы в бензине, хлороформе, бензоле.
Молекула воска
Слайд 12Третья группа – жиры. В отличие от предыдущих двух групп на
Слайд 14амилацетат
этилбутират
изоамилацетат
изоамилформиат
изобутилформиат
бутилбутират
октилацетат
амилформиат
метилбутират
Слайд 15 "Одежда украшает внешность, а духи отражают внутренний мир..."
Виды запахов:
o ГОРЬКИЕ: герань, лимон, мандарин, пион, сирень,
флердоранж (цветок апельсина).
o ТОНКИЕ: акация, гелиотроп, ирис, левкой, магнолия, мимоза, настурция, пион, роза.
o СЛАДКОВАТЫЕ: акация, мандарин, тубероза, ваниль.
o ЗЕЛЕНЫЕ: гвоздика, фиалка (листья), нарцисс, гальбанум (смола), мирра.
o ТЕПЛЫЕ: акация, душистый горошек, персик, сандал, тубероза, жимолость, животные запахи.
o ГУСТЫЕ, ТЯЖЕЛЫЕ: гвоздика, ладан, лилия, пачули, тубероза, ладан.
o ПРЯНЫЕ: жасмин, пачули, цикламен, корица, гвоздика, ветивер (корни), ладан.
o ЗАПАХ КОЖИ, ТАБАКА получают из бессмертника.
o ЖИВОТНЫЕ запахи: Серая амбра-железа кашалота выделяет секрет, который дает живой, теплый
Слайд 16
Сложные эфиры могут быть получены при взаимодействии карбоновых кислот со спиртами
Катализаторами являются минеральные кислоты.
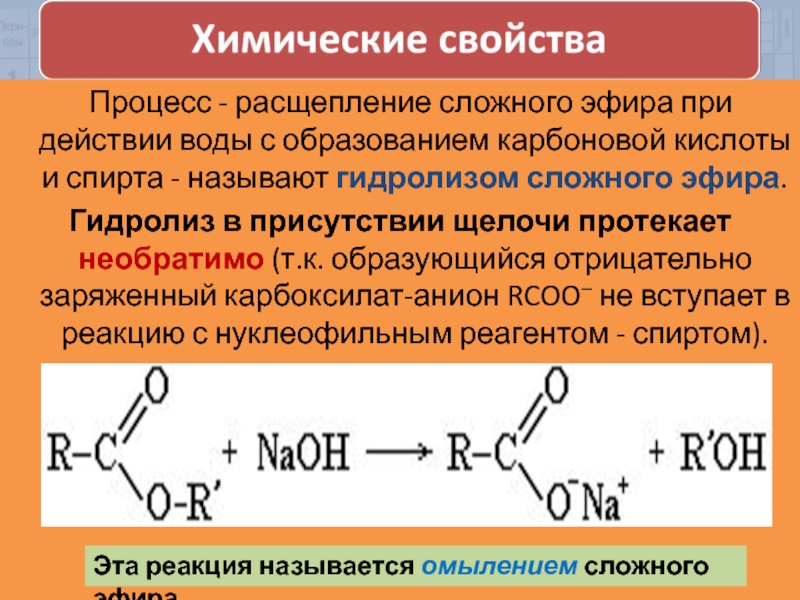
Слайд 20 Процесс - расщепление сложного эфира при действии воды с
Гидролиз в присутствии щелочи протекает необратимо (т.к. образующийся отрицательно заряженный карбоксилат-анион RCOO– не вступает в реакцию с нуклеофильным реагентом - спиртом).
Эта реакция называется омылением сложного эфира.
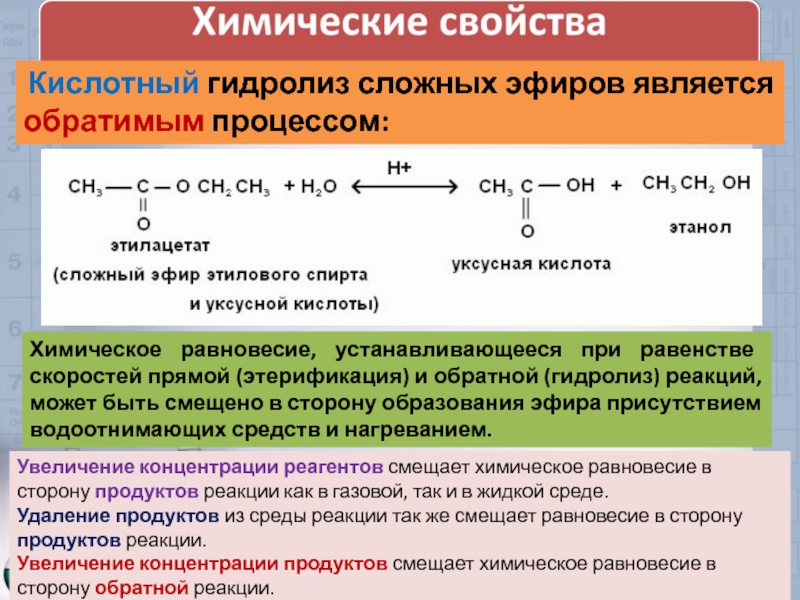
Слайд 21 Кислотный гидролиз сложных эфиров является обратимым процессом:
Химическое равновесие, устанавливающееся при
Увеличение концентрации реагентов смещает химическое равновесие в сторону продуктов реакции как в газовой, так и в жидкой среде.
Удаление продуктов из среды реакции так же смещает равновесие в сторону продуктов реакции.
Увеличение концентрации продуктов смещает химическое равновесие в сторону обратной реакции.
Слайд 22лекарственные средства
синтетические и искусственные волокна
лаки
производство напитков и кондитерских изделий
парфюмерия и косметика
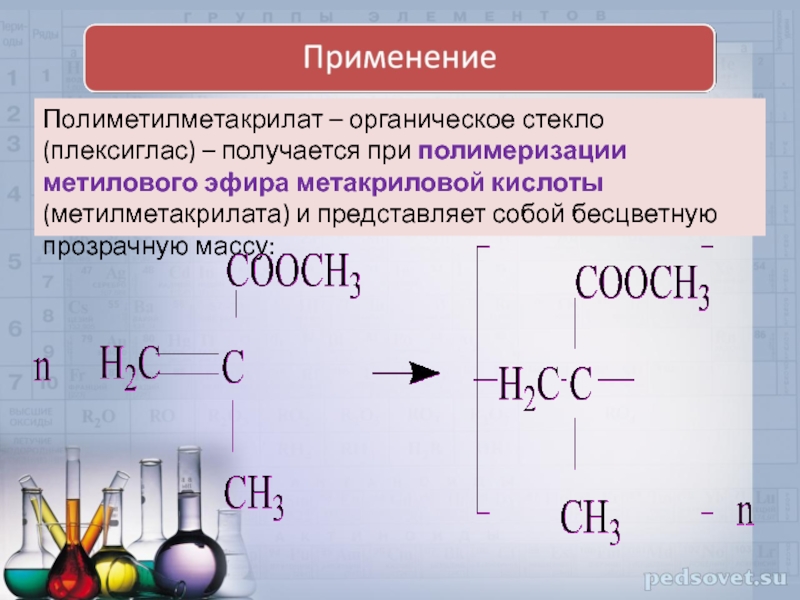
Слайд 23Полиметилметакрилат – органическое стекло (плексиглас) – получается при полимеризации метилового эфира
Слайд 24Полиэтилентерефталат – ПЭТ, ПЭТФ (PET, валокс, ULTRADUR, CELANEX, RYNITE) — это
Реакция поликонденсации между терефталевой кислотой и этиленгликолем