уравнения реакций
Вещества каких классов могут вступать в реакции обмена?
Подтвердить теоретические знания практическими наблюдениями
- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Реакции обмена презентация
Содержание
Слайд 3Тема урока: « Реакции обмена»
AB+CD = AD+CB
Сложные вещества обмениваются своими составными
частями
Реакции обмена – это такие реакции, в результате которых два сложных вещества обмениваются своими составными частями (атомами или группами атомов).
Слайд 4Эксперимент №1
NaOH + HCl = NaCl + H2O
2 KOH+H2SO4=K2SO4+ 2H2O
Внимание
В
результате взаимодействия кислоты и основания получилась вода, то есть среда стала нейтральной, поэтому
Реакция обмена между кислотами и щелочами называется реакция нейтрализации
Реакция обмена между кислотами и щелочами называется реакция нейтрализации
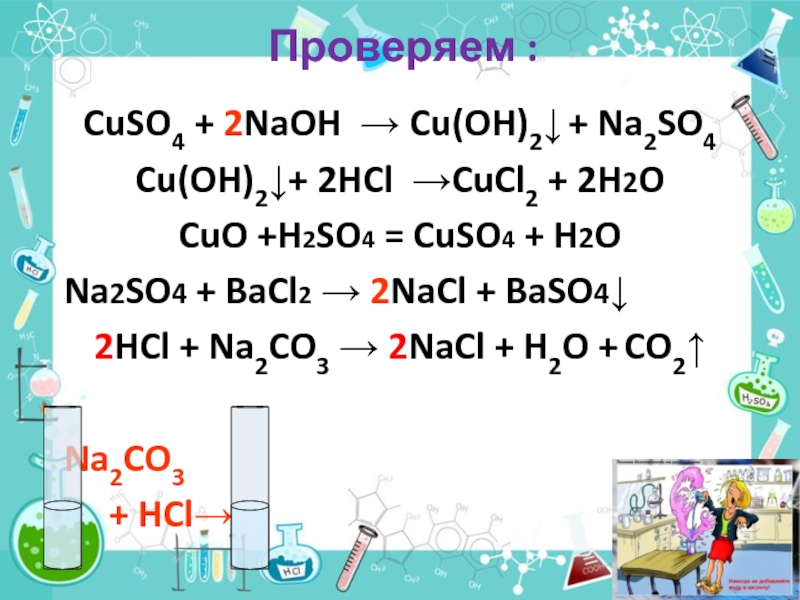
Слайд 5Проверяем :
CuSO4 + 2NaOH → Cu(OH)2↓ + Na2SO4
Cu(OH)2↓+ 2HCl →CuCl2 +
2H2O
CuO +H2SO4 = CuSO4 + H2O
Na2SO4 + BaCl2 → 2NaCl + BaSO4↓
2HCl + Na2CO3 → 2NaCl + H2O + CO2↑
Na2CO3
+ HCl→
CuO +H2SO4 = CuSO4 + H2O
Na2SO4 + BaCl2 → 2NaCl + BaSO4↓
2HCl + Na2CO3 → 2NaCl + H2O + CO2↑
Na2CO3
+ HCl→
Слайд 6Эксперимент №3:
Взаимодействие серной кислоты с раствором хлорида бария
Наблюдайте. Сделайте выводы о признаке протекания реакций. Расставьте коэффициенты
BaCl2 + H2SO4→ BaSO4 ↓+ 2HCl
BaCl2 + H2SO4→ BaSO4 ↓+ 2HCl
+H2SO4→
BaCl2