- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Правила ориентации в монозамещённых и дизамещённых ароматических углеводородах презентация
Содержание
- 1. Правила ориентации в монозамещённых и дизамещённых ароматических углеводородах
- 2. Содержание 1.Особенности электронного строения бензола 2. Правила
- 3. 1.Особенности строения бензола Бензол плоская молекула, в
- 4. Схема образования δ связей в молекуле бензола
- 5. У каждого sp2 гибридизованного атома углерода остаётся
- 6. 2.Правило ориентации в моно замещённых ароматических углеводородах
- 7. 2.1. Метод изолированных состояний электроны могут смещаться
- 8. 2.2.Метод переходных состояний 2.2.1. Электронодонорные заместители
- 9. 2.2.2. Электроноакцепторные заместители а б
- 10. 3. Правило ориентации в дизамещённых ароматических углеводородах согласованная ориентация (совпадающая)
- 11. Несогласованная ориентация наблюдается в том случае
Слайд 2Содержание
1.Особенности электронного строения бензола
2. Правила ориентации в моно замещённых ароматических углеводородах
2.1.
2.2.Метод переходных состояний
2.2.1. Электронодонорные заместители
2.2.2. Электроноакцепторные заместители
3. Правила ориентации в дизамещённых ароматических углеводородах
Домашнее задание…….
Слайд 31.Особенности строения бензола
Бензол плоская молекула, в которой шесть атомов углерода объединены
Все длинны С—С равноценны и составляют величину 0,1397 нм.
Молекула бензола не полярна и в магнитном поле симметрична.
Все атомы углерода в sp2 гибридизованном состоянии.
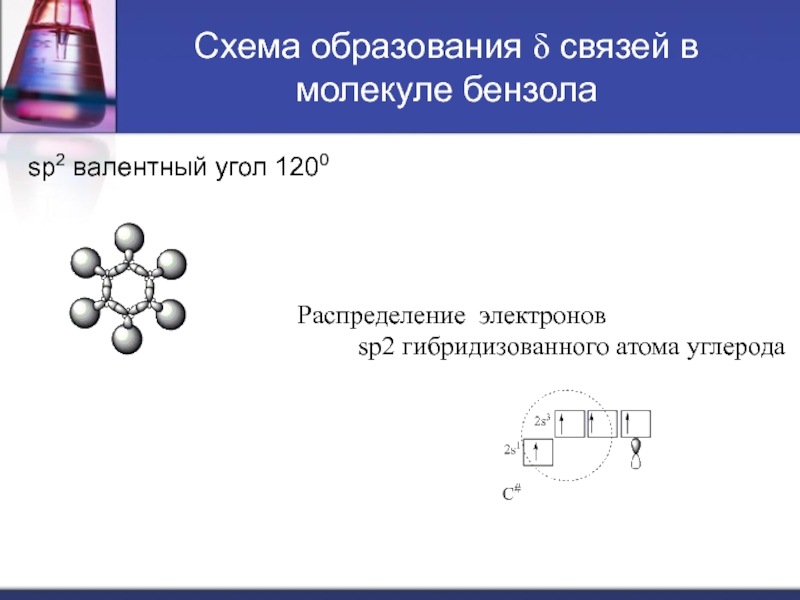
Слайд 4Схема образования δ связей в молекуле бензола
sp2 валентный угол 1200
Распределение электронов
sp2 гибридизованного атома углерода
Слайд 5 У каждого sp2 гибридизованного атома углерода остаётся один не спаренный гибридный
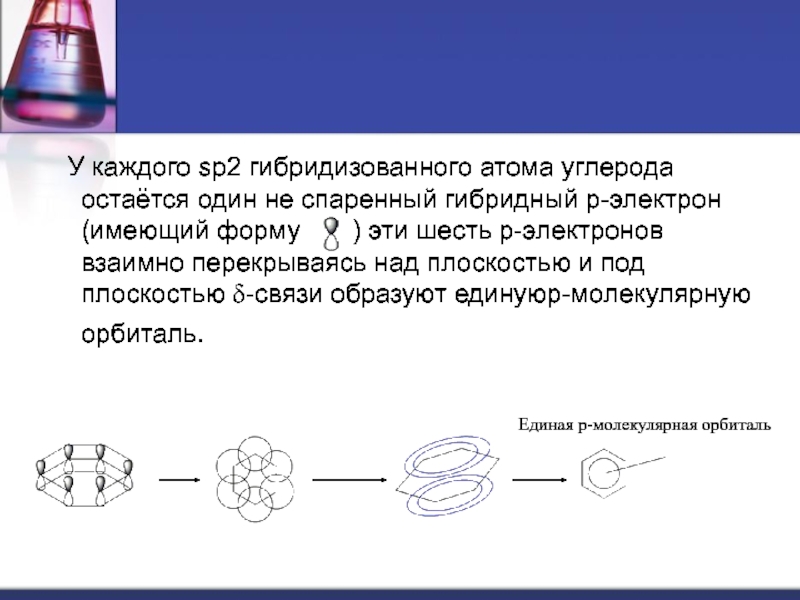
Единая p-молекулярная орбиталь
У каждого sp2 гибридизованного атома углерода остаётся один не спаренный гибридный p-электрон (имеющий форму ) эти шесть p-электронов взаимно перекрываясь над плоскостью и под плоскостью δ-связи образуют единуюp-молекулярную орбиталь.
У каждого sp2 гибридизованного атома углерода остаётся один не спаренный гибридный p-электрон (имеющий форму ) эти шесть p-электронов взаимно перекрываясь над плоскостью и под плоскостью δ-связи образуют единуюp-молекулярную орбиталь.
У каждого sp2 гибридизованного атома углерода остаётся один не спаренный гибридный p-электрон (имеющий форму ) эти шесть p-электронов взаимно перекрываясь над плоскостью и под плоскостью δ-связи образуют единуюp-молекулярную орбиталь.
Единая p-молекулярная орбиталь
Единая p-молекулярная орбиталь
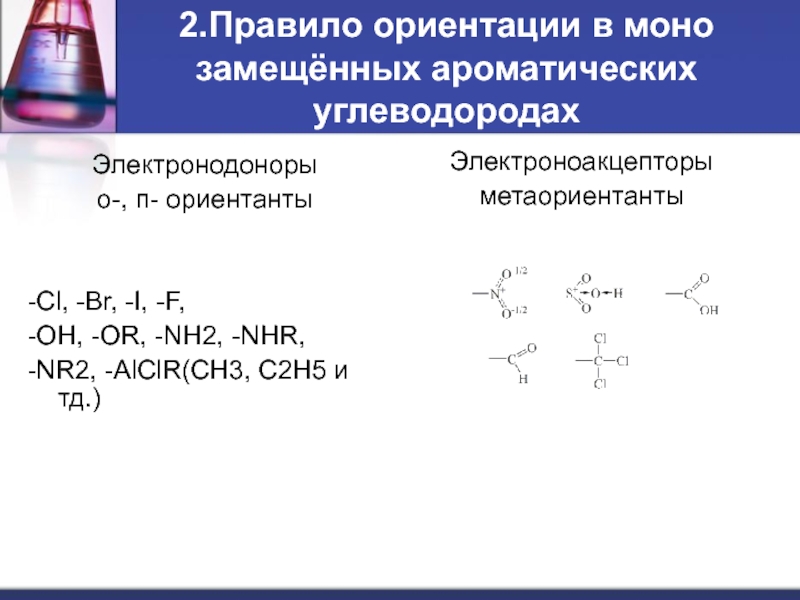
Слайд 62.Правило ориентации в моно замещённых ароматических углеводородах
Электронодоноры
о-, п- ориентанты
-Cl, -Br, -I,
-OH, -OR, -NH2, -NHR,
-NR2, -AlClR(CH3, C2H5 и тд.)
Электроноакцепторы
метаориентанты
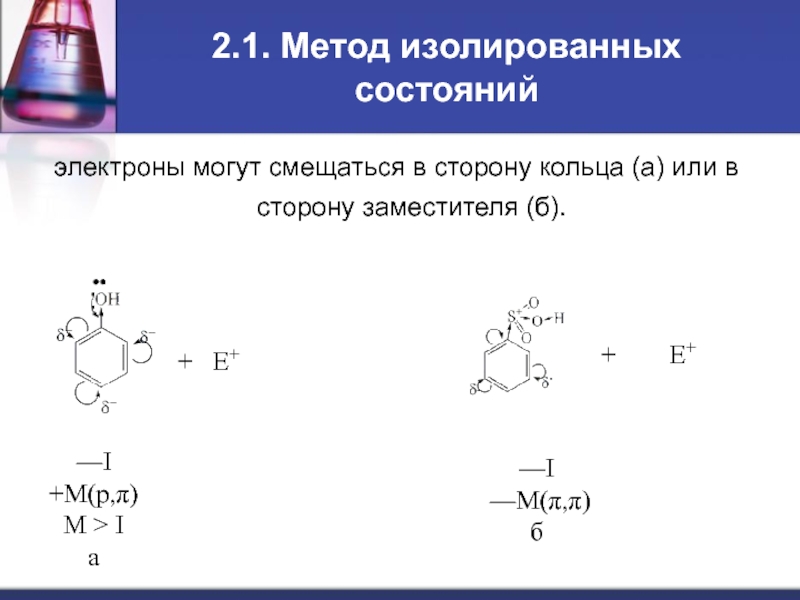
Слайд 72.1. Метод изолированных состояний
электроны могут смещаться в сторону кольца (а) или
+ E+
+ E+
—I
+M(p,π)
M > I
а
—I
—M(π,π)
б
Слайд 82.2.Метод переходных состояний
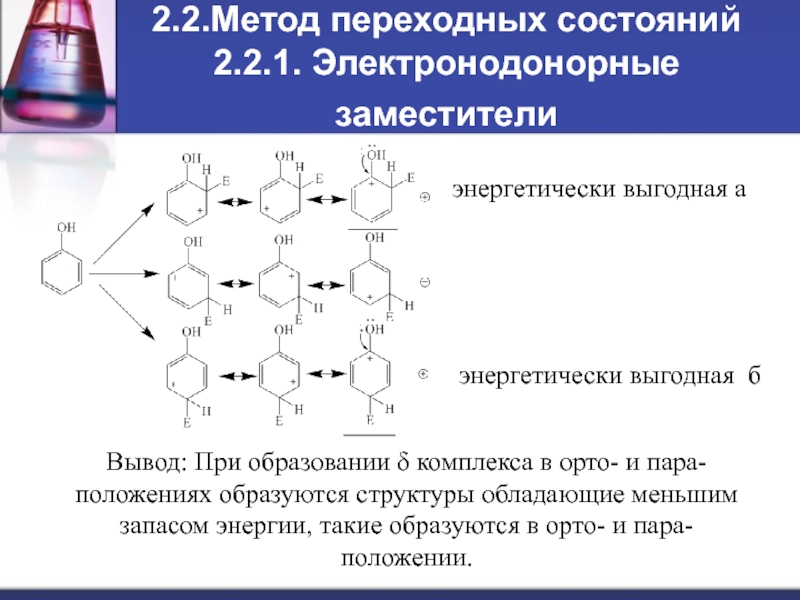
2.2.1. Электронодонорные заместители
энергетически выгодная а
энергетически выгодная
Вывод: При образовании δ комплекса в орто- и пара- положениях образуются структуры обладающие меньшим запасом энергии, такие образуются в орто- и пара- положении.
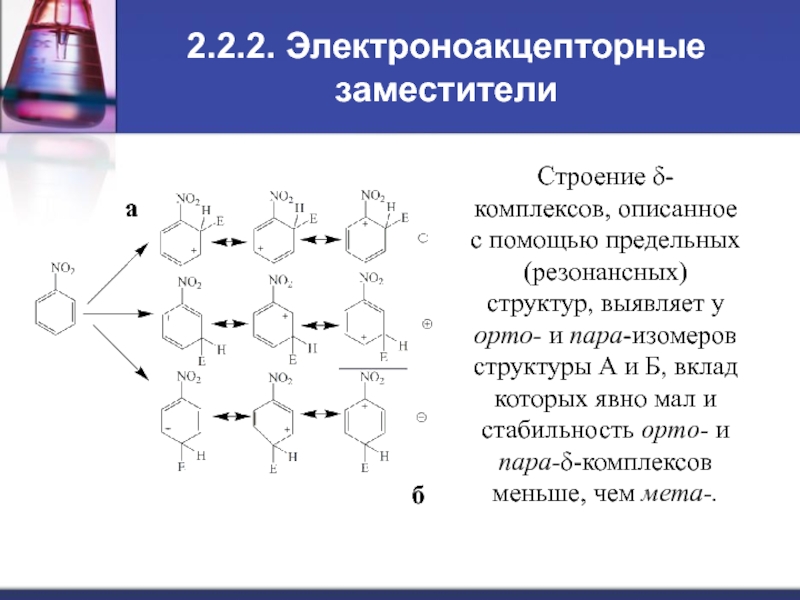
Слайд 92.2.2. Электроноакцепторные заместители
а
б
Строение δ-комплексов, описанное с помощью предельных (резонансных)
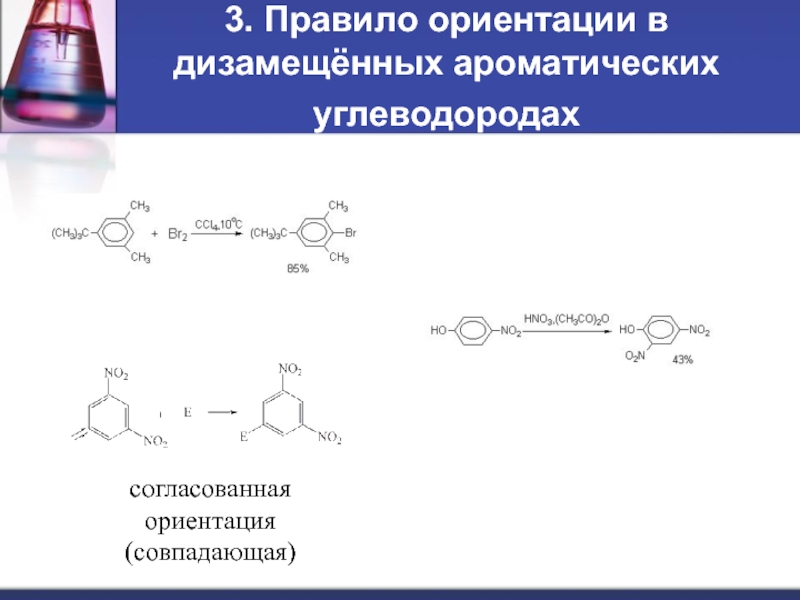
Слайд 103. Правило ориентации в дизамещённых ароматических углеводородах
согласованная
ориентация
(совпадающая)
Слайд 11
Несогласованная ориентация наблюдается в том случае если в ароматическом кольце есть
ориентация не
согласованная