- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Поверхностные явления презентация
Содержание
- 1. Поверхностные явления
- 2. План лекции Общие понятия Поверхностное натяжение Процессы,
- 3. Поверхностный слой вещества Промежуточная фаза, содержащая один
- 4. Поверхностные явления незначительны, если соотношения между массой
- 5. Поверхностная энергия Гиббса GS ΔGS = σ
- 6. Поверхностное натяжение σ Работа, совершаемая на создание
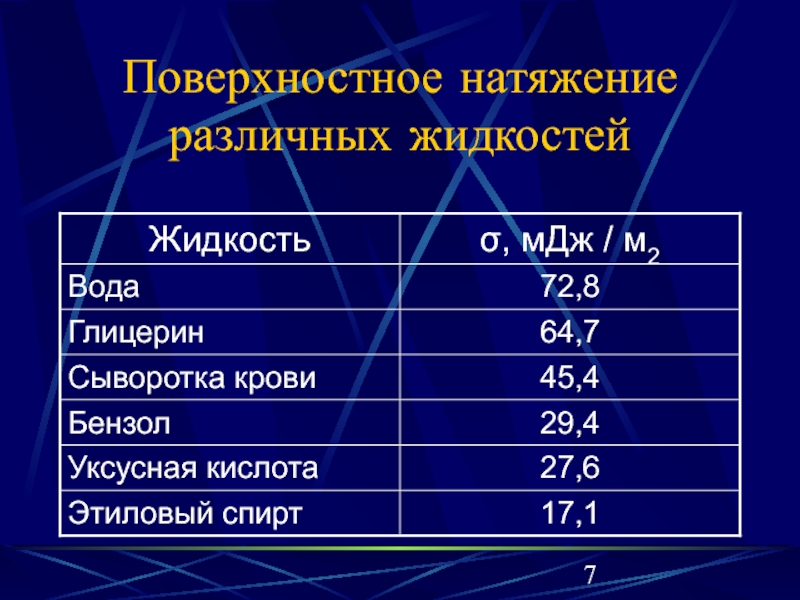
- 7. Поверхностное натяжение различных жидкостей
- 8. Процессы на подвижных поверхностях Сорбция – поглощение
- 9. Величина адсорбции Г Выражается количеством молей вещества
- 10. Поверхностные явления Происходят в следующих системах: Газ
- 11. Поверхностные явления в растворах Накопление растворенного вещества
- 12. Уравнение Гиббса С
- 13. Анализ уравнение Гиббса Δσ ------ =
- 14. Свойства ПАВ Ограниченно растворимы Обладают меньшим поверхностным натяжением, чем жидкости Резко изменяют поверхностные свойства жидкости
- 15. Классификация ПАВ Молекулярные или неионогенные – спирты,
- 16. Строение ПАВ Дифильное – разные участки молекулы
- 17. Правило Траубе-Дюкло Удлинение цепи на радикал –
- 18. Изотерма адсорбции Г∞ – предельная адсорбция; наблюдается
- 19. Изотерма поверхностного натяжения Графическая зависимость поверхностного натяжения от концентрации растворенного вещества
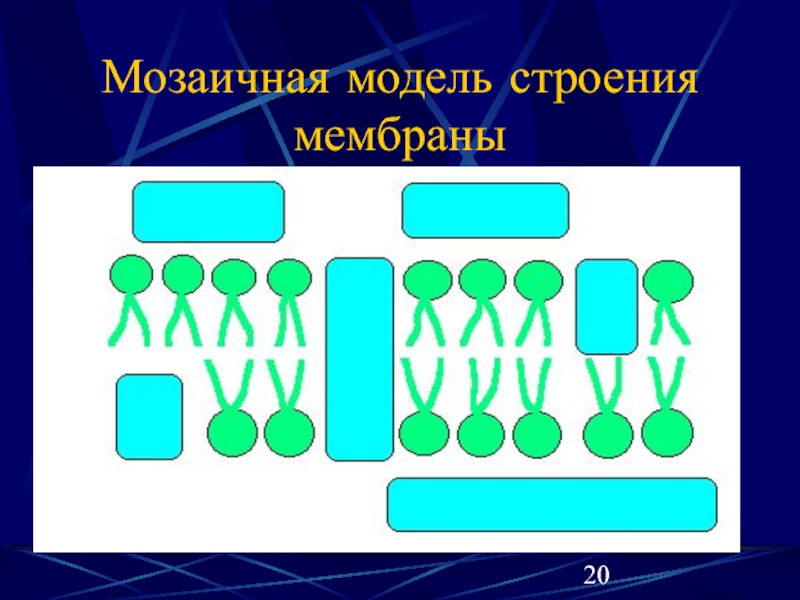
- 20. Мозаичная модель строения мембраны
- 21. Значение поверхностных явлений Всасывание питательных веществ Обмен
- 22. Применение ПАВ Получение растворимых форм лекарственных веществ
- 23. Межфазное поверхностное натяжение на границе жидкость/жидкость Поверхностное
- 24. Способы измерения поверхностного натяжения жидкости Метод отрыва
Слайд 2План лекции
Общие понятия
Поверхностное натяжение
Процессы, происходящие на подвижных поверхностях
Уравнение Гиббса
Поверхностно активные вещества
Слайд 3Поверхностный слой вещества
Промежуточная фаза, содержащая один или несколько молекулярных слоев
Особенности:
Внутри объема
чистого вещества все силы межмолекулярного взаимодействия уравновешены
Равнодействующая всех сил, воздействующих на поверхностные молекулы, направлена внутрь жидкости
Равнодействующая всех сил, воздействующих на поверхностные молекулы, направлена внутрь жидкости
Слайд 4Поверхностные явления незначительны, если соотношения между массой тела и поверхностью в
пользу массы тела
Поверхностные явления приобретают значение, когда вещество находится в раздробленном состоянии или в виде тончайшего слоя (пленки)
1 см3 → 10-7, S = 6 000 м2
1мм крови → 4 - 5 млн эритроцитов; 1л → > 30 млр клеток, S = 1000 м2
S альвеол = 800 -1000 м2; S капилляров печени = 600 м2
Поверхностные явления приобретают значение, когда вещество находится в раздробленном состоянии или в виде тончайшего слоя (пленки)
1 см3 → 10-7, S = 6 000 м2
1мм крови → 4 - 5 млн эритроцитов; 1л → > 30 млр клеток, S = 1000 м2
S альвеол = 800 -1000 м2; S капилляров печени = 600 м2
Слайд 5Поверхностная энергия Гиббса GS
ΔGS = σ ⋅ S
σ – поверхностное натяжение
Уменьшение
энергии Гиббса:
За счет уменьшения площади поверхности (укрупнение частиц)
За счет уменьшения величины поверхностного натяжения (сорбция)
За счет уменьшения площади поверхности (укрупнение частиц)
За счет уменьшения величины поверхностного натяжения (сорбция)
Слайд 6Поверхностное натяжение σ
Работа, совершаемая на создание единицы поверхности
Единицы измерения Дж/м2
Сила, действующая
на единицу длины линии, ограничивающей поверхность жидкости и направленную в сторону уменьшения этой поверхности
Единицы измерения Н/м2
Единицы измерения Н/м2
Слайд 8Процессы на подвижных поверхностях
Сорбция – поглощение каким-либо веществом других веществ
Сорбент –
вещество, которое поглощает другое
Сорбтив – поглощаемое вещество
Адсорбция – процесс поглощения вещества поверхностью сорбента
Абсорбция – процесс поглощения вещества всем объемом сорбента
Десорбция – процесс, обратный сорбции
Хемосорбция – процесс сорбции, сопровождающийся химической реакцией
Сорбтив – поглощаемое вещество
Адсорбция – процесс поглощения вещества поверхностью сорбента
Абсорбция – процесс поглощения вещества всем объемом сорбента
Десорбция – процесс, обратный сорбции
Хемосорбция – процесс сорбции, сопровождающийся химической реакцией
Слайд 9Величина адсорбции Г
Выражается количеством молей вещества (сорбтива), приходящегося на единицу площади
(массы) поверхности адсорбента
Х Х
Г = -----, моль/м2 Г = -----, моль/кг
S m
Х Х
Г = -----, моль/м2 Г = -----, моль/кг
S m
Слайд 10Поверхностные явления
Происходят в следующих системах:
Газ / твердое тело
Газ / жидкость
Жидкость /
твердое тело
Жидкость / жидкость
Жидкость / жидкость
Слайд 11Поверхностные явления в растворах
Накопление растворенного вещества в поверхностном слое
Процесс диффузии по
градиенту концентрации, обусловленный тепловым движением
Количественно процесс адсорбции в поверхностном слое раствора описывается уравнением Гиббса
Количественно процесс адсорбции в поверхностном слое раствора описывается уравнением Гиббса
Слайд 12Уравнение Гиббса
С Δσ
Г = – ------ ⋅
------
RT ΔС
Г – величина адсорбции на поверхности раствора
Δσ
------ – поверхностная активность вещества
ΔС
С dσ
Г = – ------ ⋅ ------
RT dС
RT ΔС
Г – величина адсорбции на поверхности раствора
Δσ
------ – поверхностная активность вещества
ΔС
С dσ
Г = – ------ ⋅ ------
RT dС
Слайд 13Анализ уравнение Гиббса
Δσ
------ = 0; Г = 0
ΔС
Поверхностно
неактивные (нейтральные) вещества: сахароза
Δσ
------ > 0; Г < 0
ΔС
Поверхностно инактивные вещества: неорганические кислоты, щелочи, соли, муравьиная кислота
Δσ
------ < 0; Г > 0
ΔС
Поверхностно-активные вещества
Δσ
------ > 0; Г < 0
ΔС
Поверхностно инактивные вещества: неорганические кислоты, щелочи, соли, муравьиная кислота
Δσ
------ < 0; Г > 0
ΔС
Поверхностно-активные вещества
Слайд 14Свойства ПАВ
Ограниченно растворимы
Обладают меньшим поверхностным натяжением, чем жидкости
Резко изменяют поверхностные свойства
жидкости
Слайд 15Классификация ПАВ
Молекулярные или неионогенные – спирты, желчь, белковые вещества
Ионогенные анионактивные –
мыла, сульфокислоты и их соли, карбоновые кислоты
Ионогенные катионактивные – органические азотсодержащие основания и их соли
Ионогенные катионактивные – органические азотсодержащие основания и их соли
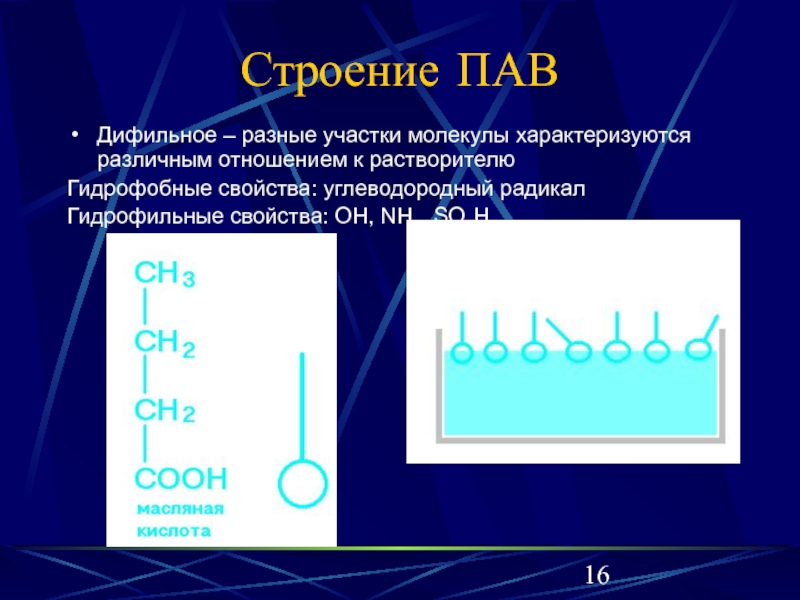
Слайд 16Строение ПАВ
Дифильное – разные участки молекулы характеризуются различным отношением к растворителю
Гидрофобные
свойства: углеводородный радикал
Гидрофильные свойства: OH, NH2, SO3H
Гидрофильные свойства: OH, NH2, SO3H
Слайд 17Правило Траубе-Дюкло
Удлинение цепи на радикал – CH2 – увеличивает способность жирных
кислот к адсорбции в 3,2 раза
Применимо только для разбавленных растворов и для температур, близких к комнатной, т.к. с повышением температуры увеличивается десорбция
Применимо только для разбавленных растворов и для температур, близких к комнатной, т.к. с повышением температуры увеличивается десорбция
Слайд 18Изотерма адсорбции
Г∞ – предельная адсорбция; наблюдается в случае большой концентрации ПАВ,
когда на поверхности раствора образуется сплошной мономолекулярный слой («частокол Ленгмюра»)
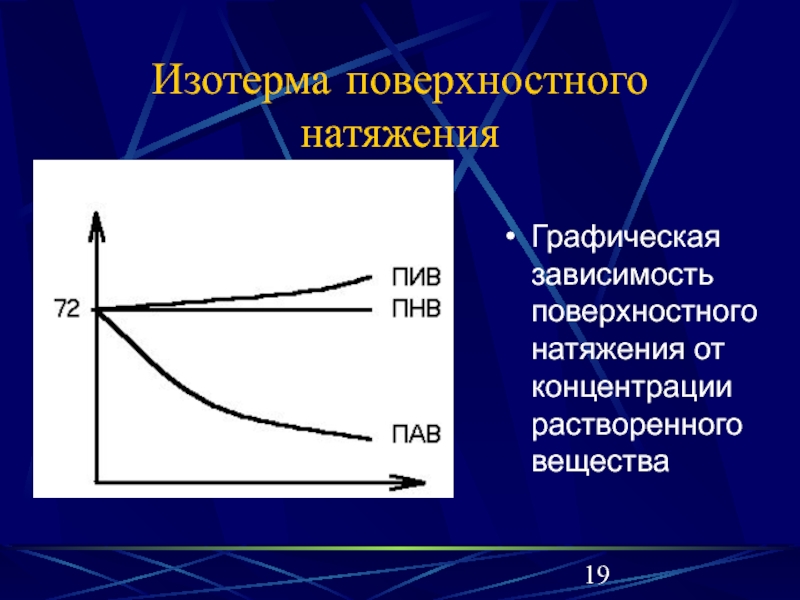
Слайд 19Изотерма поверхностного натяжения
Графическая зависимость поверхностного натяжения от концентрации растворенного вещества
Слайд 21Значение поверхностных явлений
Всасывание питательных веществ
Обмен веществ через стенку кровеносных сосудов и
клеточные мембраны
Развитие кессонной болезни
Развитие кессонной болезни
Слайд 22Применение ПАВ
Получение растворимых форм лекарственных веществ (твины и спаны)
В качестве антисептиков
в хирургии – влияют на проницаемость мембран и на ферментативную активность микробов
В качестве моющих средств в быту
Получение эмульсий масла в воде, пеногасителей
В качестве моющих средств в быту
Получение эмульсий масла в воде, пеногасителей
Слайд 23Межфазное поверхностное натяжение на границе жидкость/жидкость
Поверхностное натяжение значительно меньше, чем на
границе жидкость/газ
Коэффициент межфазного натяжения равен разности коэффициентов поверхностных натяжений их взаимно насыщенных растворов
Добавление третьего компонента приводит к снижению межфазного поверхностного натяжения
Коэффициент межфазного натяжения равен разности коэффициентов поверхностных натяжений их взаимно насыщенных растворов
Добавление третьего компонента приводит к снижению межфазного поверхностного натяжения
Слайд 24Способы измерения поверхностного натяжения жидкости
Метод отрыва кольца от поверхности жидкости
Метод подсчета
числа капель определенного объема исследуемой жидкости, вытекающей из капилляра (сталагмометрический)
Метод определения давления, которое необходимо для отрыва пузырька воздуха от капилляра, погруженного в жидкость (метод Ребиндера)
Метод измерения высоты поднятия жидкости в капилляре, стенки которого хорошо ею смачиваются
Метод определения давления, которое необходимо для отрыва пузырька воздуха от капилляра, погруженного в жидкость (метод Ребиндера)
Метод измерения высоты поднятия жидкости в капилляре, стенки которого хорошо ею смачиваются