- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Подготовка к итоговой контрольной работе. (9 класс) презентация
Содержание
- 1. Подготовка к итоговой контрольной работе. (9 класс)
- 2. Часть А. Тестовые задания. 1.
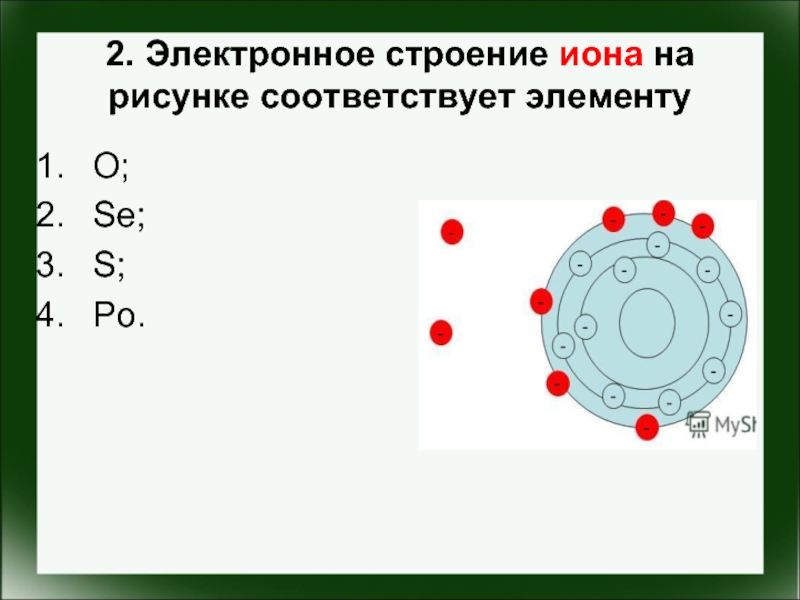
- 3. 2. Электронное строение иона на рисунке соответствует элементу O; Se; S; Po.
- 4. 3. Ряд элементов расположенных в порядке увеличения электроотрицательности: F-Cl-Br; K-Na-Li; C-Si-Ge; Si-Al-Mg.
- 5. 4. Вещество имеющее кристаллическое строение это: NaCl; H2O; HCl; CH3COOH.
- 6. 5. Оксид углерода (II) является: Амфотерным; Кислотным; Несолеобразующим; Основным.
- 7. 6. Ряд формул веществ реагирующих с гидроксидом
- 8. 7. Необратимая химическая реакция произойдёт при сливании
- 9. 8. Степень окисления серы S 2- в соединении формула которого: S; SO2; H2S; H2SO4.
- 10. 9. Уравнению реакции S+O2=SO2 соответствует схема превращения: S0→S-2; S+6→S0; S0→S-6; S0→S+4.
- 11. 10. Взаимодействию гидроксида бария и хлороводорода соответствует краткое ионное уравнение Ba2++2Cl-=BaCl2; OH-+H+=H2O; Ba2++2OH-+2H++2Cl-=Ba2+2Cl-+2H2O; 2OH-+2H+ =2H2O.
- 12. Часть Б. Задания со свободным ответом. 11.
- 13. 12. По краткому ионному уравнению CO32-+2H+=H2O+CO2 составьте молекулярное уравнение.
- 14. 13. Дана схема превращений. Барий→Оксид бария→X→Карбонат
- 15. 14. Задача ? Повторить! Строение атомов и
Слайд 2 Часть А. Тестовые задания. 1. Схема распределения электронов по энергетическим уровням
в атоме химического элемента, образующего соединения, соответствующие общим формулам H2Э и ЭО3:
2е 8е 1е;
2е 6е;
2е 8е 6е;
2е 4е.
Слайд 43. Ряд элементов расположенных в порядке увеличения электроотрицательности:
F-Cl-Br;
K-Na-Li;
C-Si-Ge;
Si-Al-Mg.
Слайд 76. Ряд формул веществ реагирующих с гидроксидом калия:
Al, CO2, HCl;
H2SiO3, CuO,
SO3;
Na2SO4, S, CuCl2;
BaO, H2SO4, FeCl2.
Na2SO4, S, CuCl2;
BaO, H2SO4, FeCl2.
Слайд 87. Необратимая химическая реакция произойдёт при сливании растворов веществ, формулы которых:
NaNO3
и H2SO4;
KOH и СaCl2;
СаСO3 и HCl;
BaCl2 и Ca(NO3)2.
KOH и СaCl2;
СаСO3 и HCl;
BaCl2 и Ca(NO3)2.
Слайд 1110. Взаимодействию гидроксида бария и хлороводорода соответствует краткое ионное уравнение
Ba2++2Cl-=BaCl2;
OH-+H+=H2O;
Ba2++2OH-+2H++2Cl-=Ba2+2Cl-+2H2O;
2OH-+2H+ =2H2O.
Слайд 12Часть Б. Задания со свободным ответом. 11. Составьте уравнения химических реакций между
веществами формулы которых:
K+ O2=;
K+H2O=;
K+H2SO4(разб)=;
K+Cl2=.
Слайд 1413. Дана схема превращений. Барий→Оксид бария→X→Карбонат бария Напишите молекулярные уравнения реакций, с
помощью которых можно осуществить указанные превращения. Для третьего превращения составьте сокращённое ионное уравнение реакции.
Слайд 1514. Задача ?
Повторить!
Строение атомов и ионов химических элементов;
Изменение свойств элементов по
периодам и группам элементов;
Формы существования веществ, аллотропия;
Классы соединений неорганических веществ;
Химические свойства изученных групп элементов;
Реакции ионного обмена;
Степени окисления и окислительно-восстановительные реакции;
Цепочки превращений неорганических веществ.
Формы существования веществ, аллотропия;
Классы соединений неорганических веществ;
Химические свойства изученных групп элементов;
Реакции ионного обмена;
Степени окисления и окислительно-восстановительные реакции;
Цепочки превращений неорганических веществ.