- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Основы органической химии. Углеводороды. Алкины презентация
Содержание
- 1. Основы органической химии. Углеводороды. Алкины
- 2. Алкины Алкины (ацетиленовые углеводороды) –
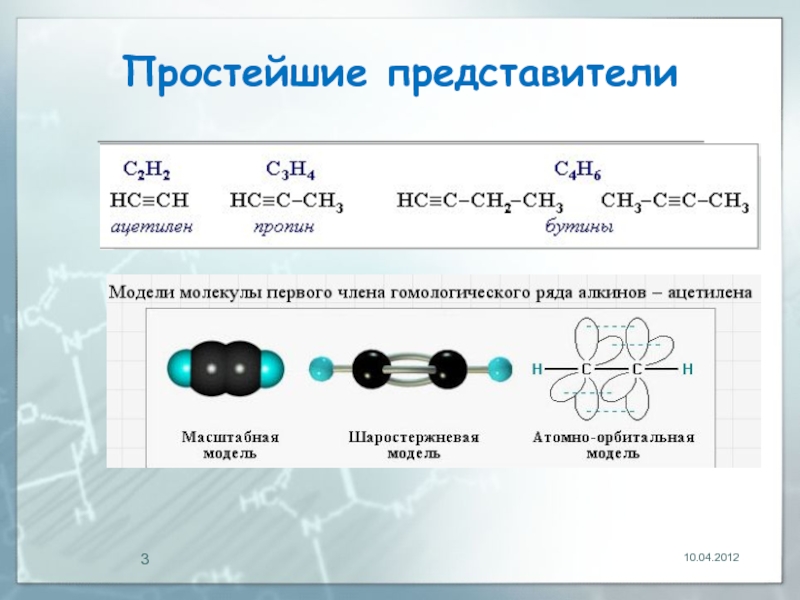
- 3. Простейшие представители 10.04.2012
- 4. Алкины Тройную связь осуществляют шесть общих
- 5. Строение С=С связи Каждый из атомовимеет по
- 6. Получение алкинов Получение и свойства ацетилена. Уравнения
- 7. Строение С≡С связи Тройная связь является комбинацией
- 8. Строение С≡С связи Образование связей в молекуле ацетилена можно изобразить следующей схемой: 10.04.2012
- 9. Строение С≡С связи π-Cвязи располагаются во взаимно
- 10. Номенклатура алкинов названия алкинов производят от названий
- 11. Номенклатура алкинов Нумерацию углеродных атомов начинают с
- 12. Номенклатура алкинов Для простейших алкинов применяются исторически
- 13. Номенклатура алкинов Если кроме тройной связи в
- 14. Назовите следующие алкины: CH2≡CH2 CH3—CH ≡ CH2
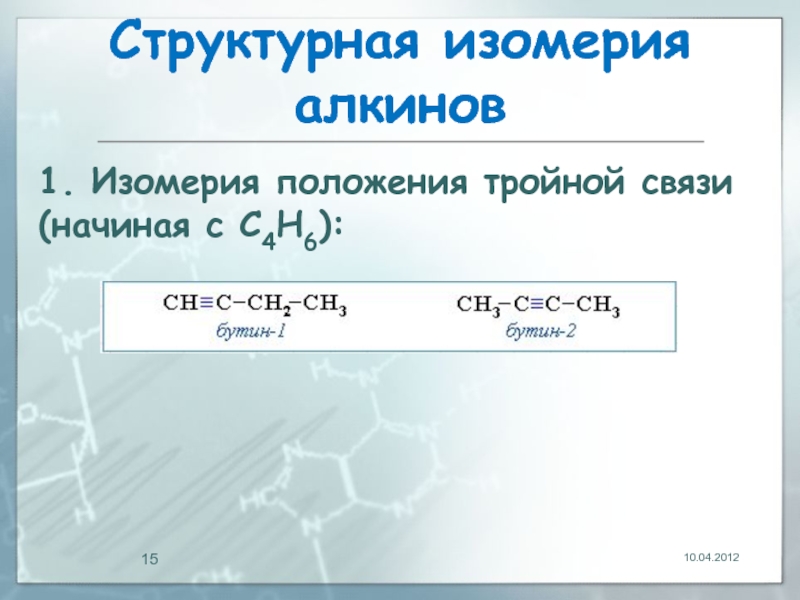
- 15. Структурная изомерия алкинов 10.04.2012 1. Изомерия положения тройной связи (начиная с С4Н6):
- 16. Структурная изомерия алкинов 10.04.2012 2. Изомерия углеродного скелета (начиная с С5Н8):
- 17. Структурная изомерия алкинов 10.04.2012 3. Межклассовая изомерия с алкадиенами и циклоалкенами, начиная с С4Н6:
- 18. Пространственная изомерия алкинов Пространственная изомерия относительно тройной
- 19. Физические свойства алкинов Температуры кипения и плавления
- 20. Физические свойства алкинов Температуры кипения и плавления алкинов выше, чем у соответствующих алкенов: 10.04.2012
- 21. Химические свойства алкинов сходны с алкенами, что обусловлено их ненасыщенностью: 10.04.2012
- 22. Гидрирование (присоединение водорода) В присутствии металлических
- 23. Галогенирование (присоединение галогенов) Электрофильное присоединение галогенов
- 24. Галогенирование (присоединение галогенов) Алкины обесцвечивают бромную воду (качественная реакция): 10.04.2012
- 25. Гидрогалогенирование (присоединение галогеноводородов) Присоединение галогеноводородов также идет
- 26. Гидрогалогенирование (присоединение галогеноводородов) Гидрохлорирование ацетилена используется в
- 27. Гидрогалогенирование (присоединение галогеноводородов) Реакция ускоряется в присутствии
- 28. Гидратация (реакция Кучерова) Присоединение воды происходит
- 29. Гидратация (присоединение воды) или в кетон
- 30. Полимеризация алкинов 1. Димеризация под действием водно-аммиачного раствора меди (CuCl): 10.04.2012
- 31. Полимеризация алкинов 2. Тримеризация ацетилена над активированным углем приводит к образованию бензола (реакция Зелинского): 10.04.2012
- 32. Полимеризация алкинов 3. Реакция полимеризации с образованием циклических или линейных молекул: 10.04.2012
- 33. Полимеризация алкинов 4. окислительная поликонденсация ацетилена в
- 34. Образование солей Алкины-1 вследствие полярности связи С(sp)-Н
- 35. Образование солей Если тройная связь находится не
- 36. Окисление алкинов Ацетилен и его гомологи окисляются
- 37. Окисление алкинов Алкины обесцвечивают раствор KMnO4, что используется для их качественного определения: 10.04.2012
- 38. Окисление алкинов При сгорании (полном окислении) ацетилена
- 39. Получение алкинов I. Термический крекинг (пиролиз) метана : 10.04.2012
- 40. Получение алкенов II. Отщепление (элиминирование) двух
- 41. Получение алкинов II. Гидролиз карбида кальция
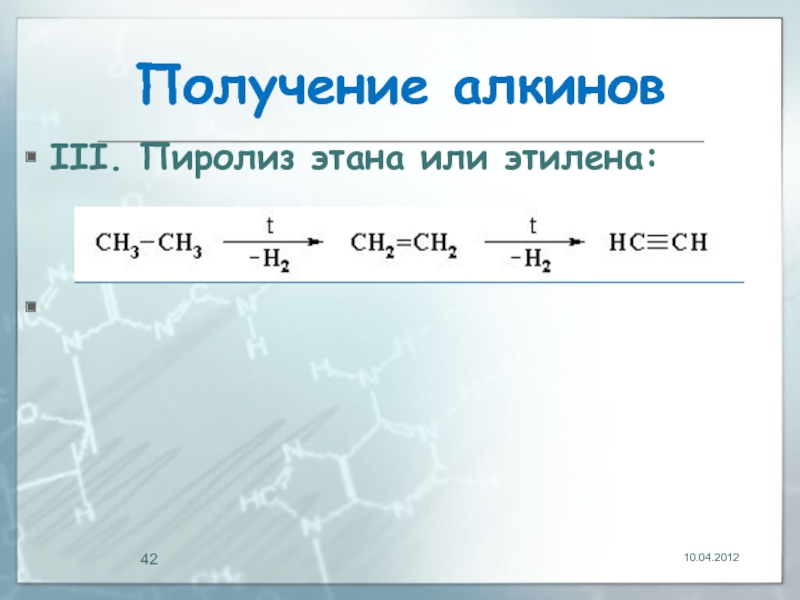
- 42. Получение алкинов III. Пиролиз этана или этилена: 10.04.2012
- 43. Применение алкинов Алкины применяются в качестве
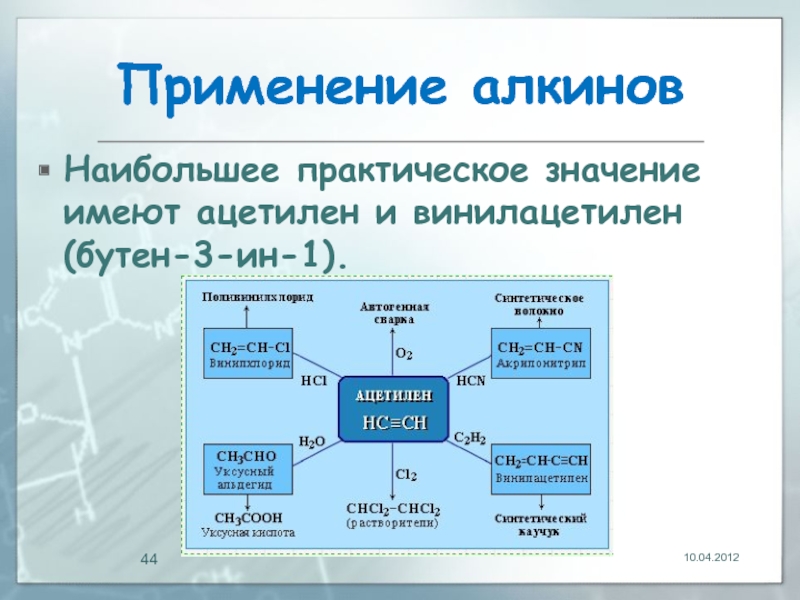
- 44. Применение алкинов Наибольшее практическое значение имеют ацетилен и винилацетилен (бутен-3-ин-1). 10.04.2012
- 45. Применение алкинов Винилацетилен является важным промежуточным
- 46. 1.Контрольная работа 10.04.2012 Назовите и нарисуйте приведенные
- 47. 2. Контрольная работа 10.04.2012 Дайте названия следующих
- 48. 3.Контрольная работа 10.04.2012 Тройная связь является сочетанием:
- 49. 4. Контрольная работа 10.04.2012 Какова гибридизация атомов
- 50. 5. Контрольная работа 10.04.2012 Изомерами 3-метилпентина-1 являются:
- 51. 6. Контрольная работа 10.04.2012 Взрывчатое вещество образуется
- 52. 7. Контрольная работа 10.04.2012 Из технического карбида
- 53. 8. Контрольная работа 10.04.2012 Укажите продукт Z
- 54. Сравните получение алканов, алкенов, алкинов, проанализировав видеоролики из папки «Лабораторные опыты». 10.04.2012
- 55. Получение алканов Получение и свойства метана
- 56. Получение алканов Получение и свойства метана. Уравнения
- 57. Свойства алканов Взаимодействия алканов с бромом. Уравнения
- 58. Получение алкенов Получение и свойства этилена. Уравнения
- 59. Получение алкинов Получение и свойства ацетилена. Уравнения
Слайд 1Основы органической химии
Семинар-9. Углеводороды.Алкины
E-mail: irkrav66@gmail.com
лектор:
проф. Рохин Александр
Слайд 2Алкины
Алкины (ацетиленовые углеводороды) – непредельные алифатические углеводороды, молекулы которых
Общая формула алкинов:
10.04.2012
Слайд 4Алкины
Тройную связь осуществляют шесть общих электронов:
В образовании тройной связи
10.04.2012
Слайд 5Строение С=С связи
Каждый из атомовимеет по три 2sp2-гибридных орбитали, направленных друг
10.04.2012
Слайд 6Получение алкинов
Получение и свойства ацетилена.
Уравнения реакций:
(видеоролик exp5.exe в папке лабораторные опыты)
Опишите
10.04.2012
Слайд 7Строение С≡С связи
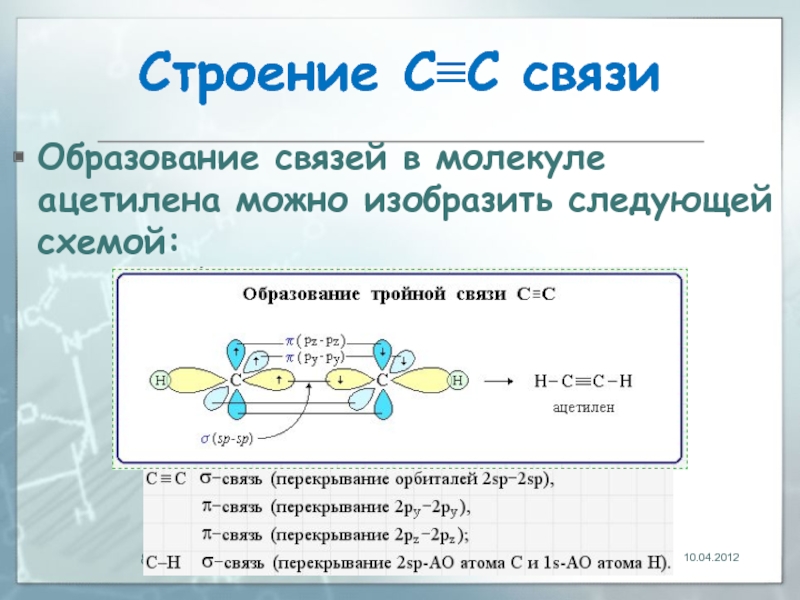
Тройная связь является комбинацией из одной σ-и двух π-связей,
σ-связь возникает при осевом перекрывании sp-гибридных орбиталей соседних атомов углерода; одна из π -связей образуется при боковом перекрывании рy-орбиталей, другая – при боковом перекрывании рz-орбиталей.
10.04.2012
Слайд 8Строение С≡С связи
Образование связей в молекуле ацетилена можно изобразить следующей схемой:
10.04.2012
Слайд 9Строение С≡С связи
π-Cвязи располагаются во взаимно перпендикулярных плоскостях.
σ-Cвязи, образуемые sp–гибридными
Поэтому молекула ацетилена имеет линейное строение:
10.04.2012
Слайд 10Номенклатура алкинов
названия алкинов производят от названий соответствующих алканов (путем замены суффикса
2 атома С → этан → этин; 3 атома С →пропан → пропин
Главная цепь выбирается таким образом, чтобы она обязательно включала в себя тройную связь.
10.04.2012
Слайд 11Номенклатура алкинов
Нумерацию углеродных атомов начинают с ближнего к тройной связи конца
Цифра, обозначающая положение тройной связи, ставится обычно после суффикса –ин.
Например:
10.04.2012
Слайд 12Номенклатура алкинов
Для простейших алкинов применяются исторически сложившиеся названия: ацетилен (этин), аллилен
В номенклатуре наиболее часто используются следующие одновалентные радикалы алкинов:
10.04.2012
Слайд 13Номенклатура алкинов
Если кроме тройной связи в молекуле есть двойные связи, то
10.04.2012
Слайд 14Назовите следующие алкины:
CH2≡CH2
CH3—CH ≡ CH2
CH3—CH3—CH ≡ CH2
CH3—CH ≡ CH—CH3
CH2 ≡ CH—CH=CH2
CH3—CH
|
CH3
10.04.2012
Слайд 17Структурная изомерия алкинов
10.04.2012
3. Межклассовая изомерия с алкадиенами и циклоалкенами, начиная с
Слайд 18Пространственная изомерия алкинов
Пространственная изомерия относительно тройной связи в алкинах не проявляется,
10.04.2012
Слайд 19Физические свойства алкинов
Температуры кипения и плавления ацетиленовых углеводородов увеличиваются с ростом
При обычных условиях алкины С2Н2-С4Н6 – газы, С5Н8-С16Н30 – жидкости, с С17Н32 – твердые вещества.
Алкины плохо растворимы в воде, лучше – в органических растворителях.
10.04.2012
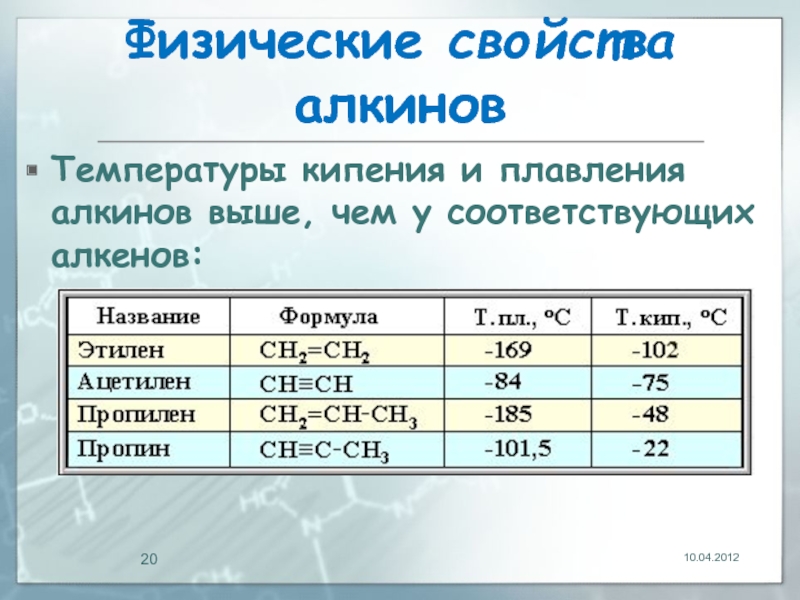
Слайд 20Физические свойства алкинов
Температуры кипения и плавления алкинов выше, чем у соответствующих
10.04.2012
Слайд 22Гидрирование
(присоединение водорода)
В присутствии металлических катализаторов (Pt, Ni) алкины присоединяют водород
10.04.2012
Слайд 23Галогенирование
(присоединение галогенов)
Электрофильное присоединение галогенов к алкинам протекает медленнее, чем для
10.04.2012
Слайд 24Галогенирование
(присоединение галогенов)
Алкины обесцвечивают бромную воду (качественная реакция):
10.04.2012
Слайд 25Гидрогалогенирование (присоединение галогеноводородов)
Присоединение галогеноводородов также идет по электрофильному механизму.
Продукты присоединения
10.04.2012
Слайд 26Гидрогалогенирование (присоединение галогеноводородов)
Гидрохлорирование ацетилена используется в одном из промышленных способов получения
Винилхлорид является исходным веществом (мономером) в производстве поливинилхлорида (ПВХ).
10.04.2012
Слайд 27Гидрогалогенирование (присоединение галогеноводородов)
Реакция ускоряется в присутствии катализаторов (соли ртути или меди)
10.04.2012
Слайд 28Гидратация
(реакция Кучерова)
Присоединение воды происходит в присутствии катализатора соли ртути (II)
10.04.2012
Слайд 29Гидратация
(присоединение воды)
или в кетон (в случае других алкинов) по нуклеофильному
10.04.2012
Слайд 30Полимеризация алкинов
1. Димеризация под действием водно-аммиачного раствора меди (CuCl):
10.04.2012
Слайд 31Полимеризация алкинов
2. Тримеризация ацетилена над активированным углем приводит к образованию бензола
10.04.2012
Слайд 32Полимеризация алкинов
3. Реакция полимеризации с образованием циклических или линейных молекул:
10.04.2012
Слайд 33Полимеризация алкинов
4. окислительная поликонденсация ацетилена в присутствии CuCl (высокомолекулярное вещество –
10.04.2012
Слайд 34Образование солей
Алкины-1 вследствие полярности связи С(sp)-Н проявляют слабые кислотные свойства: атомы
При этом образуются соли – ацетилениды:
10.04.2012
Слайд 35Образование солей
Если тройная связь находится не на конце цепи, то кислотные
10.04.2012
Слайд 36Окисление алкинов
Ацетилен и его гомологи окисляются перманганатом калия с расщеплением тройной
10.04.2012
Слайд 37Окисление алкинов
Алкины обесцвечивают раствор KMnO4, что используется для их качественного определения:
10.04.2012
Слайд 38Окисление алкинов
При сгорании (полном окислении) ацетилена выделяется большое количества тепла:
Температура ацетиленово-кислородного
10.04.2012
Слайд 40Получение алкенов
II. Отщепление (элиминирование) двух атомов или групп атомов от
дегидратация
дегидрогалогенирование
10.04.2012
Слайд 41Получение алкинов
II. Гидролиз карбида кальция :
Карбид кальция образуется при нагревании
10.04.2012
Слайд 43Применение алкинов
Алкины применяются в качестве исходных продуктов в производстве полимерных
10.04.2012
Слайд 44Применение алкинов
Наибольшее практическое значение имеют ацетилен и винилацетилен (бутен-3-ин-1).
10.04.2012
Слайд 45Применение алкинов
Винилацетилен является важным промежуточным продуктом в производстве масло- и
10.04.2012
Слайд 461.Контрольная работа
10.04.2012
Назовите и нарисуйте приведенные соединения. Какие из них относятся к
а)
б)
в)
г)
д)
Слайд 472. Контрольная работа
10.04.2012
Дайте названия следующих алкинов, полученных из алканов:
- бутан
- октан
- пропан
- пентан
- гексан
Слайд 483.Контрольная работа
10.04.2012
Тройная связь является сочетанием:
Ответ 1 : трех σ-связей
Ответ 2
Слайд 494. Контрольная работа
10.04.2012
Какова гибридизация атомов углерода в следующей молекуле:
Ответ 1 :
Слайд 505. Контрольная работа
10.04.2012
Изомерами 3-метилпентина-1 являются:
Ответ 1 : а, в, д
Ответ
Слайд 516. Контрольная работа
10.04.2012
Взрывчатое вещество образуется в реакции:
Ответ 1 :
Ответ 2
Слайд 527. Контрольная работа
10.04.2012
Из технического карбида кальция массой 1 кг получен ацетилен
Слайд 538. Контрольная работа
10.04.2012
Укажите продукт Z в схеме превращений:
Ответ 1 : а
Слайд 54Сравните получение алканов, алкенов, алкинов, проанализировав видеоролики из папки «Лабораторные опыты».
10.04.2012
Слайд 55Получение алканов
Получение и свойства метана
(видеоролик exp3.exe в папке лабораторные опыты)
10.04.2012
Слайд 56Получение алканов
Получение и свойства метана.
Уравнения реакций:
Опишите роль каждого реактива в опытах
10.04.2012
Слайд 57Свойства алканов
Взаимодействия алканов с бромом.
Уравнения реакций:
(видеоролик exp2.exe в папке лабораторные опыты)
Опишите
10.04.2012
Слайд 58Получение алкенов
Получение и свойства этилена.
Уравнения реакций:
(видеоролик exp4.exe в папке лабораторные опыты)
Опишите
10.04.2012
Слайд 59Получение алкинов
Получение и свойства ацетилена.
Уравнения реакций:
(видеоролик exp5.exe в папке лабораторные опыты)
Опишите
10.04.2012