- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Основы органической химии презентация
Содержание
- 1. Основы органической химии
- 2. Взаимное влияние атомов Взаимное влияние атомов в
- 3. Заместители - 04.03.2016 любой атом (кроме
- 4. Электронные эффекты 04.03.2016 Смещение электронной плотности в
- 5. Электронодонорные заместители атомная группировка (или атом), повышающая электронную плотность на остальной части молекулы 04.03.2016
- 6. Электроноакцепторные заместители атомная группировка (или атом), понижающая
- 7. Электроноакцепторные заместители Два вида влияний заместителей: индуктивный
- 8. Индуктивный эффект Передача по цепи сигма-связей электронного
- 9. Индуктивный эффект Направление смещения электронной плотности σ-связей
- 10. Индуктивный эффект Из-за слабой поляризуемости σ-связей I-эффект
- 11. -I-эффект Проявляет заместитель, уменьшающий электронную плотность Заместитель
- 12. Определение -I-эффекта 04.03.2016
- 13. +I-эффект Проявляет заместитель, увеличива-ющий электронную плотность Заместитель
- 14. Определение +I-эффекта 04.03.2016
- 15. Мезомерный эффект Передача электронного влияния заместителей по
- 16. Мезомерный эффект Графически изображают изогнутыми стрелками. В
- 17. Правила определения величины и знака М-эффекта 04.03.2016
- 18. Правило 1. Величина М-эффекта растет с увеличением
- 19. Правило 2 -М-эффект заместителей тем сильнее, чем больше электроотрицательность имеющихся в заместителе элементов: 04.03.2016
- 20. Правило 3 -М-эффект заместителей тем сильнее, чем
- 21. Правило 3 Группа С=О в этом случае
- 22. Правило 3 В хлорацильной группе -С(О)Cl атом
- 23. Правило 4 +М-эффект заместителя тем сильнее, чем меньше электроотрицательность гетероатома, входящего в его состав: 04.03.2016
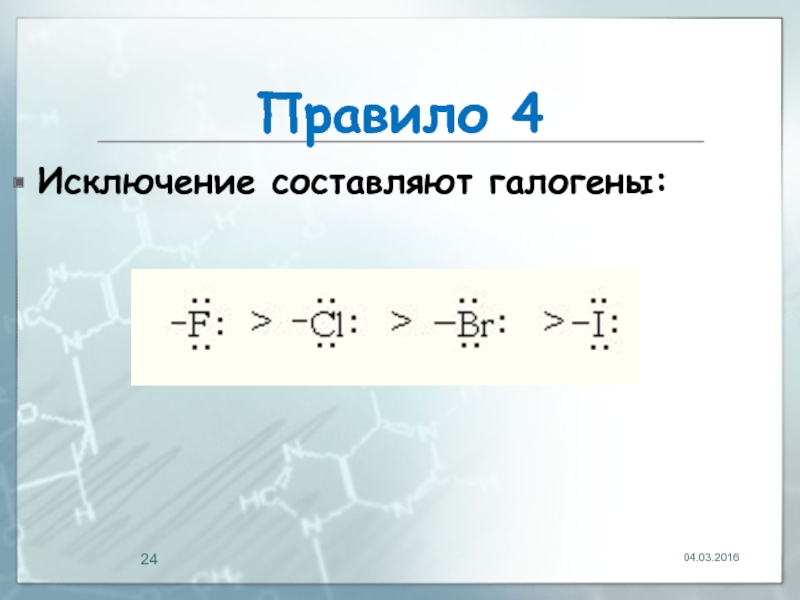
- 24. Правило 4 Исключение составляют галогены: 04.03.2016
- 25. Правило 4 Причина этого явления заключается в
- 26. +М-эффект Характерен для групп:-OH, -NH2, -OR. В
- 27. -М-эффект Характерен для групп СOH, СООН, NО2.
- 28. Суммарный электронный эффект В случае противоположной направленности
- 29. Суммарный электронный эффект в молекуле анилина аминогруппа
- 30. Суммарный электронный эффект аминогруппа является электроно-донорным заместителем,
- 31. Суммарный электронный эффект Аналогичная ситуация (+М >
- 32. Суммарный электронный эффект В случае галогенов, напротив,
- 33. Суммарный электронный эффект 04.03.2016
- 34. Пространственные эффекты (стерические) эффекты определяют доступность реакционных
- 35. Пространственные эффекты Скорость реакции присоединения по С=О-группе снижается в ряду: 04.03.2016
- 36. Эффект сверхсопряжения Группа метил CH3 (в меньшей
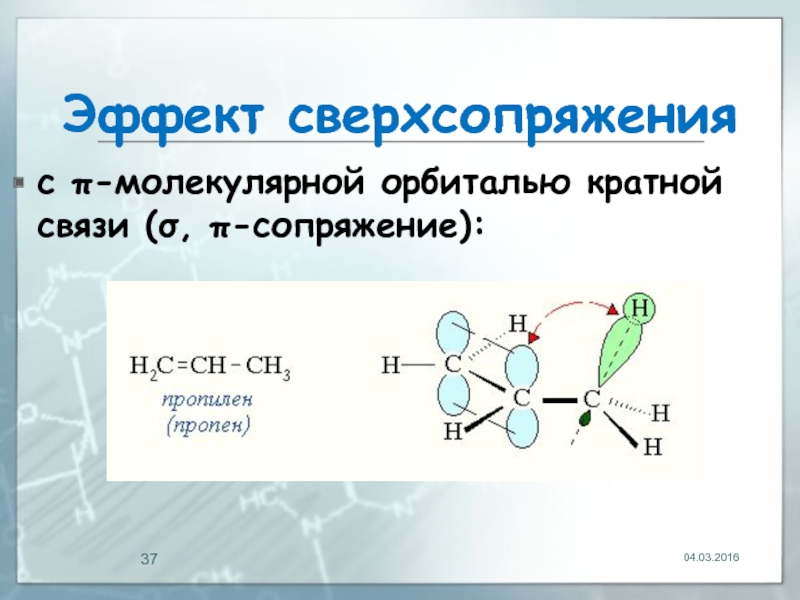
- 37. Эффект сверхсопряжения с π-молекулярной орбиталью кратной связи (σ, π-сопряжение): 04.03.2016
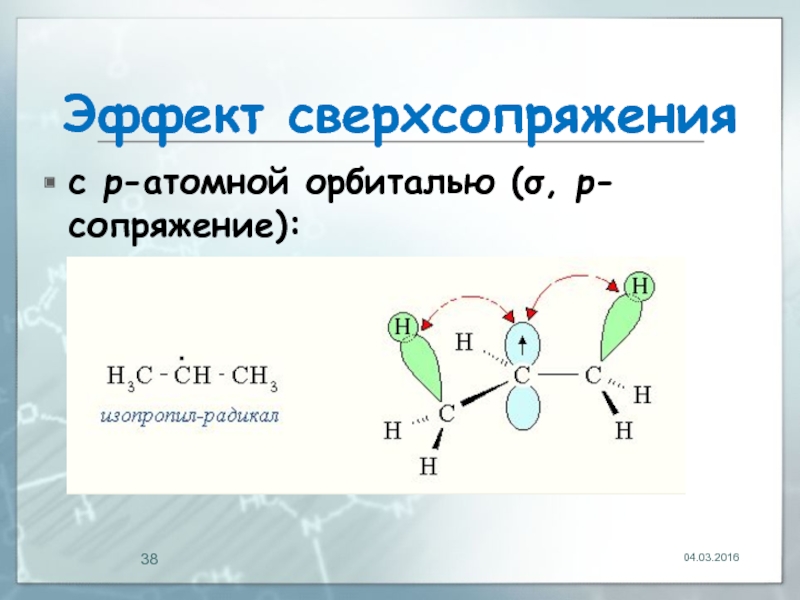
- 38. Эффект сверхсопряжения с р-атомной орбиталью (σ, р-сопряжение): 04.03.2016
- 39. Эффект сверхсопряжения Графически эффект сверхсопряжения обозначается изогнутой
- 40. Эффект сверхсопряжения Направление стрелки показывает смещение σ-электронов
- 41. Эффект сверхсопряжения сверхсопряжение является слабым эффектом,
- 42. Эффект сверхсопряжения Именно этим фактором, в частности, объясняется увеличение устойчивости свободных радикалов в ряду: 04.03.2016
- 43. Эффект сверхсопряжения В той же последовательности возрастает
- 44. Эффект сверхсопряжения Наибольшая стабильность трет-бутил-катиона +C(CH3)3 объясняется
- 45. 1.Контрольная работа 04.03.2016
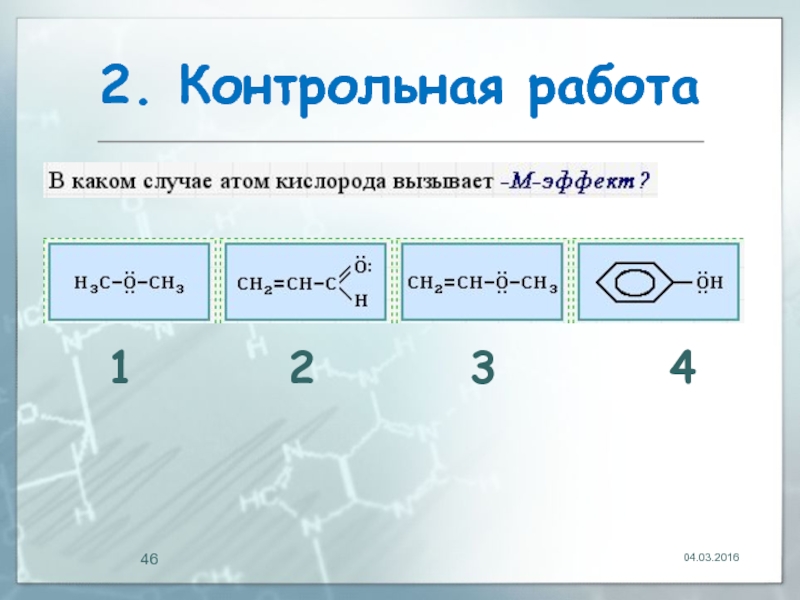
- 46. 2. Контрольная работа 04.03.2016 1
- 47. 3.Контрольная работа 04.03.2016
- 48. 4. Контрольная работа 04.03.2016
- 49. 5. Контрольная работа К какому типу органических
- 50. 6. Контрольная работа Функциональной группой фенолов является
- 51. 7. Контрольная работа Какие из приведенных соединений
Слайд 1Основы органической химии
Семинар-4. Взаимное влияние атомов
E-mail: irkrav66@gmail.com
лектор:
проф. Рохин Александр
Слайд 2Взаимное влияние атомов
Взаимное влияние атомов в молекуле, ионе, радикале осуществляется под
Это позволяет определить реакционную способность органических соединений.
04.03.2016
Слайд 3Заместители -
04.03.2016
любой атом (кроме водорода), который непосредственно не участвует в
Слайд 4Электронные эффекты
04.03.2016
Смещение электронной плотности в молекуле, ионе, радикале под влияние заместителей,
- электронодонорные;
- электроноакцепторные.
Слайд 5Электронодонорные заместители
атомная группировка (или атом), повышающая электронную плотность на остальной части
04.03.2016
Слайд 6Электроноакцепторные заместители
атомная группировка (или атом), понижающая электронную плотность на связанном с
04.03.2016
Слайд 7Электроноакцепторные заместители
Два вида влияний заместителей:
индуктивный эффект (±I);
мезомерный эффект (±M).
В зависимости от
04.03.2016
Слайд 8Индуктивный эффект
Передача по цепи сигма-связей электронного влияния заместителей, которое обусловлено различиями
04.03.2016
Слайд 9Индуктивный эффект
Направление смещения электронной плотности σ-связей обозначается стрелками и символами частичных
04.03.2016
Слайд 10Индуктивный эффект
Из-за слабой поляризуемости σ-связей I-эффект быстро ослабевает с удалением заместителя
В зависимости от смещения наблюдают положительные +I-эффекты и отрицательные -I-эффекты.
I-эффект водорода равен нулю.
04.03.2016
Слайд 11-I-эффект
Проявляет заместитель, уменьшающий электронную плотность
Заместитель приобретает частичный отрицательный заряд, атом углерода
04.03.2016
Слайд 13+I-эффект
Проявляет заместитель, увеличива-ющий электронную плотность
Заместитель приобретает частичный положительный заряд, атом углерода
04.03.2016
Слайд 15Мезомерный эффект
Передача электронного влияния заместителей по сопряжённой π-системе.
Благодаря подвижности π-электронов передаётся
04.03.2016
Слайд 16Мезомерный эффект
Графически изображают изогнутыми стрелками.
В зависимости от направления смещения электронной плотности
Величина эффекта определяется рядом правил.
04.03.2016
Слайд 18Правило 1.
Величина М-эффекта растет с увеличением заряда заместителя.
Ионы проявляют наиболее
04.03.2016
Слайд 19Правило 2
-М-эффект заместителей тем сильнее, чем больше электроотрицательность имеющихся в заместителе
04.03.2016
Слайд 20Правило 3
-М-эффект заместителей тем сильнее, чем меньше их внутренняя мезомерия (делокализация
04.03.2016
Слайд 21Правило 3
Группа С=О в этом случае связана с группировками, +М-эффект которых
04.03.2016
Слайд 22Правило 3
В хлорацильной группе -С(О)Cl атом хлора проявляет +М-эффект, однако он
мезомерное взаимодействие невелико вследствие относительно малой степени перекрывания существенно различаю-щихся орбиталей – 2р-АО sp2-гибридизованного атома углерода и 3р-АО хлора
04.03.2016
Слайд 23Правило 4
+М-эффект заместителя тем сильнее, чем меньше электроотрицательность гетероатома, входящего в
04.03.2016
Слайд 25Правило 4
Причина этого явления заключается в том, что эффективность перекрывания 2р-АО
04.03.2016
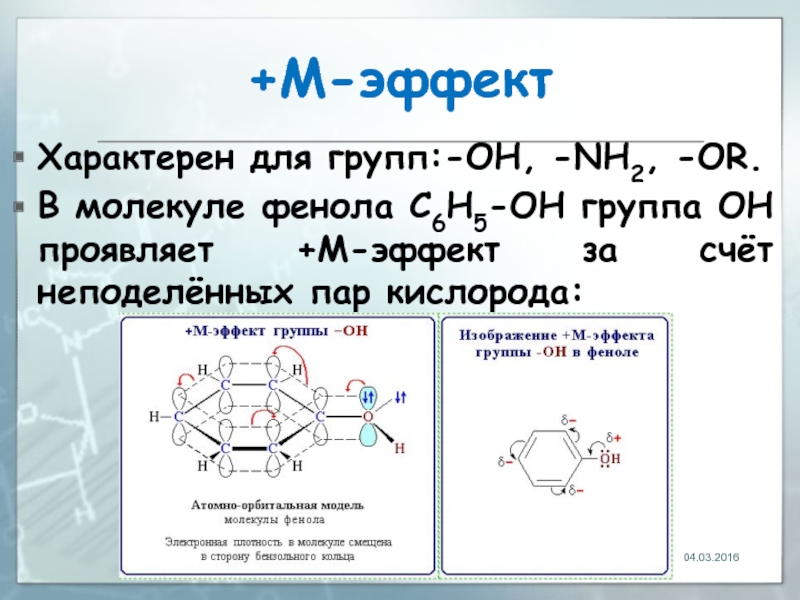
Слайд 26+М-эффект
Характерен для групп:-OH, -NH2, -OR.
В молекуле фенола C6H5-OH группа ОН проявляет
04.03.2016
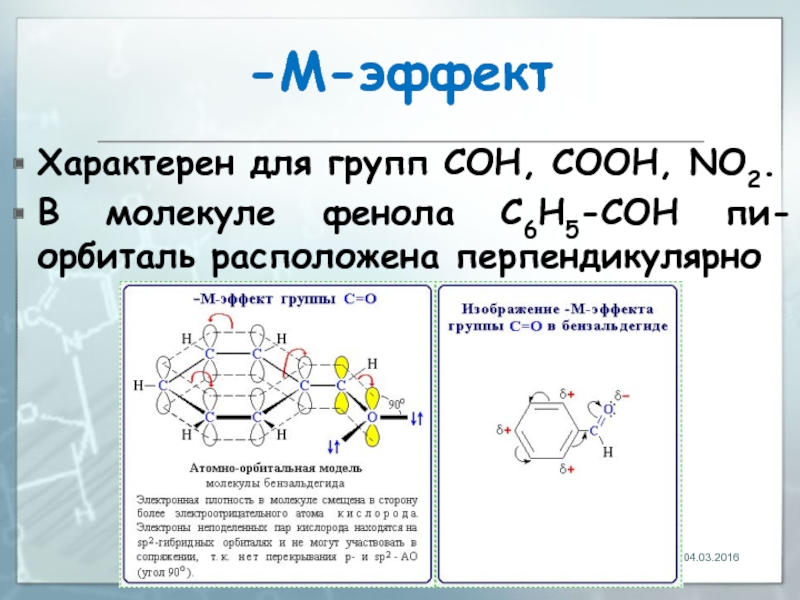
Слайд 27-М-эффект
Характерен для групп СOH, СООН, NО2.
В молекуле фенола C6H5-СOH пи-орбиталь расположена
04.03.2016
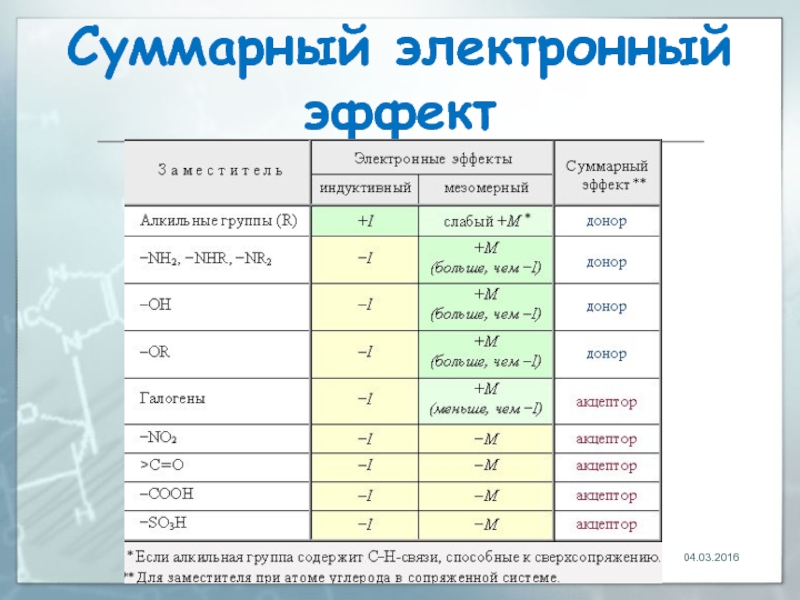
Слайд 28Суммарный электронный эффект
В случае противоположной направленности индуктивного и мезомерного эффектов общее
04.03.2016
Слайд 29Суммарный электронный эффект
в молекуле анилина аминогруппа NH2 одновременно проявляет -I-эффект (за
04.03.2016
Слайд 30Суммарный электронный эффект
аминогруппа является электроно-донорным заместителем, т.к. преобладает более сильный +М-эффект.
отрицательный I-эффект относительно слаб:
04.03.2016
Слайд 31Суммарный электронный эффект
Аналогичная ситуация (+М > -I) характерна для групп:
-NHR,
04.03.2016
Слайд 32Суммарный электронный эффект
В случае галогенов, напротив, преобладает -I-эффект, поскольку, кроме максимально
04.03.2016
Слайд 34Пространственные эффекты
(стерические) эффекты определяют доступность реакционных центров в молекуле.
Объёмные группы могут
04.03.2016
Слайд 35Пространственные эффекты
Скорость реакции присоединения по С=О-группе снижается в ряду:
04.03.2016
Слайд 36Эффект сверхсопряжения
Группа метил CH3 (в меньшей степени, CH2R и СHR2), связанная
Этот эффект обусловлен перекрыванием s-молекулярной орбитали связи С-Н .
04.03.2016
Слайд 39Эффект сверхсопряжения
Графически эффект сверхсопряжения обозначается изогнутой стрелкой, охватывающей С-Н связи и
04.03.2016
Слайд 40Эффект сверхсопряжения
Направление стрелки показывает смещение σ-электронов связи С-Н в сторону кратной
метильная группа при sp2- (или sp-) атоме проявляет электронодонорные свойства не только за счет +I-эффекта, но и в результате сверхсопряжения.
04.03.2016
Слайд 41Эффект сверхсопряжения
сверхсопряжение является слабым эффектом,
но его роль в стабилизации вторичных
04.03.2016
Слайд 42Эффект сверхсопряжения
Именно этим фактором, в частности, объясняется увеличение устойчивости свободных радикалов
04.03.2016
Слайд 43Эффект сверхсопряжения
В той же последовательности возрастает устойчивость карбокатионов, которая обусловлена как
04.03.2016
Слайд 44Эффект сверхсопряжения
Наибольшая стабильность трет-бутил-катиона +C(CH3)3 объясняется не только действием +I-эффекта, но
04.03.2016
Слайд 495. Контрольная работа
К какому типу органических соединений относится хлоропрен (вещество для
04.03.2016
Ответ 1: к непредельным алициклическим
Ответ 2: к непредельным ациклическим
Ответ 3: к предельным алифатическим
Ответ 4: к непредельным гетероциклическим
Слайд 506. Контрольная работа
Функциональной группой фенолов является . . .
04.03.2016
Ответ 1: группа
Слайд 517. Контрольная работа
Какие из приведенных соединений относятся к классу:
а) спиртов; б) карбоновых
04.03.2016
I. C3H7OH; II. CH3CHO;
III. CH3COOH; IV. CH3NO2
Ответ 1 : а) III; б) IV
Ответ 2 : а) I; б) II
Ответ 3 : а) II; б) I
Ответ 4 : а) I; б) III