- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Основные понятия и законы химии презентация
Содержание
- 1. Основные понятия и законы химии
- 2. План занятия: Основные понятия и законы химии
- 3. Что такое химия? Химия – наука о веществах, их строении, свойствах и превращениях.
- 4. Что такое вещество? Физические свойства вещества: агрегатное
- 5. Что такое вещество? Агрегатное состояние:
- 6. Что такое вещество? Физические явления – это
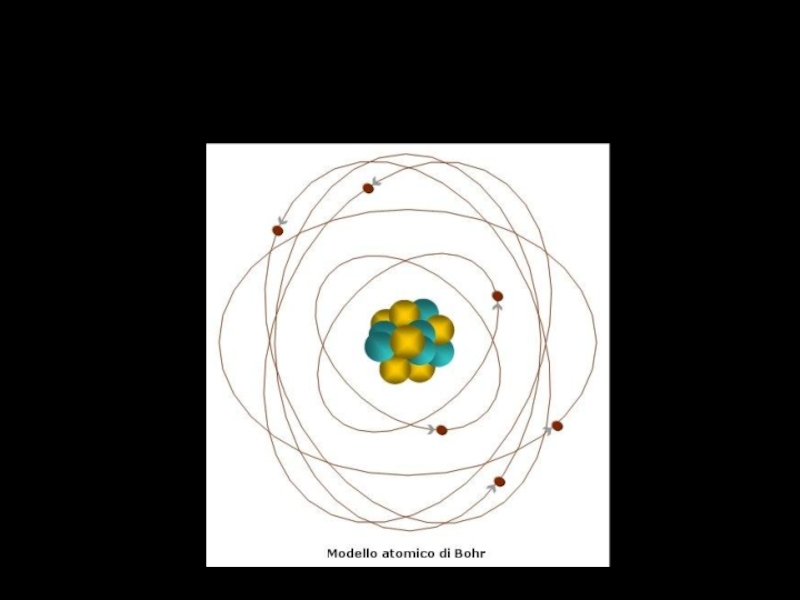
- 7. Строение атома.
- 8. Строение атома. ЯДРО: Протон – частица, которая
- 9. Строение атома.
- 10. Строение атома. Вокруг ядра движутся электроны, которые
- 11. Строение атома. Главная характеристика любого атома –
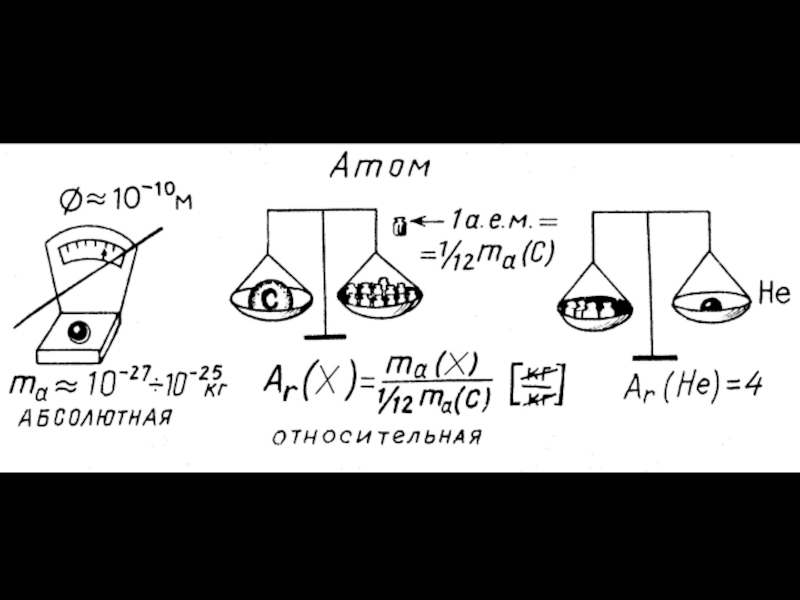
- 12. Размеры и массы атомов. Размеры: выражаются ангстремами
- 13. Размеры и массы атомов. Массы: Абсолютная атомная масса
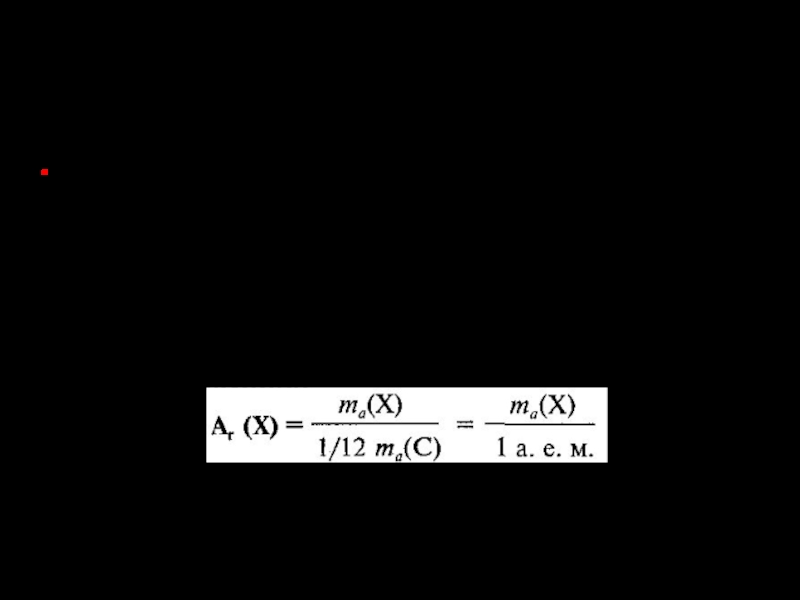
- 14. Размеры и массы атомов. Относительная атомная масса:
- 15. Размеры и массы атомов. Сейчас массы атомов
- 16. Размеры и массы атомов.
- 17. Размеры и массы атомов. Относительная атомная масса
- 19. Размеры и массы атомов. Рассчитайте относительные атомные
- 20. Размеры и массы атомов. Решение:
Слайд 2План занятия:
Основные понятия и законы химии
Вещество и его свойства.
Строение атома.
Размеры и
массы атомов.
Слайд 4Что такое вещество?
Физические свойства вещества: агрегатное состояние, плотность, растворимость, температура плавления,
температура кипения, цвет, вкус, запах.
Химические свойства вещества – это способность данного вещества превращаться в другие вещества.
Химические свойства вещества – это способность данного вещества превращаться в другие вещества.
Слайд 6Что такое вещество?
Физические явления – это изменение формы или агрегатного состояния
веществ, в результате которых не образуются новые вещества.
Химические явления – превращение одних веществ в другие.
Химические явления – превращение одних веществ в другие.
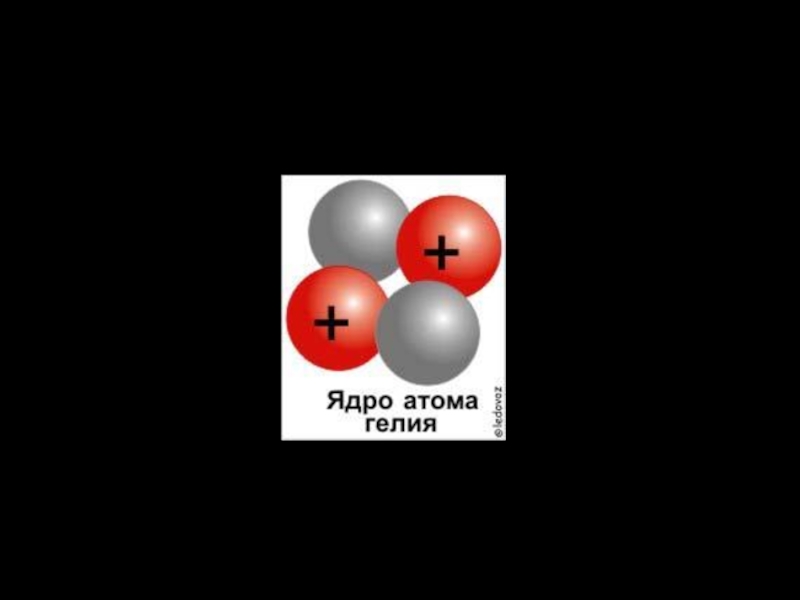
Слайд 8Строение атома.
ЯДРО:
Протон – частица, которая имеет положительный заряд. Заряд протона в
условных единицах равен +1.
Нейтрон – нейтральная частица, заряд нейтрона равен 0.
Протоны и нейтроны называются нуклонами.
Ядра атомов имеют положительный заряд.
Нейтрон – нейтральная частица, заряд нейтрона равен 0.
Протоны и нейтроны называются нуклонами.
Ядра атомов имеют положительный заряд.
Слайд 10Строение атома.
Вокруг ядра движутся электроны, которые имеют отрицательный заряд. Заряд электрона
в условных единицах равен -1.
Слайд 11Строение атома.
Главная характеристика любого атома – заряд ядра, который равен числу
протонов.
Вид атомов с одинаковым зарядом ядра называется химическим элементом.
Вид атомов с одинаковым зарядом ядра называется химическим элементом.
Слайд 12Размеры и массы атомов.
Размеры: выражаются ангстремами и нанометрами.
Диаметр атома водорода равен:
В
ангстремах и нанометрах:
Слайд 14Размеры и массы атомов.
Относительная атомная масса:
Масса атома U 0, 000 000
000 000 000 000 000 4 г
или 4*10-2
По массе атома можно судить сравнивая ее с массой другого атома.
или 4*10-2
По массе атома можно судить сравнивая ее с массой другого атома.
Размеры и массы атомов.
Слайд 15Размеры и массы атомов.
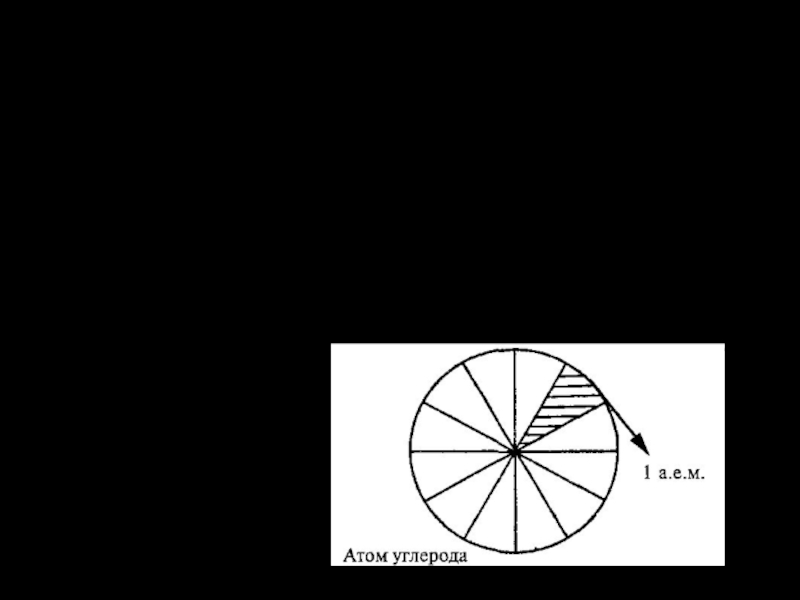
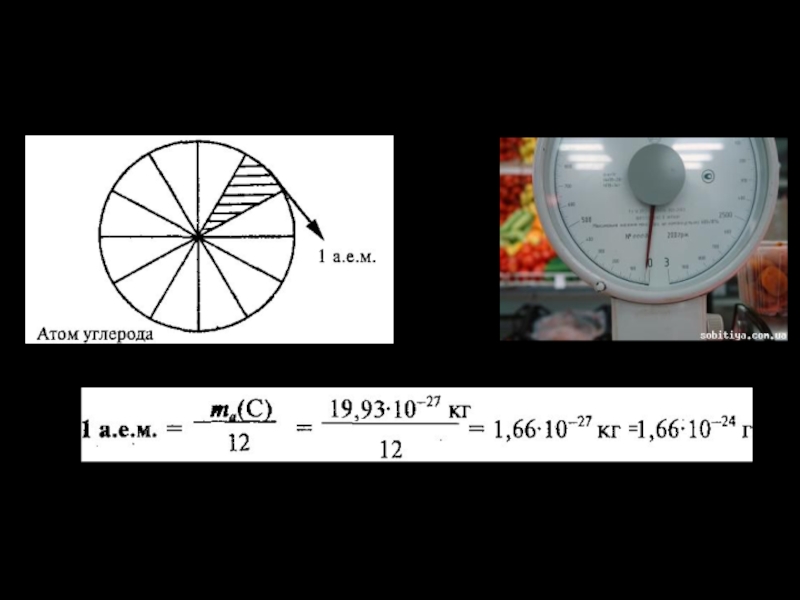
Сейчас массы атомов сравнивают с 1/12 массы атома
углерода.
а. е. м. – это 1/12 часть абсолютной массы атома углерода.
а. е. м. – это 1/12 часть абсолютной массы атома углерода.
Слайд 17Размеры и массы атомов.
Относительная атомная масса – это число, которое показывает,
во сколько раз абсолютная масса атома данного элемента больше 1/12 части абсолютной массы атома углерода, т. е. атомной единице массы.
Слайд 19Размеры и массы атомов.
Рассчитайте относительные атомные массы водорода и кислорода:
абсолютная масса
атома Н = 1,67*10-27кг
абсолютная масса атома О = 26,67*10-27кг
абсолютная масса атома О = 26,67*10-27кг