Слайд 1 ОРГАНИЧЕСКАЯ ХИМИЯ
Лекция
Гидроксикислоты.
Классификация. Номенклатура. Отдельные представители
Общие химические свойства
гидроксикислот (свойства карбоновых кислот и спиртов).
Специфические свойства алифатических гидроксикислот (отношение к нагреванию).
Фенолокислоты. Салициловая кислота и фармпрепараты на ее основе.
Лектор: кандидат биологических наук, доцент
Атавина Ольга Васильевна
ОМСКАЯ ГОСУДАРСТВЕННАЯ МЕДИЦИНСКАЯ АКАДЕМИЯ
КАФЕДРА ХИМИИ
Слайд 2Цели лекции:
Обучающая - Сформировать знания о строении, номенклатуре и реакционной способности
гидроксикислот.
Развивающая – Расширить кругозор обучающихся на основе интеграции знаний; развивать логическое мышление.
Воспитательная – Содействовать формированию у обучающихся устойчивого интереса к изучению дисциплины «Органическая химия»
Слайд 3Классификация. Номенклатура.
Гидроксикислоты – производные карбоновых кислот, у которых один или несколько
атомов водорода в радикале замещены на гидроксильную группу –ОН.
Классификация.
В зависимости от строения радикала различают алифатические (спиртокислоты) и ароматические(фенолокислоты)
По взаимному расположению карбоксильных и гидроксильных групп различают α, β, γ, δ и т.д. гидроксикислоты
По количеству карбоксильных групп различают основность гидроксикислот (одно-, двух-, трехосновные)
По количеству гидроксильных групп различают атомность гидроксикислот (одно-, двух-, трех-, четырехатомные)
Слайд 4Классификация. Номенклатура.
Номенклатура.
По заместительной номенклатуре ИЮПАК название производят от названия соответствующей карбоновой
кислоты с префиксом «гидрокси», отмечая положение ОН-группы арабской цифрой.
Используют тривиальные названия
Используют локанты α, β, γ и т.д. (в настоящее время применяется редко).
Слайд 5Отдельные представители
Отдельные представители:
1. Молочная кислота (2-гидроксипропановая кислота,
α-гидроксипропионовая кислота)
Алифатическая, одноосновная,
двухатомная.
Соли – лактаты.
Молочная кислота образуется в результате молочнокислого брожения углеводов, содержится в кислом молоке, квашеной капусте, различных солениях. L(+) молочная кислота при интенсивной физической работе накапливается в мышцах.
Лактаты кальция и железа(II) применяются в качестве лекарственных препаратов при заболевания, связанных с недостатком кальция в организме и при анемиях.
Слайд 6Отдельные представители
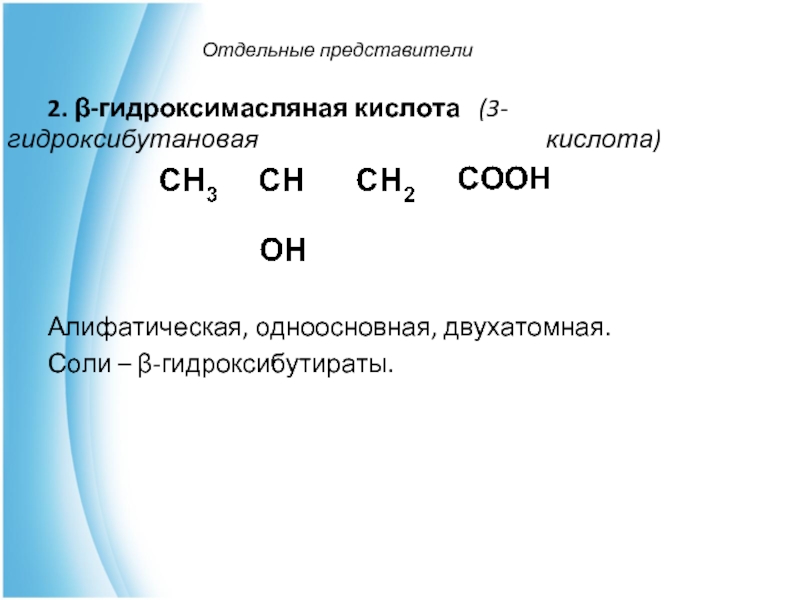
2. β-гидроксимасляная кислота (3-гидроксибутановая кислота)
Алифатическая,
одноосновная, двухатомная.
Соли – β-гидроксибутираты.
Слайд 7Отдельные представители
3. Яблочная кислота (2-гидроксибутандиовая кислота,
α-гидроксиянтарная кислота)
Алифатическая, двухосновная, трехатомная.
Соли – малаты.
Содержится
в незрелых яблоках, ягодах рябины, клюквы, малины.
В природе встречается L(-) яблочная кислота. В живых организмах образуется в процессе обмена углеводов, принимает участие в цикле трикарбоновых кислот(цикл Кребса).
Слайд 8Отдельные представители
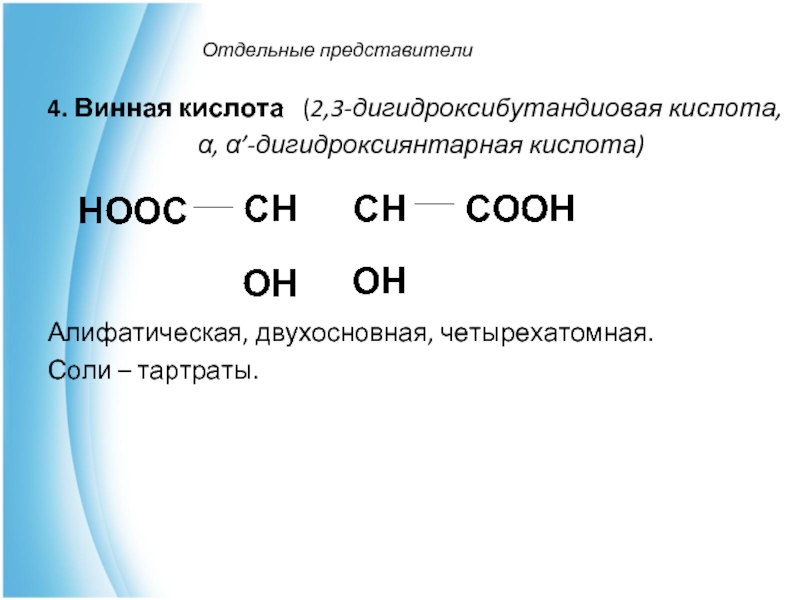
4. Винная кислота (2,3-дигидроксибутандиовая кислота,
α, α’-дигидроксиянтарная кислота)
Алифатическая, двухосновная, четырехатомная.
Соли – тартраты.
Слайд 9Отдельные представители
Калиево-натриевая соль винной кислоты называется сегнетовой (сеньетовой) солью:
При взаимодействии с
гидроксидом меди (II) в щелочной среде сегнетовая соль образует комплекс ярко-синего цвета, получивший название реактив Фелинга, применяемый для качественного обнаружения альдегидной группы.
Слайд 10Отдельные представители
5. Лимонная кислота
(2-гидроксипропан-1,2,3-трикарбоновая кислота)
Алифатическая, трехосновная, четырехатомная.
Соли - цитраты.
Широко используются в
пищевой промышленности и медицине, например, тринатриевая соль - цитрат натрия применяется в медицине для консервирования донорской крови.
Слайд 11Отдельные представители
6. Салициловая кислота (2-гидроксибензойная кислота)
Ароматическая, одноосновная, двухатомная.
Соли - салицилаты.
Обладает
антисептическими свойствами, находит применение как консервант пищевых продуктов. Широко используются фарм. препараты на ее основе.
Слайд 12Химические свойства.
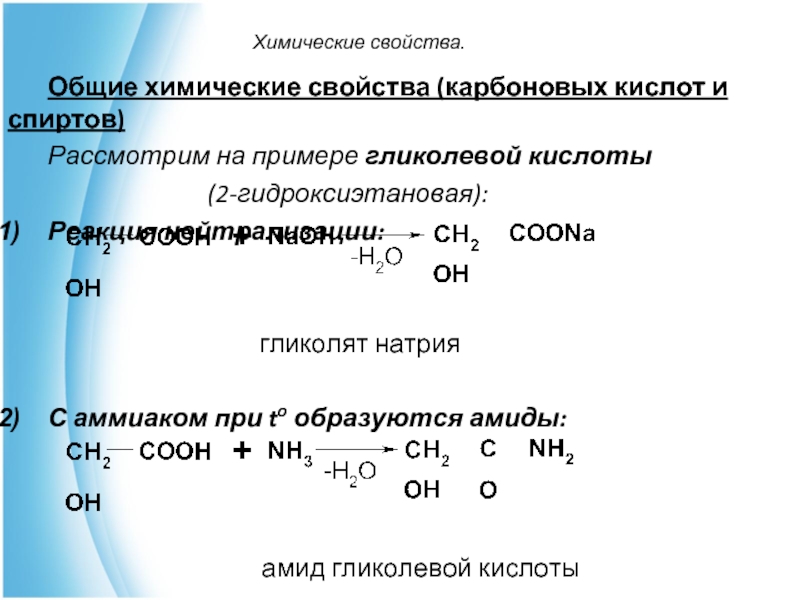
Общие химические свойства (карбоновых кислот и спиртов)
Рассмотрим на примере гликолевой
кислоты
(2-гидроксиэтановая):
Реакция нейтрализации:
гликолят натрия
С аммиаком при to образуются амиды:
амид гликолевой кислоты
Слайд 13Химические свойства.
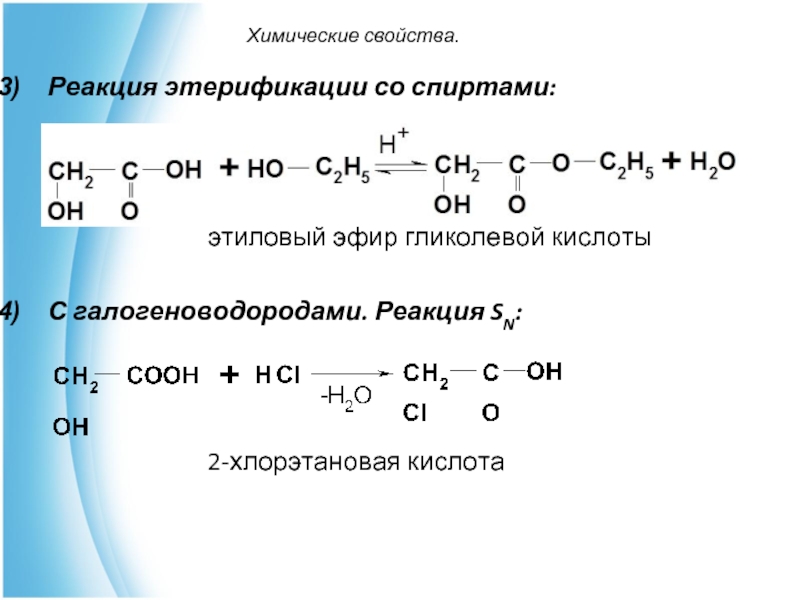
Реакция этерификации со спиртами:
этиловый эфир гликолевой кислоты
С галогеноводородами. Реакция
SN:
2-хлорэтановая кислота
Слайд 14Химические свойства.
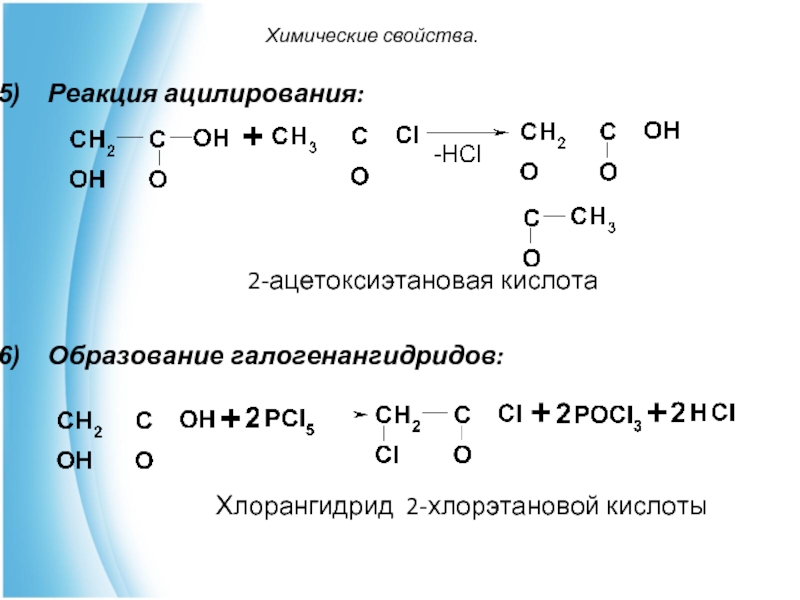
Реакция ацилирования:
2-ацетоксиэтановая кислота
Образование галогенангидридов:
Хлорангидрид 2-хлорэтановой кислоты
Слайд 15Химические свойства.
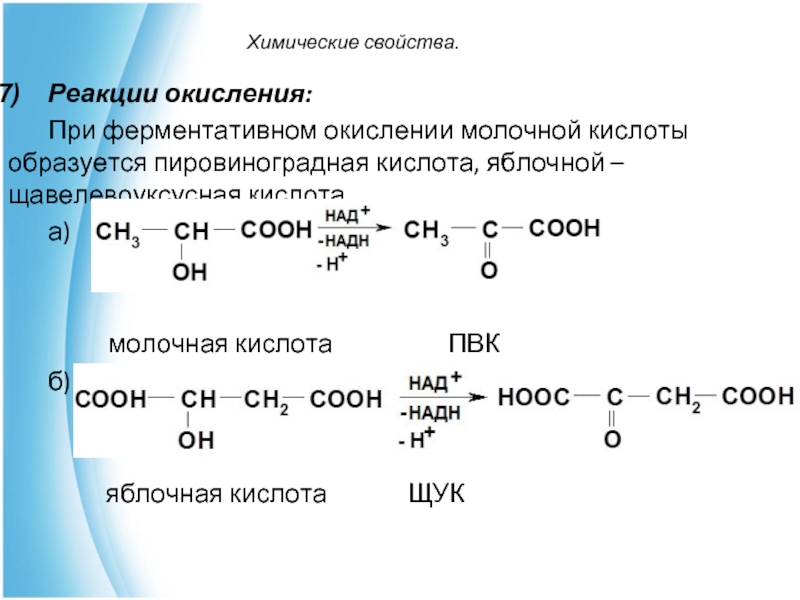
Реакции окисления:
При ферментативном окислении молочной кислоты образуется пировиноградная кислота, яблочной
– щавелевоуксусная кислота.
а)
молочная кислота ПВК
б)
яблочная кислота ЩУК
Слайд 16Специфические свойства гидроксикислот.
Специфические свойства гидроксикислот
(отношение к нагреванию).
α-гидроксикислоты
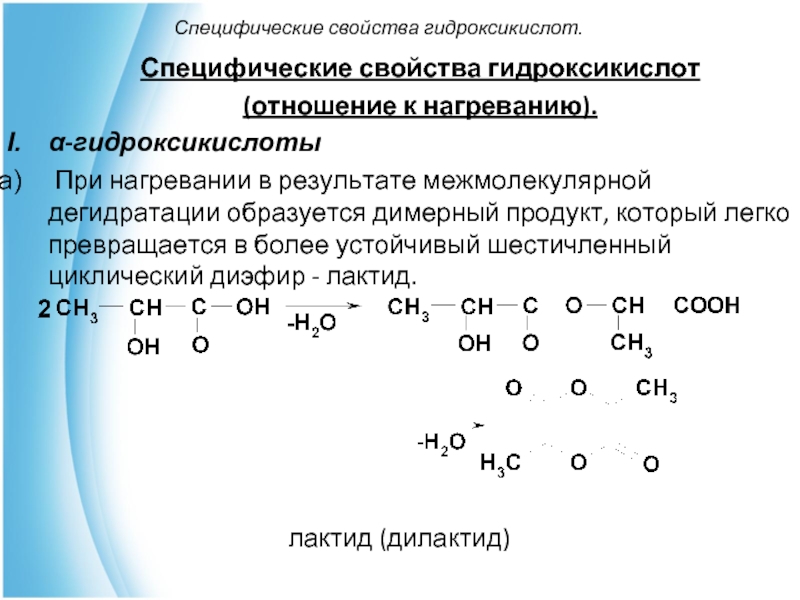
При нагревании в результате межмолекулярной дегидратации образуется димерный продукт, который легко превращается в более устойчивый шестичленный циклический диэфир - лактид.
лактид (дилактид)
Слайд 17Специфические свойства гидроксикислот.
Лактидами называются циклические эфиры, построенные из двух и более
остатков гидроксикислот (не обязательно α-гидроксикислот).
Название лактидов включает основу тривиального названия гидроксикислоты, суффикс -ид и умножающий префикс ди-, три- и т.д., указывающий число молекул, образующих лактид.
Например: Дигликолид – от гликолевой кислоты
Дилактид – от молочной кислоты
Слайд 18Специфические свойства гидроксикислот.
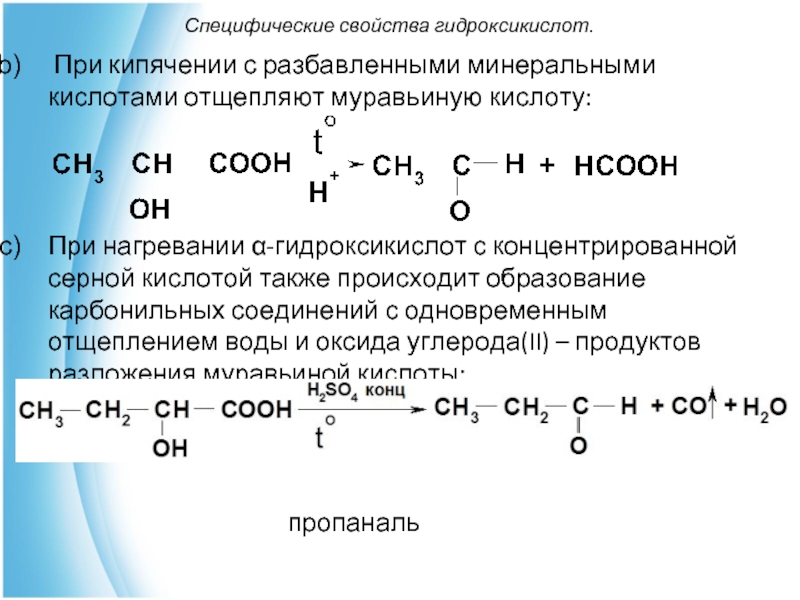
При кипячении с разбавленными минеральными кислотами отщепляют муравьиную
кислоту:
При нагревании α-гидроксикислот с концентрированной серной кислотой также происходит образование карбонильных соединений с одновременным отщеплением воды и оксида углерода(II) – продуктов разложения муравьиной кислоты:
пропаналь
Слайд 19Специфические свойства гидроксикислот.
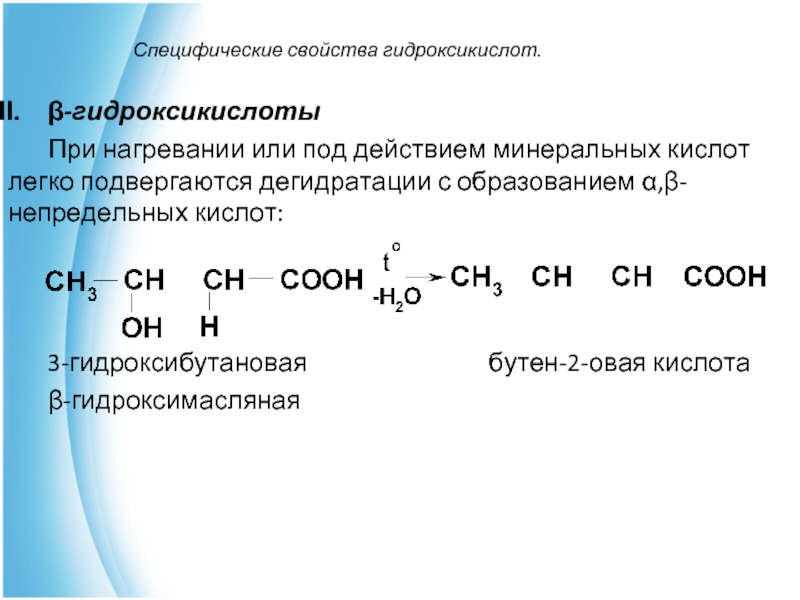
β-гидроксикислоты
При нагревании или под действием минеральных кислот легко подвергаются
дегидратации с образованием α,β-непредельных кислот:
3-гидроксибутановая бутен-2-овая кислота
β-гидроксимасляная
Слайд 20Специфические свойства гидроксикислот.
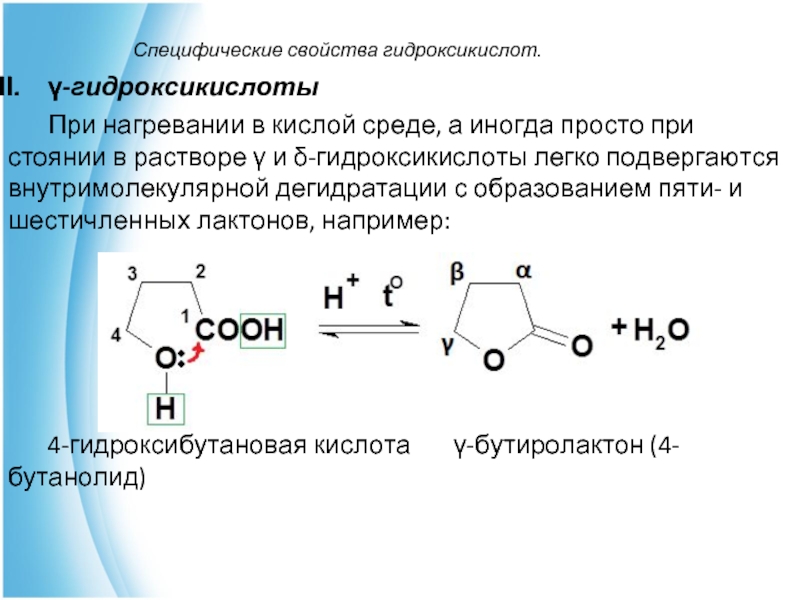
γ-гидроксикислоты
При нагревании в кислой среде, а иногда просто при
стоянии в растворе γ и δ-гидроксикислоты легко подвергаются внутримолекулярной дегидратации с образованием пяти- и шестичленных лактонов, например:
4-гидроксибутановая кислота γ-бутиролактон (4-бутанолид)
Слайд 21Специфические свойства гидроксикислот.
Лактонами называются внутренние сложные эфиры гидроксикислот.
По номенклатуре ИЮПАК
лактоны, образованные из алифатических кислот, называют, добавляя суффикс – олид к названию углеводорода с тем же числом атомов углерода. Цифрой обозначают место замыкания цикла, начиная нумерацию от карбонильного атома углерода.
Легкость образования лактонов из γ и δ-гидроксикислот объясняется повышенной термодинамической устойчивостью пяти- и шестичленных циклических соединений. Циклы меньшего или большего размера в этих условиях не образуются.
Лактоны, подобно сложным эфирам, при нагревании в кислой и щелочной среде легко гидролизуются до соответствующих гидроксикислот. Реакция гидролиза в щелочной среде необратима. Наибольшую устойчивость к гидролизу проявляют δ-лактоны.
Слайд 22Ароматические гидроксикислоты.
Ароматические гидроксикислоты (фенолокислоты)
Это производные ароматических карбоновых кислот, у которых один
или несколько атомов в ароматическом кольце заменены на гидроксильные группы –ОН.
Наиболее важными для фармации являются:
Галловая кислота:
3,4,5-тригидроксибензойная кислота
Входит в состав дубильных веществ (дубовой коре, листьях чая и др.). Водные растворы танинов – гликозидов галловой кислоты обладают способностью свертывать и осаждать белки. На этом основано применение танина в качестве кровоостанавливающего средства.
Слайд 23Ароматические гидроксикислоты.
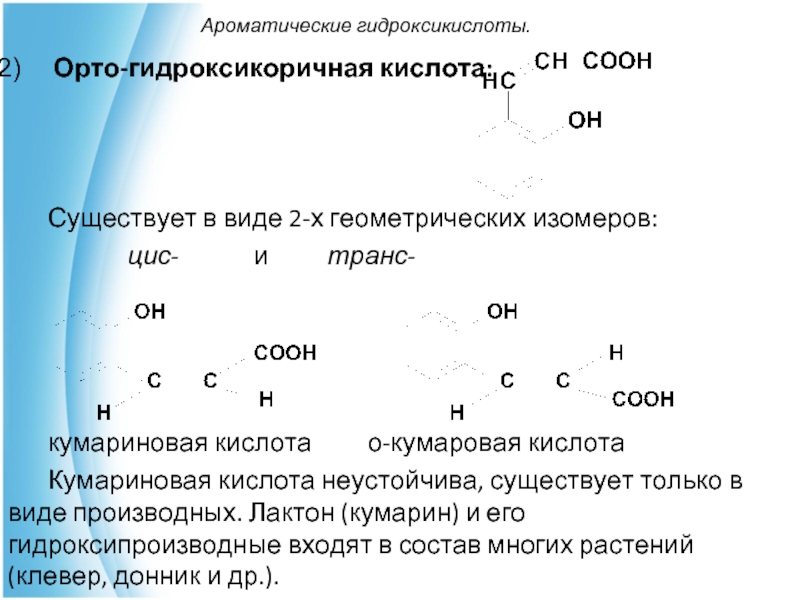
Орто-гидроксикоричная кислота:
Существует в виде 2-х геометрических изомеров:
цис- и
транс-
кумариновая кислота о-кумаровая кислота
Кумариновая кислота неустойчива, существует только в виде производных. Лактон (кумарин) и его гидроксипроизводные входят в состав многих растений (клевер, донник и др.).
Слайд 24Ароматические гидроксикислоты.
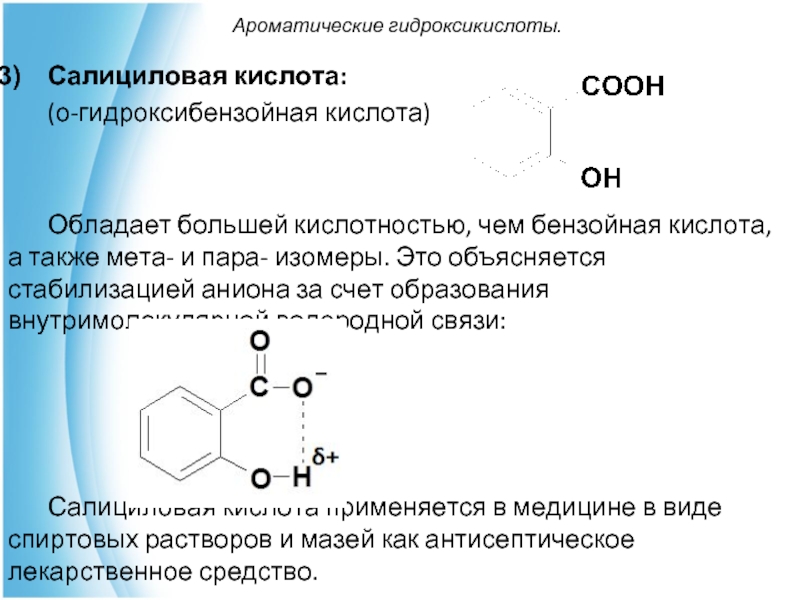
Салициловая кислота:
(о-гидроксибензойная кислота)
Обладает большей кислотностью, чем бензойная кислота,
а также мета- и пара- изомеры. Это объясняется стабилизацией аниона за счет образования внутримолекулярной водородной связи:
Салициловая кислота применяется в медицине в виде спиртовых растворов и мазей как антисептическое лекарственное средство.
Слайд 25Ароматические гидроксикислоты.
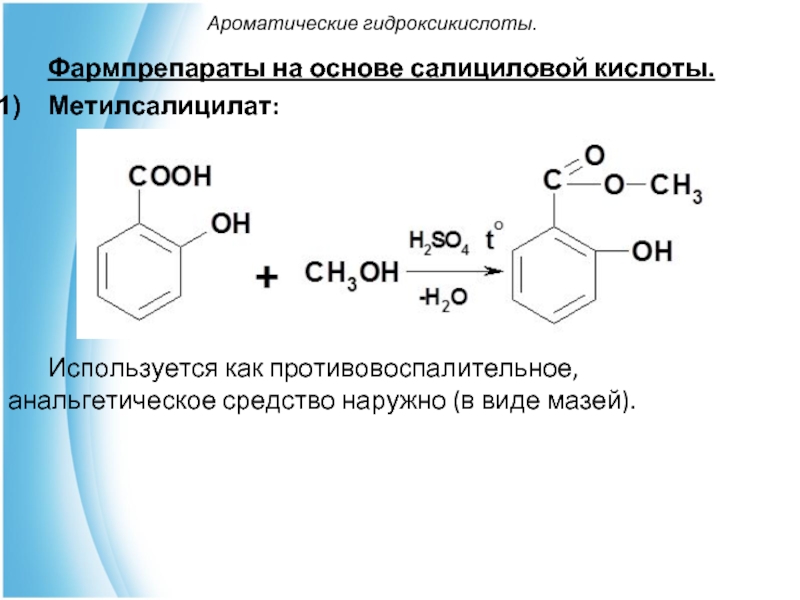
Фармпрепараты на основе салициловой кислоты.
Метилсалицилат:
Используется как противовоспалительное, анальгетическое средство наружно
Слайд 26Ароматические гидроксикислоты.
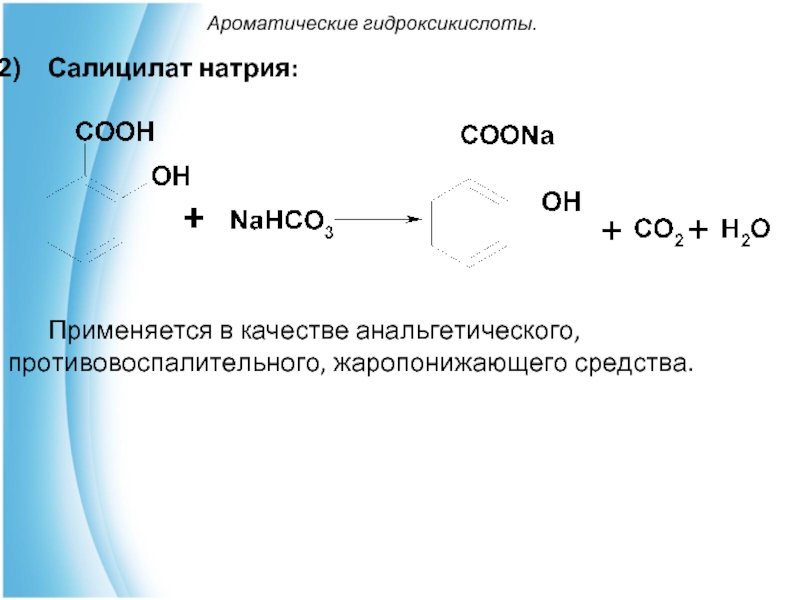
Салицилат натрия:
Применяется в качестве анальгетического, противовоспалительного, жаропонижающего средства.
Слайд 27Ароматические гидроксикислоты.
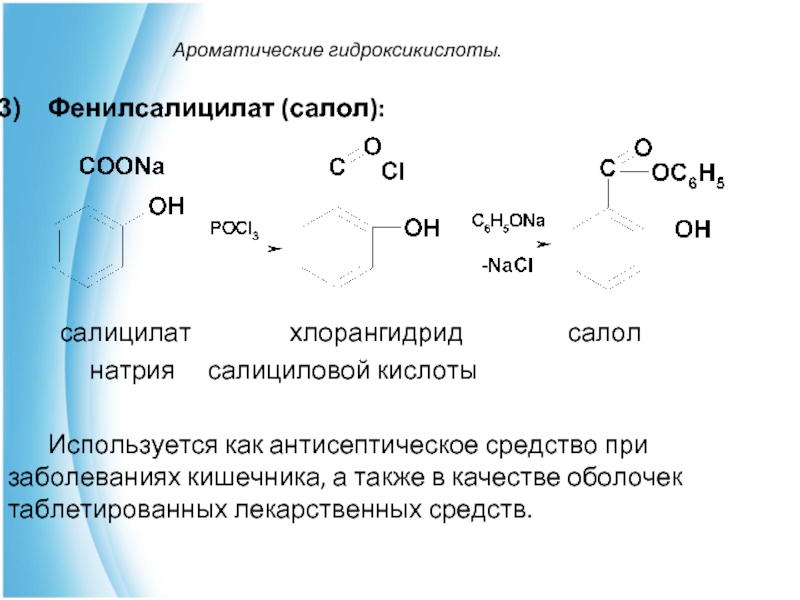
Фенилсалицилат (салол):
салицилат
хлорангидрид салол
натрия салициловой кислоты
Используется как антисептическое средство при заболеваниях кишечника, а также в качестве оболочек таблетированных лекарственных средств.
Слайд 28Ароматические гидроксикислоты.
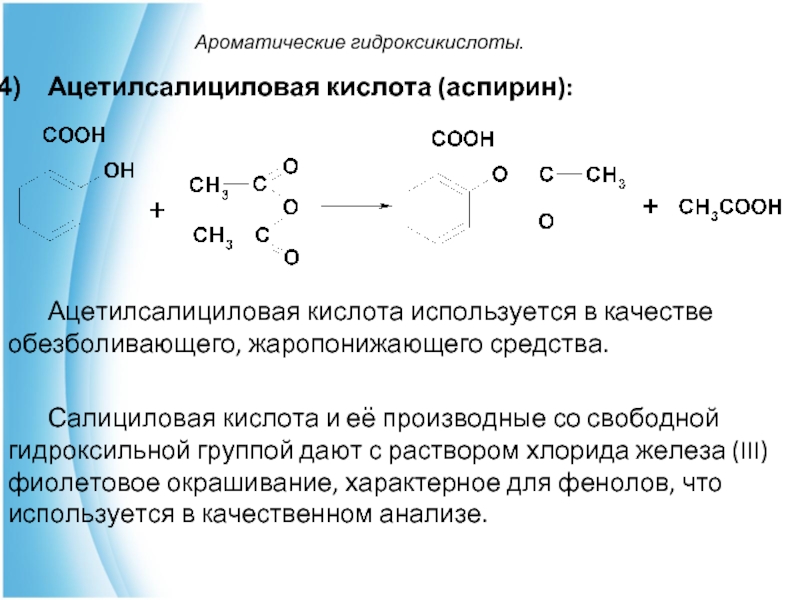
Ацетилсалициловая кислота (аспирин):
Ацетилсалициловая кислота используется в качестве обезболивающего, жаропонижающего средства.
Салициловая
кислота и её производные со свободной гидроксильной группой дают с раствором хлорида железа (III) фиолетовое окрашивание, характерное для фенолов, что используется в качественном анализе.