- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Оксиды. Классификация. Химические и физические свойства презентация
Содержание
- 1. Оксиды. Классификация. Химические и физические свойства
- 2. КЛАССИФИКАЦИЯ ОКСИДОВ Оксиды
- 3. ОПРЕДЕЛЕНИЕ ГРУПП ОКСИДОВ Основными называются оксиды, которые
- 4. НАПМИСАТЬ ХИМИЧЕСКИЕ ФОРМУЛЫ ОКСИДОВ
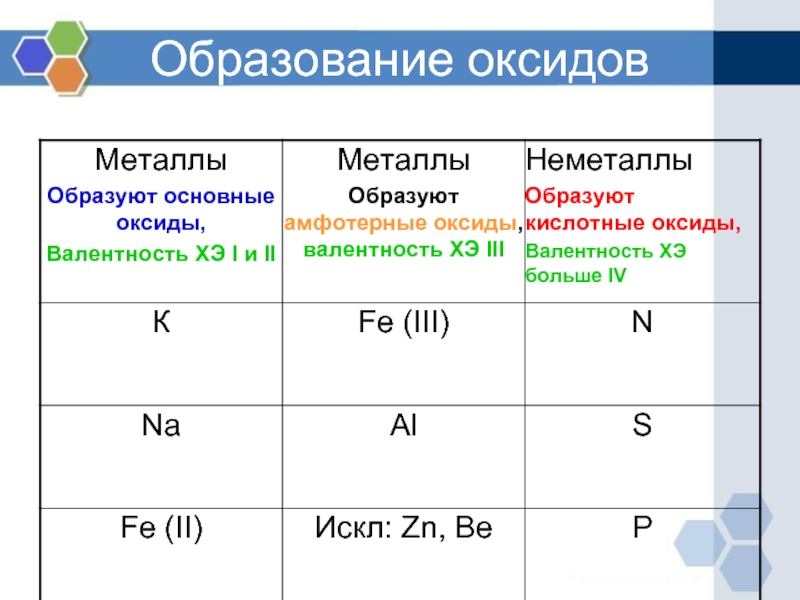
- 5. Образование оксидов
- 6. ФОРМУЛЫ ОКСИДОВ
- 7. ФИЗИЧЕСКИЕ СВОЙСТВА ОКСИДОВ
- 8. ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВНЫХ ОКСИДОВ (О.О.) 1)
- 9. Химические свойства кислотных оксидов (К.О.) 1) К.О.
- 10. Амфотерные оксиды
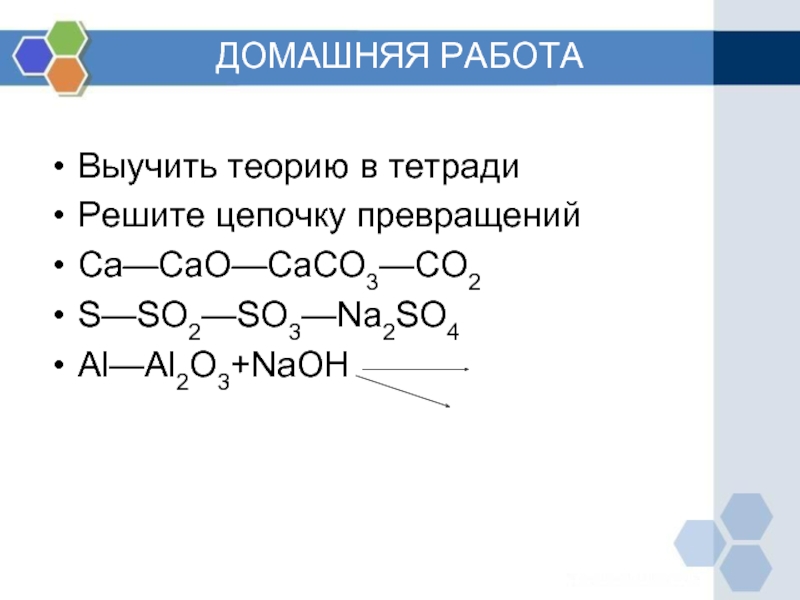
- 11. ДОМАШНЯЯ РАБОТА Выучить теорию в тетради Решите цепочку превращений Ca—CaO—CaCO3—CO2 S—SO2—SO3—Na2SO4 Al—Al2O3+NaOH
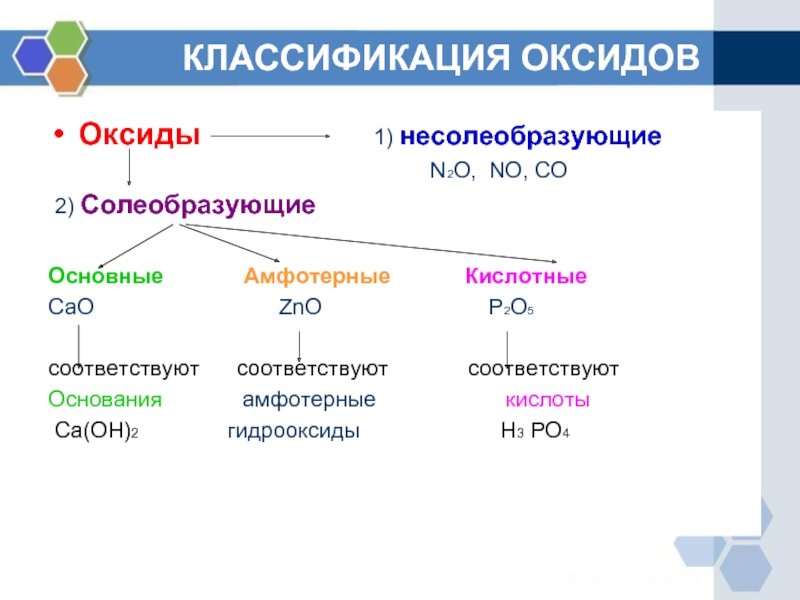
Слайд 2КЛАССИФИКАЦИЯ ОКСИДОВ
Оксиды
1) несолеобразующие
N2O, NO, CO
2) Солеобразующие
Основные Амфотерные Кислотные
CaO ZnO P2O5
соответствуют соответствуют соответствуют
Основания амфотерные кислоты
Ca(OH)2 гидрооксиды H3 PO4
N2O, NO, CO
2) Солеобразующие
Основные Амфотерные Кислотные
CaO ZnO P2O5
соответствуют соответствуют соответствуют
Основания амфотерные кислоты
Ca(OH)2 гидрооксиды H3 PO4
Слайд 3ОПРЕДЕЛЕНИЕ ГРУПП ОКСИДОВ
Основными называются оксиды, которые образуют соли при взаимодействии с
кислотами или кислотными оксидами.
Кислотными называются оксиды, которые образуют соли при взаимодействии с основаниями или основными оксидами.
Амфотерными оксидами, называют оксиды которые проявляют свойства как кислот, так и оснований.
Кислотными называются оксиды, которые образуют соли при взаимодействии с основаниями или основными оксидами.
Амфотерными оксидами, называют оксиды которые проявляют свойства как кислот, так и оснований.
Слайд 4НАПМИСАТЬ ХИМИЧЕСКИЕ ФОРМУЛЫ ОКСИДОВ
1)Оксид серы(IV)
2)Оксид азота(V)
3)Оксид калия (I)
4)Оксид железа(II)
5)Оксид фосфора(V)
6) оксид натрия (I)
3)Оксид калия (I)
4)Оксид железа(II)
5)Оксид фосфора(V)
6) оксид натрия (I)
Слайд 6 ФОРМУЛЫ ОКСИДОВ
1)Оксид серы(IV)
2)Оксид азота(V)
3)Оксид калия (I)
4)Оксид железа(II)
5)Оксид фосфора(V)
6) оксид натрия (I)
3)Оксид калия (I)
4)Оксид железа(II)
5)Оксид фосфора(V)
6) оксид натрия (I)
Слайд 8ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВНЫХ ОКСИДОВ (О.О.)
1) О.О. + кислота =соль + вода
(реакция обмена)
CaO + H2 SO4 → CaSO4 + H2O
2) О.О. + кислотный оксид = соль
(реакция соединения)
СaO + SiO2 = CaSiO3
3) О.О.(раств) + вода = основание (щелочь)
(реакция соединения)
Na2O + H2O → 2NaOH
CaO + H2 SO4 → CaSO4 + H2O
2) О.О. + кислотный оксид = соль
(реакция соединения)
СaO + SiO2 = CaSiO3
3) О.О.(раств) + вода = основание (щелочь)
(реакция соединения)
Na2O + H2O → 2NaOH
Слайд 9Химические свойства кислотных оксидов (К.О.)
1) К.О. + основание = соль +
вода (реакция обмена)
SO3 + 2NaOH → Na2SO4 + H2O
2) К.О. +О.О. = СОЛЬ (реакция соединения)
SO3 + Na2O → Na2SO4.
3) К.О. + вода = кислота (кроме SiO2 )
(реакция соединения)
P2O5 + 3H2O → 2H3PO4
SO3 + 2NaOH → Na2SO4 + H2O
2) К.О. +О.О. = СОЛЬ (реакция соединения)
SO3 + Na2O → Na2SO4.
3) К.О. + вода = кислота (кроме SiO2 )
(реакция соединения)
P2O5 + 3H2O → 2H3PO4
Слайд 10Амфотерные оксиды
1) с кислотами как основные
ZnO + 2HCl = ZnCl2 + H2O
2) с основаниями как кислотные
ZnO + 2NaOH = Na2ZnO + H2O
(цинкат натрия)
ZnO + 2NaOH +H2O = Na2[Zn(OH)4] (тетрагидроксоцинкат натрия)
2) с основаниями как кислотные
ZnO + 2NaOH = Na2ZnO + H2O
(цинкат натрия)
ZnO + 2NaOH +H2O = Na2[Zn(OH)4] (тетрагидроксоцинкат натрия)