- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Окислительно-восстановительные реакции презентация
Содержание
- 1. Окислительно-восстановительные реакции
- 2. На направление ОВР влияют многие факторы
- 3. Правила составления ОВР 3 Если элемент
- 4. Наиболее часто применяемые восстановители и окислители и
- 5. Наиболее часто применяемые восстановители и окислители и
- 6. Наиболее часто применяемые восстановители и окислители и
- 7. Наиболее часто применяемые восстановители и окислители и
- 8. Наиболее часто применяемые восстановители и окислители и
- 9. Наиболее часто применяемые восстановители и окислители и
- 10. В кислой среде 5 2 3
- 11. KMnO4 + HCl -1 +7
- 12. В нейтральной среде KMnO4
- 13. В щелочной среде KMnO4 +
- 14. спасибо
Слайд 2На направление ОВР влияют многие факторы
Природа реагирующих веществ
Характер среды
Температура
Cl2 + 2NaOH
3Cl2 + 6NaOH NaClO3 + 5NaCl + 3H2O
Концентрация
H2SO4 конц. , HNO3 разб. и конц.
Катализаторы
t
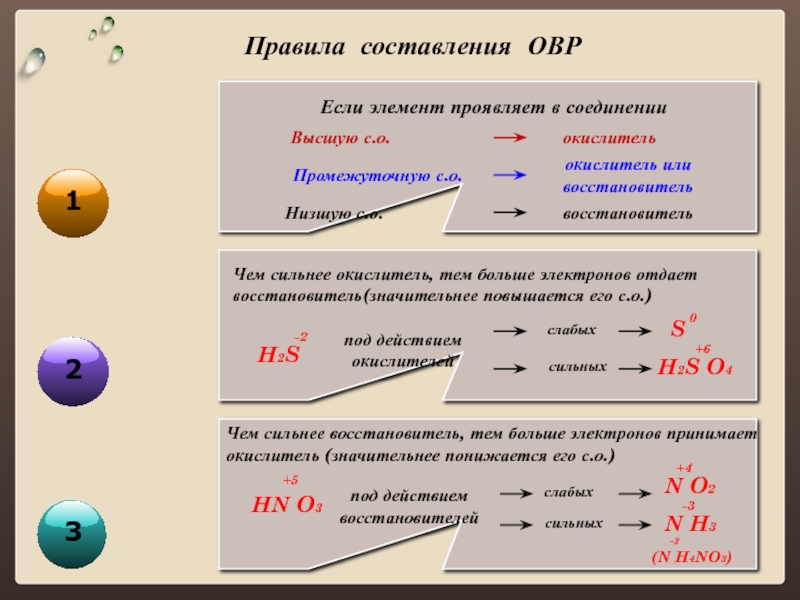
Слайд 3Правила составления ОВР
3
Если элемент проявляет в соединении
Высшую с.о.
окислитель
Промежуточную с.о.
Низшую с.о.
окислитель или
восстановитель
Чем сильнее окислитель, тем больше электронов отдает восстановитель(значительнее повышается его с.о.)
слабых
под действием окислителей
H2S
-2
сильных
H2S O4
S
+6
0
Чем сильнее восстановитель, тем больше электронов принимает окислитель (значительнее понижается его с.о.)
HN O3
+5
под действием восстановителей
слабых
сильных
N O2
+4
N H3
-3
(N H4NO3)
-3
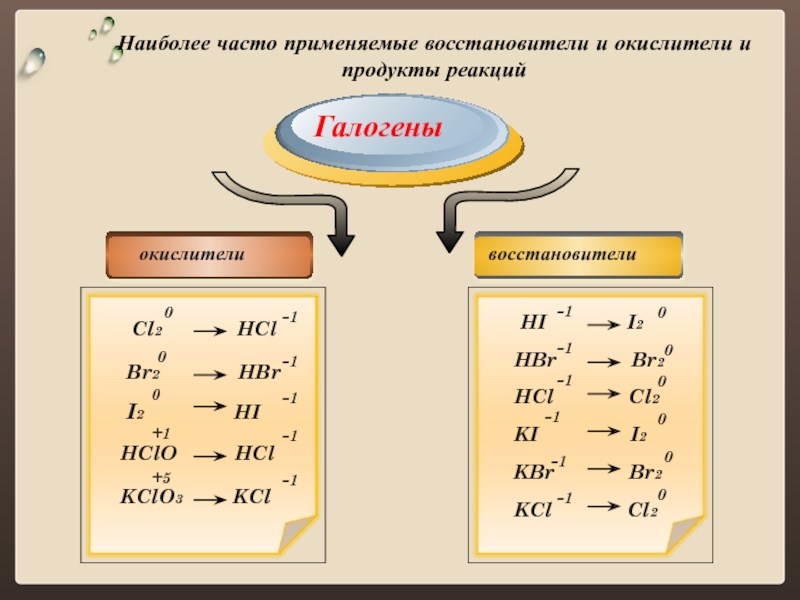
Слайд 4Наиболее часто применяемые восстановители и окислители и продукты реакций
KBr
HI I2
HBr Br2
HCl Cl2
KI I2
KCl Cl2
Галогены
Br2 HBr
Cl2 HCl
I2 HI
HClO HCl
KClO3 KCl
-1
-1
-1
-1
-1
-1
+1
-1
+5
-1
-1
-1
-1
0
0
0
0
0
0
0
0
0
Слайд 5Наиболее часто применяемые восстановители и окислители и продукты реакций
H2S
Na2S O3 Na2S O4
S SO2
Соединения серы
H2S O4 S
H2S O4 H2S
0
-2
0
+
0
+6
H
с KBr
с KJ
+6
Na2S O3 S
(в кислой среде)
+4
-2
+4
+6
0
+4
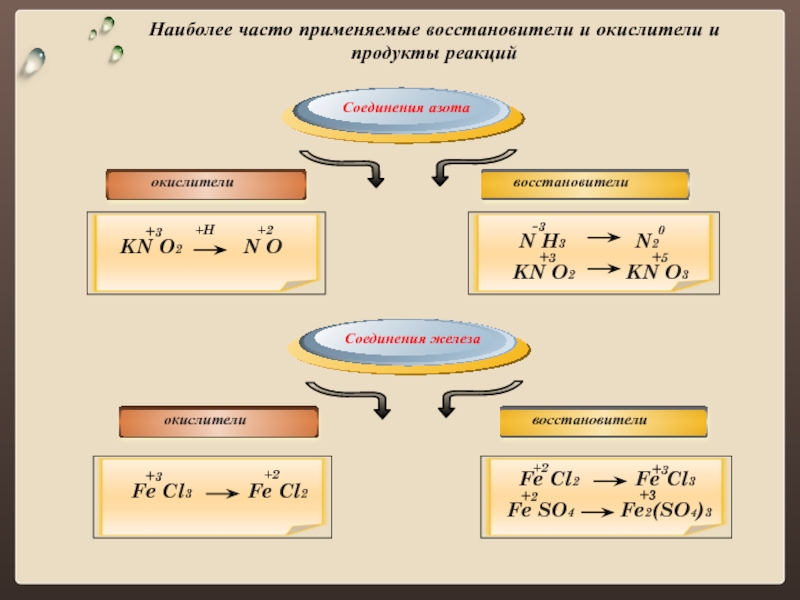
Слайд 6Наиболее часто применяемые восстановители и окислители и продукты реакций
Соединения азота
+5
Соединения железа
KN
+3
+H
+2
N H3 N2
-3
0
KN O2 KN O3
+3
Fe Cl3 Fe Cl2
+3
+2
Fe Cl2 Fe Cl3
+2
+3
Fe SO4 Fe2(SO4)3
+3
+2
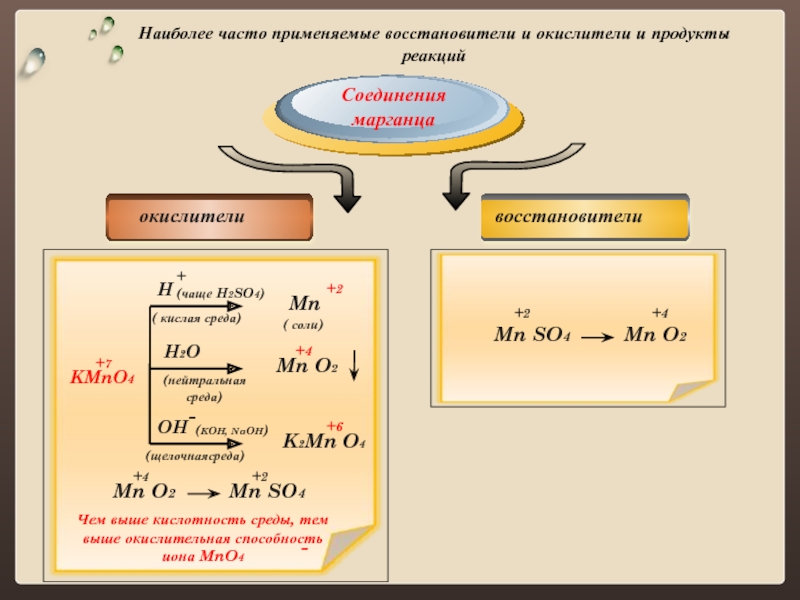
Слайд 7Наиболее часто применяемые восстановители и окислители и продукты реакций
Mn SO4
Соединения
марганца
+
+6
( кислая среда)
+4
+2
+4
+2
KMnO4
(нейтральная
среда)
(щелочнаясреда)
H
(чаще H2SO4)
K2Mn O4
Mn O2
Mn
H2O
OH
-
(KOH, NaOH)
Mn O2 Mn SO4
+4
+2
Чем выше кислотность среды, тем выше окислительная способность иона MnO4
-
+7
( соли)
Слайд 8Наиболее часто применяемые восстановители и окислители и продукты реакций
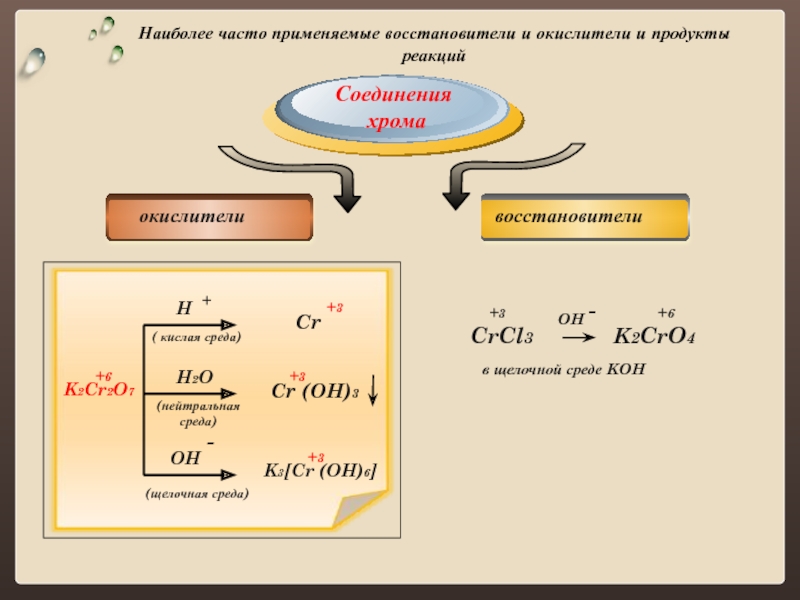
CrCl3
Соединения
хрома
+
( кислая среда)
+3
+6
+3
K2Cr2O7
(нейтральная
среда)
(щелочная среда)
H
K3[Cr (OH)6]
Cr (OH)3
Cr
H2O
OH
-
+3
+3
+6
OH
-
в щелочной среде KOH
Слайд 9Наиболее часто применяемые восстановители и окислители и продукты реакций
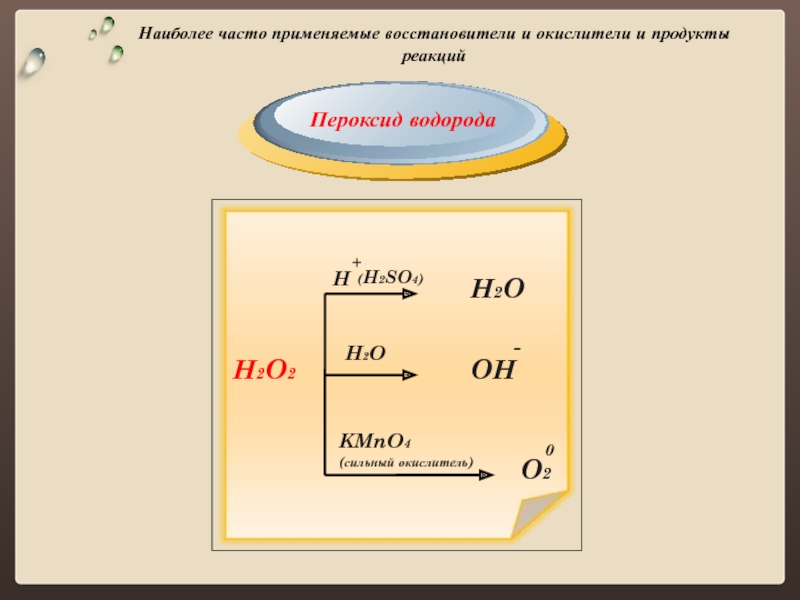
Пероксид водорода
+
(сильный окислитель)
H
KMnO4
-
OH
0
H2O2
(H2SO4)
H2O
H2O
O2
Слайд 12
В нейтральной среде
KMnO4 + K2SO3 + H2O
+4
+7
KMnO4
-2
+7
K2Cr2O7 + H2S + H2O
-2
+6
.
2
3
2
2
3
2
2
2
3
2
3
3
2 3 2