- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
ОГЭ по химии. (Занятие 6) презентация
Содержание
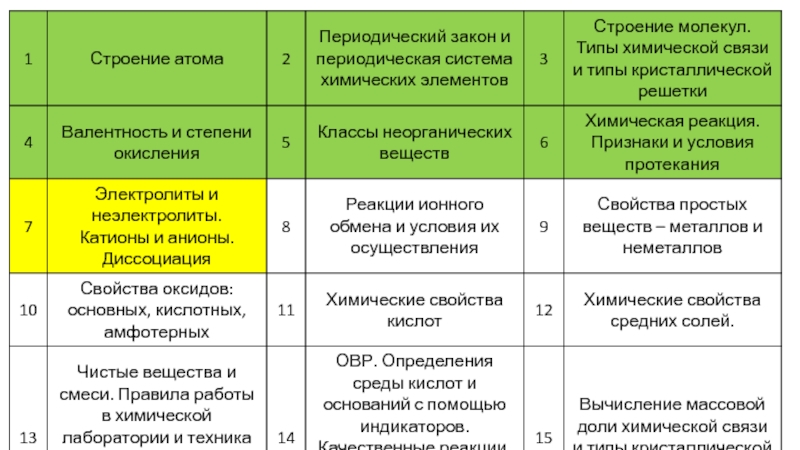
- 1. ОГЭ по химии. (Занятие 6)
- 4. Диссоциация - разновидность диссоциации, при которой молекулы
- 5. Диссоциировать могут соли, кислоты, щелочи. Наиболее хорошо
- 6. Металлы – группа элементов, в виде простых
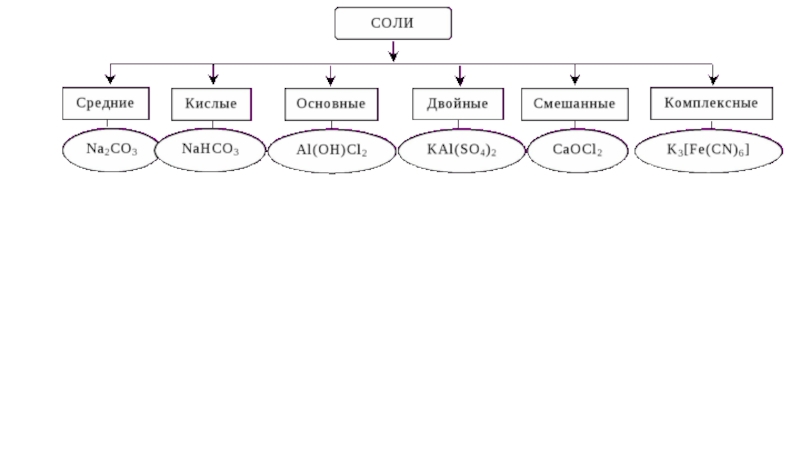
- 7. Сложные неорганические вещества Оксиды Основания Кислоты Соли
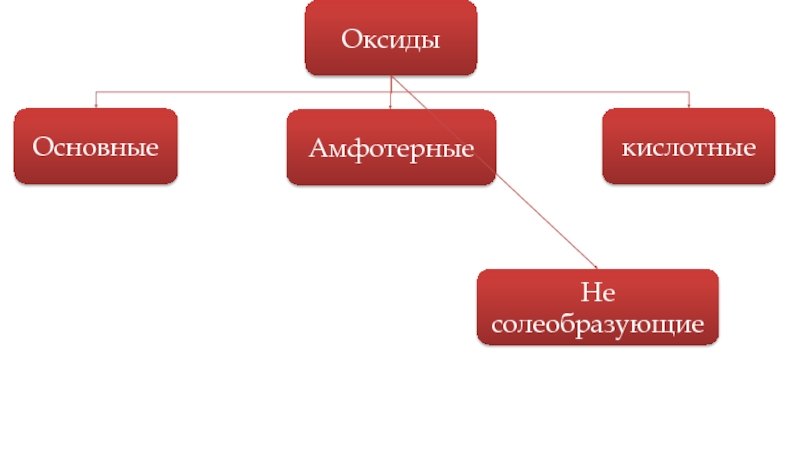
- 8. Оксиды Основные Амфотерные кислотные Не солеобразующие
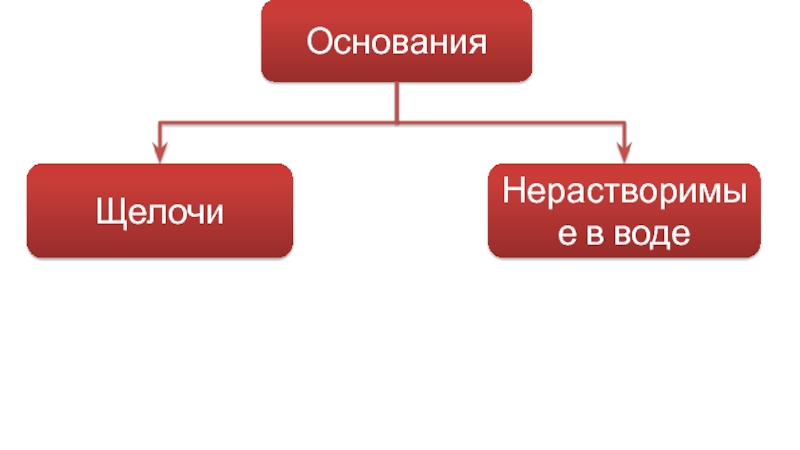
- 9. Основания Щелочи Нерастворимые в воде
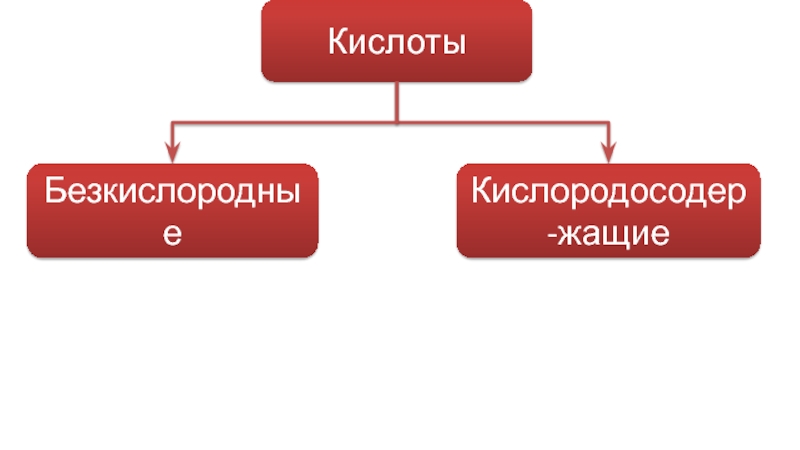
- 10. Кислоты Безкислородные Кислородосодер-жащие
- 12. 6.1 При полной диссоциации 1 моля HCl
- 13. 6.1 При полной диссоциации 1 моля HCl
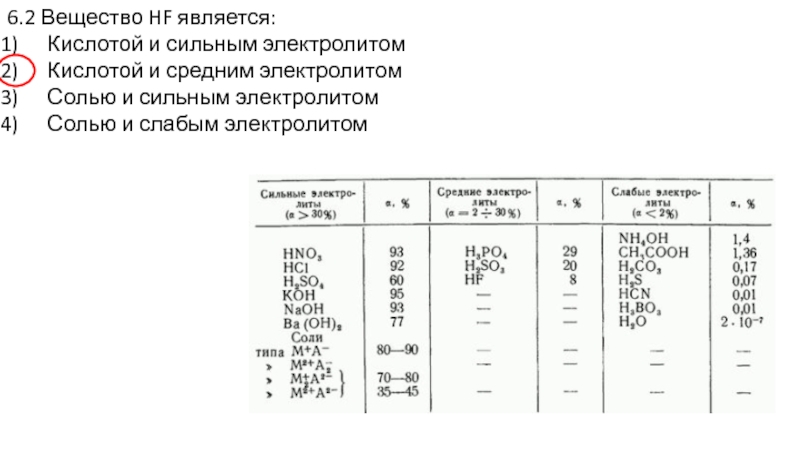
- 14. 6.2 Вещество HF является: Кислотой и сильным
- 15. 6.2 Вещество HF является: Кислотой и сильным
- 16. 6.3 Число молей катионов в 2 раза
- 17. 6.3 Число молей катионов в 2 раза
- 18. 6.4 Установите соответствие межу двумя веществами и
- 19. 6.4 Установите соответствие межу двумя веществами и
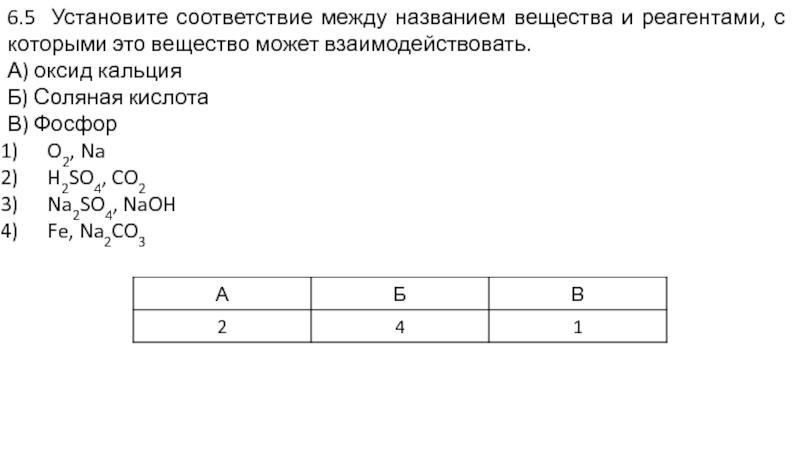
- 20. 6.5 Установите соответствие между названием вещества и
- 21. 6.5 Установите соответствие между названием вещества и
- 22. 6.6 Число молей катионов, равное числу молей
- 23. 6.6 Число молей катионов, равное числу молей
- 24. 6.7 Установите соответствие между двумя веществами и
- 25. 6.7 Установите соответствие между двумя веществами и
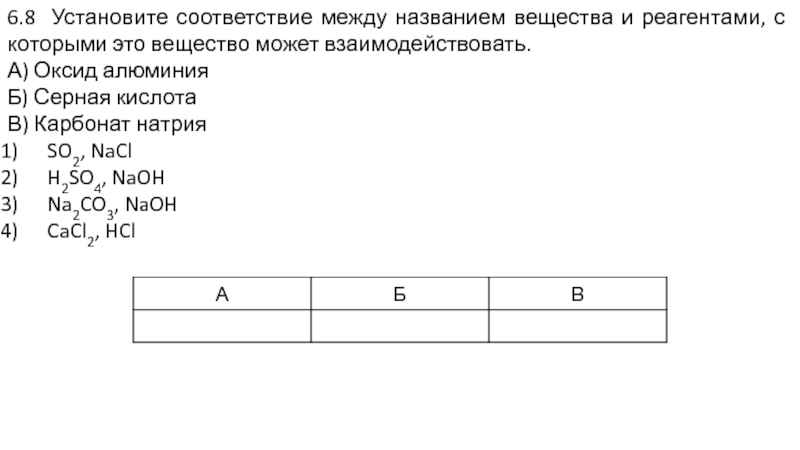
- 26. 6.8 Установите соответствие между названием вещества и
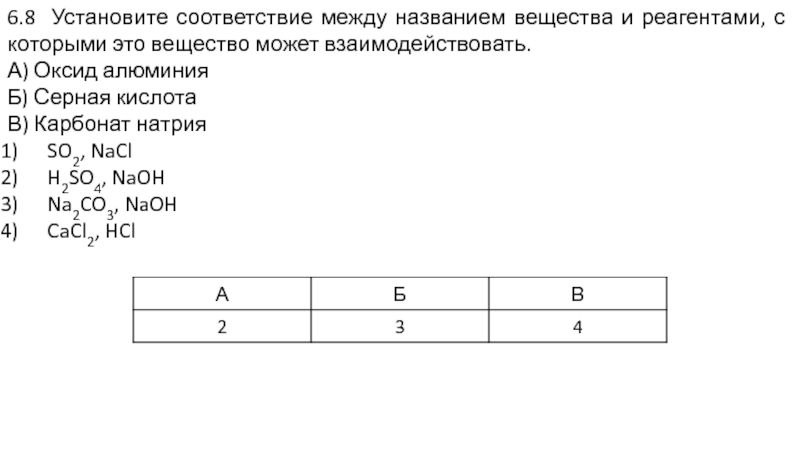
- 27. 6.8 Установите соответствие между названием вещества и
- 28. 6.8 Большое число ионов образуется при полной
- 29. 6.8 Большое число ионов образуется при полной
- 30. 6.9 Установите соответствие между двумя веществами и
- 31. 6.9 Установите соответствие между двумя веществами и
- 32. 6.9 Установите соответствие между двумя веществами и
- 33. 6.10 Практически не осуществима реакция между раствором
- 34. 6.10 Практически не осуществима реакция между раствором
- 35. Т.1 Установите соответствие между названием вещества и
- 36. Т.2 Электрический ток проводит: Жидкий хлороводород Твёрдый хлорид натрия Дистиллированная вода Раствор хлорида натрия
- 37. Т.3 Установите соответствие между двумя веществами
- 38. Т.4 Установите соответствие между названием вещества и
- 39. Т.5 Самое большое число катионов образуется при
- 40. Т.6 К электролитам относятся Оксид меди(II) Глюкоза Соляная кислота Углекислый газ
- 41. Т.7 Формула сильного электролита CaCO3 Fe(OH)2 CO2 KNO3
- 42. Т.8 Суммы всех коэффициентов в полном и
- 43. Т.9 Реакция ионного обмена идет до конца
- 44. Т. 10 Хлорид меди (II) вступает в
Слайд 4Диссоциация - разновидность диссоциации, при которой молекулы электролита распадаются на ионы
Основные положения теории электролитической диссоциации:
- Электролиты при растворении или плавлении распадаются на ионы (диссоциируют) – положительные и отрицательные.
- Под действием электрического тока ионы приобретают направленное движение: положительные ионы стремятся к катоду, отрицательные - к аноду.
- Направленное движение происходит в результате притяжения их противоположно заряженными электродами.
- Диссоциация – обратимый процесс: одновременно вещество распадается на ионы и ионы собираются в вещество.
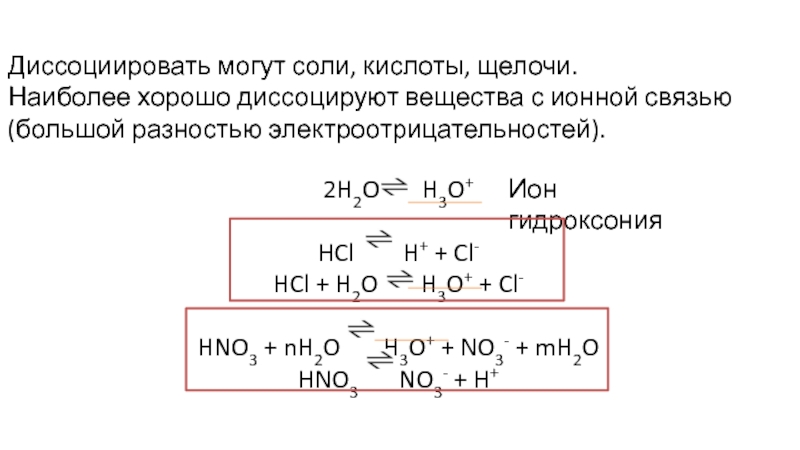
Слайд 5Диссоциировать могут соли, кислоты, щелочи.
Наиболее хорошо диссоцируют вещества с ионной связью
2H2O H3O+
HCl H+ + Cl-
HCl + H2O H3O+ + Cl-
HNO3 + nH2O H3O+ + NO3- + mH2O
HNO3 NO3- + H+
Ион гидроксония
Слайд 6Металлы – группа элементов, в виде простых веществ обладающих характерными металлическими
Неметаллы - химические элементы, которые не обладают свойствами, характерными для металлов.
Слайд 126.1 При полной диссоциации 1 моля HCl
Образуется 5 молей ионов
Образуется
Образуется 1 моль ионов
Образуется 2 моль ионов
Слайд 136.1 При полной диссоциации 1 моля HCl
Образуется 5 молей ионов
Образуется
Образуется 1 моль ионов
Образуется 2 моль ионов
Слайд 146.2 Вещество HF является:
Кислотой и сильным электролитом
Кислотой и средним электролитом
Солью и
Солью и слабым электролитом
Слайд 156.2 Вещество HF является:
Кислотой и сильным электролитом
Кислотой и средним электролитом
Солью и
Солью и слабым электролитом
Слайд 166.3 Число молей катионов в 2 раза больше, чем число молей
MgCl2
Na2CO3
MgSO4
Al(NO3)3
Слайд 176.3 Число молей катионов в 2 раза больше, чем число молей
MgCl2
Na2CO3
MgSO4
Al(NO3)3
Слайд 186.4 Установите соответствие межу двумя веществами и реактивом, с помощью которого
А) NaNO3, Na2SO4
Б) NaCl, Na3PO4
В) CaCO3, CaSO4
HCl
K2SO3
BaCl2
NaOH
Слайд 196.4 Установите соответствие межу двумя веществами и реактивом, с помощью которого
А) NaNO3, Na2SO4
Б) NaCl, Na3PO4
В) CaCO3, CaSO4
HCl
K2SO3
BaCl2
NaOH
Слайд 206.5 Установите соответствие между названием вещества и реагентами, с которыми это
А) оксид кальция
Б) Соляная кислота
В) Фосфор
O2, Na
H2SO4, CO2
Na2SO4, NaOH
Fe, Na2CO3
Слайд 216.5 Установите соответствие между названием вещества и реагентами, с которыми это
А) оксид кальция
Б) Соляная кислота
В) Фосфор
O2, Na
H2SO4, CO2
Na2SO4, NaOH
Fe, Na2CO3
Слайд 226.6 Число молей катионов, равное числу молей анионов, образуется при полной
FeCl2
K2SO4
BaSO4
NaNO3
Слайд 236.6 Число молей катионов, равное числу молей анионов, образуется при полной
FeCl2
K2SO4
BaSO4
NaNO3
Слайд 246.7 Установите соответствие между двумя веществами и реактивом, с помощью которого
А) Ba(NO3)2, Mg(NO3)2
Б) CaCl2, NaCl
В) HCl, HNO3
Na2CO3
K2SO4
NaCl
AgNO3
Слайд 256.7 Установите соответствие между двумя веществами и реактивом, с помощью которого
А) Ba(NO3)2, Mg(NO3)2
Б) CaCl2, NaCl
В) HCl, HNO3
Na2CO3
K2SO4
NaCl
AgNO3
Слайд 266.8 Установите соответствие между названием вещества и реагентами, с которыми это
А) Оксид алюминия
Б) Серная кислота
В) Карбонат натрия
SO2, NaCl
H2SO4, NaOH
Na2CO3, NaOH
CaCl2, HCl
Слайд 276.8 Установите соответствие между названием вещества и реагентами, с которыми это
А) Оксид алюминия
Б) Серная кислота
В) Карбонат натрия
SO2, NaCl
H2SO4, NaOH
Na2CO3, NaOH
CaCl2, HCl
Слайд 286.8 Большое число ионов образуется при полной диссоциации в водном растворе
CrCl3
Cr2(SO4)3
H3PO4
NaOH
Слайд 296.8 Большое число ионов образуется при полной диссоциации в водном растворе
CrCl3
Cr2(SO4)3
H3PO4
NaOH
Слайд 306.9 Установите соответствие между двумя веществами и реактивом, с помощью которого
А) KNO3, K2S
Б) FeCl2, MgCl2
B) BaCl2, Ba(NO3)2
Na2SO4
AgNO3
BaSO4
KOH
Слайд 316.9 Установите соответствие между двумя веществами и реактивом, с помощью которого
А) KNO3, K2S
Б) FeCl2, MgCl2
B) BaCl2, Ba(NO3)2
Na2SO4
AgNO3
BaSO4
KOH
Слайд 326.9 Установите соответствие между двумя веществами и реактивом, с помощью которого
А) KNO3, K2S
Б) FeCl2, MgCl2
B) BaCl2, Ba(NO3)2
Na2SO4
AgNO3
BaSO4
KOH
Слайд 336.10 Практически не осуществима реакция между раствором хлорида меди (II) и
Цинком
Серебром
Магнием
Нитратом серебра
Слайд 346.10 Практически не осуществима реакция между раствором хлорида меди (II) и
Цинком
Серебром
Магнием
Нитратом серебра
Слайд 35Т.1 Установите соответствие между названием вещества и реагентами, с которыми это
А) гидроксид натрия
Б) Оксид серы (VI)
В) Нитрат меди
NaOH, Fe
H2SO4, H2O
CaO, KOH
Al2O3, AgF
Слайд 36Т.2 Электрический ток проводит:
Жидкий хлороводород
Твёрдый хлорид натрия
Дистиллированная вода
Раствор хлорида натрия
Слайд 37Т.3
Установите соответствие между двумя веществами и реактивом, с помощью которого
А) CO2, O2
Б) Cl2, H2
В) HCl, HI
Раствор KI
Раствор KOH
РастворCa(OH)2
Раствор AgNO3
Слайд 38Т.4 Установите соответствие между названием вещества и реагентами, с которыми это
А) SiO2
Б) раствор H2SO4
В) Na3PO4
H2, Ca(OH)2
CaCO3, BaCl2
HF, NaOH
NaNO3, MgSO4
Слайд 39Т.5 Самое большое число катионов образуется при диссоциации 1 моль вещества:
Фосфата
Сульфата алюминия
Сульфата натрия
Сульфата магния
Слайд 42Т.8 Суммы всех коэффициентов в полном и сокращенном ионном уравнении реакции
14 и 8
18 и 8
18 и 6
14 и 6
Слайд 43Т.9 Реакция ионного обмена идет до конца между веществами
Сульфатом калия и
Гидроксидом натрия и хлоридом магния
Нитратом калия и сульфатом натрия
гидроксидом натрия и хлоридом калия
Слайд 44Т. 10
Хлорид меди (II) вступает в реакцию обмена с
Гидроксидом железа
Гидроксидом натрия
Нитратом серебра
Железом
Хлоридом натрия