- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Неравновесные электрохимические методы. Вольтамперометрия презентация
Содержание
- 1. Неравновесные электрохимические методы. Вольтамперометрия
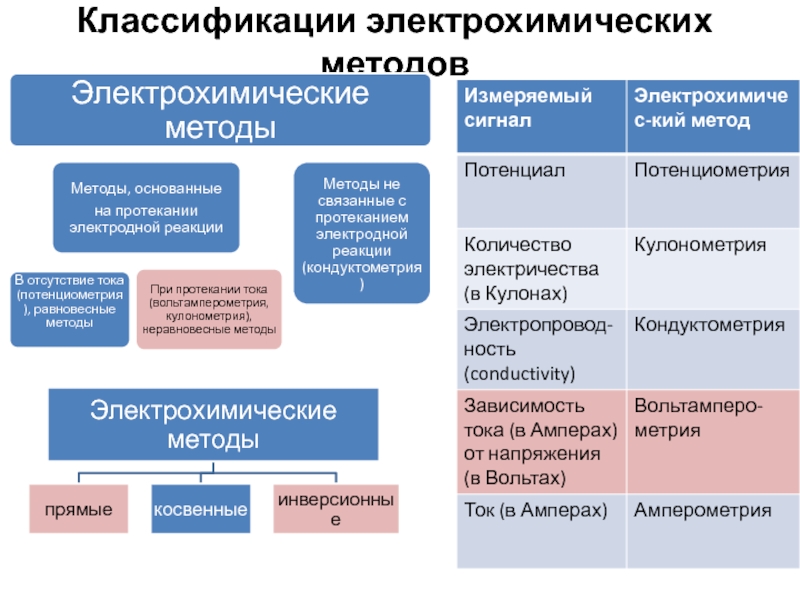
- 2. Классификации электрохимических методов
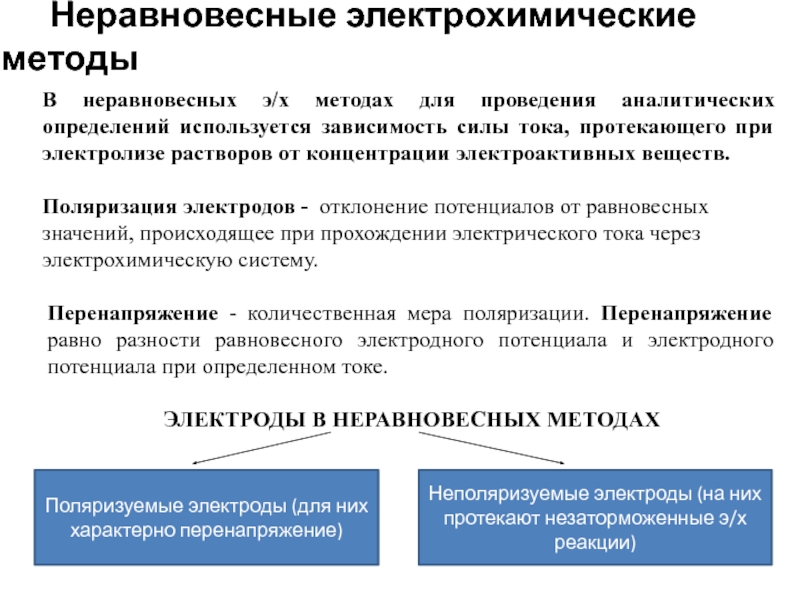
- 3. Неравновесные электрохимические методы В
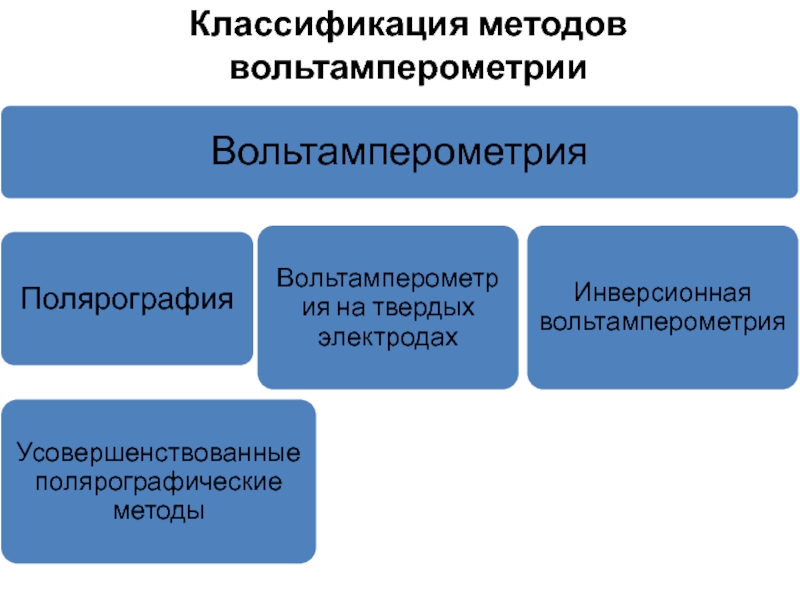
- 4. Классификация методов вольтамперометрии
- 5. Полярография I - аккумулятор; 2 - выключатель;
- 6. Ртутный капельный электрод (РКЭ) – стеклянный капилляр (внутренний диаметр 5·10-2мм)
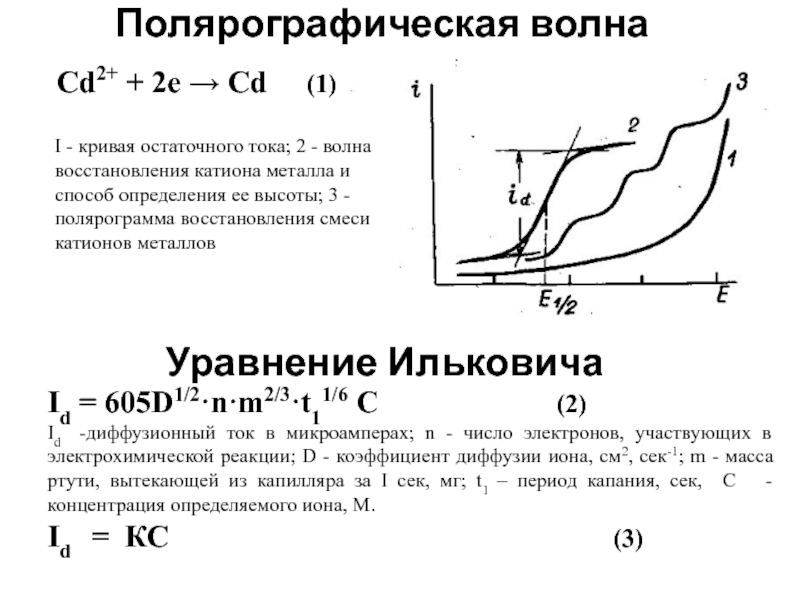
- 7. Полярографическая волна Cd2+ + 2e →
- 8. Необходимые условия количественного полярографического анализа Измеряемый ток
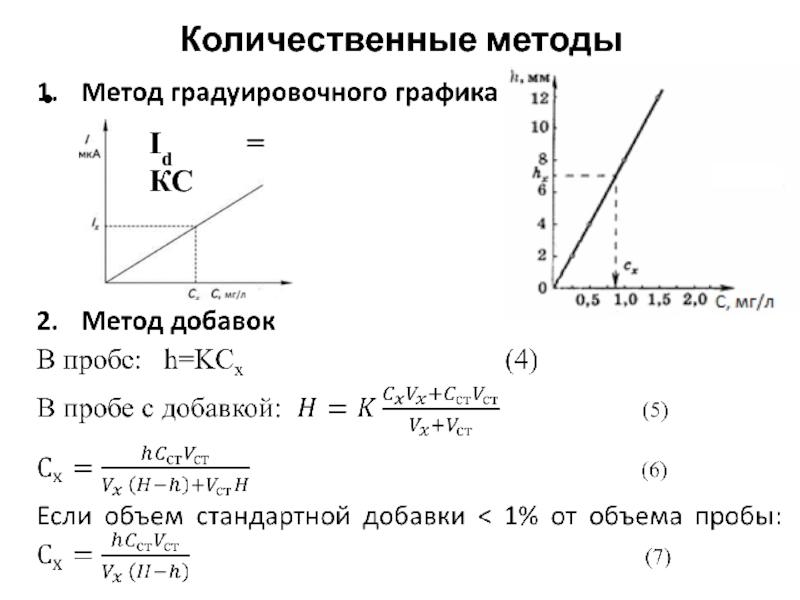
- 9. Количественные методы Id = КС
- 10. Количественные методы (продолжение) (12)
- 11. Использование полярографии в мониторинге Определение неорганических веществ
- 12. Усовершенствованные полярографические методы Производная, или дифференциальная полярография
- 13. Инверсионная вольтамперометрия (ИВА) Q = it
- 14. Инверсионная вольтамперометрия (ИВА) Подготовка проб В
- 15. Использование ИВА в мониторинге Может быть использована
- 16. Амперометрия Кислородный сенсор Кларка Условия измерения: Необходим
Слайд 1Дисциплина: Методы геохимического опробования и анализа
Тема:
Неравновесные электрохимические методы.
Вольтамперометрия
Слайд 3 Неравновесные электрохимические методы
В неравновесных э/х методах для проведения
Поляризация электродов - отклонение потенциалов от равновесных значений, происходящее при прохождении электрического тока через электрохимическую систему.
Перенапряжение - количественная мера поляризации. Перенапряжение равно разности равновесного электродного потенциала и электродного потенциала при определенном токе.
ЭЛЕКТРОДЫ В НЕРАВНОВЕСНЫХ МЕТОДАХ
Поляризуемые электроды (для них характерно перенапряжение)
Неполяризуемые электроды (на них протекают незаторможенные э/х реакции)
Слайд 5Полярография
I - аккумулятор; 2 - выключатель; 3 - потенциометр; 4 -
ЭДС = Еа – Ек + iR
Eа и Eк - потенциалы анода и катода,
iR - омическое падение напряжения в ячейке
iR 0; Eа = 0,
Принципиальная схема
тогда ЭДС = - Ек
Слайд 7Полярографическая волна
Cd2+ + 2e → Cd (1)
Id =
Id -диффузионный ток в микроамперах; n - число электронов, участвующих в электрохимической реакции; D - коэффициент диффузии иона, см2, сек-1; m - масса ртути, вытекающей из капилляра за I сек, мг; t1 – период капания, сек, С - концентрация определяемого иона, М.
Id = КС (3)
I - кривая остаточного тока; 2 - волна восстановления катиона металла и способ определения ее высоты; 3 - полярограмма восстановления смеси катионов металлов
Уравнение Ильковича
Слайд 8Необходимые условия количественного полярографического анализа
Измеряемый ток должен быть диффузионным.
Необходимо создать высокую
Из пробы необходимо удалить кислород путем продувки пробы инертным газом (N2, Ar), т.к. кислород способен восстанавливаться на РКЭ.
Следует предупреждать искажение формы полярограмм из-за образования полярографических максимумов (добавляют ПАВ).
Необходимо поддерживать постоянную температуру и неизменное положение емкости со ртутью на штативе; работать с одним капилляром (чтобы в ур.3 К=const).
При определении нескольких ионов из одной пробы необходимо увеличить разницу в Е1/2 определяемых ионов (например, используя комплексообразование).
Если потенциал разряда определяемых ионов близок или даже более отрицателен, чем потенциал разряда протонов, прибегают к изменению рН среды. Для органических веществ повышение кислотности сдвигает Е1/2 в сторону менее отрицательных потенциалов.
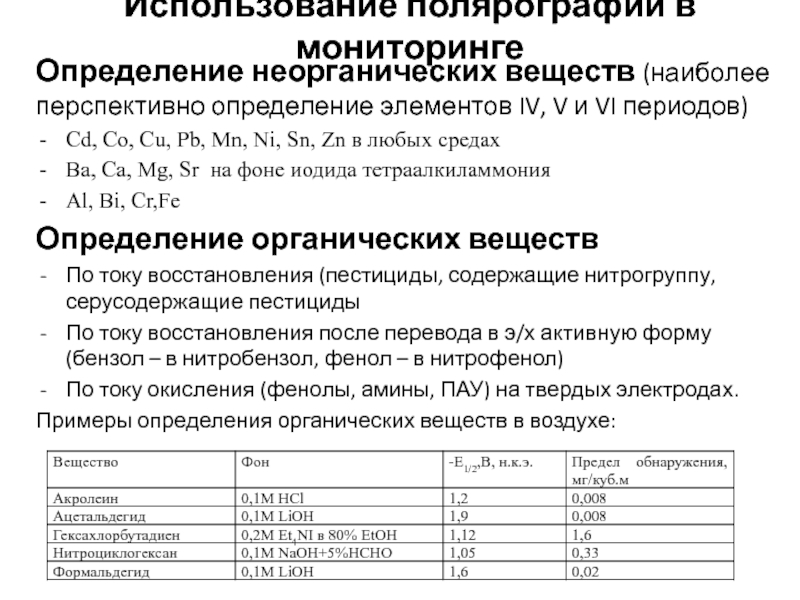
Слайд 11Использование полярографии в мониторинге
Определение неорганических веществ (наиболее перспективно определение элементов IV,
Cd, Co, Cu, Pb, Mn, Ni, Sn, Zn в любых средах
Ba, Ca, Mg, Sr на фоне иодида тетраалкиламмония
Al, Bi, Cr,Fe
Определение органических веществ
По току восстановления (пестициды, содержащие нитрогруппу, серусодержащие пестициды
По току восстановления после перевода в э/х активную форму (бензол – в нитробензол, фенол – в нитрофенол)
По току окисления (фенолы, амины, ПАУ) на твердых электродах.
Примеры определения органических веществ в воздухе:
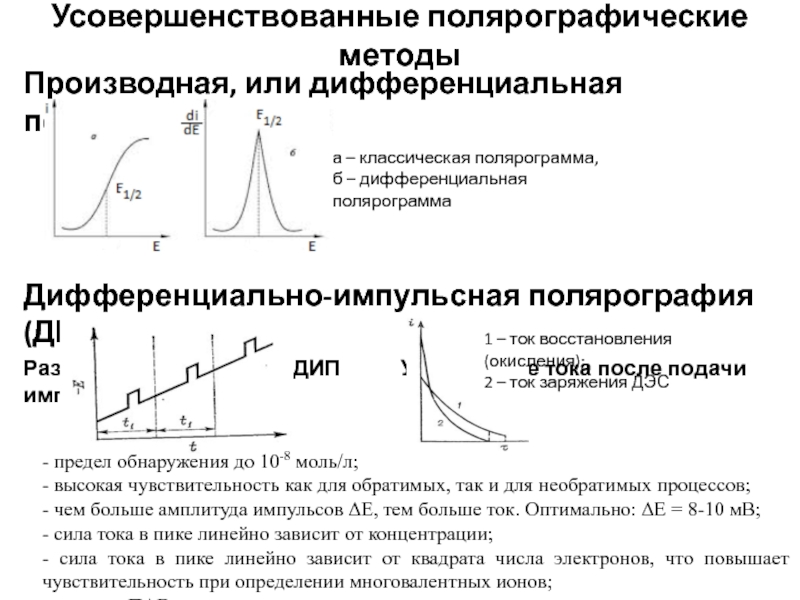
Слайд 12Усовершенствованные полярографические методы
Производная, или дифференциальная полярография
Дифференциально-импульсная полярография (ДИП)
Развертка потенциала в ДИП
1 – ток восстановления (окисления);
2 – ток заряжения ДЭС
а – классическая полярограмма,
б – дифференциальная полярограмма
- предел обнаружения до 10-8 моль/л;
- высокая чувствительность как для обратимых, так и для необратимых процессов;
- чем больше амплитуда импульсов ΔЕ, тем больше ток. Оптимально: ΔЕ = 8-10 мВ;
- сила тока в пике линейно зависит от концентрации;
- сила тока в пике линейно зависит от квадрата числа электронов, что повышает чувствительность при определении многовалентных ионов;
- мешают ПАВ
Слайд 13Инверсионная вольтамперометрия (ИВА)
Q = it
Qнакопл = Qизм
если
Предел обнаружения до 10-8 – 10-9 моль/л.
iпика = f (С) при постоянстве следующих условий:
- время и потенциал предэлектролиза,
- условия конвекции (геометрия ячейки, скорость перемешивания),
- параметры электродной поверхности (площадь, объем, материал, способ предварительной обработки),
- температура,
- состав раствора (фон),
- условия растворения концентрата (скорость развертки потенциала, амплитуда импульса).
Слайд 14Инверсионная вольтамперометрия (ИВА)
Подготовка проб
В качестве фона используются неорганические кислоты, основания,
Из пробы необходимо удалить кислород путем продувки пробы инертным газом (N2, Ar), т.к. кислород способен восстанавливаться сам, а также может окислять выделенные на катоде вещества, уменьшая эффективность стадии осаждения.
Низкий предел обнаружения ИВА предъявляет требования к подготовке проб такие же, как при анализе следов элементов:
- посуда лучше из кварца или тефлона,
- бидистиллят,
- очистка используемых для минерализации кислот и др. реактивов.
Слайд 15Использование ИВА в мониторинге
Может быть использована для определения следов металлов: Cu,
Методом ИВА можно определять и органические вещества, прежде всего те, что образуют нерастворимые соединения с ионами ртути на поверхности ртутных электродов, поляризованных при потенциалах анодного растворения ртути (катодная ИВА).
Определять ИВА можно и соединения, обладающие поверхностной активностью, которые могут накапливаться на ртутном электроде за счет адсорбции, а затем электрохимически восстанавливаться или окисляться. Так, например, определяют бифенил и его хлорпроизводные.
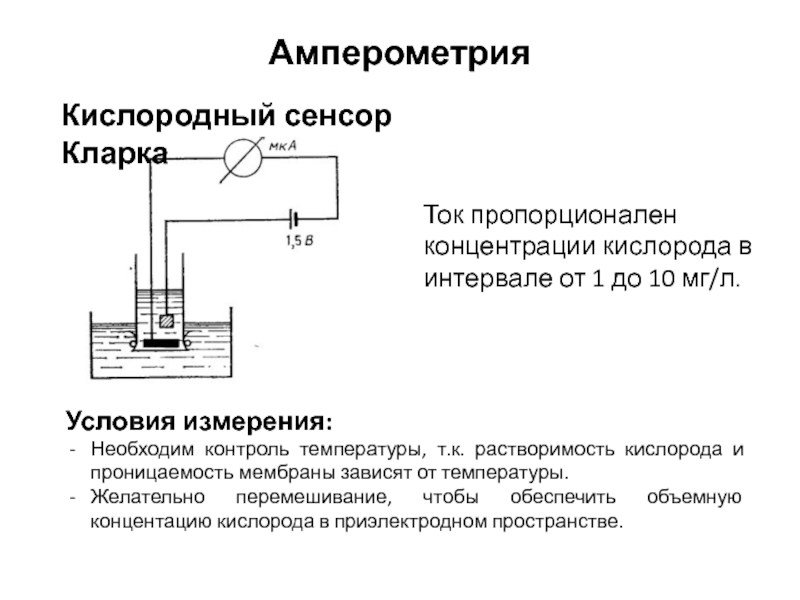
Слайд 16Амперометрия
Кислородный сенсор Кларка
Условия измерения:
Необходим контроль температуры, т.к. растворимость кислорода и проницаемость
Желательно перемешивание, чтобы обеспечить объемную концентацию кислорода в приэлектродном пространстве.
Ток пропорционален концентрации кислорода в интервале от 1 до 10 мг/л.