- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Насыщенный пар. Зависимость давления насыщенного пара от температуры. Кипение презентация
Содержание
- 1. Насыщенный пар. Зависимость давления насыщенного пара от температуры. Кипение
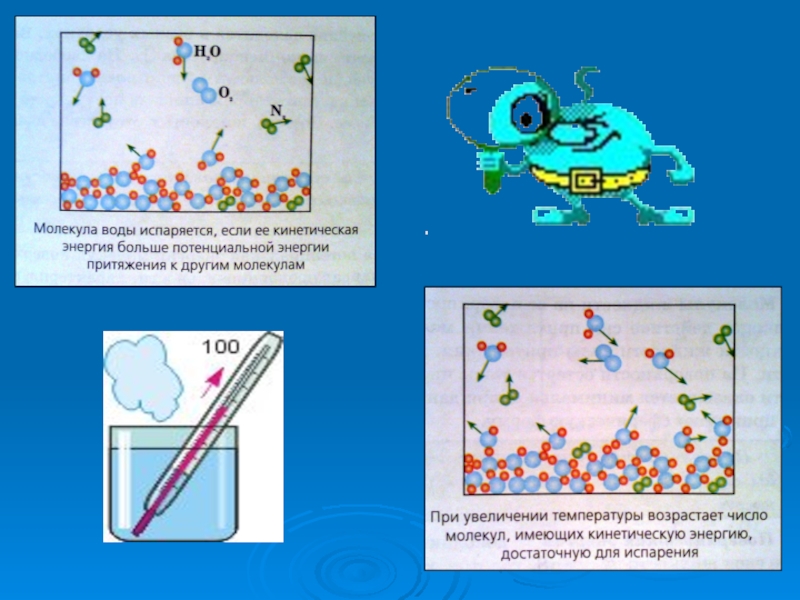
- 2. Испарение Испарение – переход вещества из жидкого состояния в газообразное.
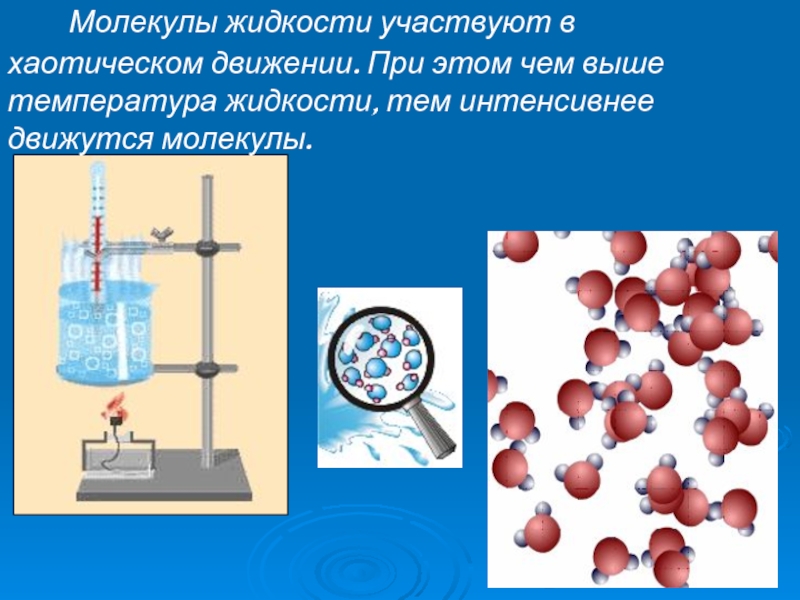
- 3. Молекулы жидкости участвуют в
- 5. Количество жидкости в открытом
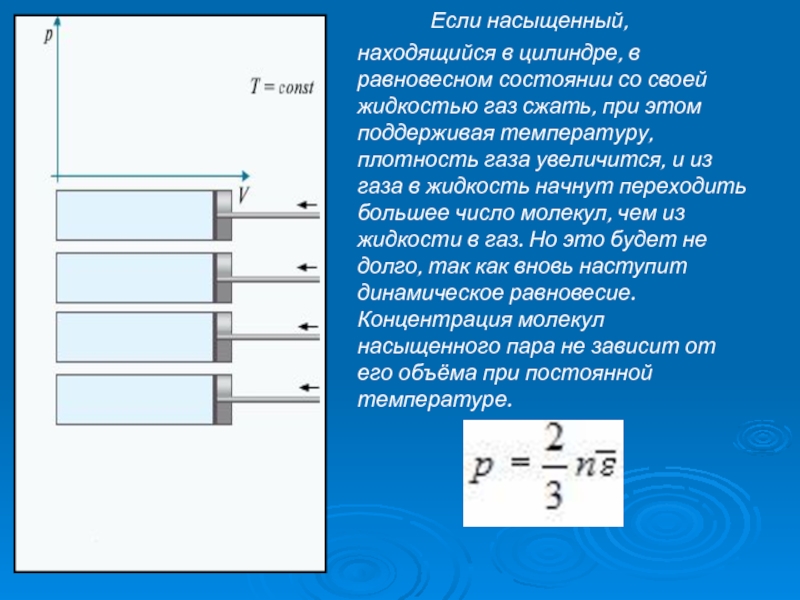
- 6. Если насыщенный, находящийся в
- 7. Пар можно перевести из ненасыщенного в насыщенный:
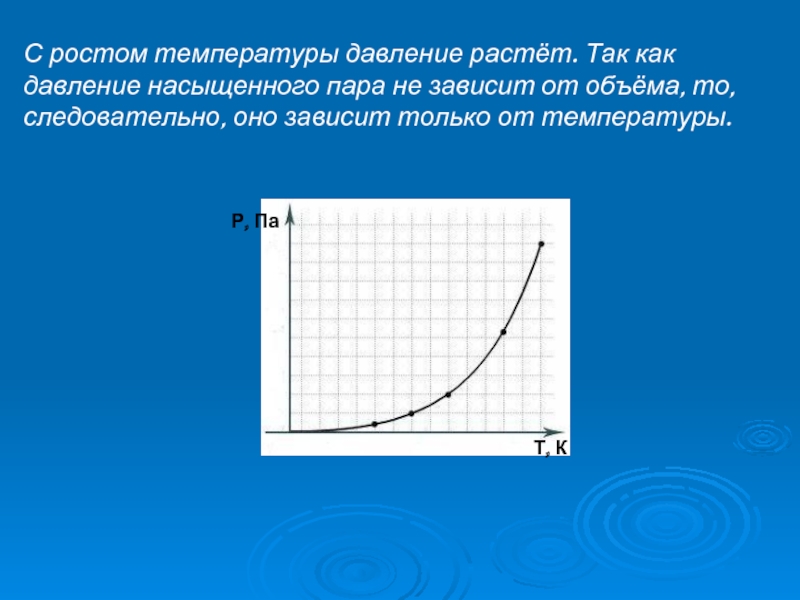
- 8. С ростом температуры давление растёт. Так как
- 9. Процесс испарения может происходить не только с
- 10. Любое вещество, находящееся в газообразном состоянии, может
Слайд 3 Молекулы жидкости участвуют в хаотическом движении. При этом
Слайд 5 Количество жидкости в открытом сосуде непрерывно уменьшается, если
Пар, находящийся в динамическом равновесии со своей жидкостью, называется насыщенным паром.
Слайд 6 Если насыщенный, находящийся в цилиндре, в равновесном состоянии
Слайд 7Пар можно перевести из ненасыщенного в насыщенный: уменьшить объём, понизить температуру.
Состояние насыщенного пара, как показывает опыт, приближёно описывается уравнением состояния идеального газа,
а его давление определяется формулой
Слайд 8С ростом температуры давление растёт. Так как давление насыщенного пара не
Р, Па
Т, К
Слайд 9Процесс испарения может происходить не только с поверхности жидкости, но и
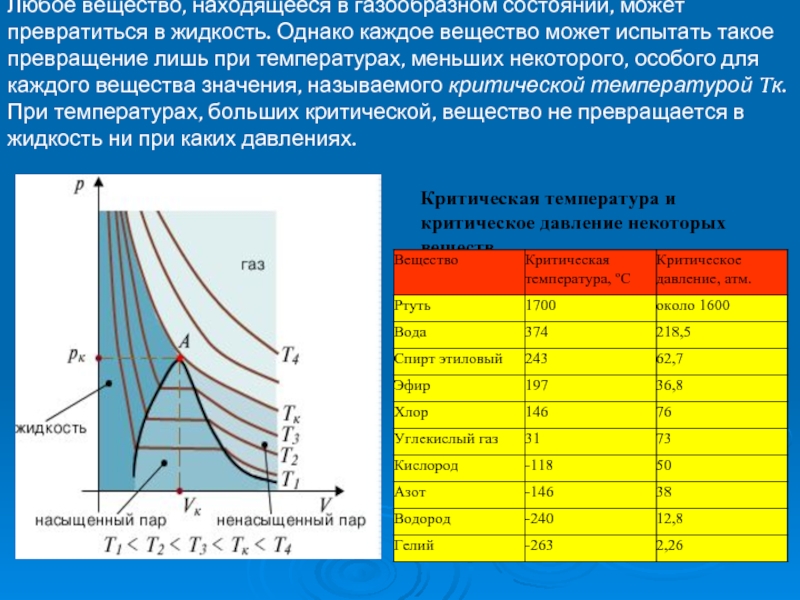
Слайд 10Любое вещество, находящееся в газообразном состоянии, может превратиться в жидкость. Однако
Критическая температура и критическое давление некоторых веществ