- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Комплексные соединения презентация
Содержание
- 1. Комплексные соединения
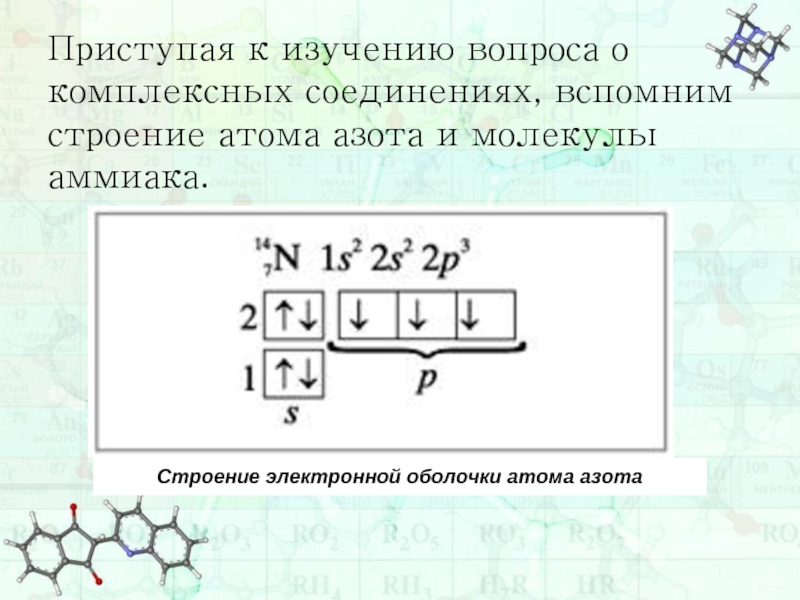
- 2. Приступая к изучению вопроса о комплексных соединениях, вспомним строение атома азота и молекулы аммиака.
- 3. В аммиаке азот затрачивает эти три неспаренных
- 4. Соединения, образование которых не связано с возникновением
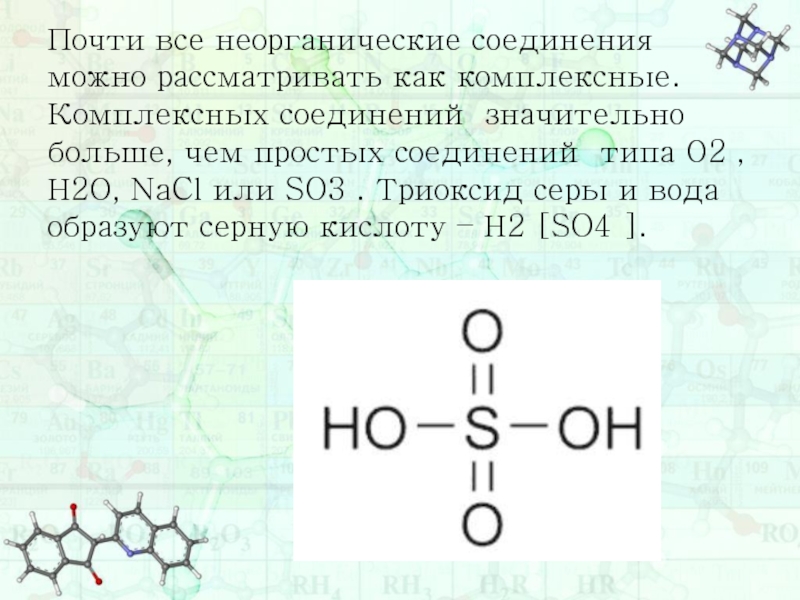
- 5. Почти все неорганические соединения можно рассматривать как
- 6. Наиболее удачно строение и своиства таких соединений
- 7. Виды комплексных соединений Комплексные соединения Соли Пример: K3[Fe(CN)6] Основания Пример: [Ag(NH3)2]OH Кислоты Пример: H[AuCl4]
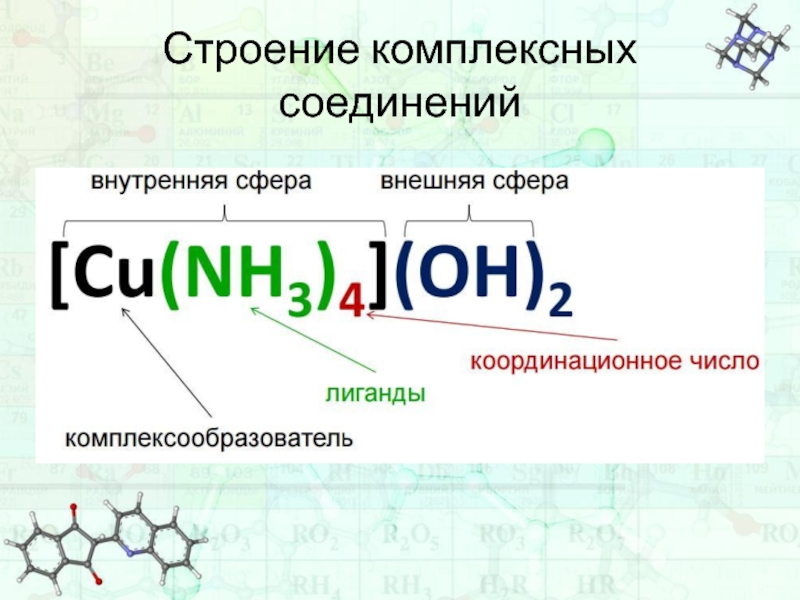
- 8. Строение комплексных соединений
- 9. 1. Установить, входит ли в
- 10. 2.Если этих лигандов больше чем
- 11. 3.После названия лигандов — ионов
- 12. 4. Затем следует название центрального
- 13. 5. В комплексных анионах добавляется суффикс «ат» к названию комплексообразователя Пример: Na[Ag(CN)2] дицианоаргентаАТ натрия
- 14. Составьте комплексные соединения, обозначьте составные части. Na[Al(OH)4
- 15. Демонстрационный опыт Cu(OH)2 + 4NH3 = [Cu(NH3 )4 ](OH)2
- 16. K3 [Fe(CN)6 ] – красная кровяная соль
- 17. К3[Fe(CN)6 ] +3 Fe SO4 = KFe[Fe(CN)6])↓ + 3K2SO4
- 18. K4 [Fe(CN)6 ] – желтая кровяная соль
- 19. 4FeCl3+3K4[Fe(CN)6]=Fe4[Fe(CN)6]3+12KCl
- 20. [Ag(NH3 )2 ]OH – аммиачныйраствор оксида серебра
- 21. Применение комплексных соединений Гальванические покрытия Электролитическое получение
- 22. Спасибо за внимание!
Слайд 2Приступая к изучению вопроса о комплексных соединениях, вспомним строение атома азота
Слайд 3В аммиаке азот затрачивает эти три неспаренных электрона на образование ковалентных
Слайд 4Соединения, образование которых не связано с возникновением новых электронных пар (общая
Слайд 5Почти все неорганические соединения можно рассматривать как комплексные. Комплексных соединений значительно
Слайд 6Наиболее удачно строение и своиства таких соединений объясняет координационная теория.
Создатель теории
Альфред Вернер
Комплексные соединения - вещества, в состав которых входят сложные частицы, содержащие молекулы или сложные ионы, способные к самостоятельному существованию
Слайд 7Виды комплексных соединений
Комплексные
соединения
Соли
Пример:
K3[Fe(CN)6]
Основания
Пример:
[Ag(NH3)2]OH
Кислоты
Пример:
H[AuCl4]
Слайд 9
1. Установить, входит ли в него комплексный катион или комплексный анион.
Название
например: ионы F– – фторо, Cl– – хлоро, I– – йодо, CN– – циано, OH– – гидроксо, CNS– – роданидо;
Составления названия комплексного соединения
гидроксид
тетраамминмеди(II)
[Cu(NH3)4]
(OH)2
Слайд 10
2.Если этих лигандов больше чем один, то их названию предшествует соответствующее
2 – ди,
3 – три,
4 – тетра,
5 – пента,
6 – гекса.
гидроксид
амминмеди(II)
[Cu(NH3) ]
(OH)2
тетра
4
Слайд 11
3.После названия лигандов — ионов название лигандов — нейтральных молекул. При
гидроксид
меди(II)
[Cu ]
(OH)2
тетра
4
аммин
(NH3)
Слайд 12
4. Затем следует название центрального иона комплексообразователя, которое производят от латинского
гидроксид
меди(II)
[Cu ]
(OH)2
тетра
4
аммин
(NH3)
Слайд 135. В комплексных анионах добавляется суффикс «ат» к названию комплексообразователя
Пример:
Na[Ag(CN)2] дицианоаргентаАТ натрия
Слайд 14Составьте комплексные соединения, обозначьте составные части.
Na[Al(OH)4 ] –
Na[Al(OH)6 ] –
Na[Al(OH)4 (H2O)2
тетрагидроксоалюминат натрия
гексагидроксоалюминат натрия
диакватетрагидроксоалюминат натрия
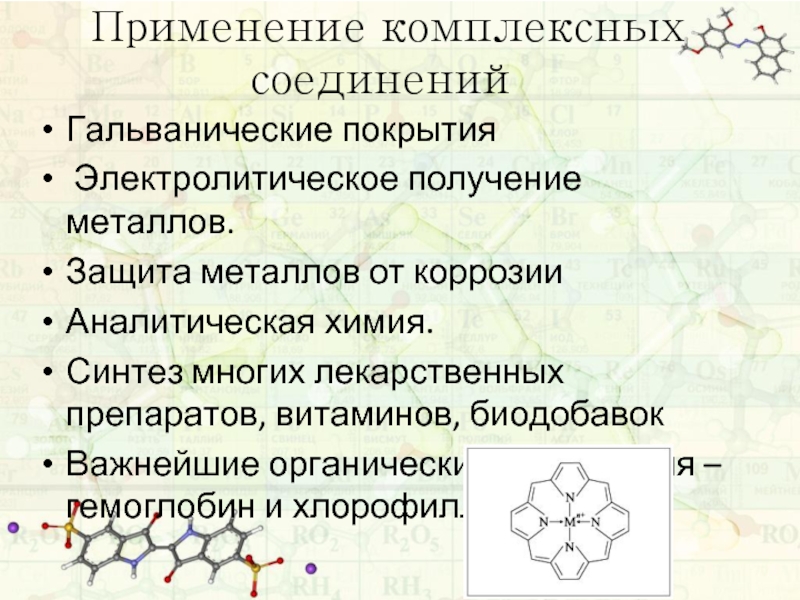
Слайд 21Применение комплексных соединений
Гальванические покрытия
Электролитическое получение металлов.
Защита металлов от коррозии
Аналитическая химия.
Синтез многих
Важнейшие органические соединения – гемоглобин и хлорофилл




![Виды комплексных соединенийКомплексные соединенияСолиПример:K3[Fe(CN)6]ОснованияПример:[Ag(NH3)2]OHКислотыПример:H[AuCl4]](/img/tmb/1/36844/13ab508c4f1fa8e552f8c683d017d280-800x.jpg)




![5. В комплексных анионах добавляется суффикс «ат» к названию комплексообразователяПример:Na[Ag(CN)2] дицианоаргентаАТ натрия](/img/tmb/1/36844/30047fea87ffdbd57ebeb8e58e89ce52-800x.jpg)
![Составьте комплексные соединения, обозначьте составные части.Na[Al(OH)4 ] –Na[Al(OH)6 ] –Na[Al(OH)4 (H2O)2 ] –тетрагидроксоалюминат натрия гексагидроксоалюминат](/img/tmb/1/36844/58b6e295a1402cb9095664499968dedd-800x.jpg)
2](/img/tmb/1/36844/207f0819643c9206e64ef4ec92c3a8d6-800x.jpg)
![K3 [Fe(CN)6 ] – красная кровяная соль](/img/tmb/1/36844/a11eeff0c24e6f25f8583cd5d4fbec1c-800x.jpg)
![К3[Fe(CN)6 ] +3 Fe SO4 = KFe[Fe(CN)6])↓ + 3K2SO4](/img/tmb/1/36844/888e68df3edafc071db0f170ea32872a-800x.jpg)
![K4 [Fe(CN)6 ] – желтая кровяная соль](/img/tmb/1/36844/c064a6acdba5fea90763bb018435532f-800x.jpg)
![4FeCl3+3K4[Fe(CN)6]=Fe4[Fe(CN)6]3+12KCl](/img/tmb/1/36844/cf105e2212132773b73bca65152d08e0-800x.jpg)
![[Ag(NH3 )2 ]OH – аммиачныйраствор оксида серебра](/img/tmb/1/36844/e9ccd33d667372bbe8c425e94c6872cf-800x.jpg)