- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Коллигативные свойства растворов презентация
Содержание
- 1. Коллигативные свойства растворов
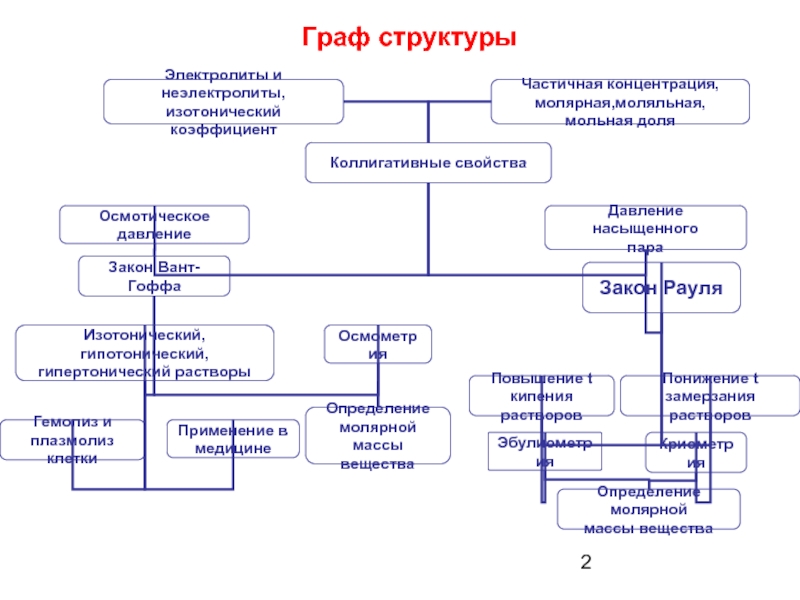
- 2. Граф структуры
- 3. Коллигативные (коллективные) - зависят от
- 4. Закон Рауля: а) Парциальное давление
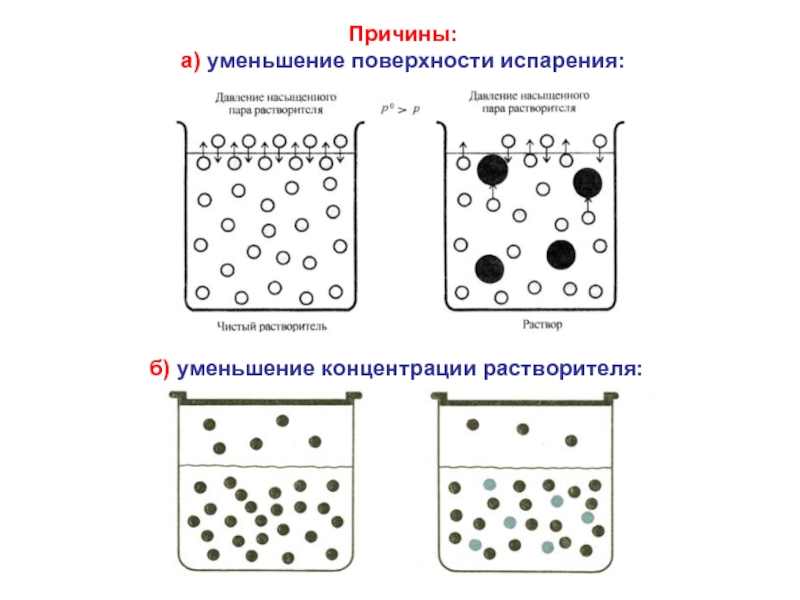
- 5. Причины: а) уменьшение поверхности испарения: б) уменьшение концентрации растворителя:
- 6. Для идеальных растворов понижение
- 7. 2. Эбулиоскопия – повышение Ткип Присутствие растворенного вещества повышает температуру кипения раствора
- 8. Кэ – эбулиоскопическая константа (град/моль·кг); m –
- 9. Значения Кэ
- 10. 3. Криоскопия – понижение Т замерзания
- 11. Криоскопия - способ определения М вещества
- 12. Значения Ккр
- 13. Растворы различных веществ в воде замерзают при
- 15. неорганические: хлориды аммония, натрия, магния,
- 16. 4. Осмос. Осмотическое давление. Осмос - самопроизвольная
- 17. Осмотическое давление – минимальное гидравлическое давление, которое
- 18. В 1901 г. Вант-Гофф стал первым лауреатом Нобелевской
- 19. Невольно большую роль в популяризации новых взглядов
- 20. Уравнение осмотического давления находит широкое применение,
- 21. За счет осмотического давления мог бы удерживаться
- 22. Ученые предполагают, что египтяне откалывали гранитные глыбы,
- 23. Осмотическое давление плазмы крови человека - 7.4-7.8
- 24. i показывает, во сколько
- 25. Осмометры а) с животной мембраной б) с
- 26. Онкотическое давление – осмотическое давление, создаваемое
- 27. Осмолярная концентрация - суммарное
- 28. Физиологические растворы 0,9%-ный ( 0,15
- 29. Изоосмия Изоосмия - постоянство осмотического
- 30. Изо-, гипер- и гипотонические растворы
- 31. Осмотический конфликт: внезапное изменение концентрации растворенных солей
- 32. Осмотический шок: пребывание в воде, которая
- 33. Изменения, происходящие с кровяными тельцами в растворах
- 34. Рабочие «горячих» цехов должны пить подсоленную воду,
- 35. Лизис, плазмолиз, гемолиз.
- 36. Изменения, происходящие с кровяными тельцами в растворах
- 37. Консервирование продуктов питания происходит
- 38. Тургор – осмотическое набухание
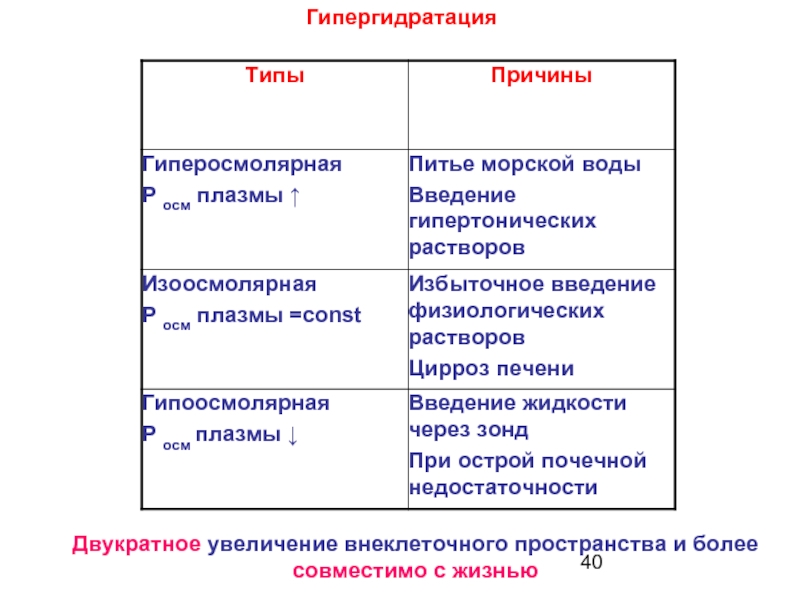
- 39. Гипергидратация – избыточное поступление воды в организм либо недостаточное ее выведение Нарушения водного обмена
- 40. Гипергидратация Двукратное увеличение внеклеточного пространства и более совместимо с жизнью
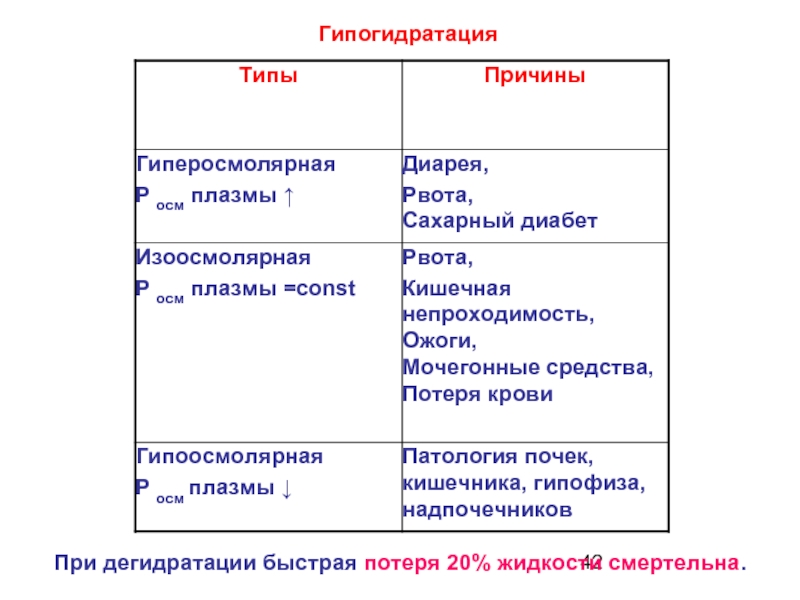
- 41. Гипогидратация – обезвоживание организма вследствие значительного
- 42. Гипогидратация При дегидратации быстрая потеря 20% жидкости смертельна.
- 43. Значение осмотического давления 1.
- 44. 2. Осмотическая очистка морской воды
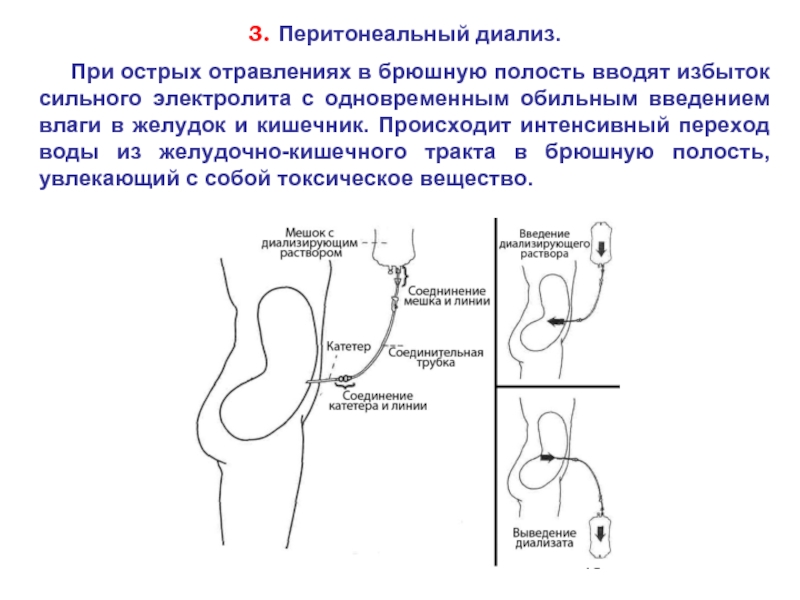
- 45. 3. Перитонеальный диализ. При
- 46. 4. При очистке ран
- 47. 6. Осмос и диализ - основа
- 48. Спасибо за внимание!
Слайд 3 Коллигативные (коллективные) - зависят от количества имеющихся молекул или
Понижение давления пара растворителя.
Повышение температуры кипения растворителя.
Понижение температуры замерзания растворителя.
Явление осмотического давления.
Коллигативные свойства позволили Аррениусу показать, что молекулы растворенного вещества в растворе диссоциируют на ионы.
Коллигативные свойства используются главным образом для определения молекулярных масс неизвестных веществ.
Слайд 4Закон Рауля:
а) Парциальное давление насыщенного пара данного компонента над
б) Относительное понижение давления растворителя равно мольной доле растворенного вещества.
1. Понижение давления пара растворителя:
(нелетучее вещество в летучем растворителе)
Основное направление научных исследований – химия растворов. Его имя связано главным образом с созданием основ криоскопии. Открыл носящий его имя закон о понижении давления пара растворителя. Сконструировал газовую горелку.
Рауль Франсуа
(10.05.1830 – 1.06.1901)
Слайд 6 Для идеальных растворов понижение давления насыщенного пара растворителя
Для реальных растворов, где имеют место межмолекулярные взаимодействия, в это уравнение необходимо ввести изотонический коэффициент:
для электролитов
для неэлектролитов
для веществ, склонных к диссоциации
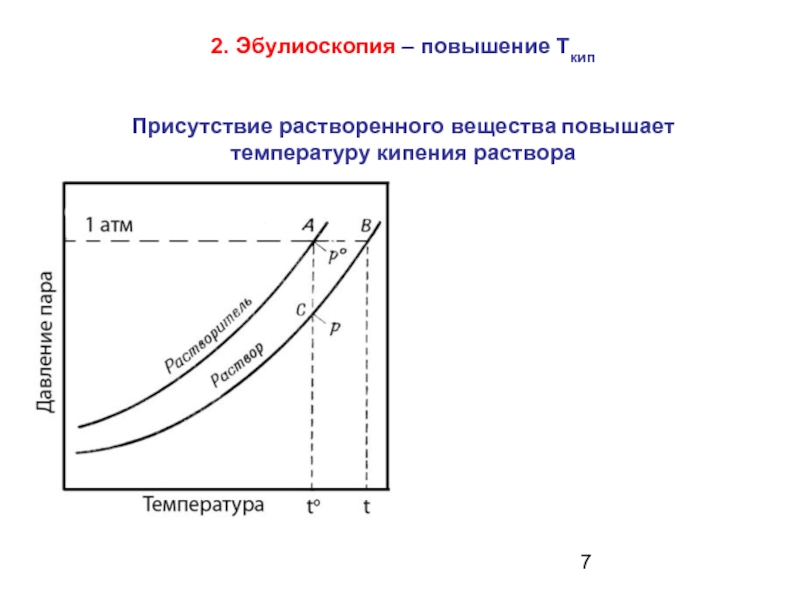
Слайд 72. Эбулиоскопия – повышение Ткип
Присутствие растворенного вещества повышает
температуру кипения раствора
Слайд 8Кэ – эбулиоскопическая константа (град/моль·кг);
m – моляльность (число моль вещества в
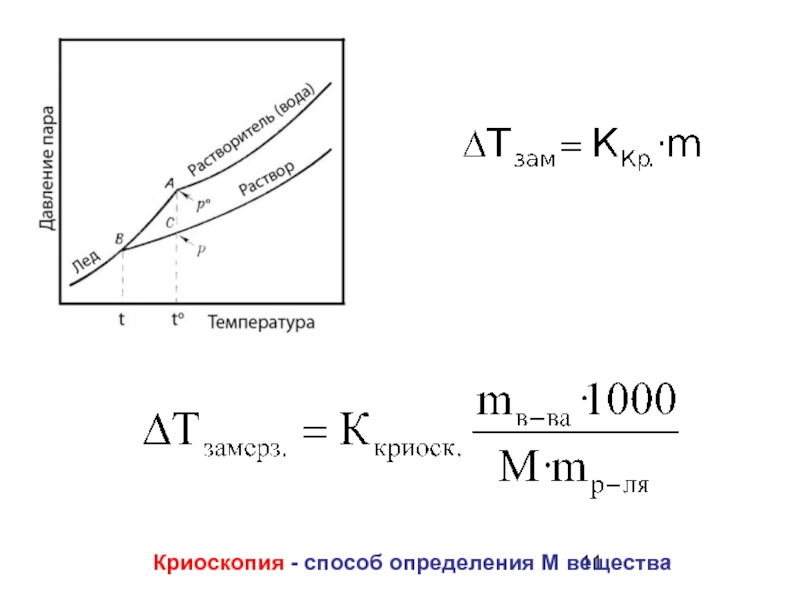
Эбулиоскопия - способ определения М вещества
Слайд 103. Криоскопия – понижение Т замерзания
Присутствие растворенного вещества понижает
температуру замерзания
Причина - молекулам растворителя сложней образовать
гомогенные кристаллы твердой фазы.
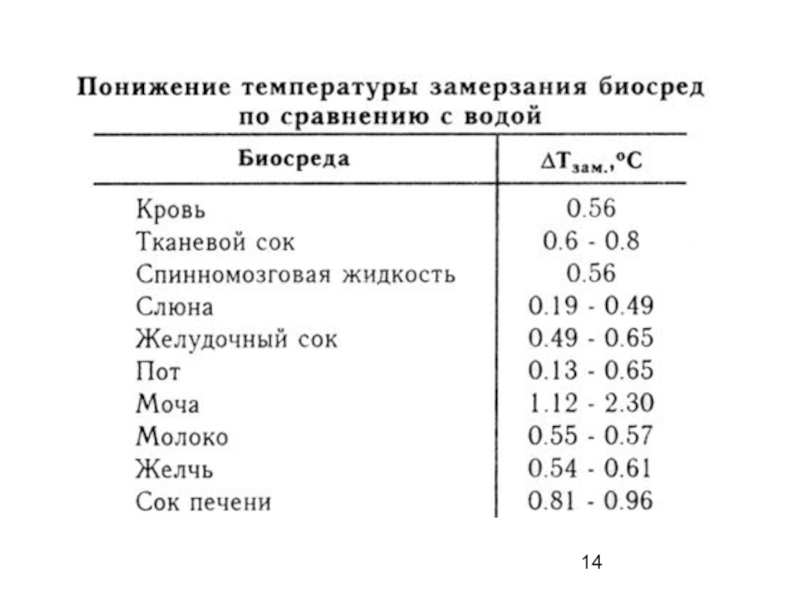
Слайд 13Растворы различных веществ в воде замерзают при температуре ниже 0oС
Одномоляльные растворы
Слайд 15 неорганические: хлориды аммония, натрия, магния, кальция, а также карбонат
органические: этиловый спирт, глицерин и этиленгликоль.
Насыщенный раствор хлористого кальция остается жидким до - 55 °С.
Антифризы - вещества, понижающие температуру замерзания водных растворов
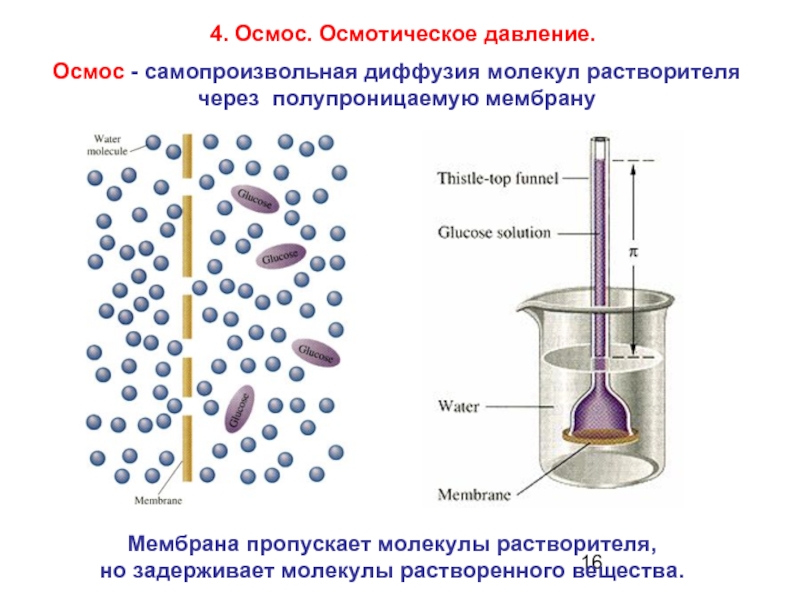
Слайд 164. Осмос. Осмотическое давление.
Осмос - самопроизвольная диффузия молекул растворителя
через полупроницаемую
Мембрана пропускает молекулы растворителя,
но задерживает молекулы растворенного вещества.
Слайд 17Осмотическое давление – минимальное гидравлическое давление, которое нужно приложить к раствору,
Причина осмоса - стремление вещества распределяться равномерно по всему объему растворителя.
Слайд 18В 1901 г. Вант-Гофф стал первым лауреатом Нобелевской премии по химии, которая
В отличие от большинства химиков своего времени Вант-Гофф имел основательную математическую подготовку. Она пригодилась ученому, когда он взялся за сложную задачу изучения скорости реакций и условий, влияющих на химическое равновесие.
Якоб Вант-Гофф
(30.08.1852 –
1.03.1911)
Его теоретические работы внесли существенный вклад в развитие учения о химической кинетике, химическом равновесии, о свойствах растворов. Создал оригинальный метод вычисления химического сродства, разработал основы стереохимии.
Слайд 19Невольно большую роль в популяризации новых взглядов Вант-Гоффа принадлежала профессору Г.
В 1845 году Георг Кольбе
синтезировал уксусную кислоту
Слайд 20 Уравнение осмотического давления находит широкое применение, при определении молекулярных весов
Закон Вант-Гоффа
Осмотическое давление вещества в растворе равно тому давлению, которое оно оказывало, если бы находилось в том же объеме, будучи в газообразном состоянии.
Вант-Гофф и Вильгельм
Оствальд в лаборатории
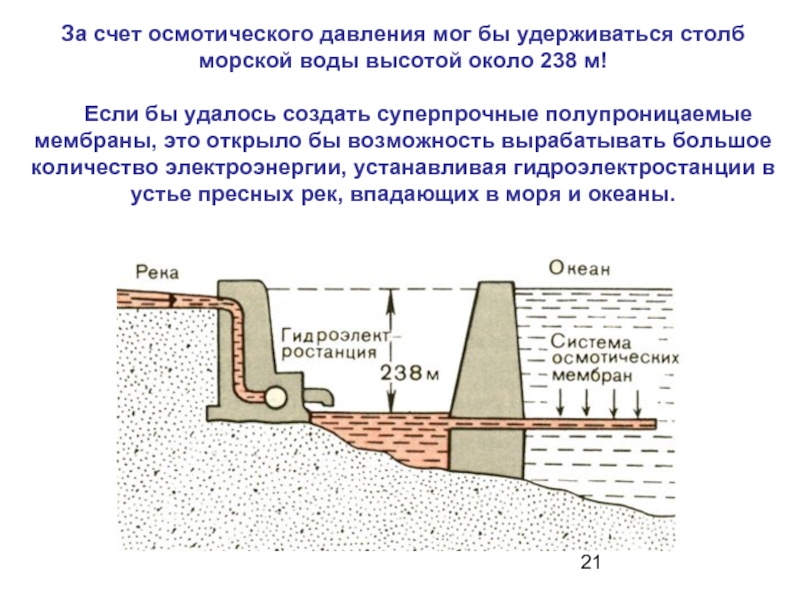
Слайд 21За счет осмотического давления мог бы удерживаться столб морской воды высотой
Если бы удалось создать суперпрочные полупроницаемые мембраны, это открыло бы возможность вырабатывать большое количество электроэнергии, устанавливая гидроэлектростанции в устье пресных рек, впадающих в моря и океаны.
Слайд 22Ученые предполагают, что египтяне откалывали гранитные глыбы, заливая помещенные в расщелины
соленым раствором.
Для 1М раствора любого вещества при T = 273 К
Росм = 2270 кПа или 22,4 атм.
1 атм = 101.325 кПа
Слайд 23Осмотическое давление
плазмы крови человека - 7.4-7.8 атм
( 740 – 780 кПа)
рыб
до15 атм.
растений
до 100 атм.
прорастающих семян
до 400 атм.
Слайд 24 i показывает, во сколько раз истинная концентрация кинетически
Коэффициент Вант-Гоффа можно определить вышеизложенными методами
Для растворов электролитов в формулу вводится
коэффициент Вант-Гоффа i
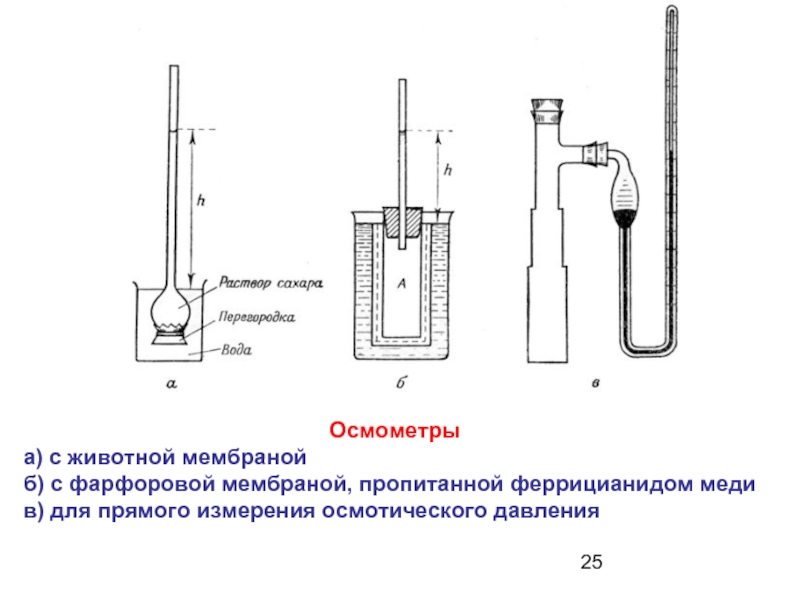
Слайд 25Осмометры
а) с животной мембраной
б) с фарфоровой мембраной, пропитанной феррицианидом меди
в)
Слайд 26Онкотическое давление
– осмотическое давление, создаваемое за счет наличия белков в
Разрушение белков при гнойных процессах сильно увеличивает величину онкотического давления.
При заболеваниях, сопровождающихся уменьшением концентрации белков крови, онкотическое давление падает. Возникают так называемые онкотические отеки подкожной клетчатки.
Онкотическое давление играет важную роль в процессах всасывания жидкости из тканей в кровеносные сосуды.
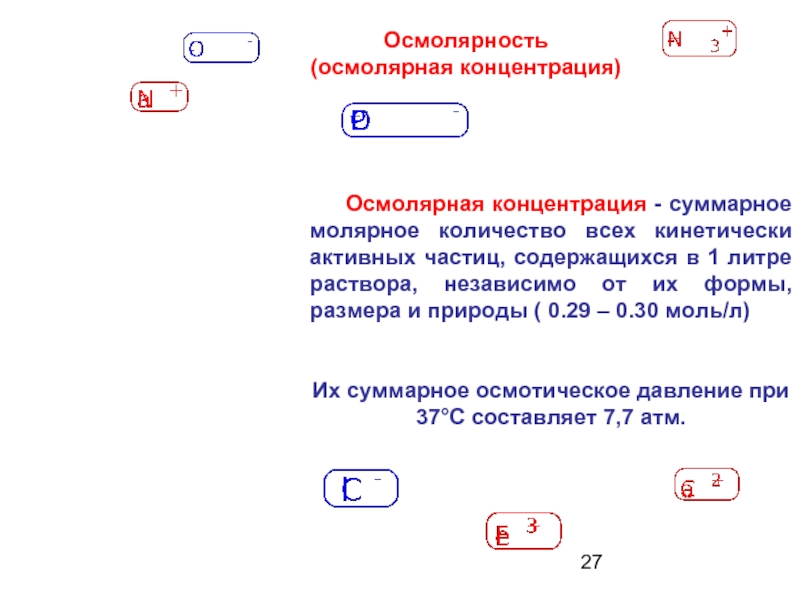
Слайд 27 Осмолярная концентрация - суммарное молярное количество всех кинетически
Их суммарное осмотическое давление при 37°С составляет 7,7 атм.
Осмолярность
(осмолярная концентрация)
Слайд 28Физиологические растворы
0,9%-ный ( 0,15 М ) раствор NаСl и 5%
Истинно физиологическими !!!
считаются растворы, включающие соли, белки и другие вещества в пропорциях, соответствующих их содержанию в крови человека и используемые в аппарате «искусственная почка»
Слайд 29Изоосмия
Изоосмия - постоянство осмотического давления физиологических сред (фундаментальное физико-химическое
Нарушение изоосмии оказывается губительным для организма гораздо раньше, чем наступает плазмолиз или лизис клеток.
Понижение осмотического давления (избыток воды, потеря солей) вызывает рвоту, судороги, затемнение сознания, вплоть до гибели организма.
Повышение же осмотического давления (потеря воды, избыток солей) вызывает их отеки, в первую очередь подкожной клетчатке.
Слайд 30Изо-, гипер- и гипотонические растворы
Изотонические - с одинаковым осмотическим
Гипертонические - с большим осмотическим давлением (>0.9%)
Гипотонические - с меньшим осмотическим давлением (<0.9%)
Во всех случаях, когда в кровяное русло, мышечную ткань, спинномозговой канал в терапевтических целях вводят растворы, необходимо избегать «осмотического конфликта».
Слайд 31Осмотический конфликт: внезапное изменение концентрации растворенных солей - например, если рыбу
Лечение. Приведите содержание минеральных солей в воде к уровню, приемлемому для данного вида рыб.
В случае осмотического шока это соответствие должно быть полным, а установить его нужно немедленно. Недавно приобретенных рыб, если они явно поражены, лучше перевести в другой аквариум с подходящим химическим составом воды (например, в карантинный аквариум, где они в любом случае должны какое-то время находиться!), вместо того чтобы изменять химический состав воды в основном аквариуме, так как это может вызвать осмотический шок у рыб, уже живущих там. Потом воду в карантинном аквариуме можно постепенно, в течение 2-3 недель, привести в соответствие с водой в основном аквариуме и тогда перевести новых рыб в их постоянное жилище.
Слайд 32
Осмотический шок: пребывание в воде, которая либо неестественно богата минеральными веществами,
В случае осмотического стресса концентрацию растворенных солей следует изменять постепенно в течение 1-2 недель, чтобы избежать осмотического шока.
Слайд 33Изменения, происходящие с кровяными тельцами в растворах NaCl различной концентрации
При введении
1) осмотический шок
2) осмотический конфликт
3) флуороз
4) ацидоз
При введении гипотонических растворов наблюдается:
1) осмотический шок
2) осмотический конфликт
3) ацидоз
4) алкалоз
Слайд 34Рабочие «горячих» цехов должны пить подсоленную воду, так как в результате
осмотическое давление у них понижается !
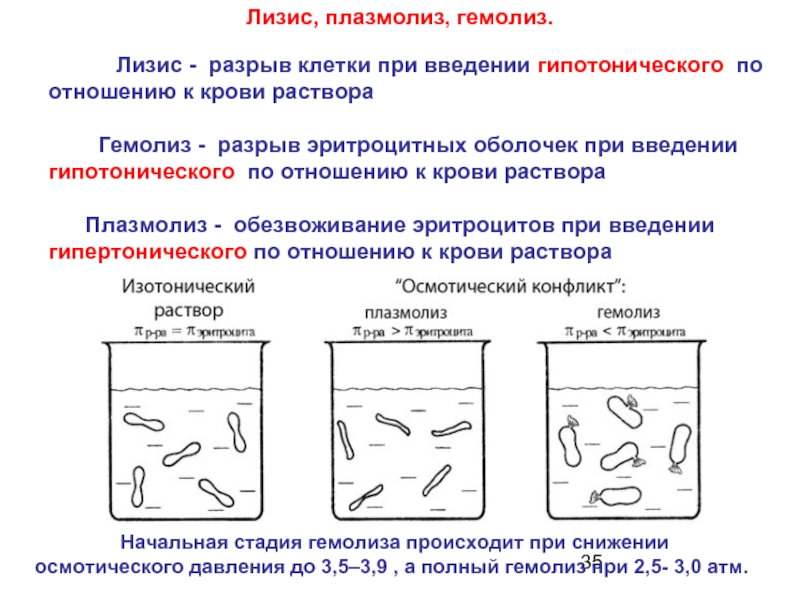
Слайд 35Лизис, плазмолиз, гемолиз.
Лизис - разрыв
Гемолиз - разрыв эритроцитных оболочек при введении
гипотонического по отношению к крови раствора
Плазмолиз - обезвоживание эритроцитов при введении
гипертонического по отношению к крови раствора
Начальная стадия гемолиза происходит при снижении
осмотического давления до 3,5–3,9 , а полный гемолиз при 2,5- 3,0 атм.
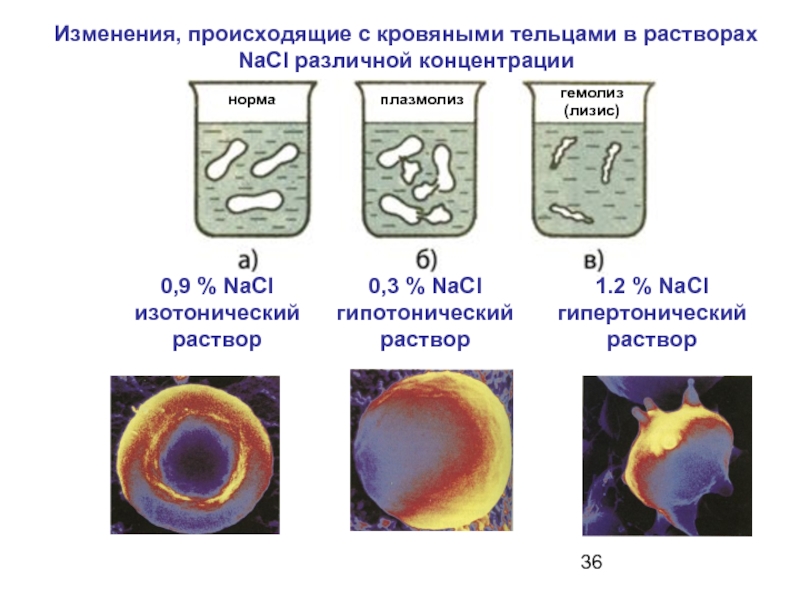
Слайд 36Изменения, происходящие с кровяными тельцами в растворах NaCl различной концентрации
норма
гемолиз
(лизис)
плазмолиз
0,9
изотонический раствор
0,3 % NaCl
гипотонический раствор
1.2 % NaCl
гипертонический раствор
Слайд 37 Консервирование продуктов питания происходит благодаря уничтожению микроорганизмов вследствие
Плазмолиз также наблюдается при посыпании ягод или фруктов сахаром, а овощей, мяса или
рыбы - солью.
Слайд 38Тургор
– осмотическое набухание клетки с появлением сильного внутреннего
Тургор определяет объем и форму клеток (эритроцитов).
Для нормального функционирования тургорное давление должно быть ниже осмотического - только в этих условиях наблюдается активный транспорт в клетку.
Испарение воды листьями в окружающую среду (транспирация) поддерживается накоплением воды через ствол и ветви за счет осмотического давления.
Слайд 39Гипергидратация – избыточное поступление воды в организм либо недостаточное ее выведение
Нарушения
Слайд 41
Гипогидратация – обезвоживание организма вследствие значительного снижения поступления воды в организм,
либо чрезмерные её потери.
Слайд 43Значение осмотического давления
1. Слабительное действие глауберовой соли Na2SO4·10H2O
Плохая всасываемость стенками желудка вызывает интенсивный переход воды внутрь кишечника, способствуя послабляющему действию.
Слайд 453. Перитонеальный диализ.
При острых отравлениях в брюшную полость
Слайд 46 4. При очистке ран от гноя и носителей
5. При глаукоме гипертонические растворы вводят внутривенно чтобы снизить внутриглазное давление.
Слайд 47 6. Осмос и диализ - основа ряда физиологических процессов:
7. Осмос при купании
В пресной воде болевые ощущения, резь в глазах более заметны (осмос воды направлен внутрь глазного яблока).
В морской воде замечается покраснение глаз с незначительными болевыми ощущениями (осмос воды направлен из глазного яблока в морскую воду)