- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Классификация химических реакций презентация
Содержание
- 1. Классификация химических реакций
- 2. Какие явления относятся к (Ф) физическим,
- 3. ПРОВЕРИМ! Ф – 1, 2, 5, 8,
- 4. ПОВТОРИМ! Что такое химическая реакция? Перечислите
- 5. Расставить коэффициенты P2O5 + H2O =HPO3
- 6. ПРОВЕРИМ! P2O5 + H2O =2HPO3 2Fe(OH)3
- 7. Классификация – распределение объектов и явлений
- 8. Классификация химических реакций по числу и составу исходных
- 9. РЕАКЦИИ СОЕДИНЕНИЯ 2H2 + O2
- 10. РЕАКЦИИ РАЗЛОЖЕНИЯ Cu(OH)2
- 11. РЕАКЦИИ ЗАМЕЩЕНИЯ Fe + CuSO4
- 12. РЕАКЦИИ ОБМЕНА BaCl2+H2SO4
- 13. ЗАКРЕПИМ! ТИПЫ РЕАКЦИЙ РАЗЛОЖЕНИЕ АВ = А+В
- 14. ЗАКРЕПИМ! P2O5 + H2O =2HPO3 2Fe(OH)3 =
- 15. Указать тип химических реакций, расставить коэффициенты.
- 16. Дописать уравнение, указать тип реакций, расставить коэффициенты.
- 17. ОБОБЩИМ! ХИМИЧЕСКИЕ РЕАКЦИИ НОВЫЕ ВЕЩЕСТВА ПРИЗНАКИ
Слайд 2Какие явления относятся к (Ф) физическим,
а какие к (Х) химическим.
кипение
образование на деревьях инея,
скисание молока,
ржавление гвоздя,
таяние льда,
горение бенгальских огней,
гниение растений,
приготовление сахарной пудры из сахара,
горение свечи,
растворение соли.
Слайд 3ПРОВЕРИМ!
Ф – 1, 2, 5, 8, 10
Х – 3, 4, 6,
«5» - без ошибок,
«4» - 1-2 ошибки,
«3» - 3-4 ошибки.
Слайд 4ПОВТОРИМ!
Что такое химическая реакция?
Перечислите признаки протекания химической реакции.
Какие условия необходимы
Приведи примеры химических реакций из повседневной жизни.
Слайд 5Расставить коэффициенты
P2O5 + H2O =HPO3
Fe(OH)3 = Fe2O3 + H2O
KClO3
Al + S = Al2S3
Zn + HCl = ZnCl2 + H2
Cu(НСО3)2 = CuO + CO2 + H2O
HgO = Hg + O2
CaCO3 + HNO3 =Ca(NO3)2 + H2CO3
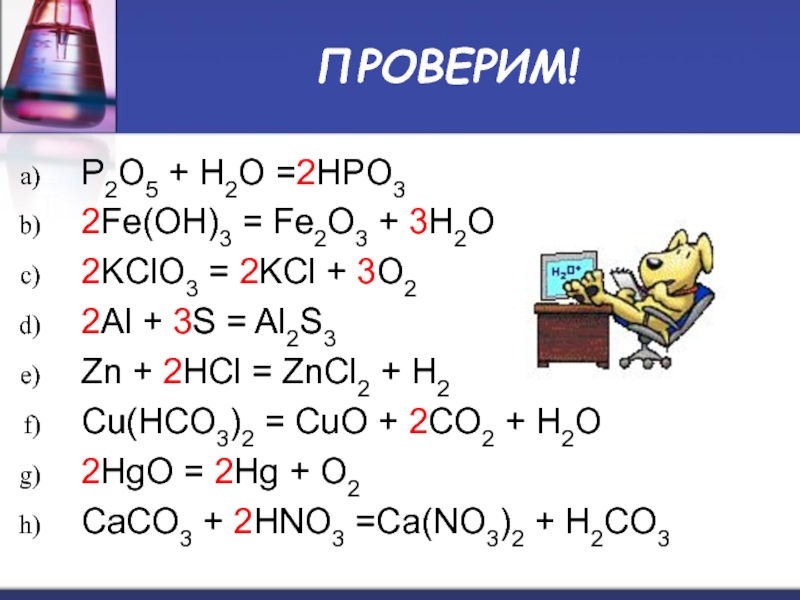
Слайд 6ПРОВЕРИМ!
P2O5 + H2O =2HPO3
2Fe(OH)3 = Fe2O3 + 3H2O
2KClO3 =
2Al + 3S = Al2S3
Zn + 2HCl = ZnCl2 + H2
Cu(НСО3)2 = CuO + 2CO2 + H2O
2HgO = 2Hg + O2
CaCO3 + 2HNO3 =Ca(NO3)2 + H2CO3
Слайд 7 Классификация –
распределение объектов и явлений по классам, группам на основе
Слайд 8Классификация химических реакций по числу и составу исходных и полученных веществ
РЕАКЦИИ СОЕДИНЕНИЯ
РЕАКЦИИ РАЗЛОЖЕНИЯ
РЕАКЦИИ
РЕАКЦИИ ОБМЕНА
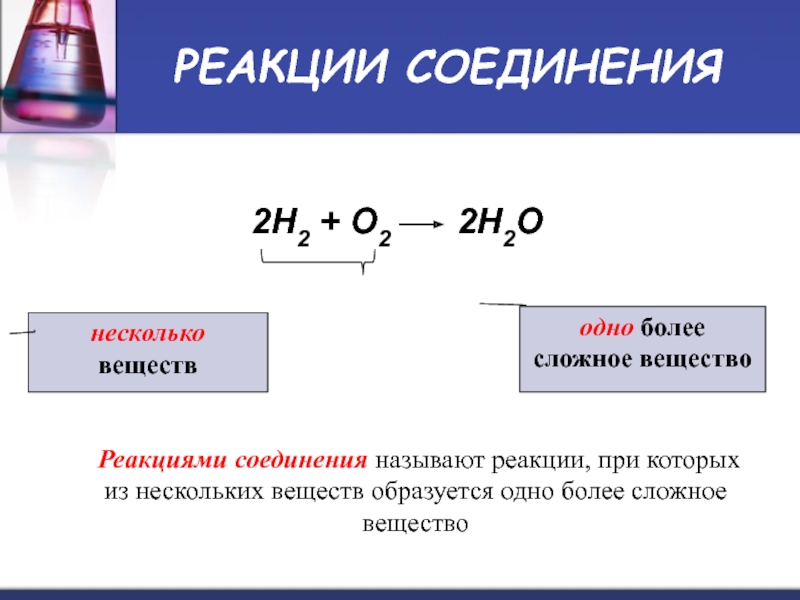
Слайд 9РЕАКЦИИ СОЕДИНЕНИЯ
2H2 + O2 2H2O
несколько
веществ
одно более
сложное
Реакциями соединения называют реакции, при которых из нескольких веществ образуется одно более сложное вещество
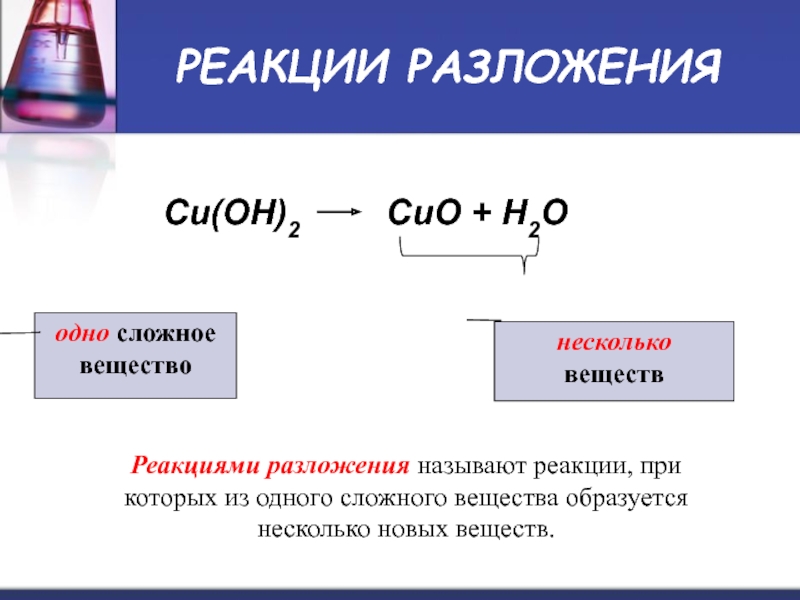
Слайд 10РЕАКЦИИ РАЗЛОЖЕНИЯ
Cu(OH)2 CuO + H2O
одно сложное вещество
несколько
веществ
Реакциями разложения называют реакции, при которых из одного сложного вещества образуется несколько новых веществ.
Слайд 11РЕАКЦИИ ЗАМЕЩЕНИЯ
Fe + CuSO4 FeSO4 +
ПРОСТОЕ ВЕЩЕСТВО
СЛОЖНОЕ ВЕЩЕСТВО
Реакциями замещения называют реакции, при которых атомы простого вещества замещают один из элементов в сложном веществе.
Слайд 12РЕАКЦИИ ОБМЕНА
BaCl2+H2SO4 BaSO4+ 2HCl
Реакциями обмена называют
Слайд 13ЗАКРЕПИМ!
ТИПЫ РЕАКЦИЙ
РАЗЛОЖЕНИЕ
АВ = А+В
ЗАМЕЩЕНИЕ
АВ+С=АС+В
АВ+С=ВС+А
ОБМЕНА
АВ+СД=АД+ВС
АВ+СД=АС+ВД
СОЕДИНЕНИЕ
А + В = АВ
Слайд 14ЗАКРЕПИМ!
P2O5 + H2O =2HPO3
2Fe(OH)3 = Fe2O3 + 3H2O
2KClO3 = 2KCl +
2Al + 3S = Al2S3
Zn + 2HCl = ZnCl2 + H2
Cu(НСО3)2 = CuO + 2CO2+H2O
2HgO = 2Hg + O2
CaCO3+2HNO3=Ca(NO3)2+H2CO3
соединение
разложение
разложение
соединение
замещение
разложение
разложение
обмена
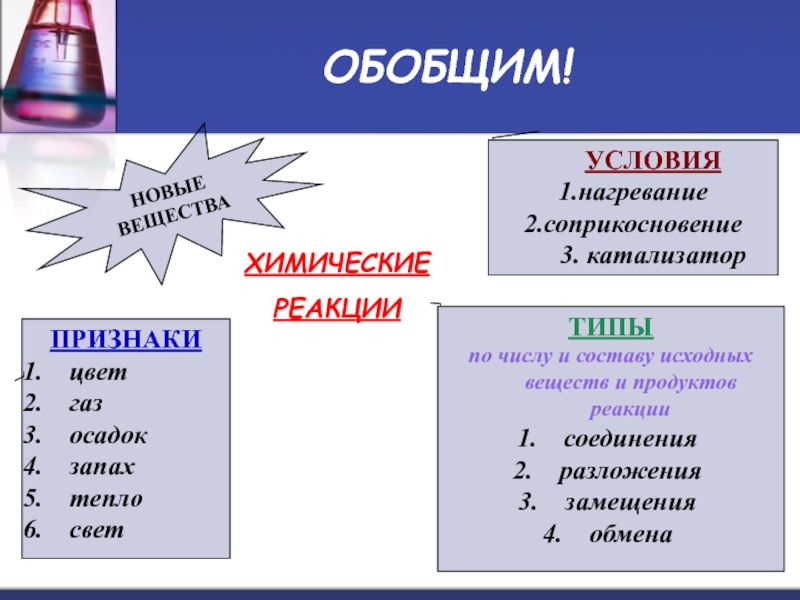
Слайд 17ОБОБЩИМ!
ХИМИЧЕСКИЕ
РЕАКЦИИ
НОВЫЕ ВЕЩЕСТВА
ПРИЗНАКИ
цвет
газ
осадок
запах
тепло
свет
УСЛОВИЯ
1.нагревание
2.соприкосновение
3. катализатор
ТИПЫ
по числу и составу исходных веществ и продуктов
соединения
разложения
замещения
обмена