- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Кислородные соединения азота презентация
Содержание
- 1. Кислородные соединения азота
- 2. N2O - Несолеобразующий оксид. При нагревании разлагается
- 3. Оксид азота (II) Оксид азота NO —
- 4. Оксид азота (III) Оксид N2O3 ( азотистый
- 5. Оксид азота (IV) Оксид азота NO2 —
- 6. Оксид азота (V) Оксид азота N2O5 (азотный
- 7. Азотная кислота Чистая азотная кислота HNO3
- 8. Царская водка Смесь, состоящая из 1 объема
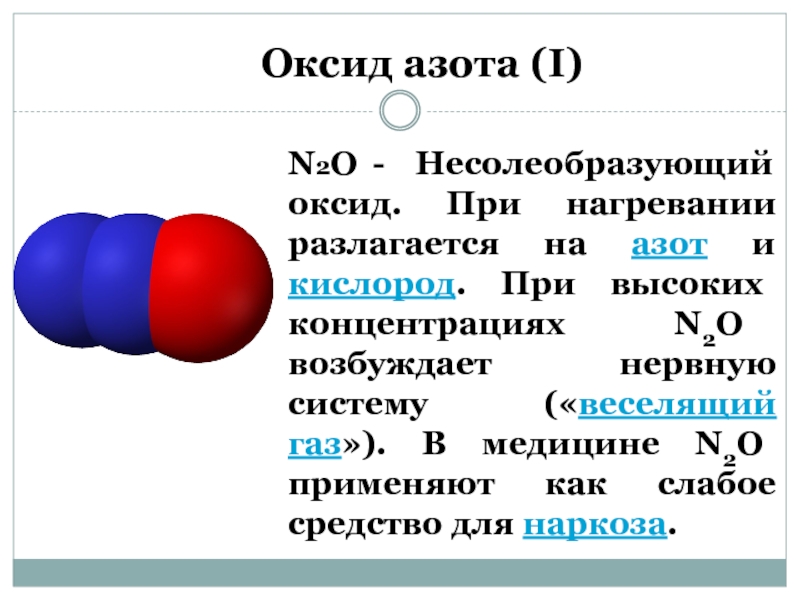
Слайд 2N2O - Несолеобразующий оксид. При нагревании разлагается на азот и кислород.
Оксид азота (I)
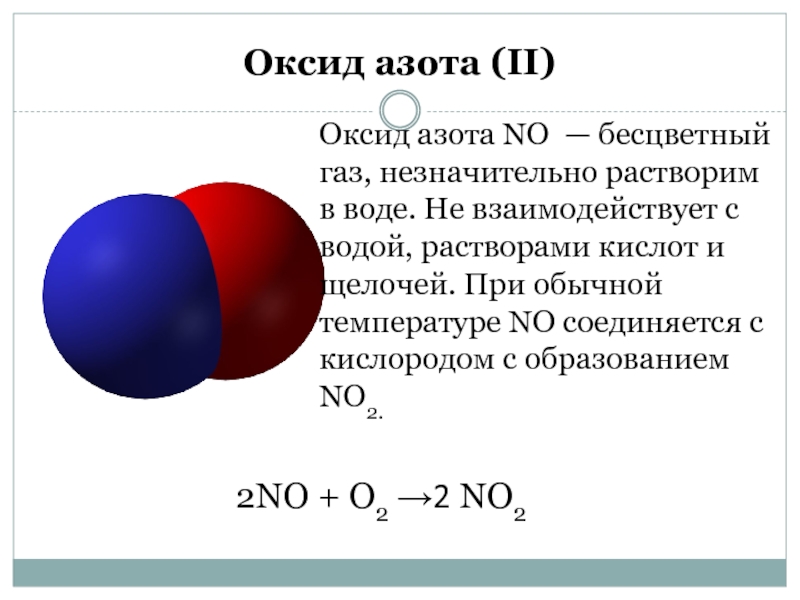
Слайд 3Оксид азота (II)
Оксид азота NO — бесцветный газ, незначительно растворим в
2NO + О2 →2 NO2
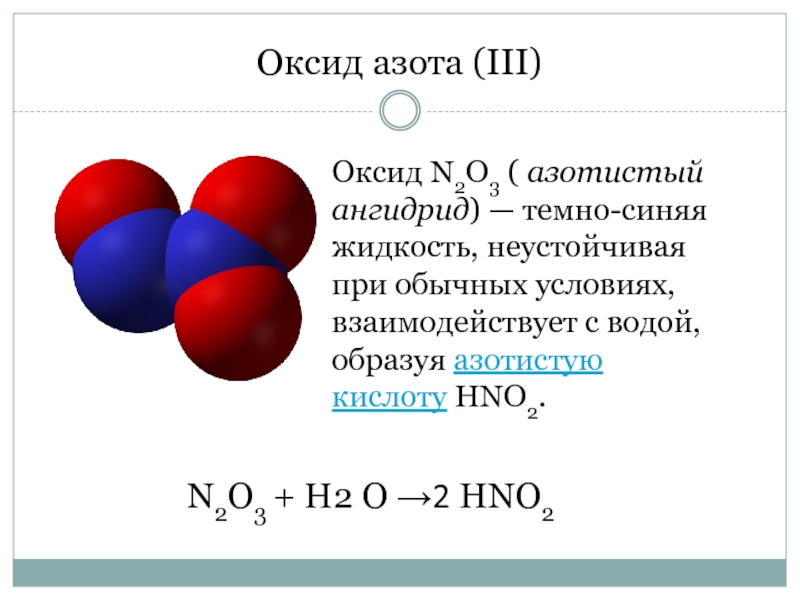
Слайд 4Оксид азота (III)
Оксид N2O3 ( азотистый ангидрид) — темно-синяя жидкость, неустойчивая
N2O3 + Н2 О →2 HNO2
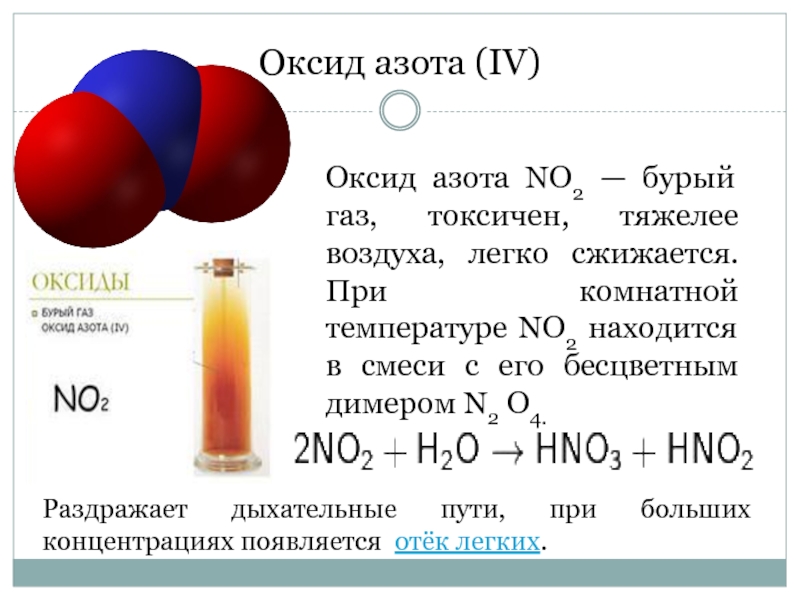
Слайд 5Оксид азота (IV)
Оксид азота NO2 — бурый газ, токсичен, тяжелее воздуха,
:
Раздражает дыхательные пути, при больших концентрациях появляется отёк легких.
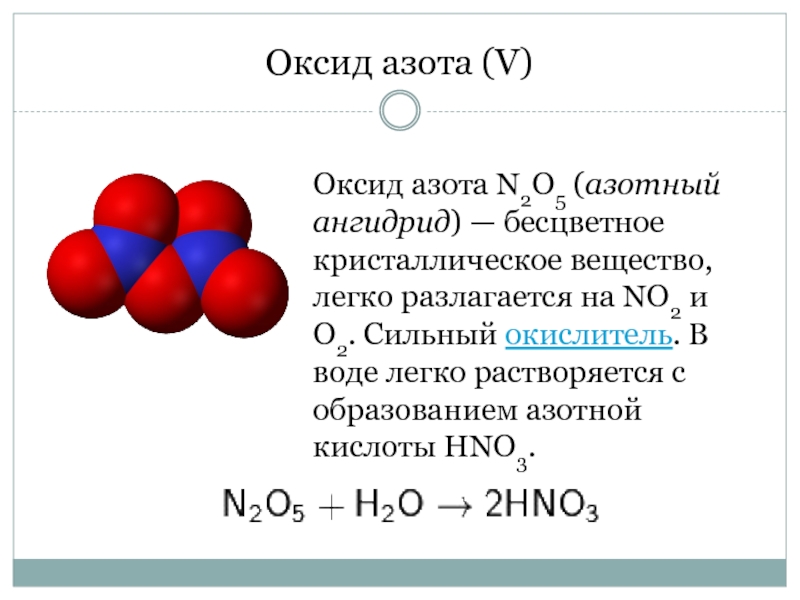
Слайд 6Оксид азота (V)
Оксид азота N2O5 (азотный ангидрид) — бесцветное кристаллическое вещество,
Слайд 7Азотная кислота
Чистая азотная кислота HNO3 —бесцветная жидкость
На воздухе она «дымит»,
Азотная кислота не отличается прочностью, Уже под влиянием света она постепенно разлагается
Слайд 8Царская водка
Смесь, состоящая из 1 объема азотной и 3—4 объемов концентрированной