- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Карбоновые кислоты презентация
Содержание
- 1. Карбоновые кислоты
- 2. 0 1 28.03.2016 Карбоновые кислоты Карбоновые кислоты
- 3. 0 2 28.03.2016 Карбоновые кислоты Карбоновые кислоты
- 4. 3 28.03.2016 Классификация По количеству карбоксильных
- 5. 4 28.03.2016 Номенклатура В основе названий
- 6. 5 28.03.2016 Изомерия Изомерия углеродной цепи.
- 7. 6 28.03.2016 Способы получения Карбоновые кислоты,
- 8. 7 28.03.2016 Химические свойства кислот Карбоновые
- 9. 8 28.03.2016 Химические свойства кислот 5.
- 10. 9 28.03.2016 Муравьиная кислота Муравьиная кислота
Слайд 20
1
28.03.2016
Карбоновые кислоты
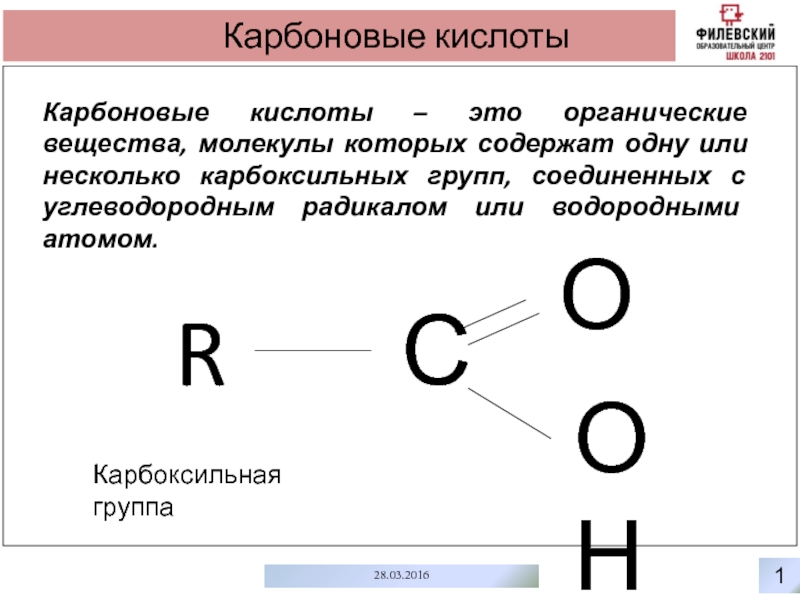
Карбоновые кислоты – это органические вещества, молекулы которых содержат одну
С
О
ОН
R
Карбоксильная группа
Слайд 30
2
28.03.2016
Карбоновые кислоты
Карбоновые кислоты – это органические вещества, молекулы которых содержат одну
С
О
ОН
R
Карбоксильная группа
Карбонильная группа Гидроксильная группа
Слайд 4
3
28.03.2016
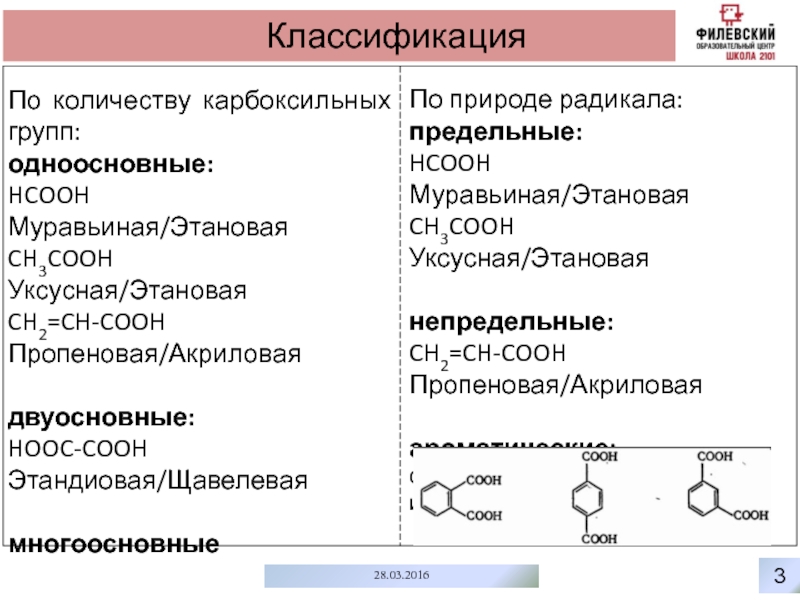
Классификация
По количеству карбоксильных групп:
одноосновные:
HCOOH Муравьиная/Этановая
CH3COOH
CH2=CH-COOH Пропеновая/Акриловая
двуосновные:
HOOC-COOH Этандиовая/Щавелевая
многоосновные
По природе радикала:
предельные:
HCOOH Муравьиная/Этановая
CH3COOH Уксусная/Этановая
непредельные:
CH2=CH-COOH Пропеновая/Акриловая
ароматические:
фталевая, тетрафталевая, изофталевая
Слайд 5
4
28.03.2016
Номенклатура
В основе названий карбоновых кислот лежат названия соответствующих углеводородов. Карбоксильная группа
Очень часто используют тривиальные названия.
Углеводородную цепь нумеруют начиная с атома углерода карбоксильной группы.
7 6 5 4 3 2 1
СН3-СН2-СН-СН2-СН2-СН-СООН
| |
CH3 Cl
2-хлор-5-метилгептановая кислота
Слайд 6
5
28.03.2016
Изомерия
Изомерия углеродной цепи. Начинается с бутановой (масляной) кислоты: масляная кислота, изомасляная
Изомерия положения кратной связи. Бутен-3-овая кислота и бутен-2-овая кислота.
Цис-транс-изомерия
Межклассовая изомерия. Масляной кислоте изомерны метиловый эфир пропановой кисолты и этиловый эфир уксусной кислоты.
Слайд 7
6
28.03.2016
Способы получения
Карбоновые кислоты, можно получить из их солей действуя на них
С
2СН3
O - Na
O
+ H2SO4
С
2СН3
O - H
O
+ Na2SO4
Окисление первичных спиртов – общий способ. В качестве окислителей применяют KMnO4 и K2Cr2O7
Гидролиз галогензамещённых углеводородов, содержащих три атома галогена у одного атома углерода.
R-CCl3 -> R-COOH + H2O
Слайд 87
28.03.2016
Химические свойства кислот
Карбоновые кислоты более сильные кислоты, чем спирты.
Из одноосновных
Муравьиная кислота легко окисляется (реакция «серебряного зеркала»).
При нагревании с концентрированной серной кислотой муравьиная кислота отщепляет воду и образуется оксид углерода (II)
HCOOH -> H2O + CO
HCOOH + Ag2O ? 2Ag +
RCOOH RCOO- + H+
Слайд 9
8
28.03.2016
Химические свойства кислот
5. Образование солей.
2RCOOH + Mg --> (RCOO)2Mg + H2
2RCOOH
RCOOH + NaOH --> RCOONa + H2O
RCOOH + NaHCO3 --> RCOONa + H2O + CO2
6. Минеральные кислоты вытесняют карбоновые из солей.
CH3COONa + HCl --> CH3COOH + NaCl
Слайд 10
9
28.03.2016
Муравьиная кислота
Муравьиная кислота HCOOH названа по кислоте содержащийся в выделениях муравьев.
Она широко применяется в фармацевтической и пищевой промышленности.
Её можно получить путём нагревания окисда углерода (II) с порошкообразным гидроксидом натрия под давлением и обработкой.
200C H2SO4
NaOH + CO ? HCOONa ? HCOOH