- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Качественный анализ (часть 2) презентация
Содержание
- 1. Качественный анализ (часть 2)
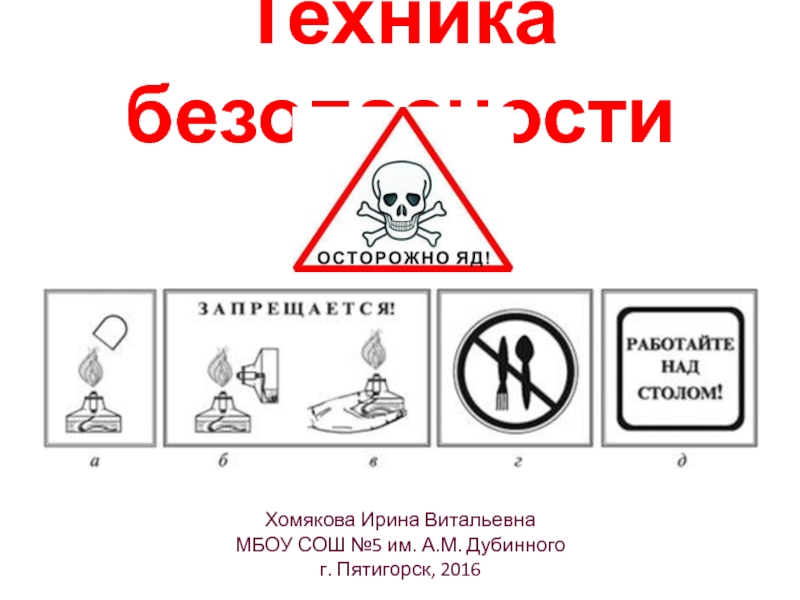
- 2. Техника безопасности Хомякова Ирина Витальевна МБОУ СОШ №5 им. А.М. Дубинного г. Пятигорск, 2016
- 3. Что такое качественный анализ? Качественный анализ –
- 4. Аналитическая реакция – это реакция, которая сопровождается
- 5. Реакции ионного обмена BaCl2 + Na2SO4 =
- 7. Качественные реакции на анионы Cl- Br- I-
- 8. Качественная реакция на Hal- Pb2+ + 2Cl-
- 9. Качественная реакция на SO42- Pb2+ + 2Cl-
- 10. Качественная реакция на CO32- Pb2+ + 2Cl-
- 11. Качественная реакция на PO43- Pb2+ + 2Cl-
- 12. Качественная реакция на SiO32- 2H+ + SiO32–
- 13. Хомякова Ирина Витальевна МБОУ СОШ №5 им. А.М. Дубинного г. Пятигорск, 2016
Слайд 2Техника безопасности
Хомякова Ирина Витальевна
МБОУ СОШ №5 им. А.М. Дубинного
г. Пятигорск,
Слайд 3Что такое качественный анализ?
Качественный анализ – это идентификация (обнаружение) компонентов анализируемых
Хомякова Ирина Витальевна
МБОУ СОШ №5 им. А.М. Дубинного
г. Пятигорск, 2016
Слайд 4Аналитическая реакция – это реакция, которая сопровождается каким-либо внешним эффектом (образование
Хомякова Ирина Витальевна
МБОУ СОШ №5 им. А.М. Дубинного
г. Пятигорск, 2016
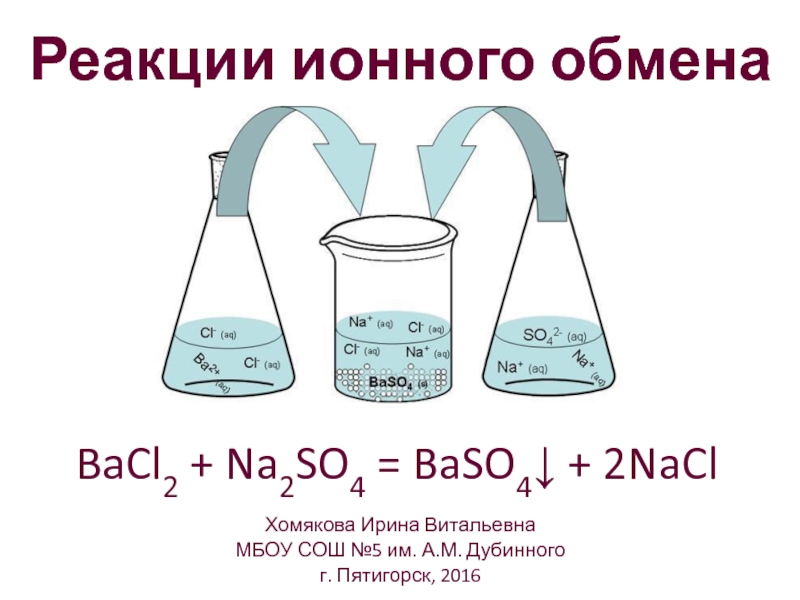
Слайд 5Реакции ионного обмена
BaCl2 + Na2SO4 = BaSO4↓ + 2NaCl
Хомякова Ирина Витальевна
МБОУ
г. Пятигорск, 2016
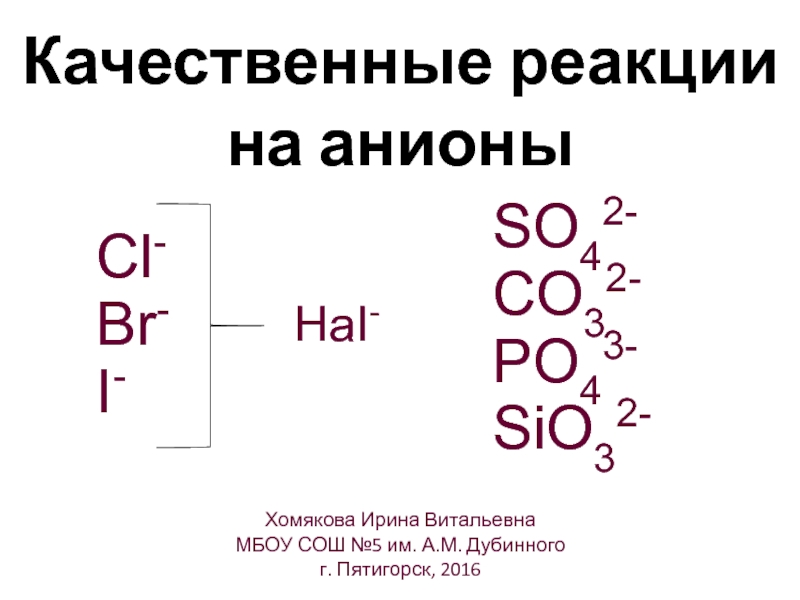
Слайд 7Качественные реакции на анионы
Cl-
Br-
I-
SO42-
CO32-
PO43-
SiO32-
HaI-
Хомякова Ирина Витальевна
МБОУ СОШ №5 им. А.М. Дубинного
г. Пятигорск, 2016
Слайд 8Качественная реакция на Hal-
Pb2+ + 2Cl- = PbCl2↓
Hg22+ + 2Cl- =
Pb2+ + 2Cl- = PbCl2↓
Hg22+ + 2Cl- = Hg2Cl2↓
Pb2+ + 2Cl- = PbCl2↓
Hg22+ + 2Cl- = Hg2Cl2↓
Pb2+ + 2Cl- = PbCl2↓
Hg22+ + 2Cl- = Hg2Cl2↓
К анализируемому раствору добавить р-р AgNO3
a) Если выпал белый осадок, то в анализируемом растворе были ионы Cl-
b) Если выпал бежевый осадок, то в анализируемом растворе были ионы Br-
c) Если выпал желтый осадок, то в анализируемом растворе были ионы l-
Хомякова Ирина Витальевна
МБОУ СОШ №5 им. А.М. Дубинного
г. Пятигорск, 2016
Слайд 9Качественная реакция на SO42-
Pb2+ + 2Cl- = PbCl2↓
Hg22+ + 2Cl- =
Pb2+ + 2Cl- = PbCl2↓
Hg22+ + 2Cl- = Hg2Cl2↓
Pb2+ + 2Cl- = PbCl2↓
Hg22+ + 2Cl- = Hg2Cl2↓
Pb2+ + 2Cl- = PbCl2↓
Hg22+ + 2Cl- = Hg2Cl2↓
Ba2+ + SO42– = BaSO4↓
К анализируемому раствору добавить р-р BaCl2
Если выпал белый осадок, то в анализируемом растворе были ионы SO42-
Хомякова Ирина Витальевна
МБОУ СОШ №5 им. А.М. Дубинного
г. Пятигорск, 2016
Слайд 10Качественная реакция на CO32-
Pb2+ + 2Cl- = PbCl2↓
Hg22+ + 2Cl- =
Pb2+ + 2Cl- = PbCl2↓
Hg22+ + 2Cl- = Hg2Cl2↓
Pb2+ + 2Cl- = PbCl2↓
Hg22+ + 2Cl- = Hg2Cl2↓
Pb2+ + 2Cl- = PbCl2↓
Hg22+ + 2Cl- = Hg2Cl2↓
2Н+ + СO32– = CO2↑ + H2O
К анализируемому раствору добавить р-р H2SO4
Если выделяется бесцветный газ без запаха, то в анализируемом растворе есть ионы СО32-
Хомякова Ирина Витальевна
МБОУ СОШ №5 им. А.М. Дубинного
г. Пятигорск, 2016
Слайд 11Качественная реакция на PO43-
Pb2+ + 2Cl- = PbCl2↓
Hg22+ + 2Cl- =
Pb2+ + 2Cl- = PbCl2↓
Hg22+ + 2Cl- = Hg2Cl2↓
Pb2+ + 2Cl- = PbCl2↓
Hg22+ + 2Cl- = Hg2Cl2↓
Pb2+ + 2Cl- = PbCl2↓
Hg22+ + 2Cl- = Hg2Cl2↓
3Ag+ + PO43– = Ag3PO4↓
К анализируемому раствору добавить р-р AgNO3
Если образовался желтый осадок, то в анализируемом растворе есть ионы PO43-
Хомякова Ирина Витальевна
МБОУ СОШ №5 им. А.М. Дубинного
г. Пятигорск, 2016
Слайд 12Качественная реакция на SiO32-
2H+ + SiO32– = H2SO3↓
К анализируемому раствору добавить
Если выпал белый осадок, то в анализируемом растворе были ионы SiO32-
Хомякова Ирина Витальевна
МБОУ СОШ №5 им. А.М. Дубинного
г. Пятигорск, 2016