- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Химия актиноидов презентация
Содержание
- 1. Химия актиноидов
- 2. ЛИТЕРАТУРА 1. Химия актиноидов: в 3-х т.
- 3. ЛИТЕРАТУРА 7. Несмеянов, Ан. Н. Радиохимия/ Ан.
- 4. ЛИТЕРАТУРА 12. Аменицкая, Р. В. Сборник задач
- 5. Актиноиды. История открытия. Период открытия: XVIII век
- 6. Трансурановые элементы 1. Происходит последовательный захват нескольких
- 7. Трансурановые элементы 3. Облучением элементов 7 периода
- 8. Актиноиды. Попытки размещения в ПС
- 9. Актиноиды. Попытки размещения в ПС Актиноидная
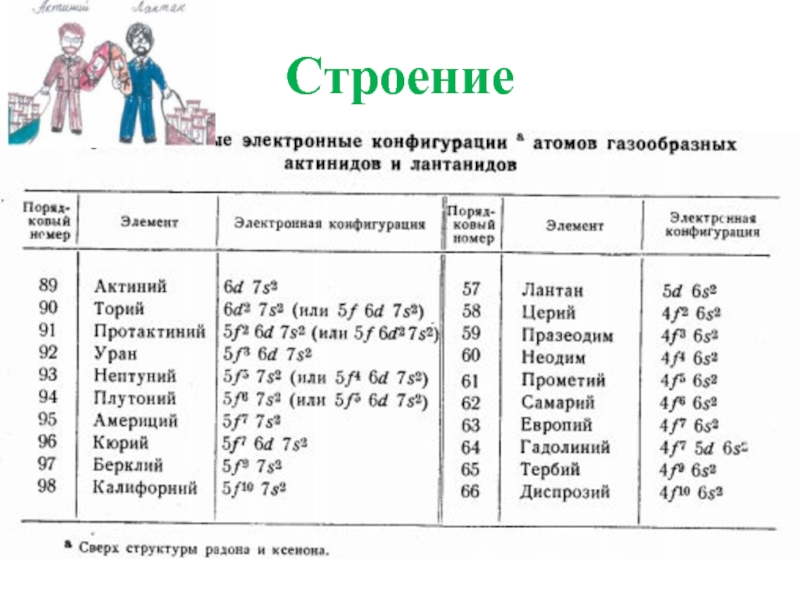
- 10. Строение
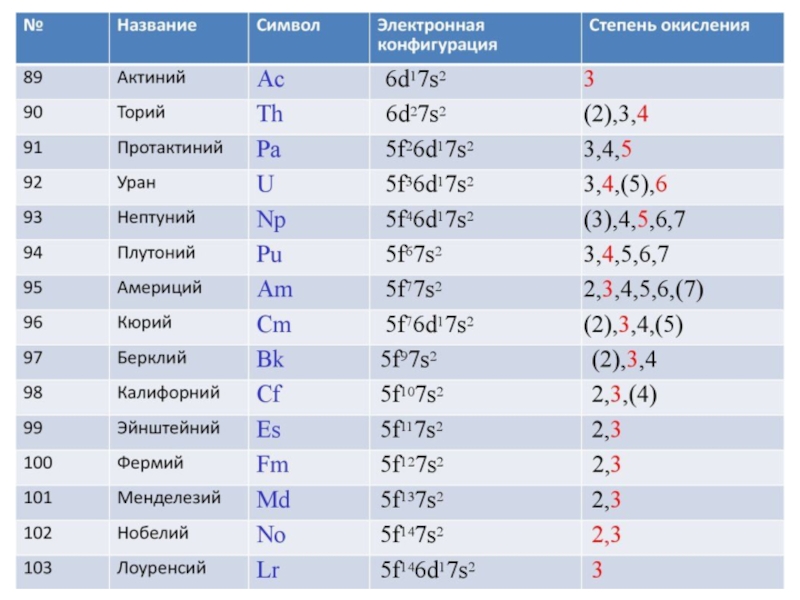
- 11. Электронная структура и степени окисления Ас и актиноидов
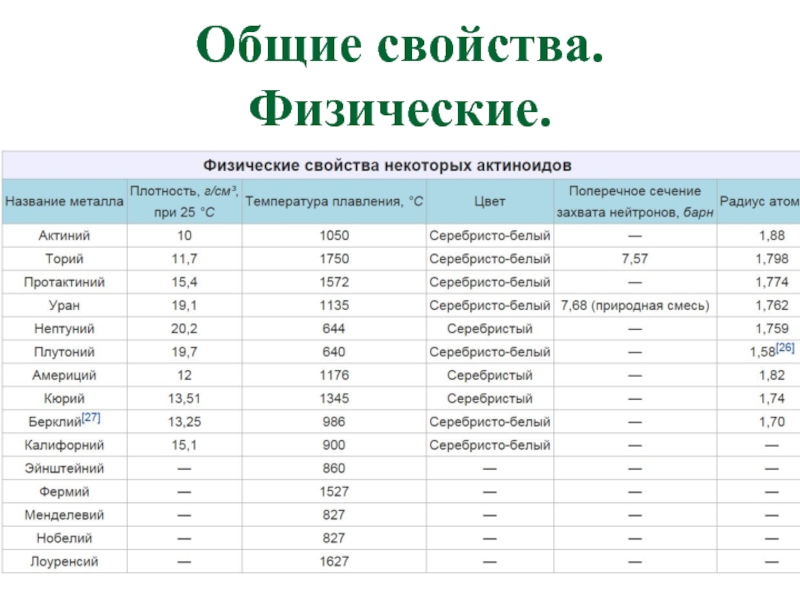
- 14. Общие свойства. Физические.
- 16. Общие свойства. Химические.
- 17. АКТИНОИДЫ. ПРОСТЫЕ ВЕЩЕСТВА
- 19. СОЕДИНЕНИЯ АКТИНОИДОВ Оксиды обладают полиморфизмом, более высоких,
- 20. СОЕДИНЕНИЯ АКТИНОИДОВ Карбиды MeC легко гидролизуются водой
- 21. Актиноиды в растворах Гидратированные ионы Me2+, Me3+,
- 22. СОЕДИНЕНИЯ АКТИНОИДОВ по степеням окисления
- 23. СОЕДИНЕНИЯ АКТИНОИДОВ по степеням окисления
- 24. СОЕДИНЕНИЯ АКТИНОИДОВ по степеням окисления
- 25. СОЕДИНЕНИЯ АКТИНОИДОВ по степеням окисления
- 26. СОЕДИНЕНИЯ АКТИНОИДОВ по степеням окисления
- 27. СОЕДИНЕНИЯ АКТИНОИДОВ по степеням окисления
- 28. ОРИЕНТИРОВОЧНЫЕ ЦВЕТА ИОНОВ В ВОДНЫХ РАСТВОРАХ
Слайд 2ЛИТЕРАТУРА
1. Химия актиноидов: в 3-х т. Пер. с англ./Под ред. Дж.
2. Бессонов, В. А. Основы радиохимии. Учебное пособие по курсу «Радиохимия»/ В. А. Бессонов - ОГТУАЭ, Обнинск 2004.
3. Гергалов, В.И. Радиохимия. Учебно-методическое пособие в 2-х частях. Мн., БГУ, 2015
4. Давыдов, Ю. П. Основы радиохимии/ Ю.П. Давыдов.- Мн.: Вышэйшая школа, 2014.
5. Бекман Н.Н. Радиохимия. Курс лекций. М., 2006
6. Бекман Н Н. Уран.
Слайд 3ЛИТЕРАТУРА
7. Несмеянов, Ан. Н. Радиохимия/ Ан. Н. Несмеянов. - М.: Химия.
8. Несмеянов, Ан. Н. Прошлое и настоящее радиохимии/ Ан. Н. Несмеянов - Л.: Химия , 1985.
9. Нефедов, В. Д. Радиохимия. Уч. пособие/ В. Д. Нефедов, Е. Н. Текстер, М. А. Тропова. - М.: Высшая школа, 1987.
10. Фридлендер, Г. Ядерная химия и радиохимия/ Г. Фридлендер, Дж. Кеннеди, Дж. Миллер - М.: Мир, 1967.
11. Гринвуд, Н., Эрншо, А. Химия элементов. (лучший зарубежный учебник) в 2-х т. (т.2) Пер. с агл. М., БИНОМ. Лаборатория знаний, 2008.
Слайд 4ЛИТЕРАТУРА
12. Аменицкая, Р. В. Сборник задач по радиохимии/ Р. В. Аменицкая
13. Вдовенко, В. Н. Современная радиохимия/ В.Н. Вдовенко. - М.: Атомиздат, 1969.
14. Жерин И.И., Амелина Г.Н. Основы радиохимии, методы выделения и разделения радиоактивных элементов. Учеб. пособ.-Изд-во Томского политех. Ун-та, 2009
15. Макаров, Л. Л. Прикладная радиохимия/ Л. Л. Макаров. - Л.: Изд. ЛГУ, 1966.
16. Старик, И. Е. Основы радиохимии/ И. Е. Старик. – Л.: Наука, 1969.
Слайд 5Актиноиды. История открытия.
Период открытия: XVIII век (U)- ХХ век (Lr)
U, Th
Ac, Pa – продукты распада урана и тория
Трансурановые элементы:
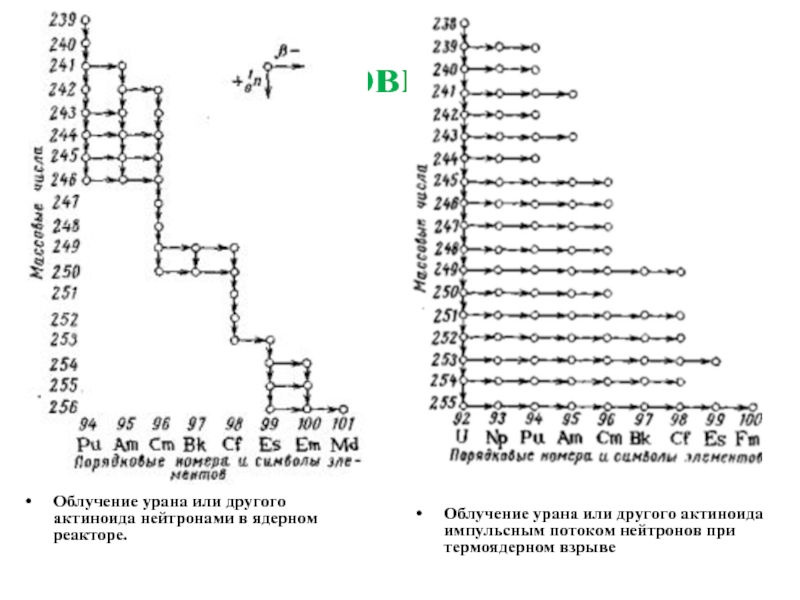
1. Облучение урана или другого актиноида нейтронами в ядерном реакторе.
2. Облучение урана или другого актиноида импульсным потоком нейтронов при термоядерном взрыве.
(Открытие эйнштейния и фермия - результат исследований продуктов взрыва термоядерного устройства, произведенного США в Тихом океане в ноябре 1952 г., операция "Майк").
3. Облучение элементов 7 периода p, d, α, 13C, 18O и т.д.
Слайд 6Трансурановые элементы
1. Происходит последовательный захват нескольких нейтронов и последующий β- -распад
Облучение урана или другого актиноида нейтронами в ядерном реакторе.
2. Происходит многократный захват нейтронов ядром и образование тяжелых актиноидов при
последующем β--распаде
Облучение урана или другого актиноида импульсным потоком нейтронов при термоядерном взрыве
Слайд 8Актиноиды.
Попытки размещения в ПС
Первая попытка размещения 5f-элементов – гипотеза М.
Концепция А.А.Чайхорского (проявление степени окисления +4 у 9 из 13 актиноидов, родоначальник – торий)
Концепции В.Г. Григоровича (1963 г.), И.А. Лебедева (1972 г.): размещение f-элементов по группам
Слайд 9Актиноиды.
Попытки размещения в ПС
Актиноидная гипотеза Г. Сиборга (1944 г.)
Элементы с
Актиноиды – промежуточное положение
между элементами f и d-серий.
Энергии связи 5f и 6d-электронов
очень близки.
Слайд 16Общие свойства. Химические.
Активные металлы, легко вступающие в реакции практически со всеми
Растворимы в разбавленных минеральных кислотах, в концентрированных HNO3 и H2SO4 – пассивируются.
Слайд 19СОЕДИНЕНИЯ АКТИНОИДОВ
Оксиды обладают полиморфизмом, более высоких, чем +4 степеней окисления –
Гидриды при повышении температуры выше 300 °С разлагаются с выделением металлов в виде пирофорных порошков.
Стабильность галогенидов падает с ростом атомного номера галогена и числа атомов галогена в соединении. Трифториды и тетрафориды не растворимы в воде, хлориды, бромиды и иодиды – растворимы.
Слайд 20СОЕДИНЕНИЯ АКТИНОИДОВ
Карбиды MeC легко гидролизуются водой с образованием углеводородов, мелкоизмельченные -
Мононитриды: нагревание металлов или карбидов в токе азота или аммиака.
Силициды: взаимодействие металлов с кремнием при высоких температурах. Соляная кислота разлагает до SiH4.
Слайд 21Актиноиды в растворах
Гидратированные ионы
Me2+, Me3+, Me4+
MeO22+(«ил»), MeO2+(«оил»), MeO53-
Диспропорционирование
2 MeO2+ +4Н+ ↔
Гидролиз,
Комплексообразование:
Me4+ > Me3+>MeO22+>MeO2+
Для оксалат и ацетат-ионов:
Me4+ > MeO22+ > Me3+ >MeO2+
Полимеризация с образованием полиядерных продуктов гидролиза
Координационное число
6-12.



![ЛИТЕРАТУРА12. Аменицкая, Р. В. Сборник задач по радиохимии/ Р. В. Аменицкая и [др] - М.:](/img/tmb/2/163058/f14c5edb1be27c4a9c4bf38b986addd9-800x.jpg)