- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Химическая очистка воды презентация
Содержание
- 1. Химическая очистка воды
- 2. 7.1. Нейтрализация
- 3. Нейтрализация Химическая реакция между веществом, обладающим
- 4. Основные способы нейтрализации Взаимная нейтрализация кислых и
- 5. 7.1.1. Нейтрализация смешением кислых и щелочных вод
- 6. Условия применения способа Наличие одновременно кислых и
- 7. 7.1.2. Нейтрализация вод реагентами
- 8. Условия применения способа При наличии только кислых
- 9. Факторы, учитываемые при выборе реагента Вид
- 10. Расчетное количество реагента
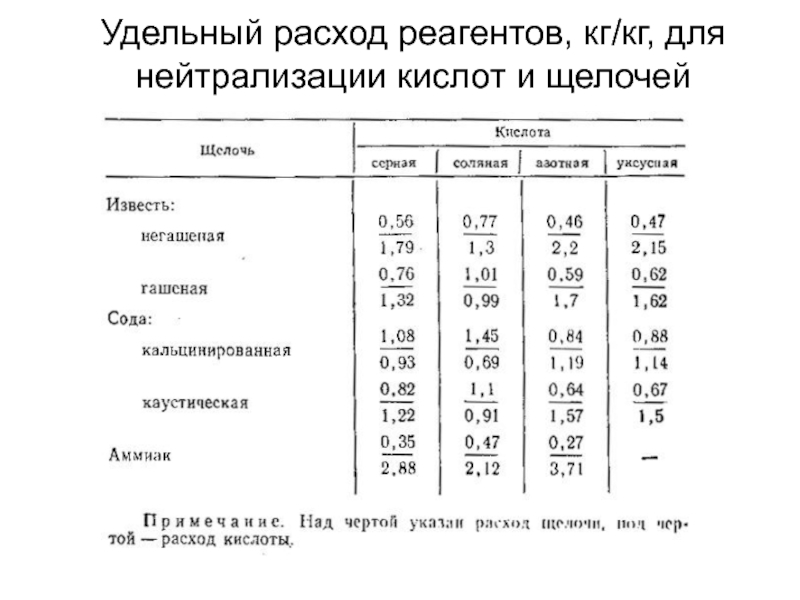
- 11. Удельный расход реагентов, кг/кг, для нейтрализации кислот и щелочей
- 12. Расчетное количество реагента с учетом осаждения ионов металлов
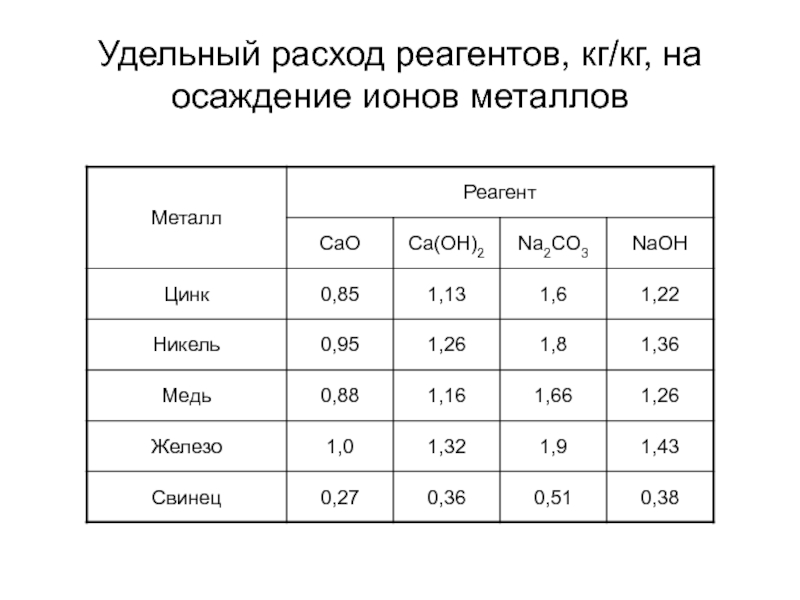
- 13. Удельный расход реагентов, кг/кг, на осаждение ионов металлов
- 14. Удельный объем осадка, %
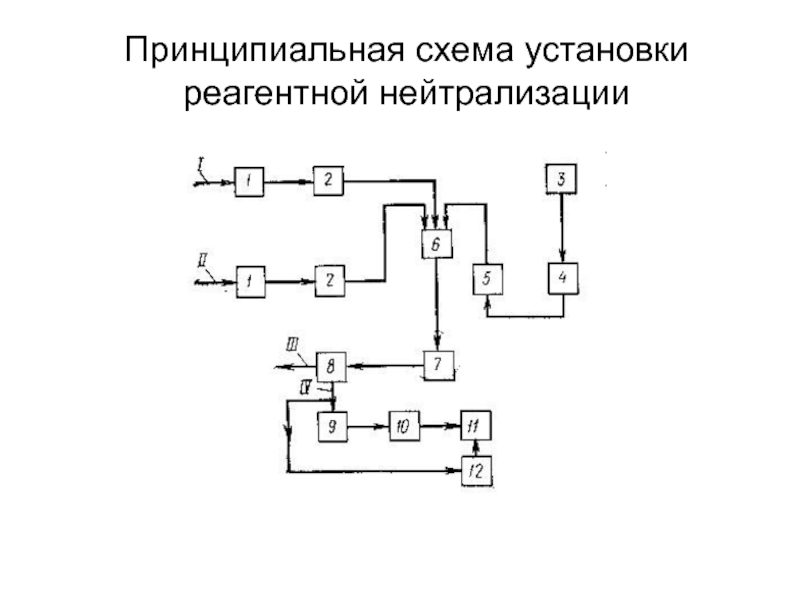
- 15. Принципиальная схема установки реагентной нейтрализации
- 16. Состав реагентного хозяйства: Склад реагента; Установка гашения
- 17. Основные типы дозаторов Дозаторы постоянного расхода реагентов;
- 18. 7.1.3. Нейтрализация вод фильтрованием через нейтрализующие материалы
- 19. Основные виды нейтрализующих материалов Доломит (CaCO3 ·
- 20. Область применения фильтров отсутствие в воде
- 21. Высота слоя загрузки
- 22. Площадь фильтрования Суточный расход загрузочного материала Фактический расход загрузочного материала
- 23. Масса загруженного в фильтр материала Продолжительность работы фильтра без смены загрузки
Слайд 3Нейтрализация
Химическая реакция между веществом, обладающим свойствами кислоты, и веществом, обладающим
Слайд 4Основные способы нейтрализации
Взаимная нейтрализация кислых и щелочных вод смешением;
Нейтрализация реагентами;
Нейтрализация фильтрованием
Нейтрализация щелочных вод дымовыми газами.
Слайд 6Условия применения способа
Наличие одновременно кислых и щелочных вод;
Установка усреднителей – накопителей,
Составление баланса кислых и щелочных вод.
Слайд 8Условия применения способа
При наличии только кислых или щелочных вод.
Основные реагенты
Растворы кислот;
Негашеная
Гашеная известь (Ca(OH)2);
Кальцинированная сода (Ca2CO3);
Каустическая сода (NaOH);
Аммиак (NH3OH) и др.
Слайд 9Факторы, учитываемые при выборе реагента
Вид кислот;
Концентрация кислот;
Режим поступления вод;
Растворимость продуктов
Слайд 16Состав реагентного хозяйства:
Склад реагента;
Установка гашения извести;
Установка приготовления рабочего раствора;
Дозаторы.
при сухом способе
при мокром способе хранения извести
Склад реагента;
Установка приготовления концентрированного известкового молочка;
Установка приготовления рабочего раствора;
Дозаторы.
Слайд 17Основные типы дозаторов
Дозаторы постоянного расхода реагентов;
Дозаторы подачи реагентов пропорционально расходу сточной
Дозаторы рассчитанные на поддержание постоянных параметров качества обработанной сточной воды.
Слайд 19Основные виды нейтрализующих материалов
Доломит (CaCO3 · MgCO3);
Известняк (CaCO3);
Магнезит (MgCO3);
Мел (CaCO3);
Обожженый магнезит
Крупность фракций нейтрализующей загрузки – 3…8 см.
Продолжительность контакта сточной воды с нейтрализующим материалом – не менее 10 мин.
Слайд 20Область применения фильтров
отсутствие в воде солей металлов, т.к. при рН
концентрация серной кислоты в сточных водах не более 1,5 мг/л, т.к. при больших концентрациях в процессе нейтрализации образуется сульфат кальция в количествах превышающих его растворимость в воде, и он выпадает в осадок. Это ограничение снимается в случае использования в качестве нейтрализующего материала магнезита (растворимость образующегося сульфата магния достаточно высока).