- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Химическая кинетика презентация
Содержание
- 1. Химическая кинетика
- 2. Контрольная работа № 3. Основы формальной кинетики
- 3. Порядок реакции - экспериментально определяемая величина, которую
- 5. Начальное количество исходного реагента N2O5 рассчитывается на
- 6. А также (из уравнения Клапейрона-Клаузиуса
- 7. Отсюда рассчитывается концентрации исходного вещества в различные
- 8. Вот она
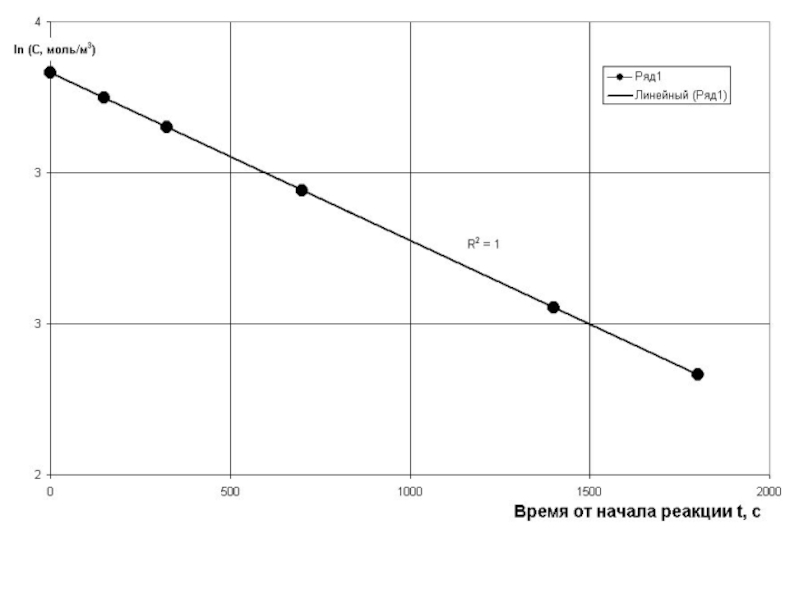
- 9. Далее переходим к определению порядка реакции графическим
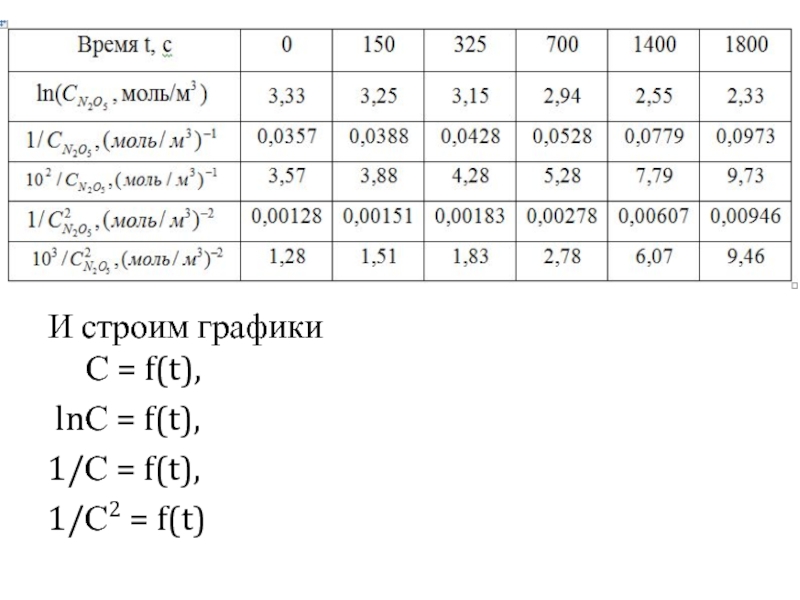
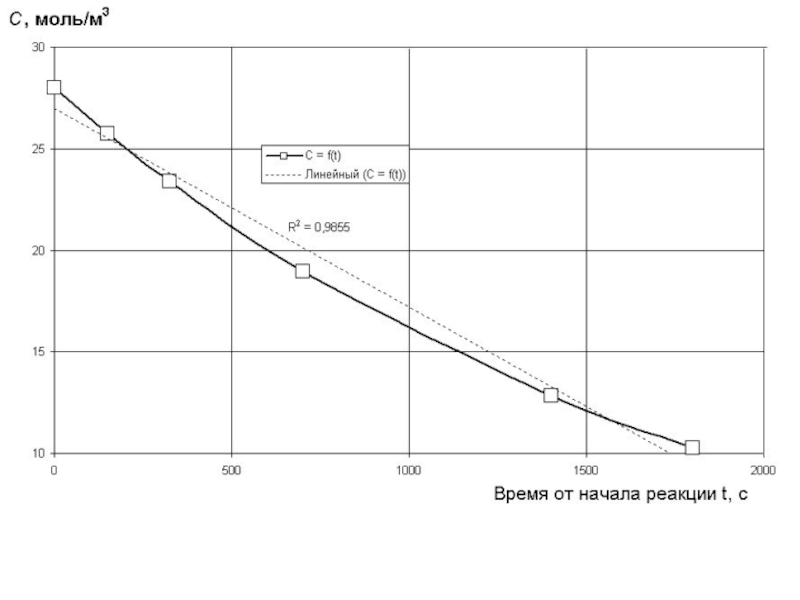
- 10. И строим графики С = f(t),
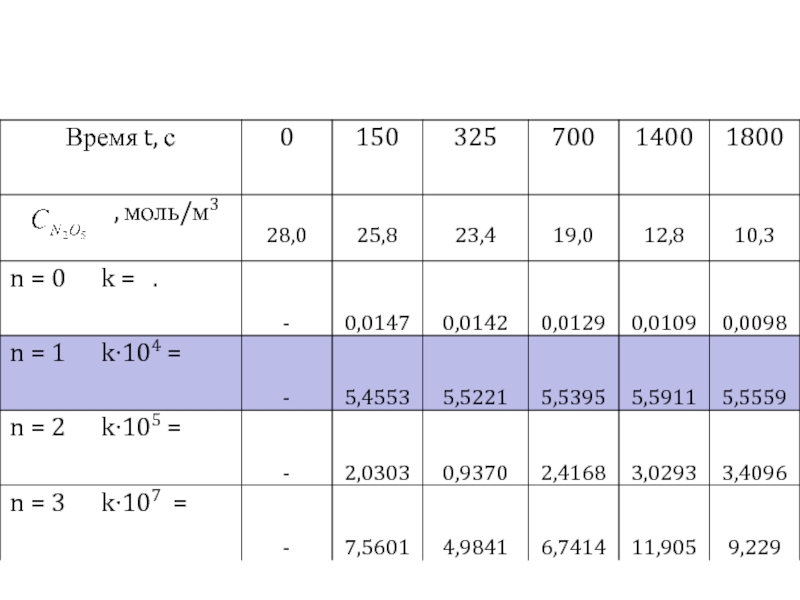
- 14. С целью проверки правильности определения порядка реакции
- 16. Из таблицы хорошо видно, что только расчет
- 17. . Тогда константа скорости химической реакции первого
- 18. Если известно, что к моменту времени t15%
- 19. Теперь, чтобы найти концентрацию N2O5 в момент
- 20. Задание 2. Определение параметров температурной зависимости скорости
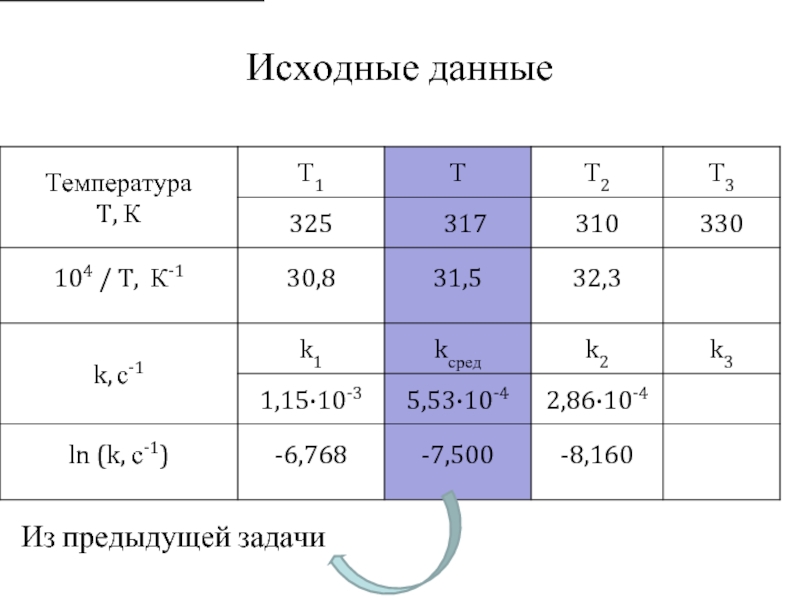
- 21. Исходные данные Из предыдущей задачи
- 22. Зависимость скорости химической реакции от температуры в
- 23. график является прямой линией в координатах ln
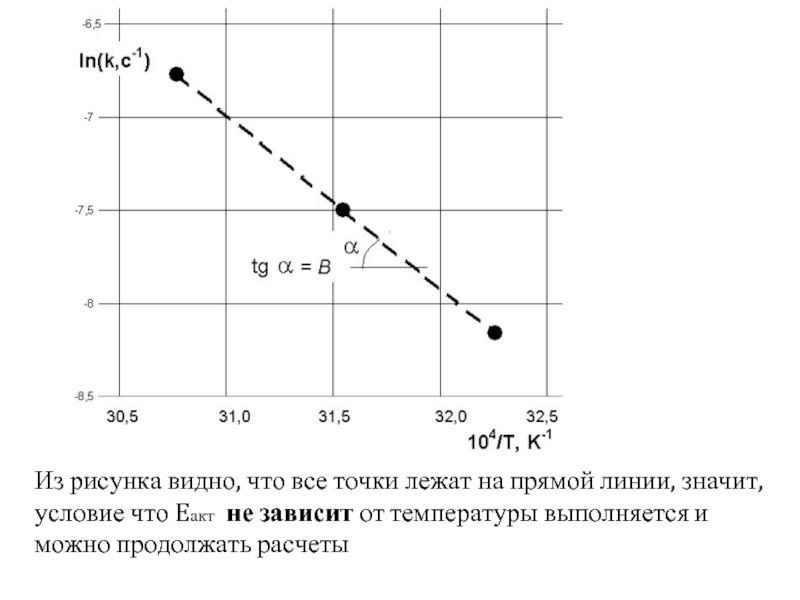
- 24. Но должно выполнятся условие что Eакт не
- 25. Из рисунка видно, что все точки лежат
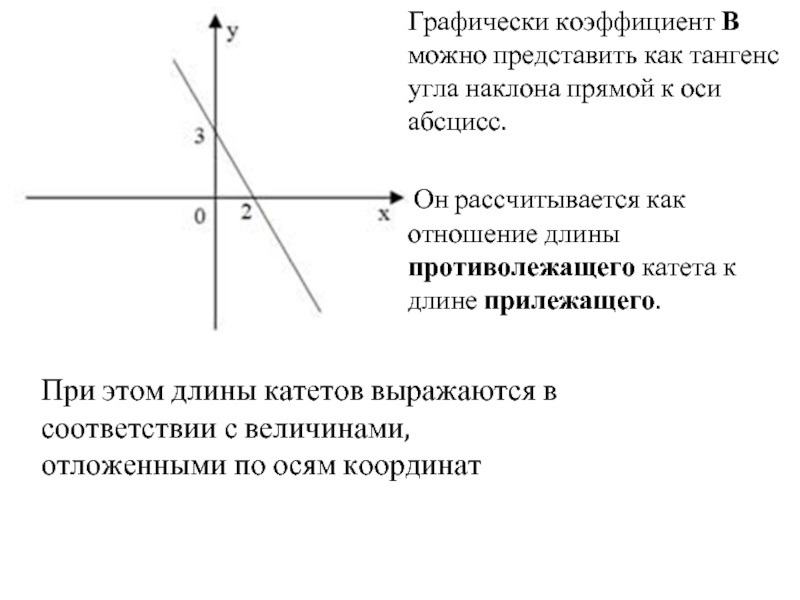
- 26. Графически коэффициент В можно представить как тангенс
- 28. Определим предэкспоненциальный множитель k0 в уравнении
- 29. Для определения температурного коэффициента скорости реакции (γ)
- 30. Логарифмируя левую и правую части, получим:
Слайд 1ХИМИЧЕСКАЯ КИНЕТИКА
Химическая кинетика занимается изучением механизмов и скоростей химических реакций.
Слайд 2Контрольная работа № 3. Основы формальной кинетики Задание 1. Определение порядка
В реакторе при постоянном объеме V = 1 м3 и температуре Т протекает газофазная реакция А. В таблице 1 для этой реакции приведены результаты измерений общего давления реакционной смеси Р в зависимости от времени её протекания t. На основании данных таблицы 1 исследуйте кинетику реакции A и определите кинетические параметры: порядок реакции, константу скорости, период полупревращения.
Слайд 3Порядок реакции - экспериментально определяемая величина, которую находят по результатам наблюдений
Пример решения
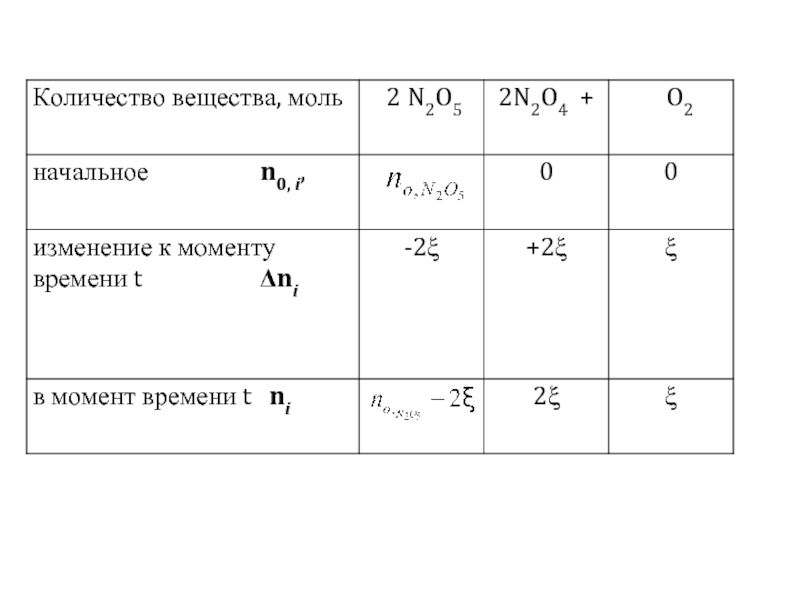
2 N2O5 = 2 N2O4 + O2
В первую очередь нужно найти количество вещества. Для этого используем химическую переменную ξ
Слайд 5Начальное количество исходного реагента N2O5 рассчитывается на основании величины общего давления
Тогда в любой промежуток времени t (кроме начального) суммарное количество вещества газов будет равно
Слайд 6А также
(из уравнения Клапейрона-Клаузиуса
Pt – общее давление в реакторе в момент времени t ≠ 0. Тогда получим
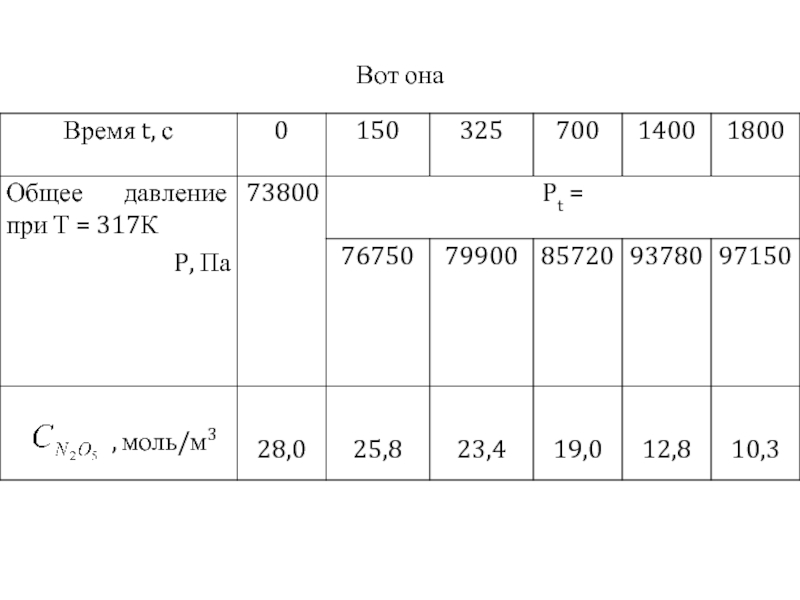
Слайд 7Отсюда рассчитывается концентрации исходного вещества в различные промежутки времени
Результаты вычислений концентрации
Слайд 9Далее переходим к определению порядка реакции графическим путем
Для этого продолжим предыдущую
Слайд 14С целью проверки правильности определения порядка реакции воспользуемся методом подстановки и
Слайд 16Из таблицы хорошо видно, что только расчет константы по уравнению для
даёт значение константы скорости, которое остаётся во времени практически неизменным
k1 ≈ k2 ≈ k3 ≈ k4 ≈ k5
Этим мы подтверждаем результаты, полученные графическим методом
Слайд 17.
Тогда константа скорости химической реакции первого порядка будет равна
,
а период полупревращения:
Слайд 18Если известно, что к моменту времени t15% прореагировало 15 % исходного
подставляя это в интегральную форму кинетического уравнения реакции (дано в разделах 4.1-4.4)получим
Слайд 19Теперь, чтобы найти концентрацию N2O5 в момент времени t1 = 12
Слайд 20Задание 2. Определение параметров температурной зависимости скорости химической реакции
В таблице приведены
а) коэффициенты A и B в интегральной форме уравнения Аррениуса вида lgk = A – B/T и составьте это уравнение с численными значениями A и B для химической реакции А;
б) графически и аналитически энергию активации (Eакт, кДж/моль) химической реакции А;
в) величину предъэкспоненциального множителя в экспоненциальной форме уравнения температурной зависимости скорости (уравнение Аррениуса) и составьте это уравнение с численными значениями параметров для химической реакции А;
г) температурный коэффициент скорости химической реакции А для интервала температур от T1 до T2;
д) константу скорости k3 реакции В при температуре Т3.
е) как изменится скорость химической реакции А, если температуру Т1 изменить на ∆Т.
Слайд 22Зависимость скорости химической реакции от температуры в дифференциальной форме имеет вид
где R – универсальная газовая постоянная, а Eакт – энергия активации химической реакции. Интегрируя это выражение, называемое уравнением Аррениуса, при условии, что Eакт не является f(T), приходят к его интегральной форме, которую записывают в виде зависимости
Слайд 23график является прямой линией в координатах ln k = f(1/T)
График –
у= ln k x=1/T
Можно вычислить энергию активации химической реакции по представленным данным, т.к. известны константы скоростей при двух температурах.
где A – константа интегрирования,
B = Eакт /R
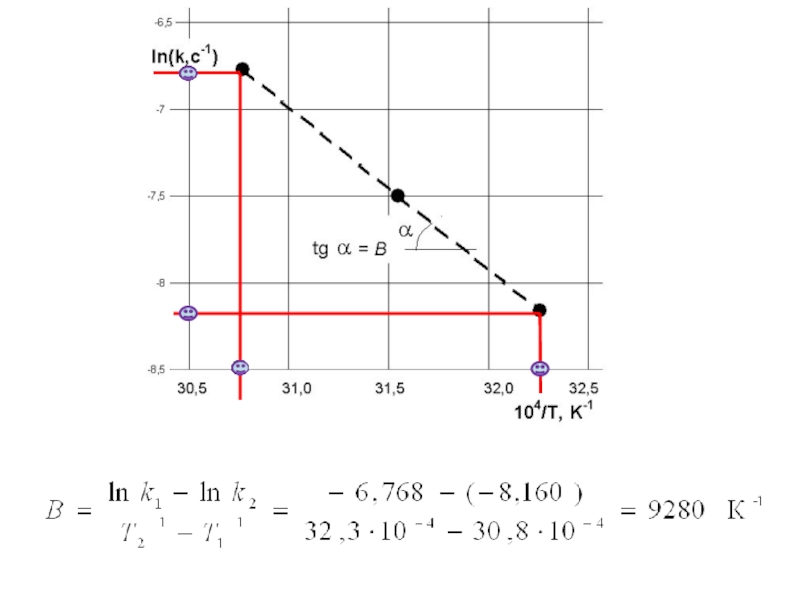
Слайд 24Но должно выполнятся условие что Eакт не зависит от температуры в
Чтобы убедиться в выполнении этого условия, необходимо построить график в координатах
ln k = f(1/T). Для построения графика воспользуемся данными таблицы
аналитическая формула для расчета энергии активации имеет вид
Слайд 25Из рисунка видно, что все точки лежат на прямой линии, значит,
Слайд 26Графически коэффициент В можно представить как тангенс угла наклона прямой к
Он рассчитывается как отношение длины противолежащего катета к длине прилежащего.
При этом длины катетов выражаются в соответствии с величинами, отложенными по осям координат
Слайд 28
Определим предэкспоненциальный множитель k0 в уравнении Аррениуса:
и составим уравнение Аррениуса для
Слайд 29Для определения температурного коэффициента скорости реакции (γ) в интервале температур от
При повышении температуры на каждые 10 градусов скорость химической реакции увеличивается в среднем в γ раз.
Величина температурного коэффициента скорости химической реакции γ, как правило, изменяется в пределах от 2 до 4
γ1,5 = 4,02
Слайд 30Логарифмируя левую и правую части, получим:
1,5 ln γ = ln 4,02
γ = exp[(ln 4,02)/1,5) = 2,53
Зная температурный коэффициент скорости реакции определим, во сколько раз изменится скорость реакции, если температуру Т изменить на 30 К:
Скорость изменится в γ 30/10 = 2.533 = 16,2 раза