- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Функциональные производные с простой связью C-“Э". Галогенпроизводные. (Лекция 5) презентация
Содержание
- 1. Функциональные производные с простой связью C-“Э". Галогенпроизводные. (Лекция 5)
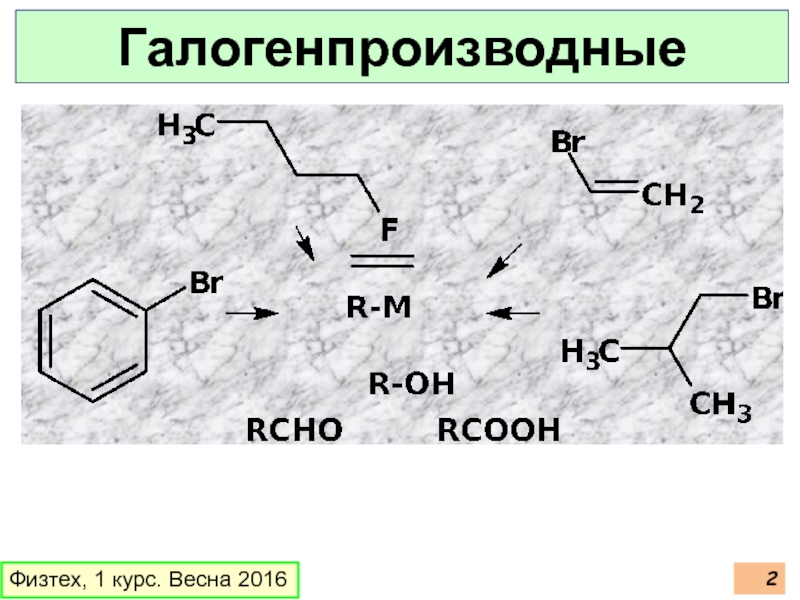
- 2. Физтех, 1 курс. Весна 2016 Галогенпроизводные
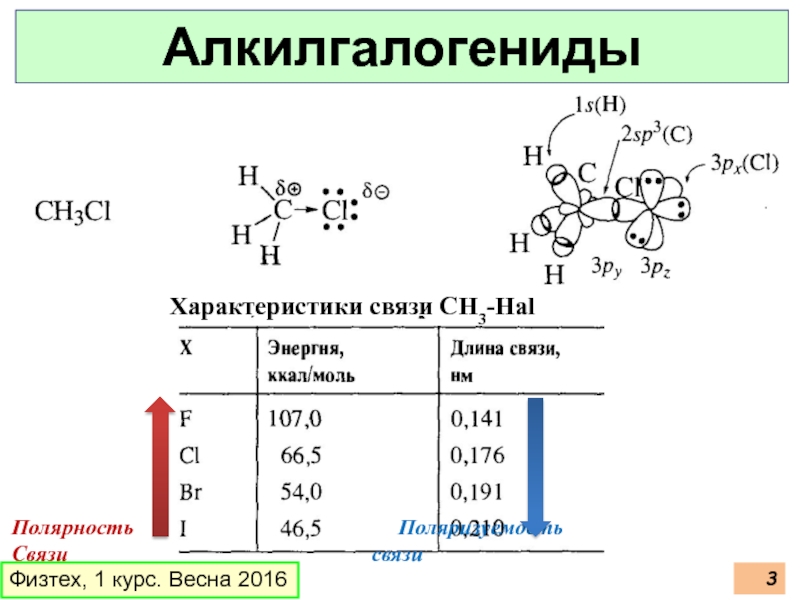
- 3. Полярность Поляризуемость
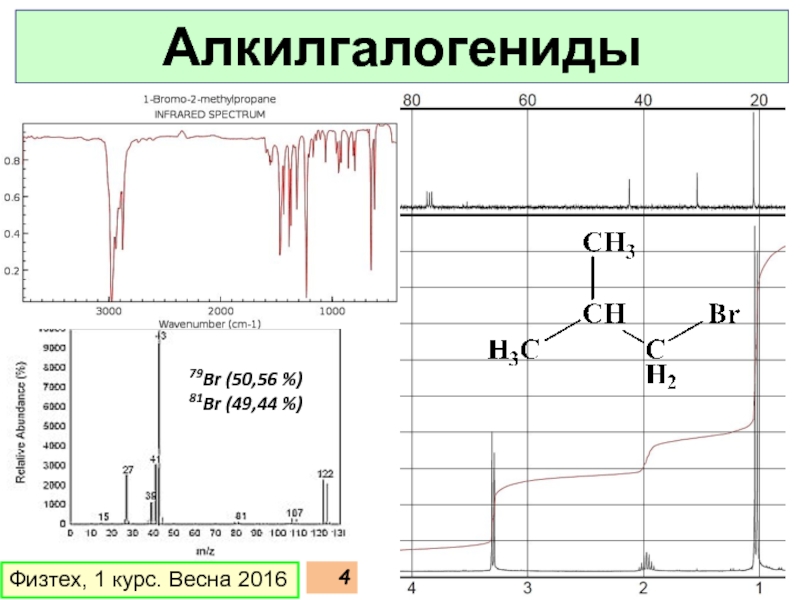
- 4. Физтех, 1 курс. Весна 2016 79Br (50,56 %) 81Br (49,44 %) Алкилгалогениды
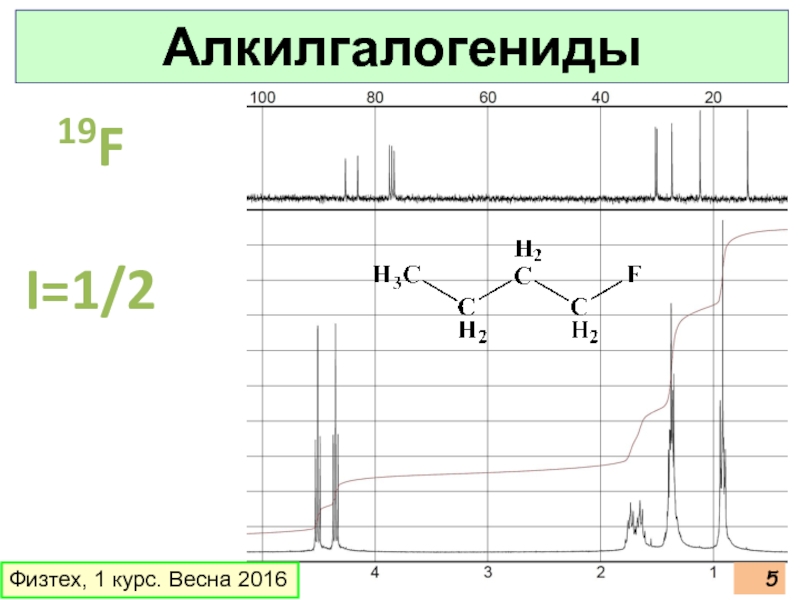
- 5. Физтех, 1 курс. Весна 2016 19F I=1/2 Алкилгалогениды
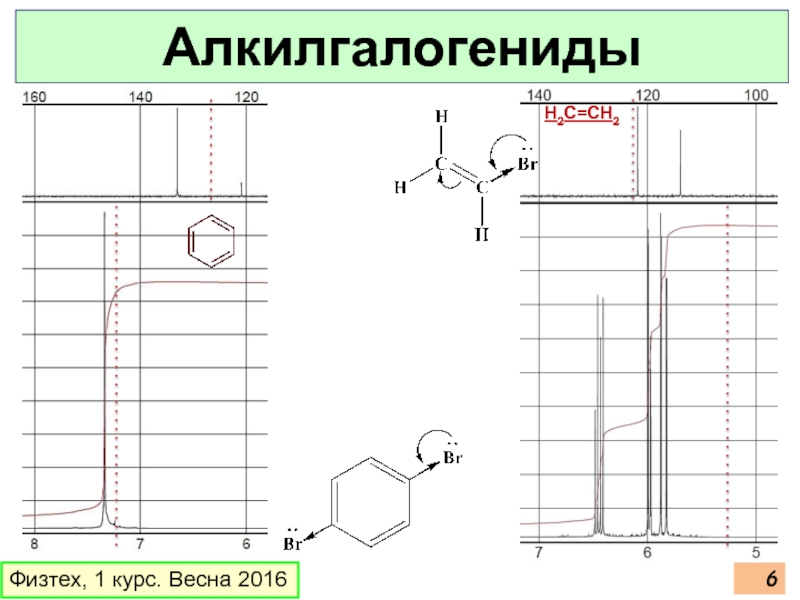
- 6. H2C=CH2 Физтех, 1 курс. Весна 2016 Алкилгалогениды
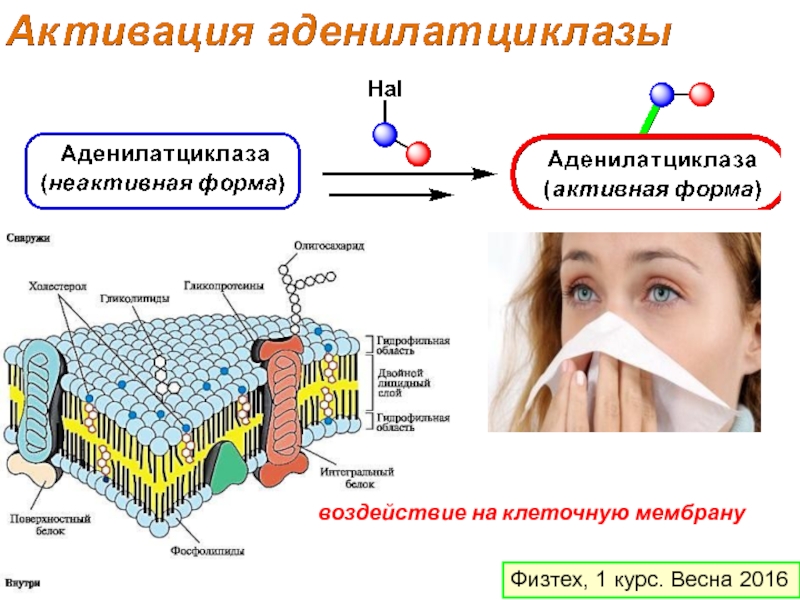
- 7. воздействие на клеточную мембрану Физтех, 1 курс. Весна 2016
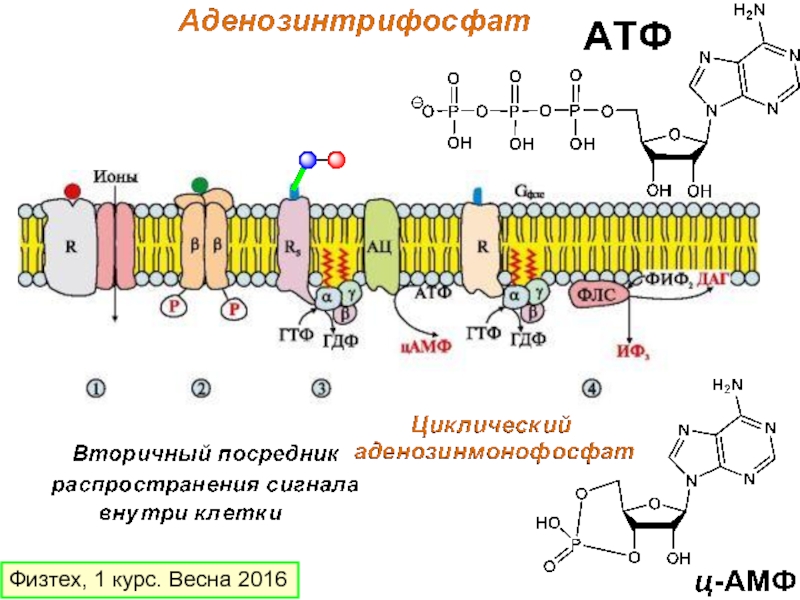
- 8. Физтех, 1 курс. Весна 2016
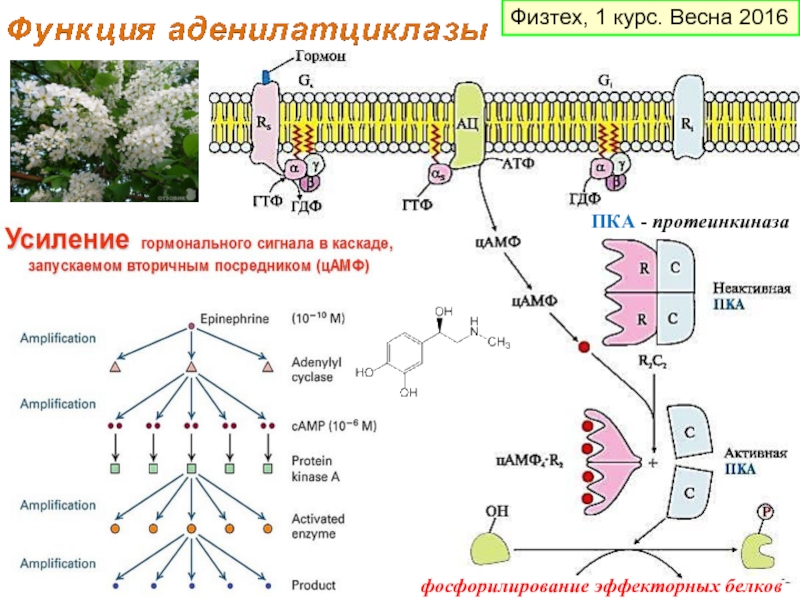
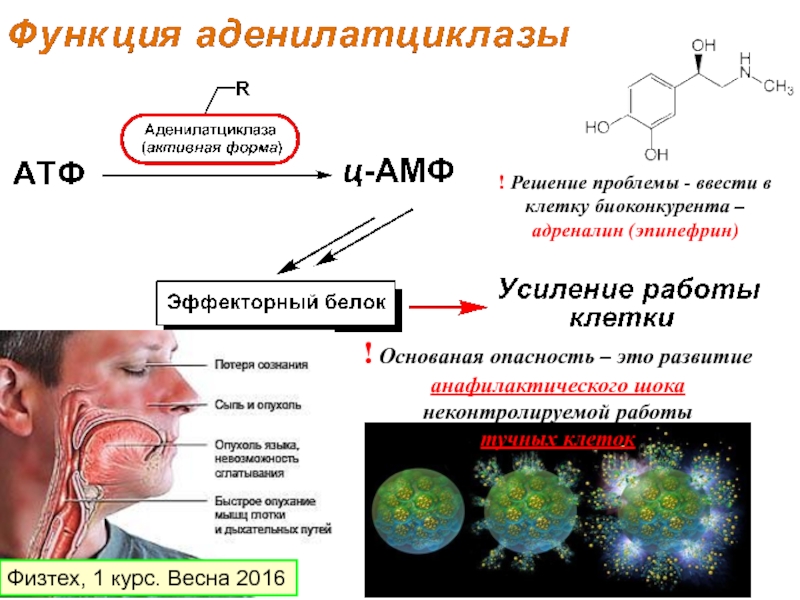
- 9. ПКА - протеинкиназа фосфорилирование эффекторных белков Физтех, 1 курс. Весна 2016
- 10. ! Основаная опасность – это развитие анафилактического
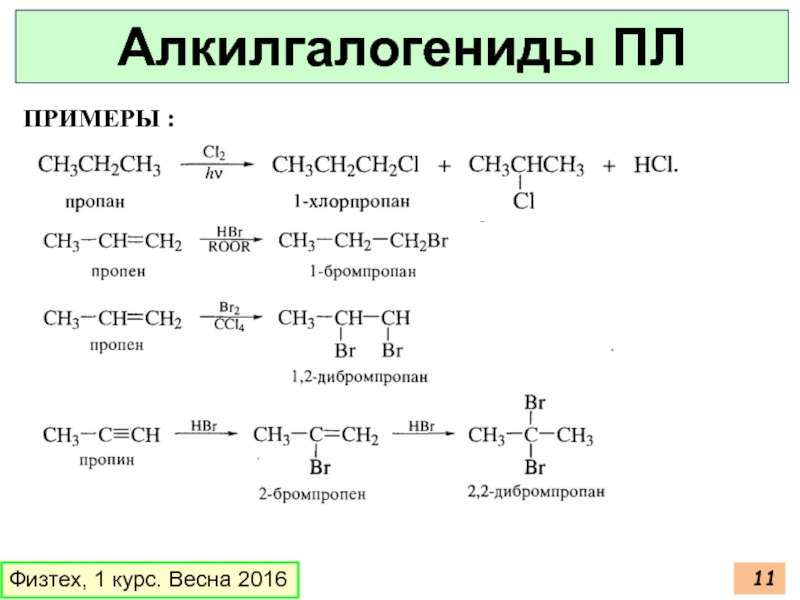
- 11. ПРИМЕРЫ : Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ
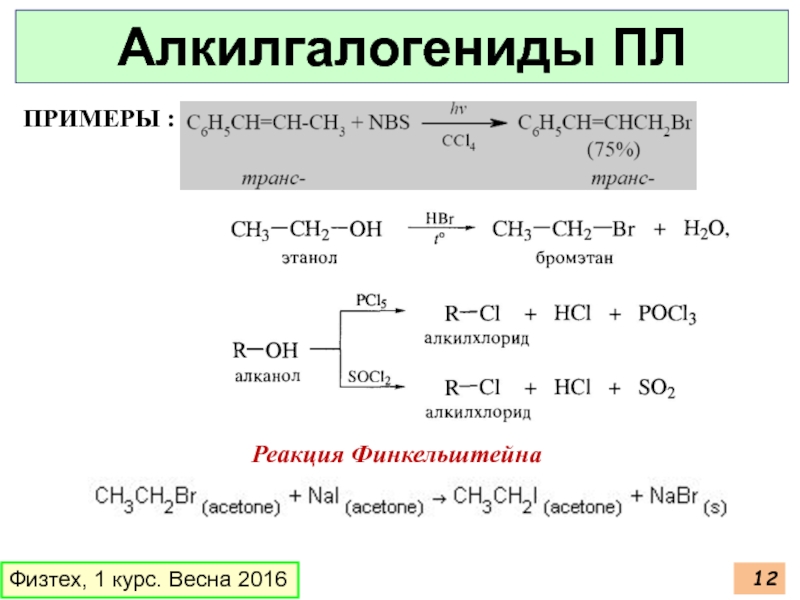
- 12. ПРИМЕРЫ : Реакция Финкельштейна Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ
- 13. Механизмы реакции: Физтех, 1 курс. Весна 2016
- 14. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ
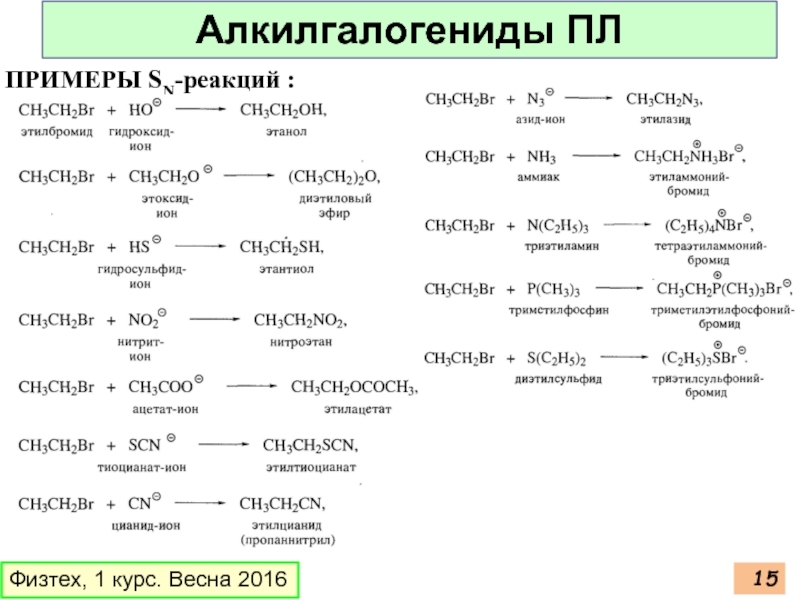
- 15. ПРИМЕРЫ SN-реакций : Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ
- 16. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ Механизм реакции
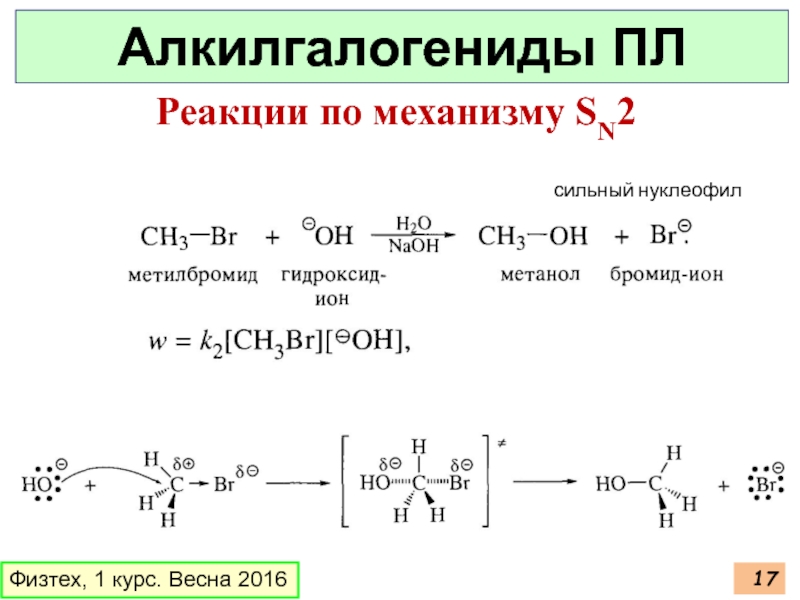
- 17. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ Реакции по механизму SN2 сильный нуклеофил
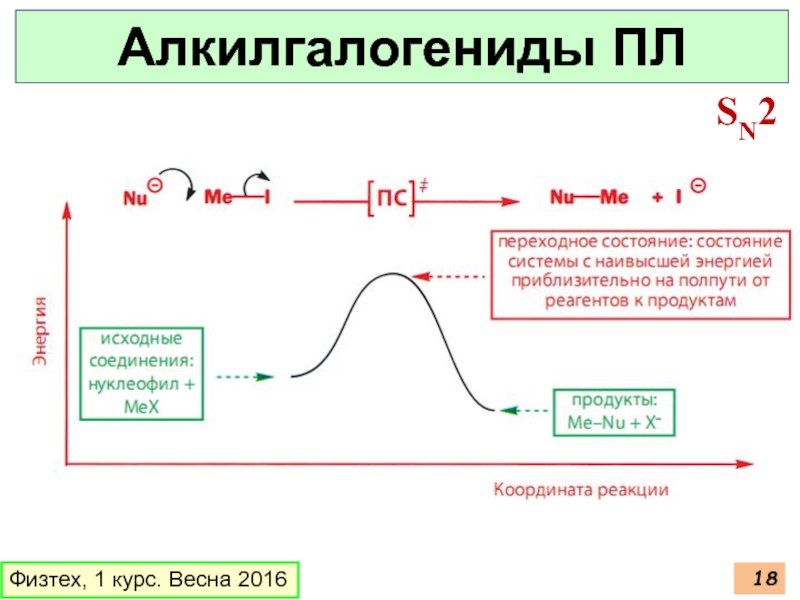
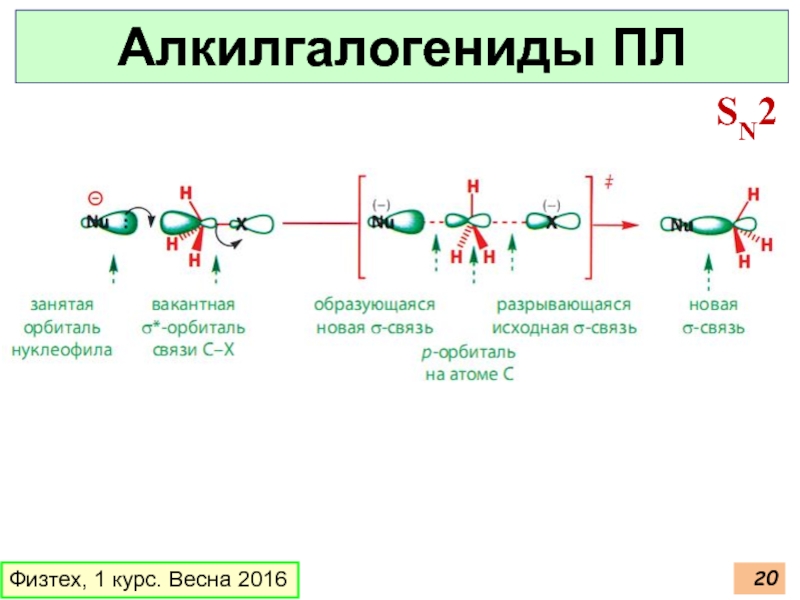
- 18. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ SN2
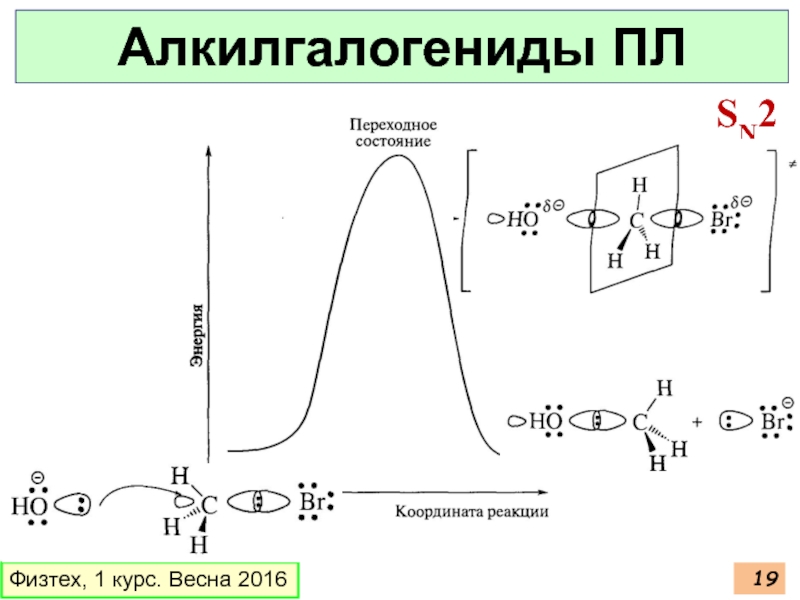
- 19. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ SN2
- 20. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ SN2
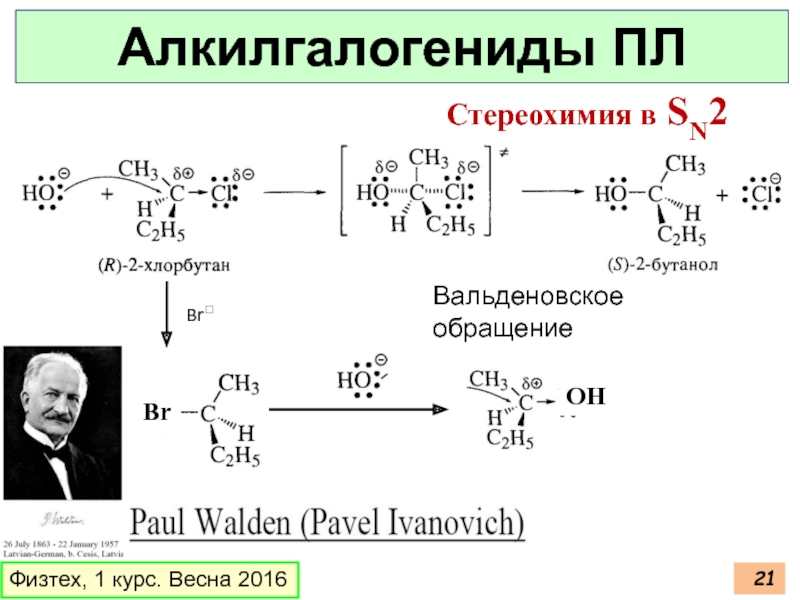
- 21. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ Стереохимия в SN2 Br Br OH Вальденовское обращение
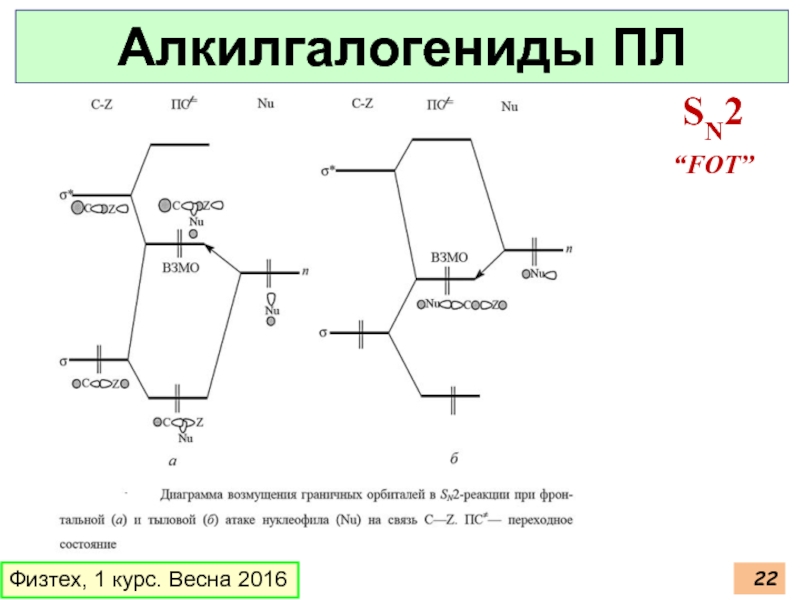
- 22. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ SN2 “FOT”
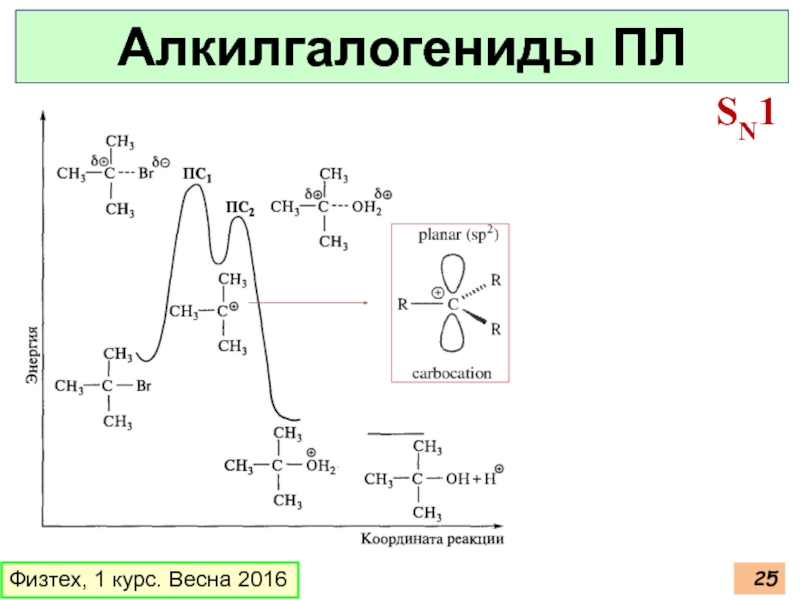
- 23. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ SN1 слабый нуклеофил, ионизирующий растворитель
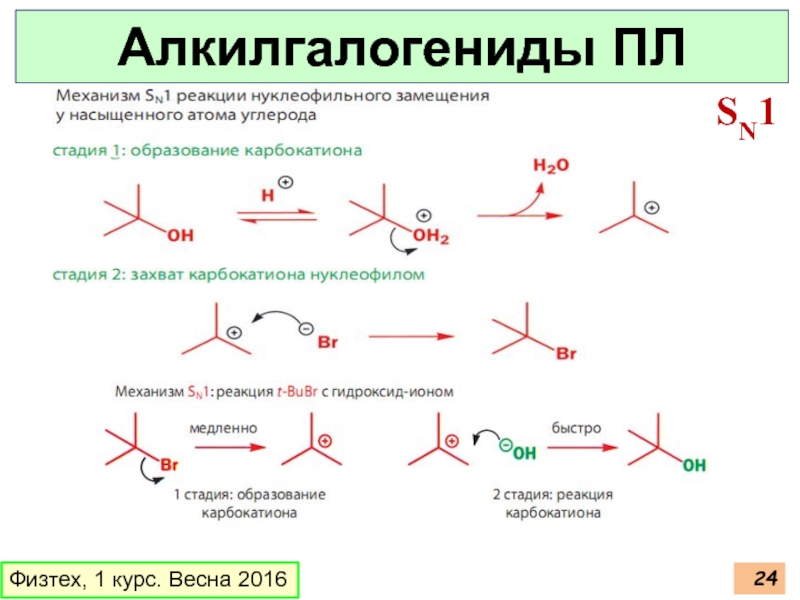
- 24. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ SN1
- 25. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ SN1
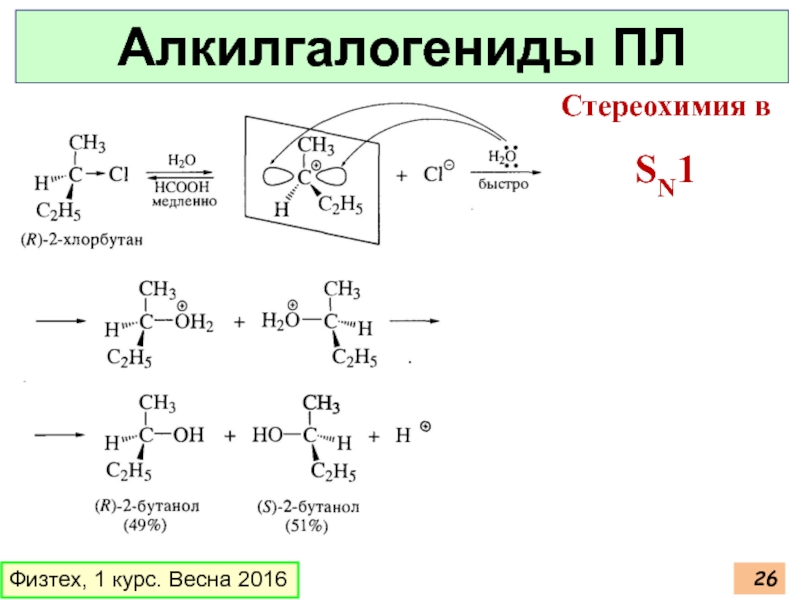
- 26. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ Стереохимия в SN1
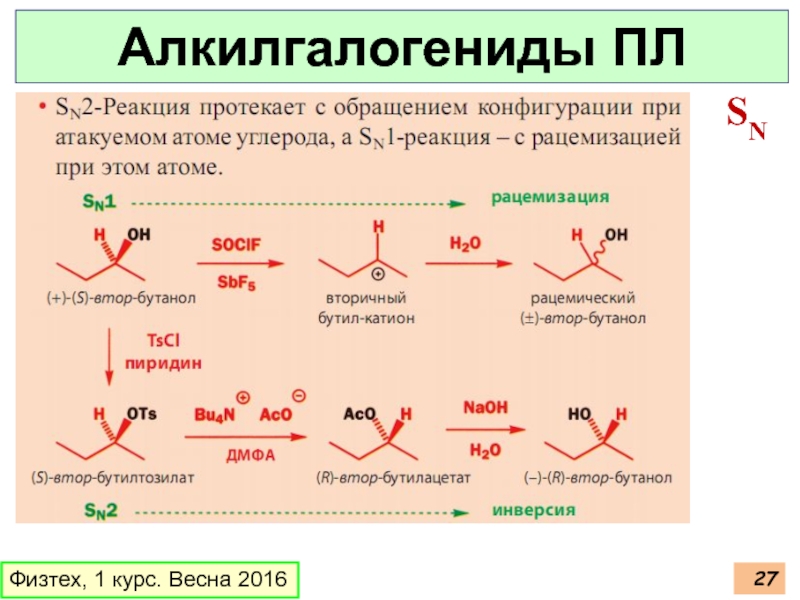
- 27. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ SN
- 28. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ
- 29. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ
- 30. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ
- 31. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ
- 32. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ
- 33. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ
- 34. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ
- 35. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ
- 36. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ
- 37. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ
- 38. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ
- 39. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ
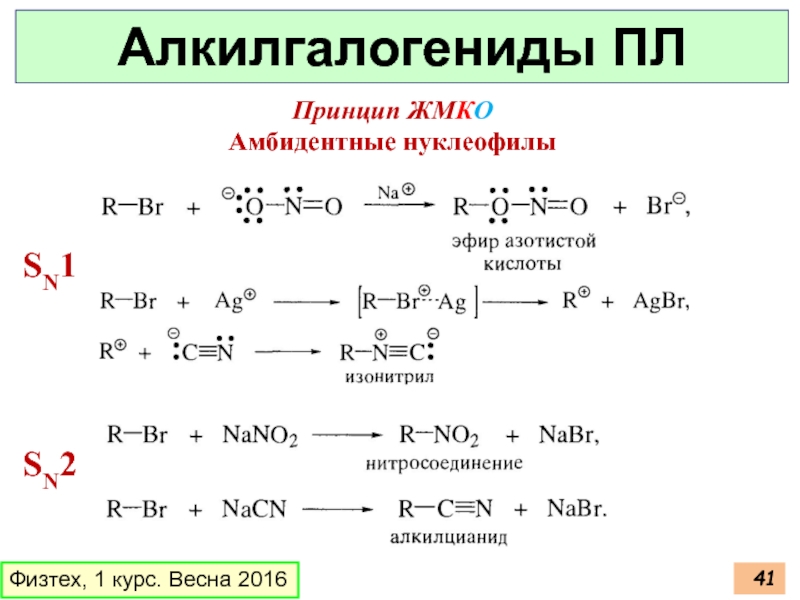
- 40. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ Принцип ЖМКО
- 41. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ SN1 SN2 Принцип ЖМКО Амбидентные нуклеофилы
- 42. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ
- 43. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ
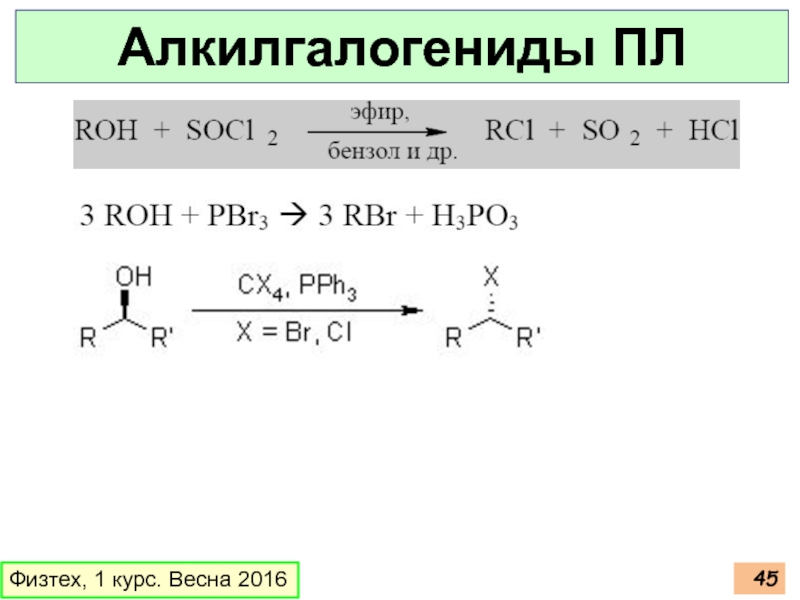
- 44. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ
- 45. Физтех, 1 курс. Весна 2016 Алкилгалогениды ПЛ
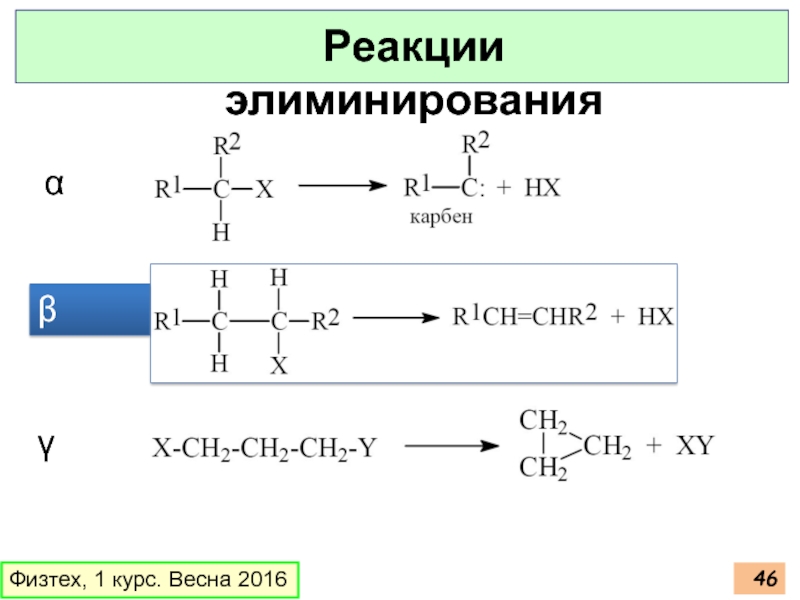
- 46. Физтех, 1 курс. Весна 2016 Реакции элиминирования α β γ
- 47. Физтех, 1 курс. Весна 2016 Реакции
- 48. Физтех, 1 курс. Весна 2016 Реакции элиминирования E2
- 49. Физтех, 1 курс. Весна 2016 Реакции
- 50. Физтех, 1 курс. Весна 2016 Реакции элиминирования E2
- 51. Физтех, 1 курс. Весна 2016 Реакции
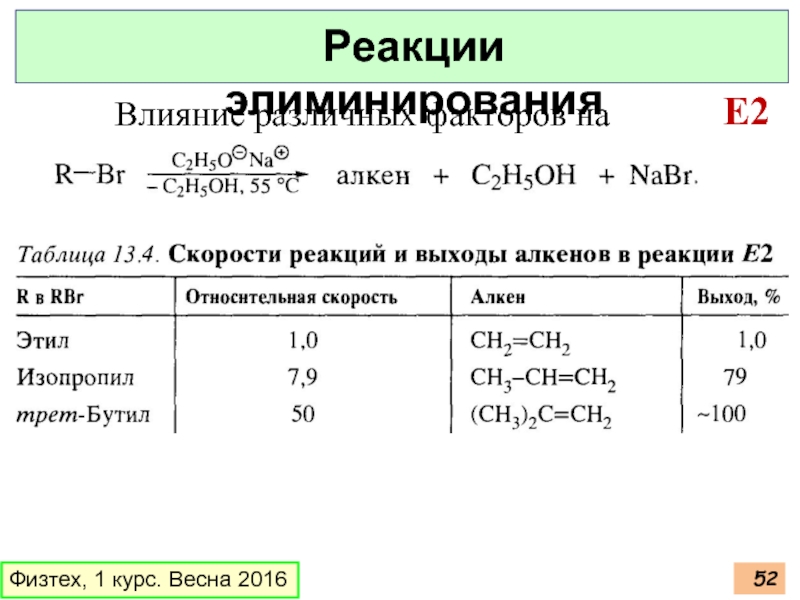
- 52. Физтех, 1 курс. Весна 2016 Реакции элиминирования E2 Влияние различных факторов на
- 53. Конкуренция между SN2 и E2 природа уходящей
- 54. Физтех, 1 курс. Весна 2016 Реакции элиминирования E vs SN
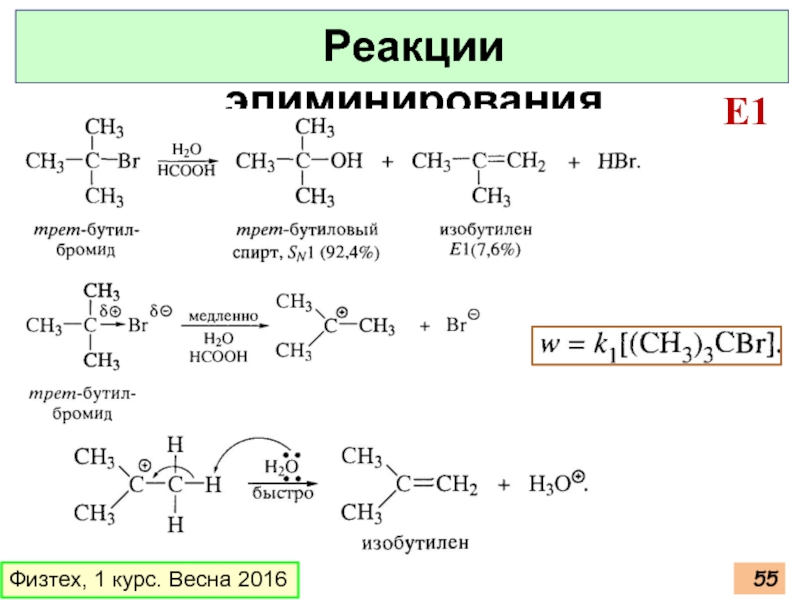
- 55. Физтех, 1 курс. Весна 2016 Реакции элиминирования E1
- 56. Физтех, 1 курс. Весна 2016 Реакции элиминирования E1
- 57. Физтех, 1 курс. Весна 2016 Реакции
- 58. Физтех, 1 курс. Весна 2016 Реакции
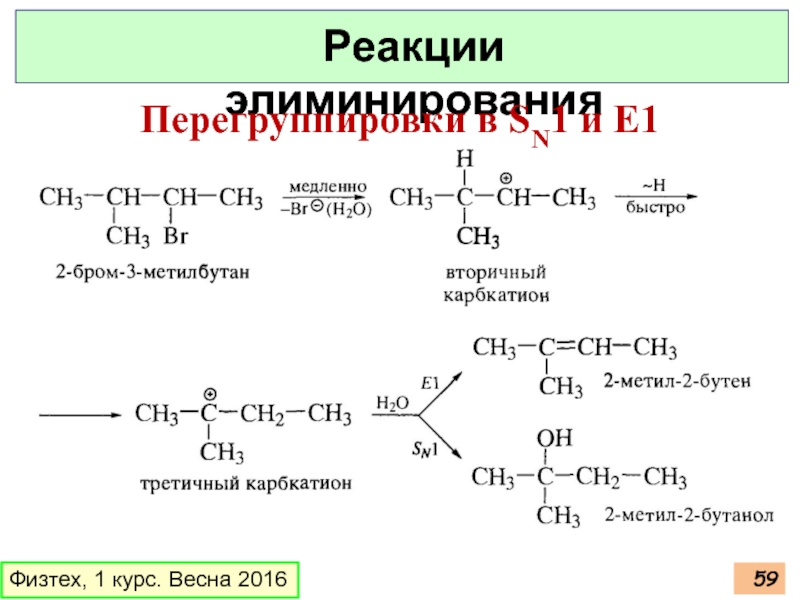
- 59. Физтех, 1 курс. Весна 2016 Реакции элиминирования Перегруппировки в SN1 и E1
Слайд 1Физтех, 1 курс. Весна 2016
Функциональные производные с простой связью C-“Э”
Часть 1
Галогенпроизводные
Слайд 3Полярность Поляризуемость
Связи связи
Физтех, 1 курс. Весна 2016
Алкилгалогениды
Характеристики
Слайд 10! Основаная опасность – это развитие анафилактического шока
неконтролируемой работы
тучных
! Решение проблемы - ввести в клетку биоконкурента – адреналин (эпинефрин)
Физтех, 1 курс. Весна 2016
Слайд 13Механизмы реакции:
Физтех, 1 курс. Весна 2016
Алкилгалогениды ПЛ
Nu: – «нуклеофил», атакающая группа
Z
≡С–Z – субстрат
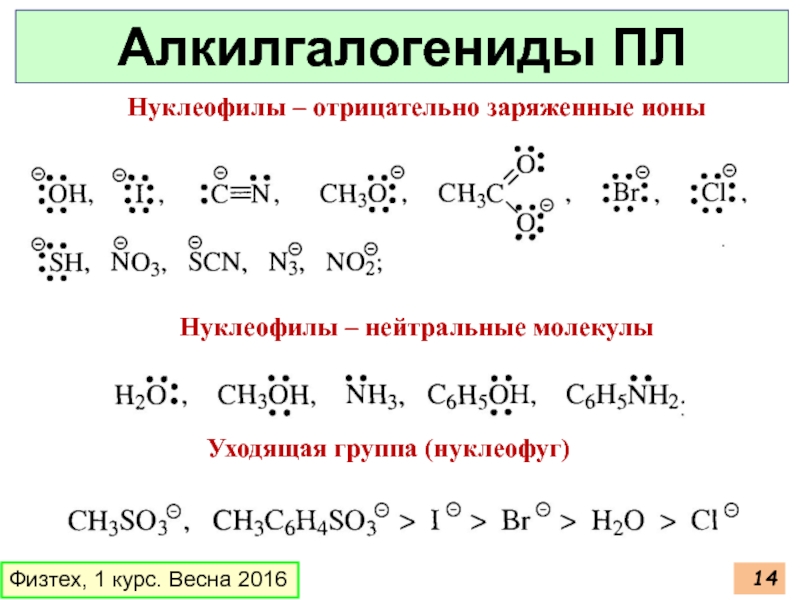
Слайд 14Физтех, 1 курс. Весна 2016
Алкилгалогениды ПЛ
Нуклеофилы – отрицательно заряженные ионы
Нуклеофилы –
Уходящая группа (нуклеофуг)
Слайд 28Физтех, 1 курс. Весна 2016
Алкилгалогениды ПЛ
SN2
+
SN1
КИП — контактная ионная пара, СИП — сольватно-разделенная ионная пара; И — свободные ионы.
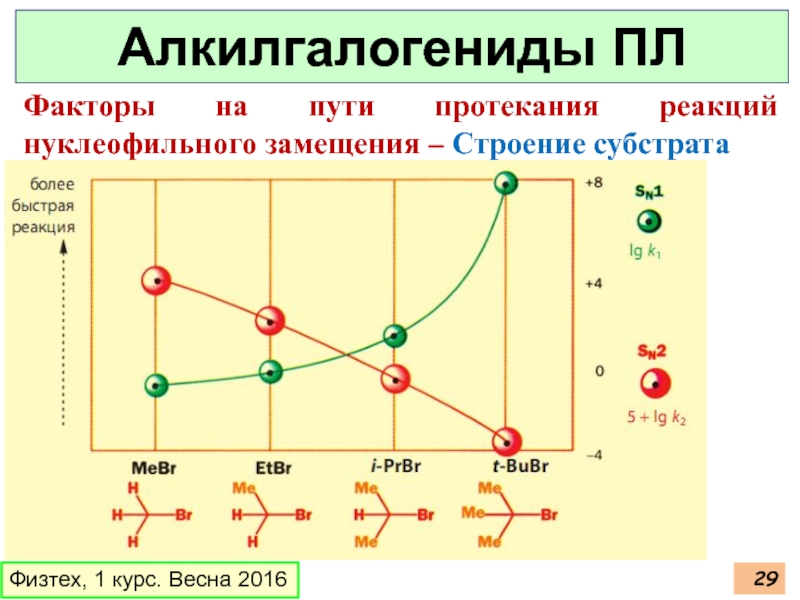
Слайд 29Физтех, 1 курс. Весна 2016
Алкилгалогениды ПЛ
Факторы на пути протекания реакций нуклеофильного
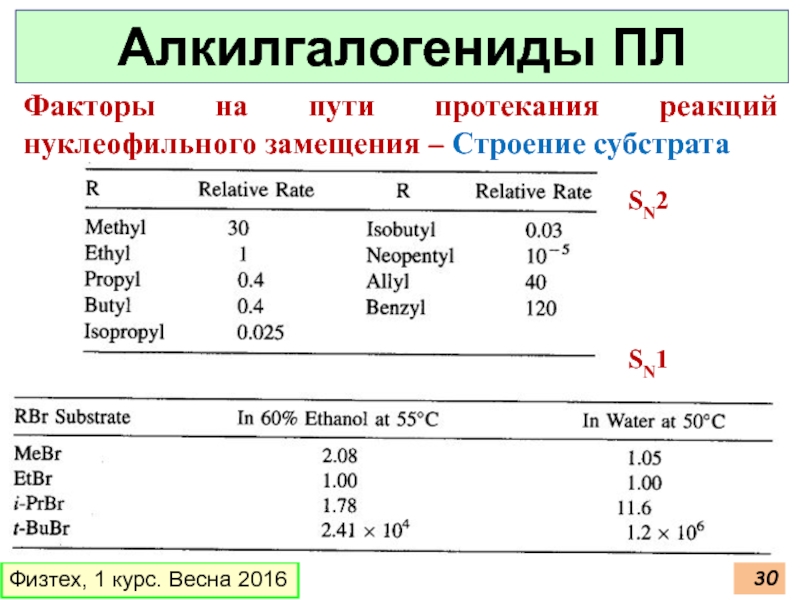
Слайд 30Физтех, 1 курс. Весна 2016
Алкилгалогениды ПЛ
SN2
SN1
Факторы на пути протекания реакций нуклеофильного
Слайд 31Физтех, 1 курс. Весна 2016
Алкилгалогениды ПЛ
Факторы на пути протекания реакций нуклеофильного
SN2 SN1
Слайд 32Физтех, 1 курс. Весна 2016
Алкилгалогениды ПЛ
Факторы на пути протекания реакций нуклеофильного
Неполярные полярные полярные протонные апротонные
Слайд 33Физтех, 1 курс. Весна 2016
Алкилгалогениды ПЛ
Факторы на пути протекания реакций нуклеофильного
SN2 SN1
Протеканию по этому механизму способствуют полярные апротонные растворители
Протеканию по этому механизму способствуют полярные протонные растворители (обладают одновременно нуклеофильными и электрофильными свойствами)
Причина – возникновение в ходе реакции катионов и анионов, возможна стабилизация и катиона и аниона
Слайд 34Физтех, 1 курс. Весна 2016
Алкилгалогениды ПЛ
SN2
Факторы на пути протекания реакций нуклеофильного
Слайд 35Физтех, 1 курс. Весна 2016
Алкилгалогениды ПЛ
Реакция идет тем быстрее, чем менее
Чем более сильная сопряженная кислота уходящей группы, тем выше ее нуклефугность
Факторы на пути протекания реакций нуклеофильного замещения – Нуклеофуг
Слайд 36Физтех, 1 курс. Весна 2016
Алкилгалогениды ПЛ
Замещение протекает тем легче, чем выше
Нуклеофильность связана с основностью и с поляризуемостью реагента (большая основность и поляризуемость – большая Н.)
Нуклеофильность зависит от природы растворителя
Анион более сильный нуклеофил, чем сопряженная кислота
Факторы на пути протекания реакций нуклеофильного замещения – сила нуклеофила
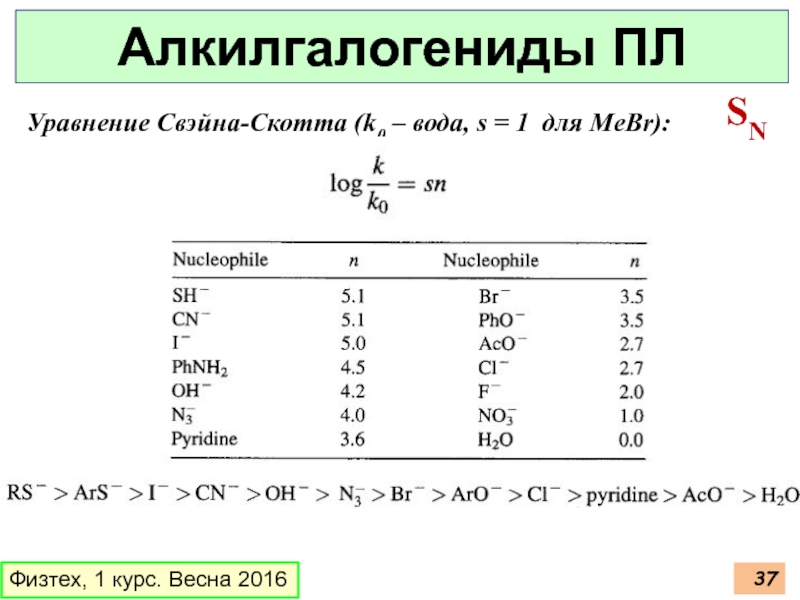
Слайд 37Физтех, 1 курс. Весна 2016
Алкилгалогениды ПЛ
SN
Уравнение Свэйна-Скотта (k0 – вода, s
Слайд 38Физтех, 1 курс. Весна 2016
Алкилгалогениды ПЛ
Метилбромид и нуклеофил в воде
Метилбромид и
SN2
SN1
I < Br < Cl < N3 CH3CO2 < < C6H5O < CN
Отсутствие сольватации основных, малополяризуемых ионов приводит к увеличению их нуклеофильности
H2O < CH3CO2 < Cl < OH < SCN < N3
Трифенилметил-катион / вода + ацетон
H2O < F < CH3CO2 < Cl < Br < C6H5O < N3 < OH < SCN < CN < I = SH
Нуклеофильность=Основность ?
Факторы на пути протекания реакций нуклеофильного замещения – нуклеофильность
Слайд 39Физтех, 1 курс. Весна 2016
Алкилгалогениды ПЛ
Мягкость и жесткость нуклеофила. Принцип ЖМКО
Пирсон (1963): жесткие основания Льюиса предпочитают координироваться с жесткими кислотами; мягкие основания - с мягкими кислотами.
Жесткость основания :
увеличивается в группе Периодической системы снизу вверх, например: I < Br < Cl < F
возрастает в периоде (в изоэлектронных сериях) слева направо: NH2 < OH < F
Жесткость кислот:
в группах периодической таблицы возрастает снизу вверх, например: Li+ > Na+ > K+
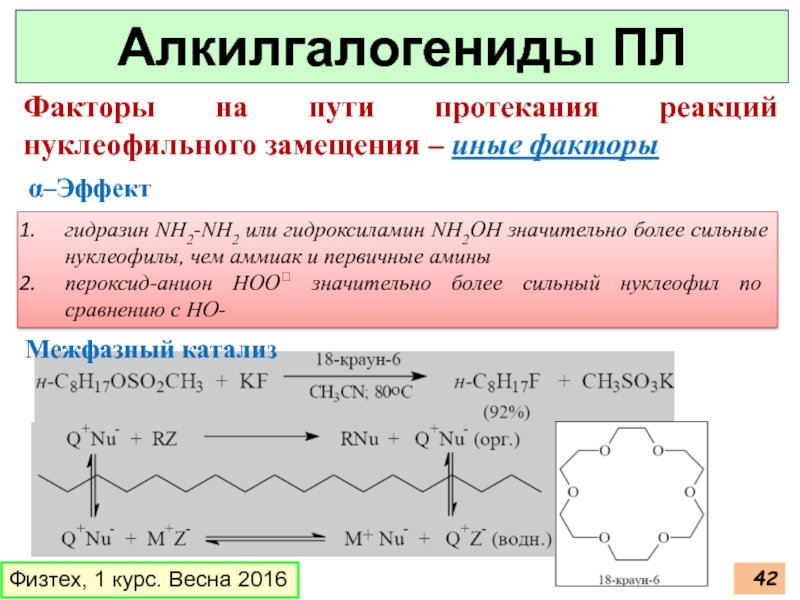
Слайд 42Физтех, 1 курс. Весна 2016
Алкилгалогениды ПЛ
Факторы на пути протекания реакций нуклеофильного
гидразин NH2-NH2 или гидроксиламин NН2OH значительно более сильные нуклеофилы, чем аммиак и первичные амины
пероксид-анион HOO значительно более сильный нуклеофил по сравнению с НО-
α–Эффект
Межфазный катализ
Слайд 43Физтех, 1 курс. Весна 2016
Алкилгалогениды ПЛ
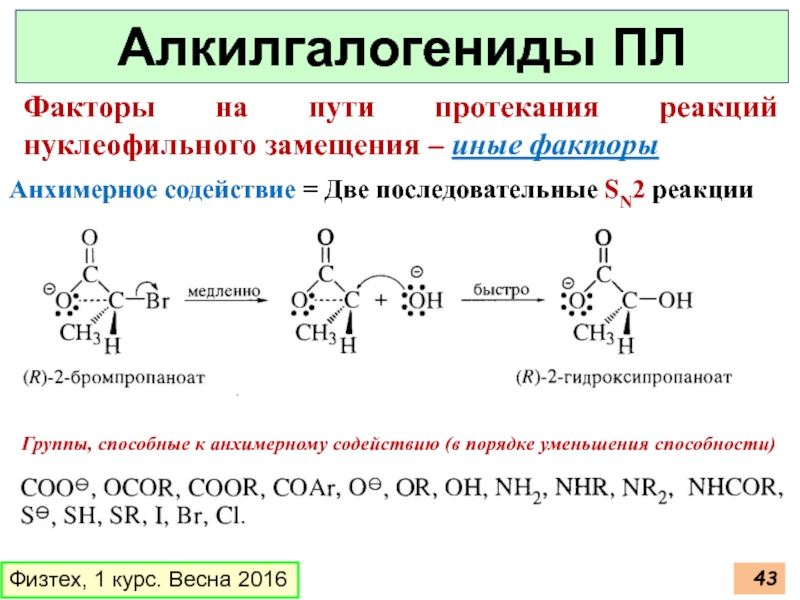
Факторы на пути протекания реакций нуклеофильного
Анхимерное содействие = Две последовательные SN2 реакции
Группы, способные к анхимерному содействию (в порядке уменьшения способности)
Слайд 44Физтех, 1 курс. Весна 2016
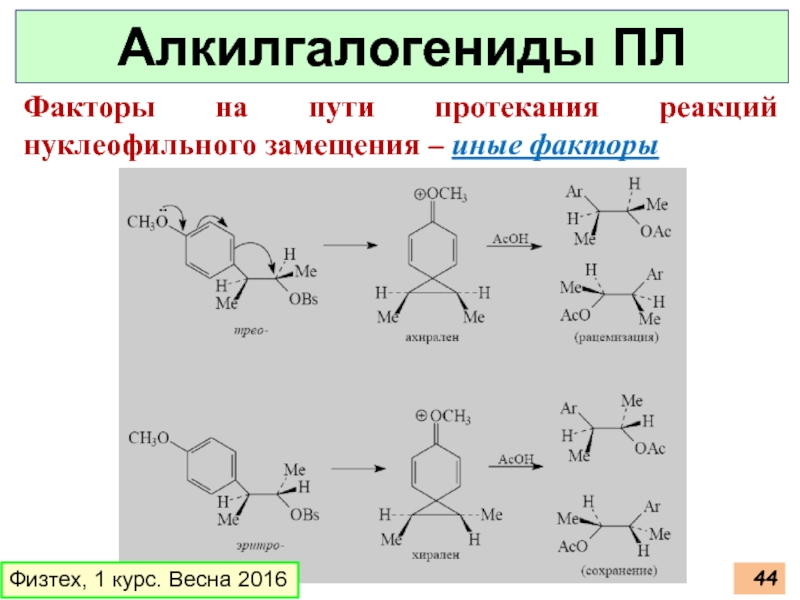
Алкилгалогениды ПЛ
Факторы на пути протекания реакций нуклеофильного
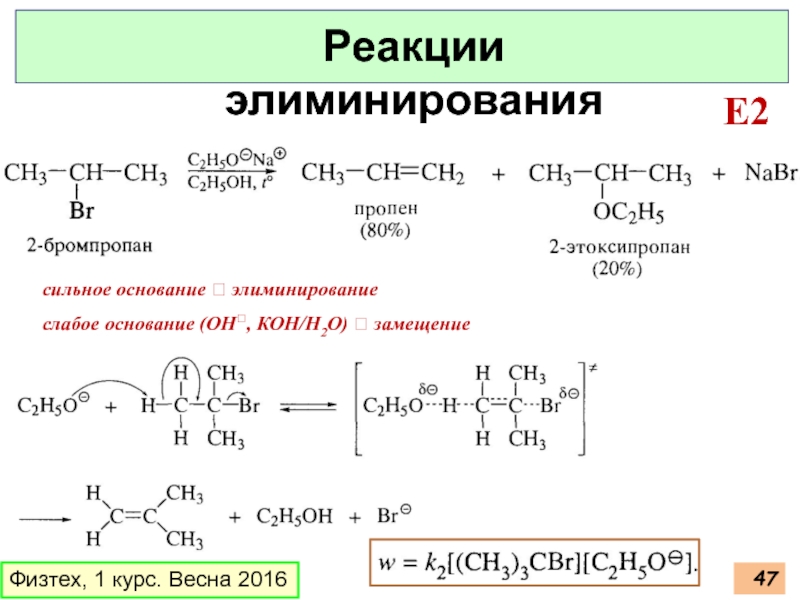
Слайд 47Физтех, 1 курс. Весна 2016
Реакции элиминирования
E2
сильное основание ? элиминирование
слабое основание (ОН,
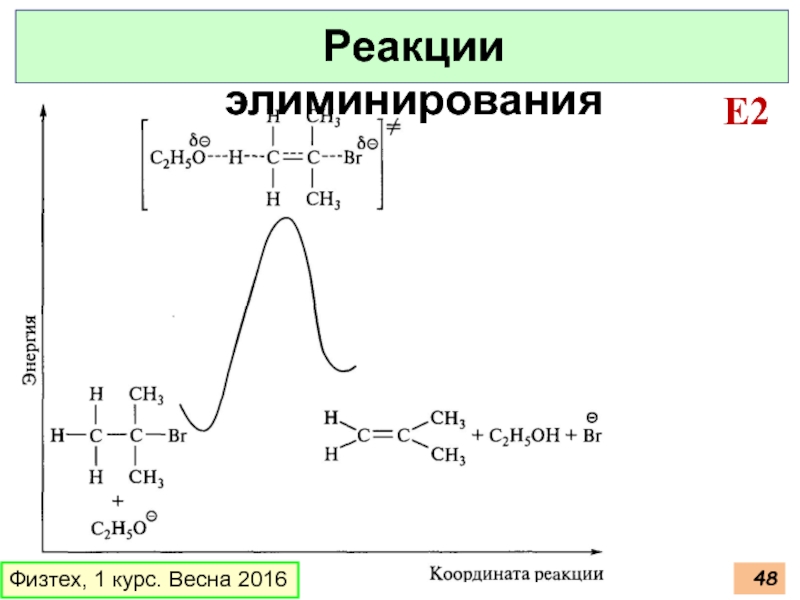
Слайд 49Физтех, 1 курс. Весна 2016
Реакции элиминирования
Региоселективность
E2
Правило Зайцева (верно для случаев, когда
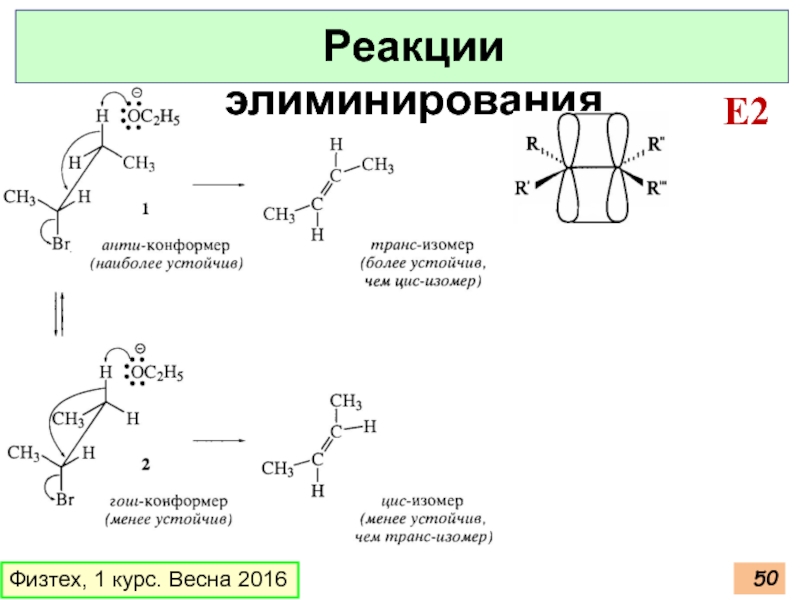
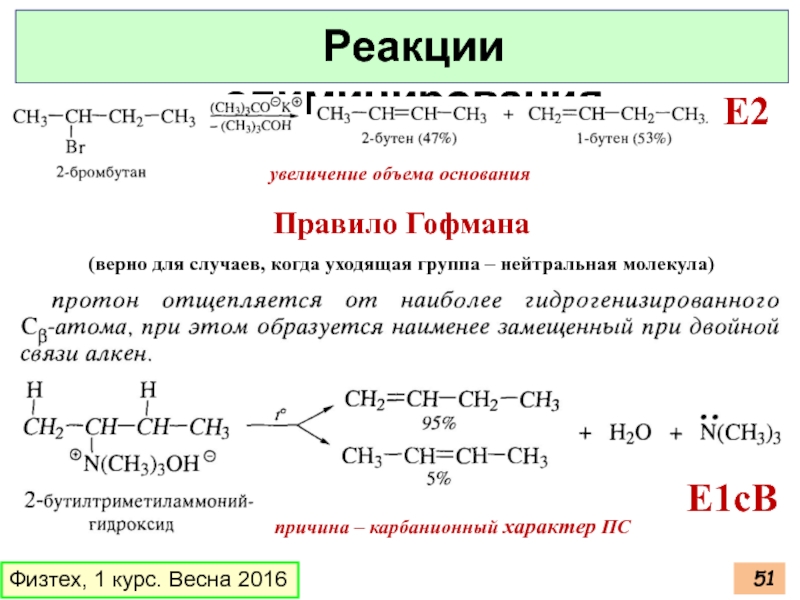
Слайд 51Физтех, 1 курс. Весна 2016
Реакции элиминирования
E2
увеличение объема основания
Правило Гофмана
(верно для случаев,
причина – карбанионный характер ПС
E1cB
Слайд 53Конкуренция между SN2 и E2
природа уходящей группы:
природа атакующего реагента
SN2
Сильные основания: NH2, OC(CH3)3
Большой объем нуклеофила
Сильные нуклеофилы и слабые основания: NH3, I Маленький объем нуклеофила
растворитель
SN2 E2
менее полярный: OН в спирте (заряд на пяти атомах в ПС)
более полярный: ОH в воде (заряд на трех атомах в ПС)
температура
SN2 E2
высокая (Еакт выше т.к. разрываются 2 связи)
низкая
ряды одинаковы
Реакции элиминирования
Физтех, 1 курс. Весна 2016
Слайд 57Физтех, 1 курс. Весна 2016
Реакции элиминирования
E1
Против правила Зайцева – стерические препятствия
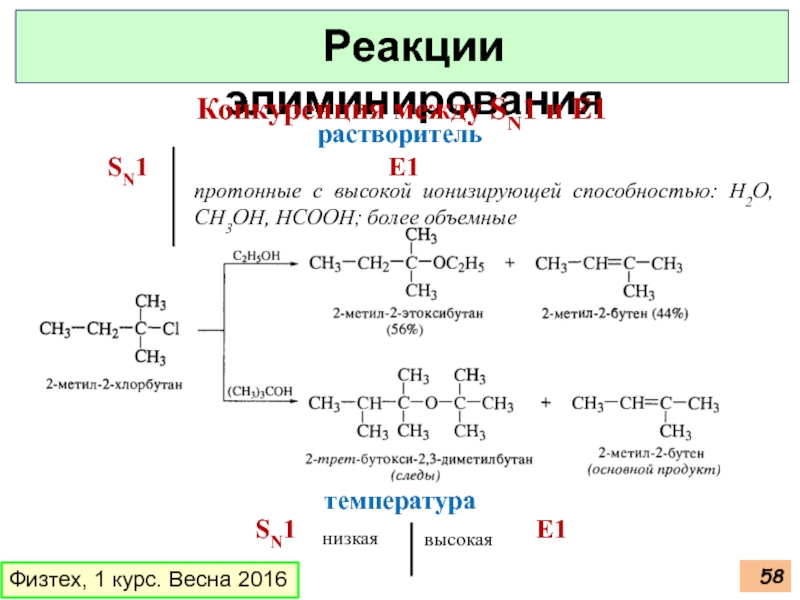
Слайд 58Физтех, 1 курс. Весна 2016
Реакции элиминирования
Конкуренция между SN1 и E1
растворитель
SN1
протонные с высокой ионизирующей способностью: Н2О, CH3OH, HCOOH; более объемные
температура
SN1 E1
высокая
низкая