- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
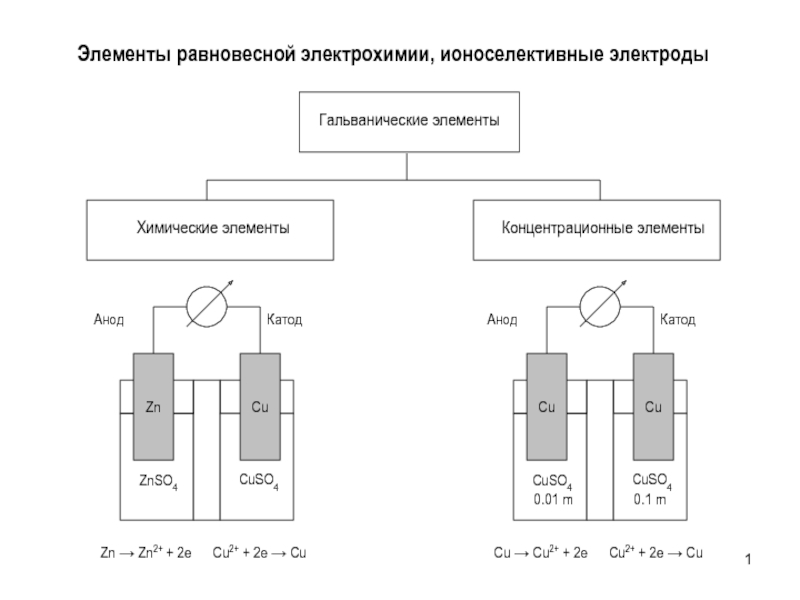
Элементы равновесной электрохимии, ионоселективные электроды презентация
Содержание
- 1. Элементы равновесной электрохимии, ионоселективные электроды
- 2. Гальванические элементы без жидкостного соединения и с
- 3. Э.д.с. элемента с жидкостным соединением Э.д.с. элемента
- 4. Ионоселективные электроды (ИСЭ) -потенциометрические датчики (сенсоры) химического
- 5. Принципы измерений с потенциометрическими сенсорами - ИСЭ
- 6. Важнейшие практические задачи, решение которых основано на
- 7. Мембранный потенциал Электролиты переходят сквозь мембрану из
- 8. Межфазный потенциал (потенциал Доннана) + +
- 9. Внутримембранный диффузионный потенциал Потенциометрические условия (нулевой ток):
- 10. Полный мембранный потенциал Потенциалопределяющий ион задает межфазный потенциал, остальные под него подстраиваются
- 11. Селективность электродов и способы ее оценки,
- 12. Стеклянные электроды Достоинства Уникальная селективность к ионам
- 13. Электроды с поли- и монокристаллическими мембранами Достоинства
- 14. ИСЭ с жидкими и полимерными мембранами
- 15. Селективность ИСЭ с мембранами на основе
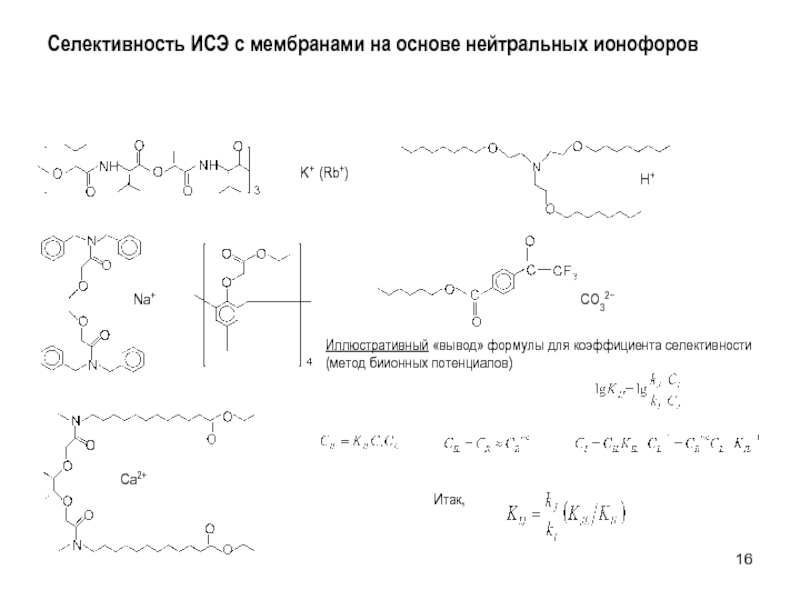
- 16. Селективность ИСЭ с мембранами на основе нейтральных ионофоров
- 17. Конструкции ИСЭ для решения различных аналитических задач
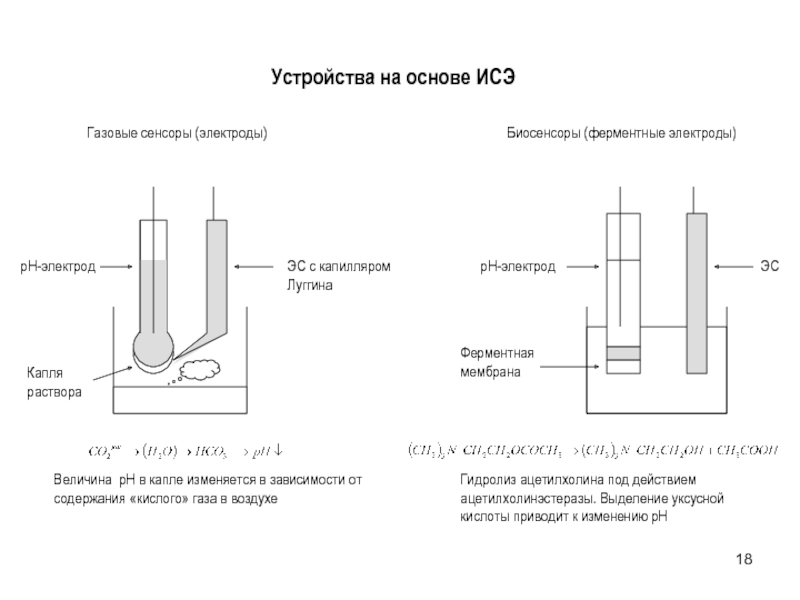
- 18. Устройства на основе ИСЭ
- 19. Элементы химической кинетики Скорость
- 20. Молекулярность и порядок реакции Молекулярность реакции –
- 21. Некоторые элементарные химические реакции
- 22. Некоторые элементарные химические реакции Обратимая реакция
- 23. Влияние температуры на скорость химической реакции, уравнение
- 24. Ферментативная кинетика, уравнение Михаэлиса-Ментен Допущения: Система находится
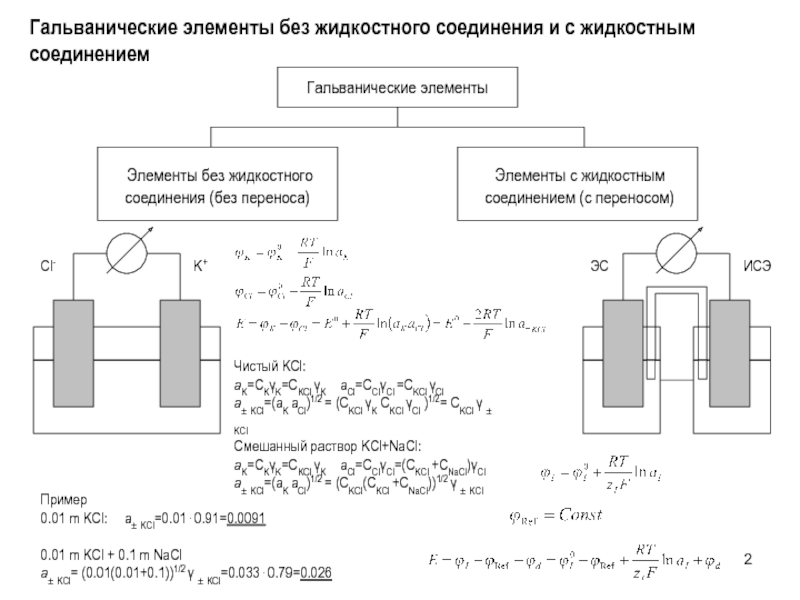
Слайд 2Гальванические элементы без жидкостного соединения и с жидкостным соединением
Чистый KCl:
aK=CKγK=CKCl
a± KCl=(aK aCl)1/2 = (CKCl γK CKCl γCl )1/2= CKCl γ ± KCl
Смешанный раствор KCl+NaCl:
aK=CKγK=CKCl γK aCl=CClγCl=(CKCl +CNaCl)γCl
a± KCl=(aK aCl)1/2 = (CKCl(CKCl +CNaCl))1/2 γ ± KCl
Пример
0.01 m KCl: a± KCl=0.01⋅0.91=0.0091
0.01 m KCl + 0.1 m NaCl
a± KCl= (0.01(0.01+0.1))1/2 γ ± KCl=0.033⋅0.79=0.026
Слайд 3Э.д.с. элемента с жидкостным соединением
Э.д.с. элемента с жидкостным соединением может быть
Уравнение Гендерсона:
Каким электролитом заполняют электролитические ключи?
KCl, LiCCl3COO, NH4NO3 Концентрация электролита: 1 моль/л и выше
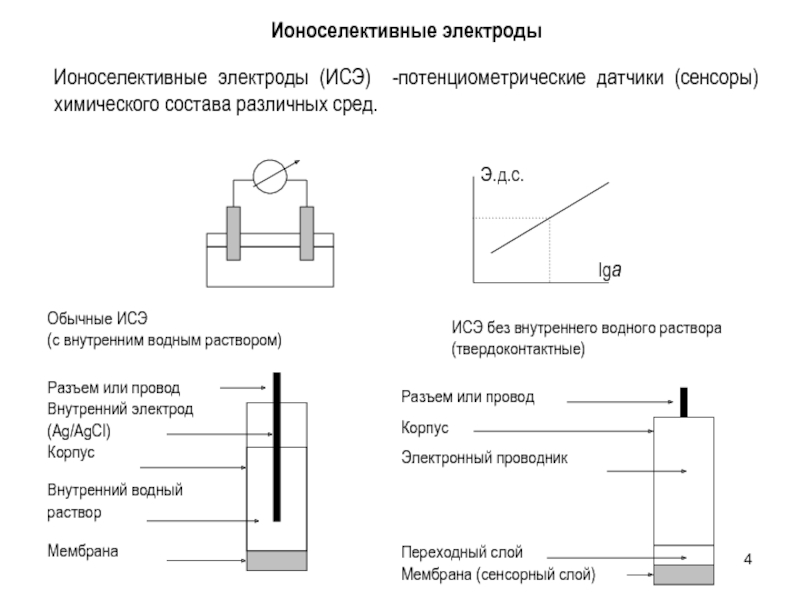
Слайд 4Ионоселективные электроды (ИСЭ) -потенциометрические датчики (сенсоры) химического состава различных сред.
Обычные ИСЭ
(с внутренним водным раствором)
ИСЭ без внутреннего водного раствора (твердоконтактные)
Ионоселективные электроды
Слайд 5Принципы измерений с потенциометрическими сенсорами - ИСЭ и ионоселективными полевыми транзисторами
-
Компенсационная схема
Современная схема на полевых транзисторах
Принцип действия полевого транзистора
Слайд 6Важнейшие практические задачи, решение которых основано на применении ИСЭ
Холинэстераза, холин, пестициды
Определение
Экологический мониторинг
Определение газов в воздухе
Пищевая промышленность
Контроль технологических процессов
Агрохимия, почвоведение
Клинический анализ
Задача
NH3, NO2, “кислые” газы
pH, Ca2+, CH3COO−
pH, Pb2+, Hg2+, Cu2+, NO3−
pH, NO3−, K+, NH4+, Ca2+, Cl−, Na+
pH, Cu2+, Ag, Au, NO3−, K+, NH4+, UO22+
pH, K+, Na+, Ca2+, Li+, Cl−, HCO3 −
Основные контролируемые ионы и вещества
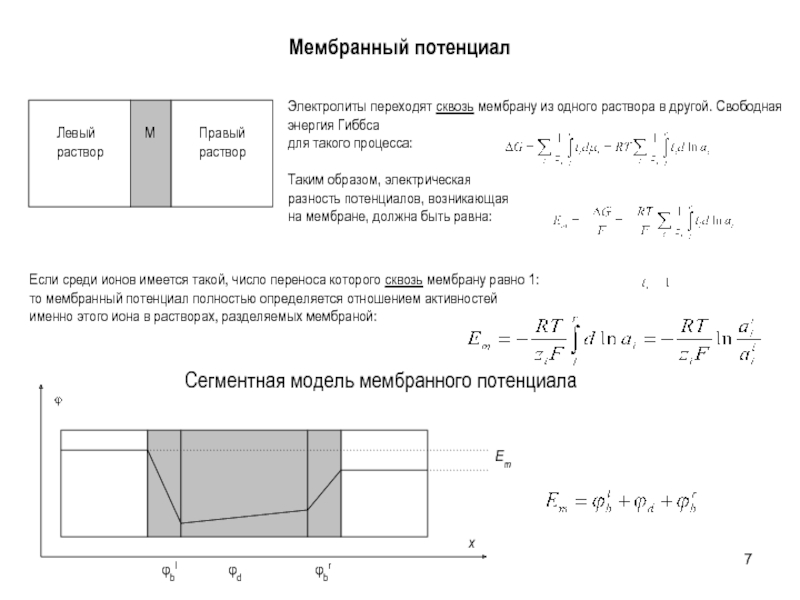
Слайд 7Мембранный потенциал
Электролиты переходят сквозь мембрану из одного раствора в другой. Свободная
для такого процесса:
Таким образом, электрическая
разность потенциалов, возникающая
на мембране, должна быть равна:
Если среди ионов имеется такой, число переноса которого сквозь мембрану равно 1:
то мембранный потенциал полностью определяется отношением активностей
именно этого иона в растворах, разделяемых мембраной:
Сегментная модель мембранного потенциала
x
Em
φbl
φbr
φd
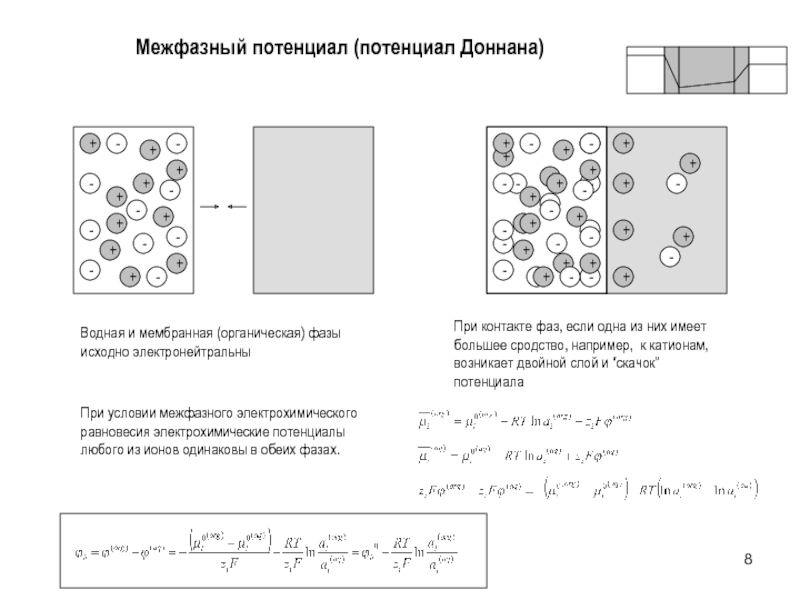
Слайд 8Межфазный потенциал (потенциал Доннана)
+
+
+
+
+
+
-
-
-
-
-
-
Водная и мембранная (органическая) фазы
исходно электронейтральны
При контакте фаз,
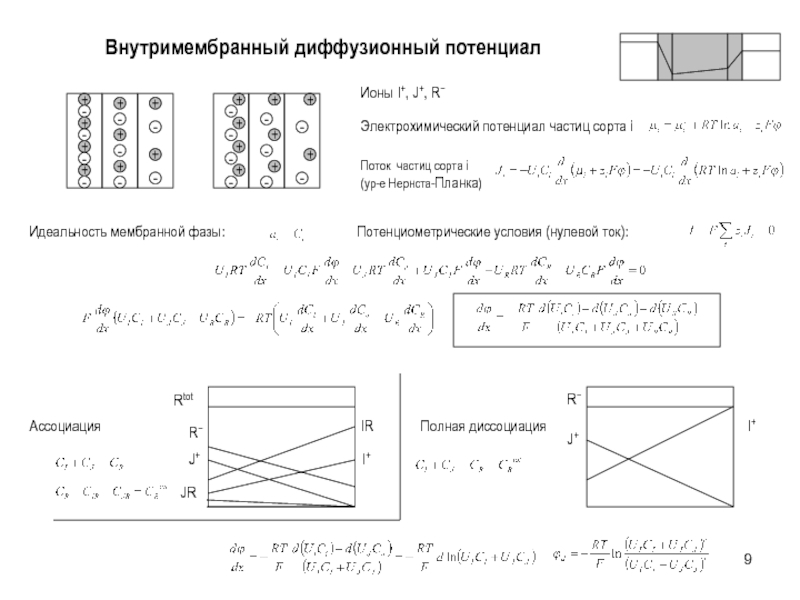
Слайд 9Внутримембранный диффузионный потенциал
Потенциометрические условия (нулевой ток):
Идеальность мембранной фазы:
Ионы I+, J+, R−
Полная
Ассоциация
Слайд 10Полный мембранный потенциал
Потенциалопределяющий ион задает межфазный потенциал, остальные под него подстраиваются
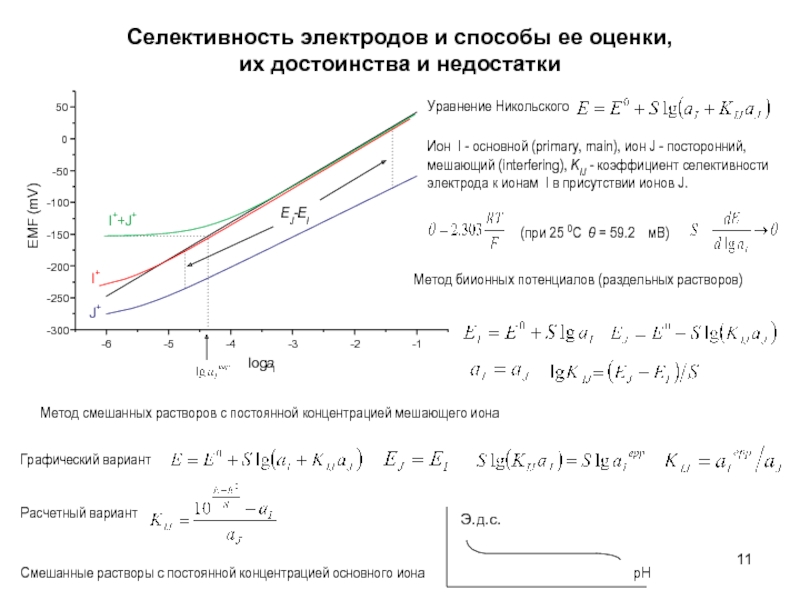
Слайд 11Селективность электродов и способы ее оценки,
их достоинства и недостатки
Ион I
Метод биионных потенциалов (раздельных растворов)
Метод смешанных растворов с постоянной концентрацией мешающего иона
Смешанные растворы с постоянной концентрацией основного иона
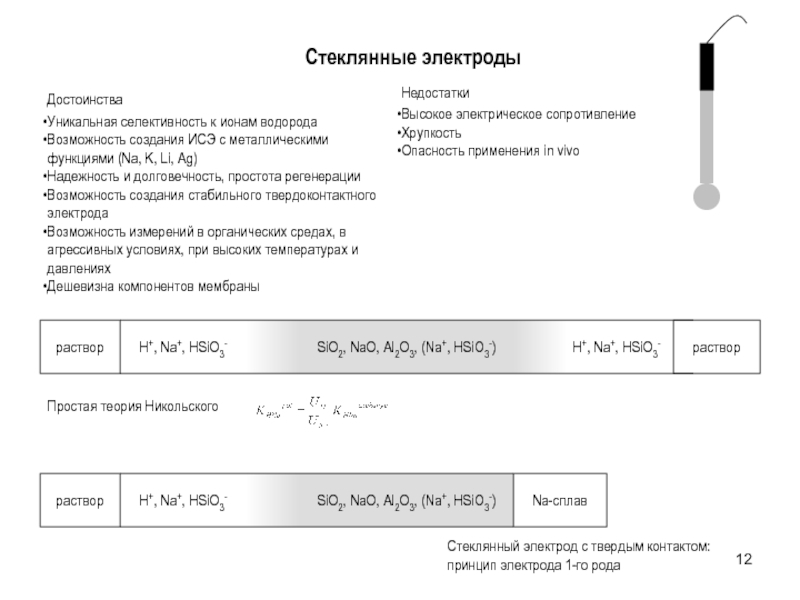
Слайд 12Стеклянные электроды
Достоинства
Уникальная селективность к ионам водорода
Возможность создания ИСЭ с металлическими функциями
Надежность и долговечность, простота регенерации
Возможность создания стабильного твердоконтактного электрода
Возможность измерений в органических средах, в агрессивных условиях, при высоких температурах и давлениях
Дешевизна компонентов мембраны
Недостатки
Высокое электрическое сопротивление
Хрупкость
Опасность применения in vivo
Слайд 13Электроды с поли- и монокристаллическими мембранами
Достоинства
Возможность создания ИСЭ с анионными и
Надежность и долговечность, простота регенерации
Возможность создания стабильного твердоконтактного электрода
Возможность измерений в органических средах, в агрессивных условиях
Низкое электрическое сопротивление
Дешевизна компонентов мембраны
Возможность создания халькогенидных стекол (допирование As)
Недостатки
Ограниченный набор ионов, к которым можно создать хорошие ИСЭ: галогениды, металлы сероводородной группы
Анионселективные (X = S2 −, Cl−, Br −, J −, SCN −, CN − )
Слайд 14ИСЭ с жидкими и полимерными мембранами
(на основе ионофоров)
Достоинства
Возможность создания самых
Недостатки
Сравнительно низкая долговечность (≈ 1 год)
Высокое электрическое сопротивление
Возможность измерений только в водных растворах
Трудность создания стабильного твердоконтактного варианта
Дороговизна компонентов мембран
Слайд 15Селективность ИСЭ с мембранами
на основе ионообменников, ряд Гофмейстера
Иллюстративный «вывод» формулы
R − > ClO4 − > SCN − ≈ J − > NO3− > Br − > Cl − ≈ HCO3 − > H2PO4 − > SO42 −
Ряд Гофмейстера
Гидратация Селективность
А если ион не теряет воду ?
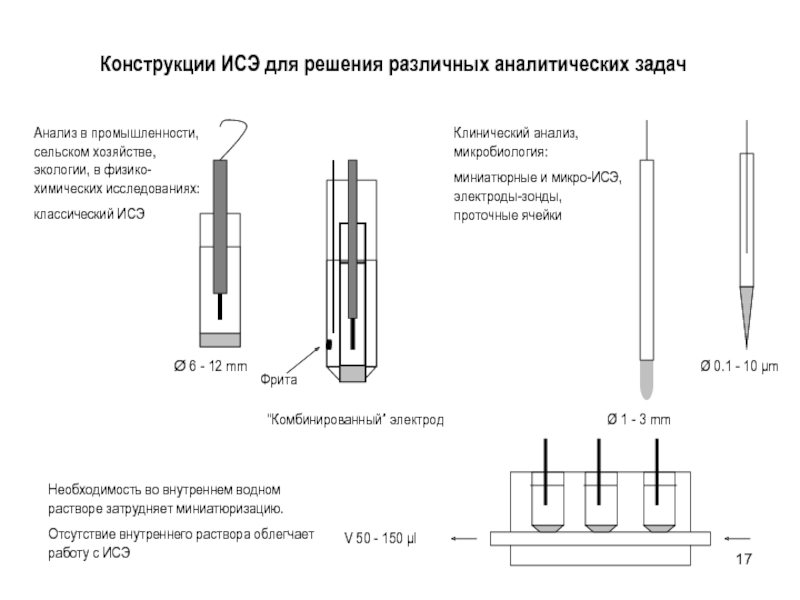
Слайд 17Конструкции ИСЭ для решения различных аналитических задач
Необходимость во внутреннем водном растворе
Отсутствие внутреннего раствора облегчает работу с ИСЭ
Слайд 19Элементы химической кинетики
Скорость химической реакции: количество молекул данного вида, реагирующих в
Постулируется, что , ni – порядок реакции по i-му
веществу. Для одностадийных реакций ni = νi. Константа скорости k=v при C1=C2= … Cl=1.
Реакция называется двусторонней если она, в принципе, может идти в обоих направлениях. При равновесии скорости прямого и обратного процессов равны, но вдали от равновесия эти скорости могут различаться на много порядков. В этом смысле реакция может быть кинетически односторонней. Чаще всего – если часть продуктов реакции уходит в другую фазу: выпадает в осадок, испаряется, и т.п.
Слайд 20Молекулярность и порядок реакции
Молекулярность реакции – число частиц, участвующих в элементарном
Мономолекулярные: изомеризация, диссоциация, радиоактивный распад, реакции, провоцируемые внешними полями или излучениями.
Бимолекулярные: результат столкновения двух молекул, например – ассоциация.
Тримолекулярные: одновременное столкновение трех молекул (очень редко).
Порядок реакции по данному веществу – число, равное показателю степени, в которой данное вещество входит в кинетическое уравнение
Порядок реакции в целом – сумма порядков по каждому из исходных веществ:
Слайд 21Некоторые элементарные химические реакции
Элементарная реакция – проходит в одну стадию и
Слайд 22
Некоторые элементарные химические реакции
Обратимая реакция вида
Считаем, что в начальный момент
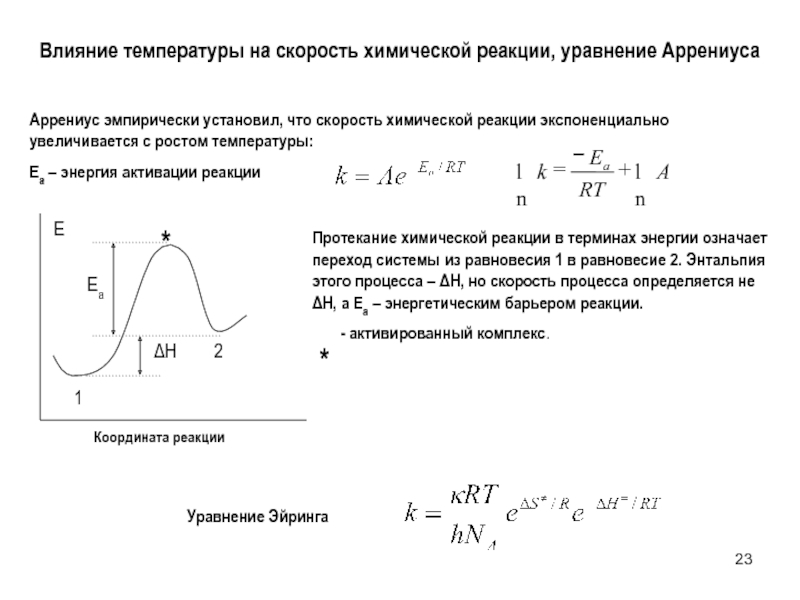
Слайд 23Влияние температуры на скорость химической реакции, уравнение Аррениуса
Протекание химической реакции в
- активированный комплекс.
*
Аррениус эмпирически установил, что скорость химической реакции экспоненциально увеличивается с ростом температуры:
Ea – энергия активации реакции
Уравнение Эйринга
Слайд 24Ферментативная кинетика, уравнение Михаэлиса-Ментен
Допущения:
Система находится в стационарном состоянии
Концентрация энзимно-субстратного комплекса всегда