органическую за счет образования с органическим реагентом комплексных соединений или сольватов.
Обязательным условием протекания экстракции – несмешивание водной и органической фаз.
- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Экстракция презентация
Содержание
- 1. Экстракция
- 2. Задачи, решаемые экстракцией. Избирательное извлечение целевого компонента,
- 3. Типичная экстракционная схема
- 4. Основные понятия Экстрагент - органическое соединение
- 5. Количественные характеристики 1. Коэффициент распределения (D) -
- 6. Основные принципы извлечения из водной фазы в
- 7. высаливание ABв = Aв+ +Bв-
- 8. высаливатель Действия одноименного иона Изменения коэффициентов активностей.
- 9. Типы экстрагентов и механизмы экстракции Нейтральные
- 10. Координационный механизм: ROоδ- + Kвn+ +
- 11. Сольватный механизм qROоδ- + Мвn+ +
- 12. Катионообменные экстрагенты монокарбоновые кислоты CnH2n+1COOH
- 13. Катионообменный механизм Mn+ (B) + n/2(HR)2 (O)
- 14. Анионообменные экстрагенты Первичные амины RH2N
Слайд 2Задачи, решаемые экстракцией.
Избирательное извлечение целевого компонента, даже при малых его концентрациях,
при этом, регулируя соотношение объемов органической и водной фаз можно многократно его сконцентрировать.
Глубокая очистка целевого компонента от примесей.
Разделение близких по свойствам металлов (цирконий и гафний; тантал и ниобий; редкоземельные элементы и т.д.).
В аналитической химии экстракция может использоваться как метод экспресс анализа и как метод концентрирования при анализе высокочистых материалов на примеси.
Глубокая очистка целевого компонента от примесей.
Разделение близких по свойствам металлов (цирконий и гафний; тантал и ниобий; редкоземельные элементы и т.д.).
В аналитической химии экстракция может использоваться как метод экспресс анализа и как метод концентрирования при анализе высокочистых материалов на примеси.
Слайд 3Типичная экстракционная схема
Экстрагент
Водная фаза
Экстракция
органическая фаза рафинат
реэкстр р-р
реэкстракция
орг фаза водный раствор (на переработку)
раствор регенерация
Экстрагент (на экстракцию)
Экстракция
органическая фаза рафинат
реэкстр р-р
реэкстракция
орг фаза водный раствор (на переработку)
раствор регенерация
Экстрагент (на экстракцию)
Слайд 4Основные понятия
Экстрагент - органическое соединение способное образовывать с ценным компонентом
комплексное соединение или сольват.
Разбавитель – органическое соединение в котором растворяют экстрагент. Основное свойство должна быть химическая инертность по отношению к ценному компоненту
Процесс обратный экстракции – реэкстракция.
Разбавитель – органическое соединение в котором растворяют экстрагент. Основное свойство должна быть химическая инертность по отношению к ценному компоненту
Процесс обратный экстракции – реэкстракция.
Слайд 5Количественные характеристики
1. Коэффициент распределения (D) - отношение аналитической концентрации распределяющегося вещества
в органической фазе (у) к его аналитической концентрации в водной фазе (х):
D = y/x.
2. Коэффициентом разделения -отношение коэффициентов распределения двух веществ:
β1/2 = D1/D2 (D1>D2; β1/2>1)
3. Степень извлечения (Е, %):
Е= Go /Gисх = yV0/( yV0+xVв)= D/(D+Vв/V0)
если VO = VB; то E = D.100/(D + 1)
D = y/x.
2. Коэффициентом разделения -отношение коэффициентов распределения двух веществ:
β1/2 = D1/D2 (D1>D2; β1/2>1)
3. Степень извлечения (Е, %):
Е= Go /Gисх = yV0/( yV0+xVв)= D/(D+Vв/V0)
если VO = VB; то E = D.100/(D + 1)
Слайд 6Основные принципы извлечения из водной фазы в органическую
Заряженным ионам энергетически невыгоден
переход из сильно полярной высокоупорядочненной фазы (водного раствора) в органическую фазу. Для такого перехода необходима предварительная нейтрализация заряда за счет образования незаряженных соединений(комплексов или ионных ассоциатов). Кроме этого необходимо полное или частичное освобождение от гидратной оболочки – дегидратация.
Это становится возможным :
при введении в систему высаливателей или комплексообразователей;
при присоединении к экстрагируемому катиону органического аниона;
при присоединении к экстрагируемому аниону органического катиона;
при замене воды в аквакомплексе на незаряженный органический лиганд.
Это становится возможным :
при введении в систему высаливателей или комплексообразователей;
при присоединении к экстрагируемому катиону органического аниона;
при присоединении к экстрагируемому аниону органического катиона;
при замене воды в аквакомплексе на незаряженный органический лиганд.
Слайд 7высаливание
ABв = Aв+ +Bв-
Aв+ +Bв-= (AB)o
k= aAB/aA·aB
k=CAB·γAB/CA·γA ·CB·γB =y/x·x· γ0/γ2
D= y/x = k ·x ·γ2/γ0
x→0 D→0
CBв=Cв++Bв-
k=y/x·(x+m) ·γ2/γ0
D= y/x = k ·(x+m) ·γ2/γ0
k= aAB/aA·aB
k=CAB·γAB/CA·γA ·CB·γB =y/x·x· γ0/γ2
D= y/x = k ·x ·γ2/γ0
x→0 D→0
CBв=Cв++Bв-
k=y/x·(x+m) ·γ2/γ0
D= y/x = k ·(x+m) ·γ2/γ0
Слайд 8высаливатель
Действия одноименного иона
Изменения коэффициентов активностей. Из уравнения видно, что введение высаливателя
должно увеличить коэффициент активности в водной фазе.
Третье действие высаливателя на экстракционную систему заключается в том, что введение в систему высаливателя способствует образованию недиссоциированных молекул, т.е. способствует процессу дегидратации.
Третье действие высаливателя на экстракционную систему заключается в том, что введение в систему высаливателя способствует образованию недиссоциированных молекул, т.е. способствует процессу дегидратации.
Слайд 9Типы экстрагентов и механизмы экстракции
Нейтральные экстрагенты.
Спирты CnH2n+1OH
, где n = 7-9
Простые эфиры C2H5-O-C2H5
Сложные эфиры O
RC
OR1
Кетоны R - C - R1
O
Сульфоксид R2SO
Трибутилфосфат
R - O
R - O - P = O, где R - C4H9
R - O
Простые эфиры C2H5-O-C2H5
Сложные эфиры O
RC
OR1
Кетоны R - C - R1
O
Сульфоксид R2SO
Трибутилфосфат
R - O
R - O - P = O, где R - C4H9
R - O
Слайд 10Координационный механизм:
ROоδ- + Kвn+ + Aвn- = [RO→K]Aо
а) сольватный
qROоδ-
+ Мвn+ + Aвn- = [М·qRО]Aо
б) гидратносольватный
qROоδ- + Н3Ов++3Н2О + Aв- = [Н9О4·qRО]Aо
в) оксониевый
qROоδ- + Нв++ Aв- = НA·qRОо
б) гидратносольватный
qROоδ- + Н3Ов++3Н2О + Aв- = [Н9О4·qRО]Aо
в) оксониевый
qROоδ- + Нв++ Aв- = НA·qRОо
Слайд 11Сольватный механизм
qROоδ- + Мвn+ + Aвn- = [М·qRО]Aо
k =
C [М·qRО]A /CROq·CM·CA
D = k· CROq· CA
D = k· CROq· CA
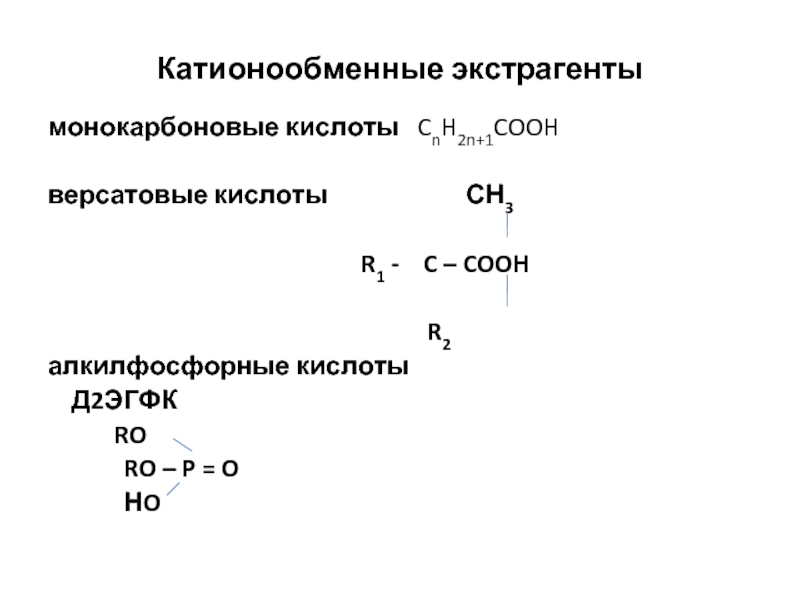
Слайд 12Катионообменные экстрагенты
монокарбоновые кислоты CnH2n+1COOH
версатовые кислоты
СН3
R1 - C – COOH
R2
алкилфосфорные кислоты
Д2ЭГФК
RO
RO – P = O
НO
R1 - C – COOH
R2
алкилфосфорные кислоты
Д2ЭГФК
RO
RO – P = O
НO
Слайд 13Катионообменный механизм
Mn+ (B) + n/2(HR)2 (O) = MRn (O) + nH+
(B)
lgD=lgk+n/2 lgCHR –nlgCH= lgk+n/2 lgCHR+npH
lgD=lgk+n/2 lgCHR –nlgCH= lgk+n/2 lgCHR+npH
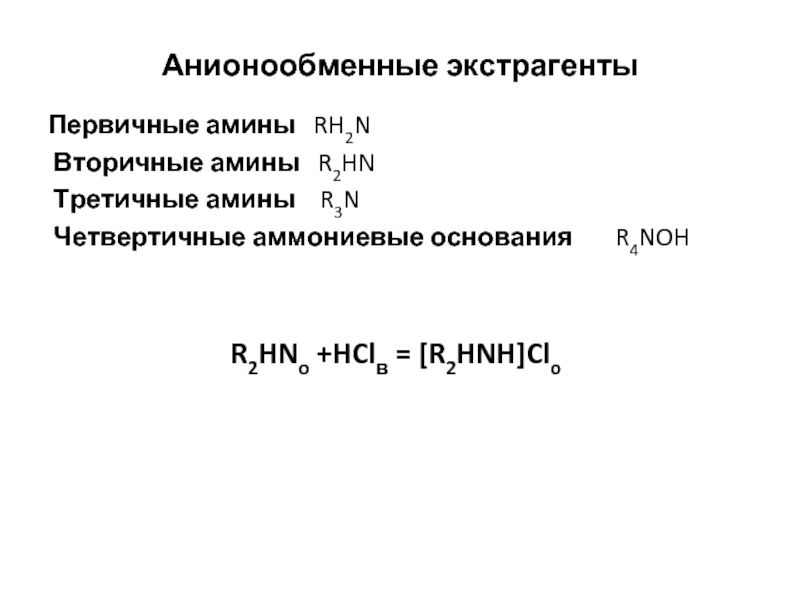
Слайд 14Анионообменные экстрагенты
Первичные амины RH2N
Вторичные амины R2HN
Третичные амины R3N
Четвертичные аммониевые основания R4NOH
R2HNo +HClв = [R2HNH]Clo
Четвертичные аммониевые основания R4NOH
R2HNo +HClв = [R2HNH]Clo









![Координационный механизм: ROоδ- + Kвn+ + Aвn- = [RO→K]Aо а) сольватныйqROоδ- + Мвn+ + Aвn-](/img/tmb/2/157546/4562cfe016c1cc0197c8bd20fd16f96b-800x.jpg)
![Сольватный механизм qROоδ- + Мвn+ + Aвn- = [М·qRО]Aо k = C [М·qRО]A /CROq·CM·CAD =](/img/tmb/2/157546/103e0eafd9cdd5ad524304f2d7e93dde-800x.jpg)