- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
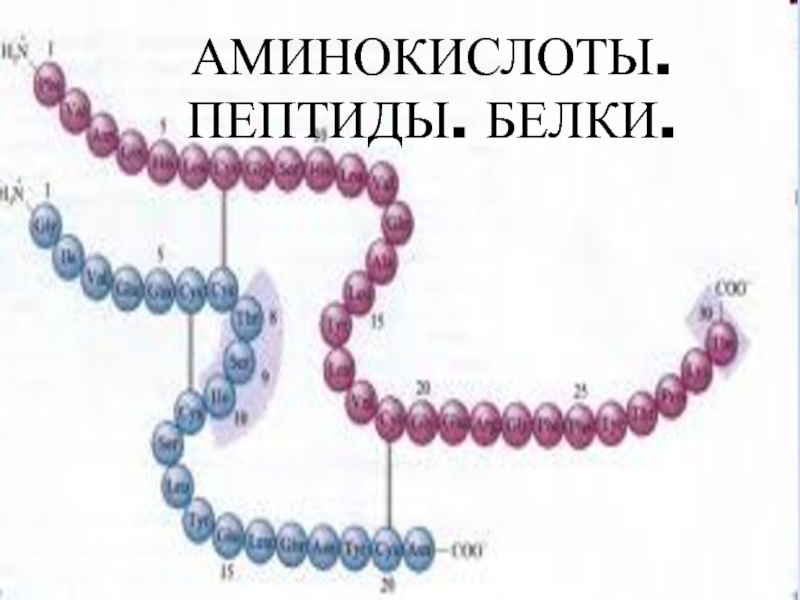
Аминокислоты. Пептиды. Белки презентация
Содержание
- 1. Аминокислоты. Пептиды. Белки
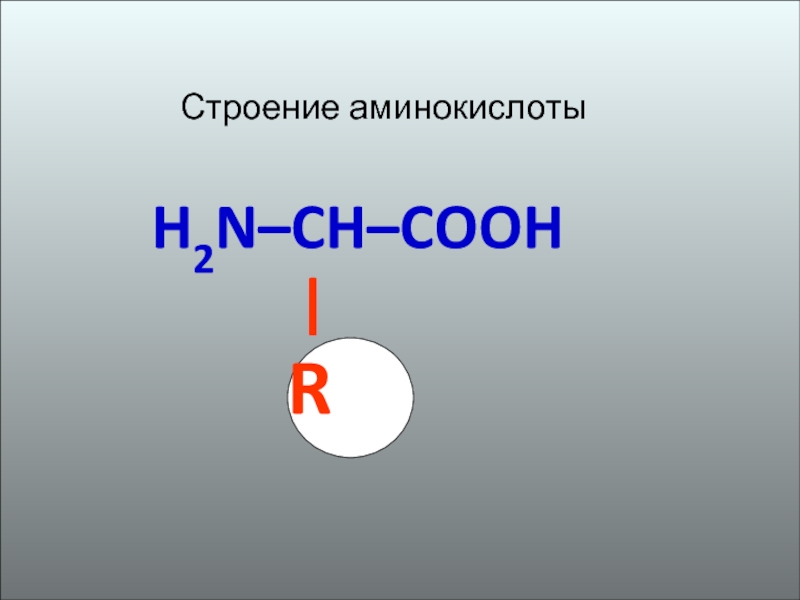
- 2. Строение аминокислоты H2N–CH–COOH
- 3. В природных объектах их обнаружено около
- 4. Классификация аминокислот 1. Моноаминомонокарбоновые 2. Моноаминодикарбоновые 3.
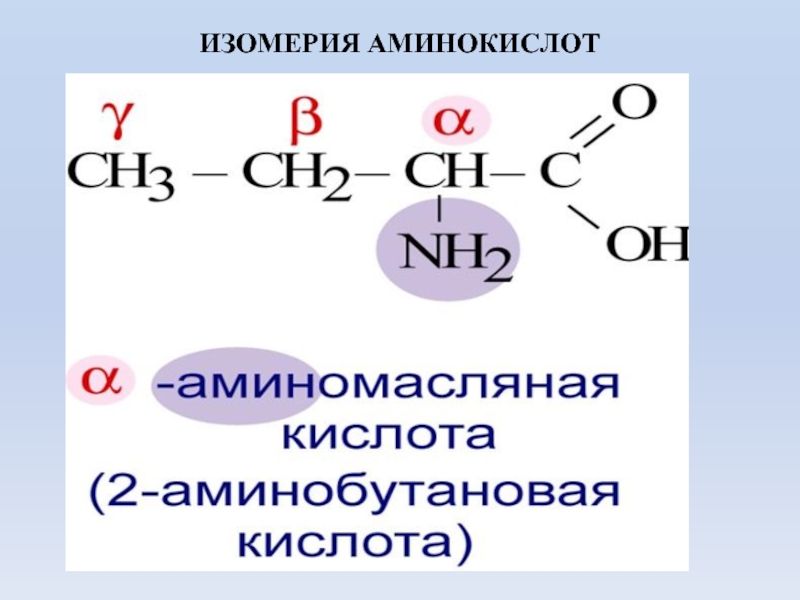
- 6. ИЗОМЕРИЯ АМИНОКИСЛОТ
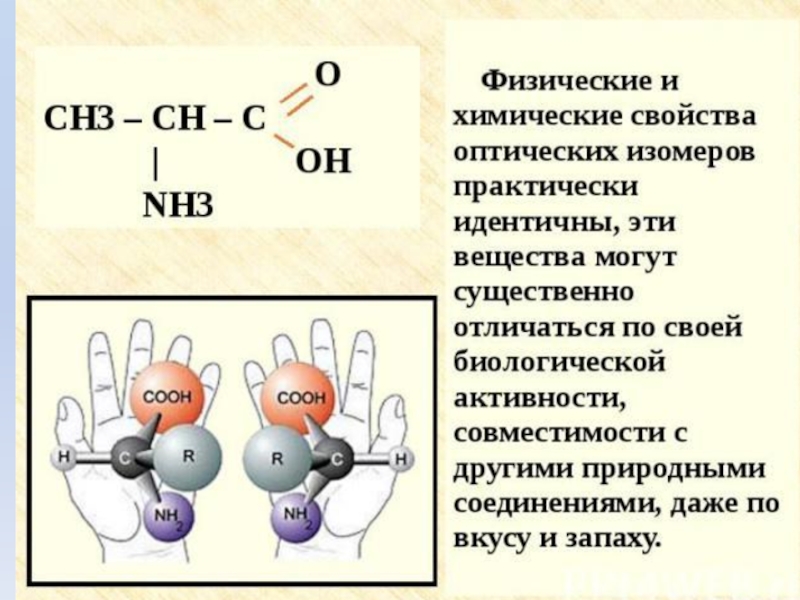
- 7. Оптическая изомерия аминокислоты существуют в виде зеркальных изомеров
- 8. Стереоизомерия. Все природные a-аминокислоты (кроме глицина) являются
- 11. По кислотно-основным свойствам аминокислоты делят на три
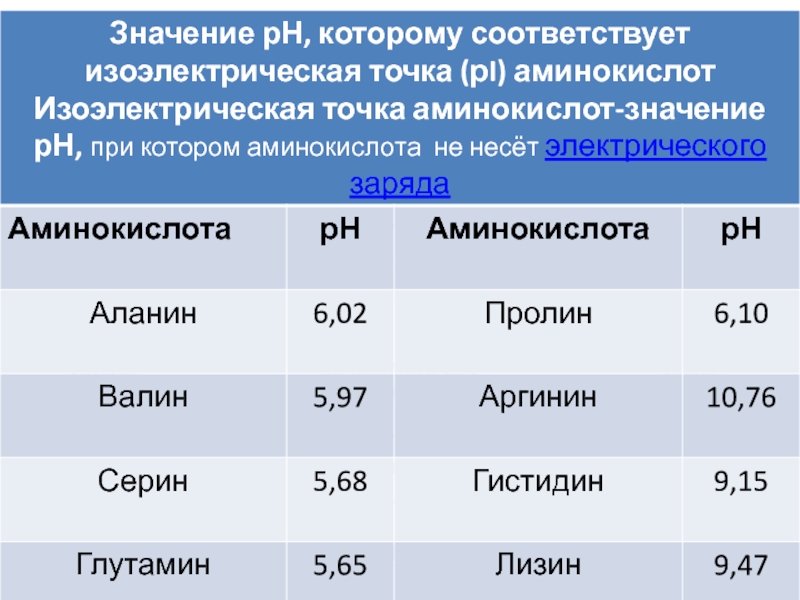
- 13. Изоэлектрическая точка (ИЭТ) – это значение
- 14. Биологически важные реакции α-аминокислот 1.Образование оснований
- 15. Образование оснований Шиффа Образование оснований Шиффа. При взаимодействии
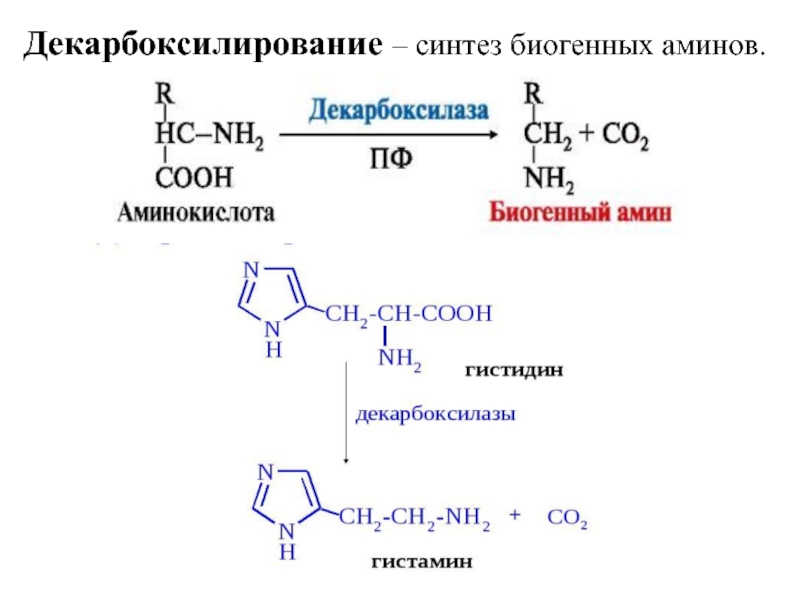
- 16. Декарбоксилирование – синтез биогенных аминов.
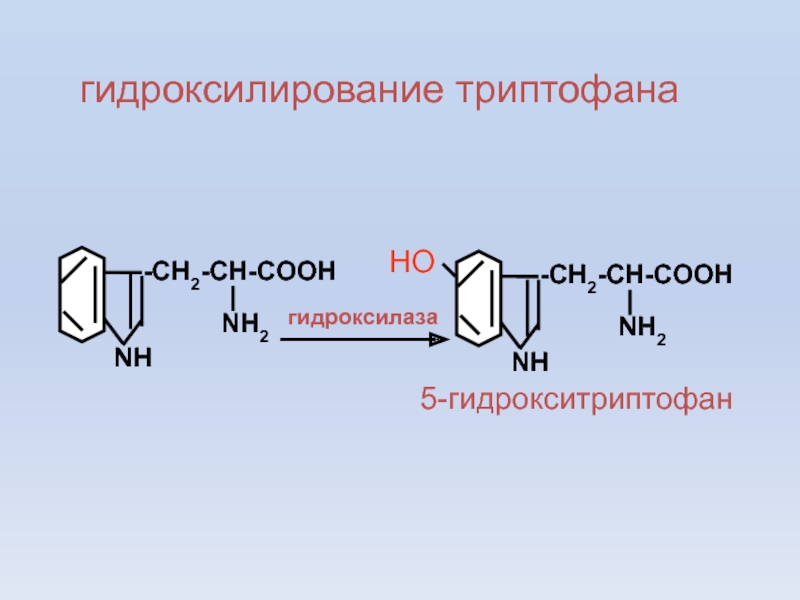
- 17. -CH2-CH-COOH NH2 NH гидроксилирование триптофана -CH2-CH-COOH NH2 NH НО гидроксилаза 5-гидрокситриптофан
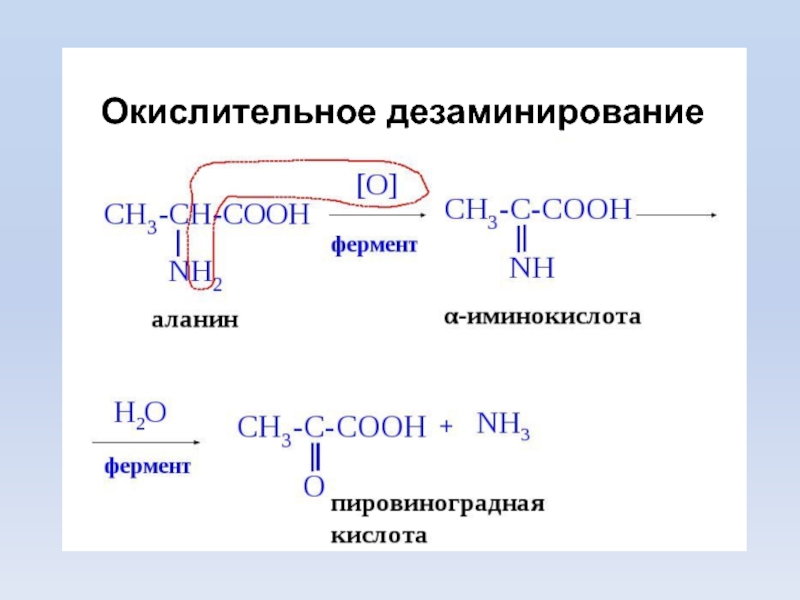
- 18. Дезаминирование – удаления α-АК, которая выделяется
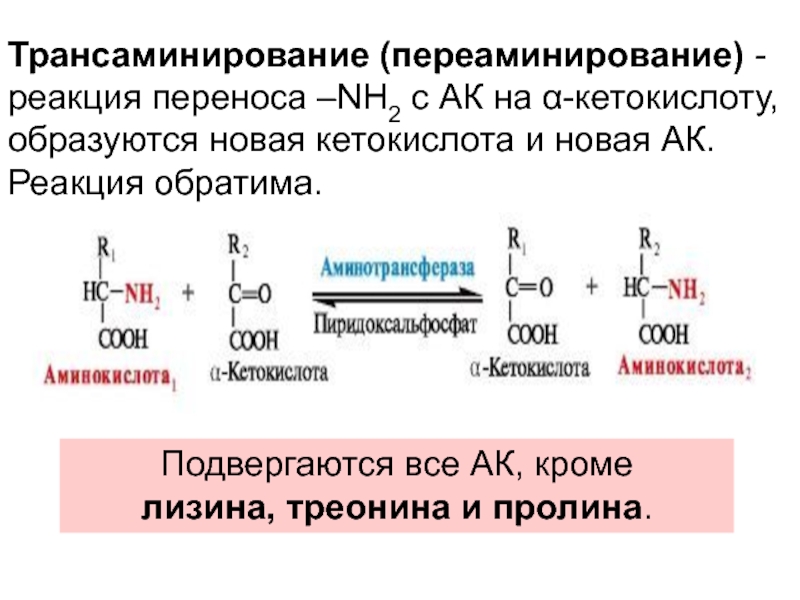
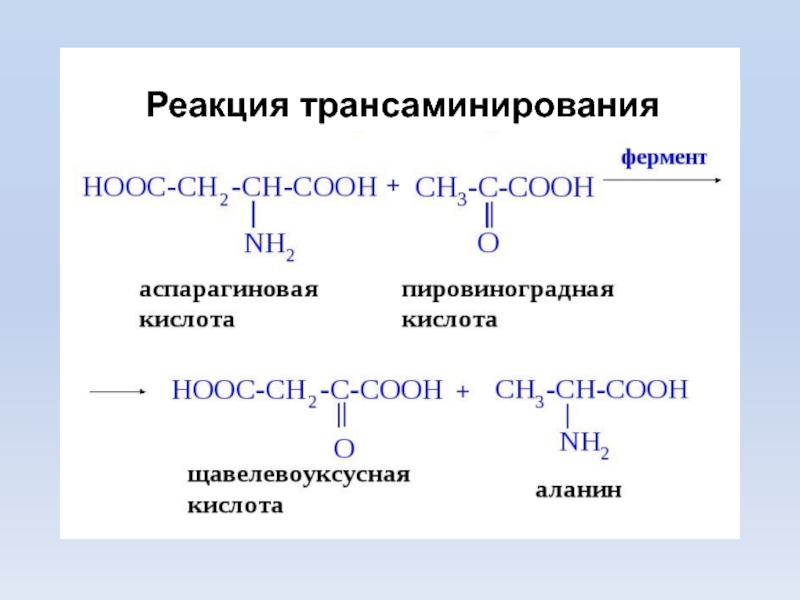
- 21. Трансаминирование (переаминирование) - реакция переноса –NH2 с
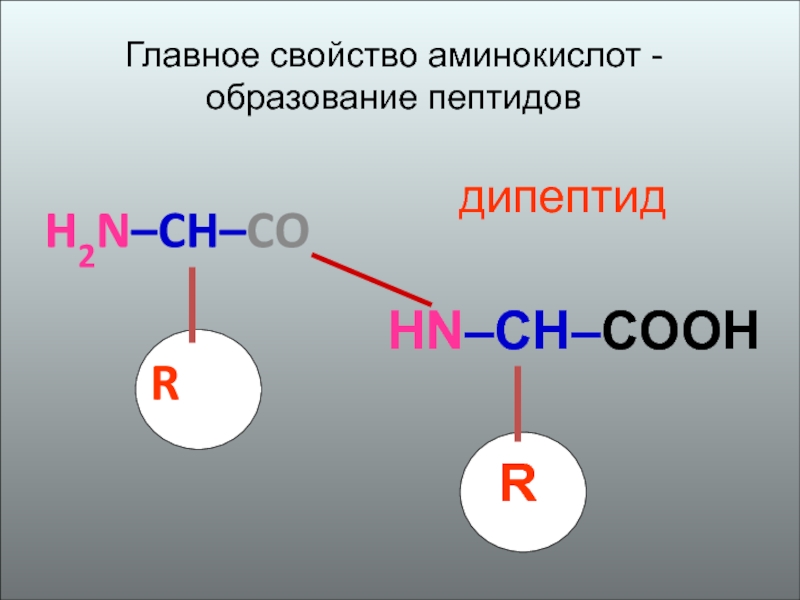
- 23. H2N–CH–CO
- 24. Образование пептидной связи
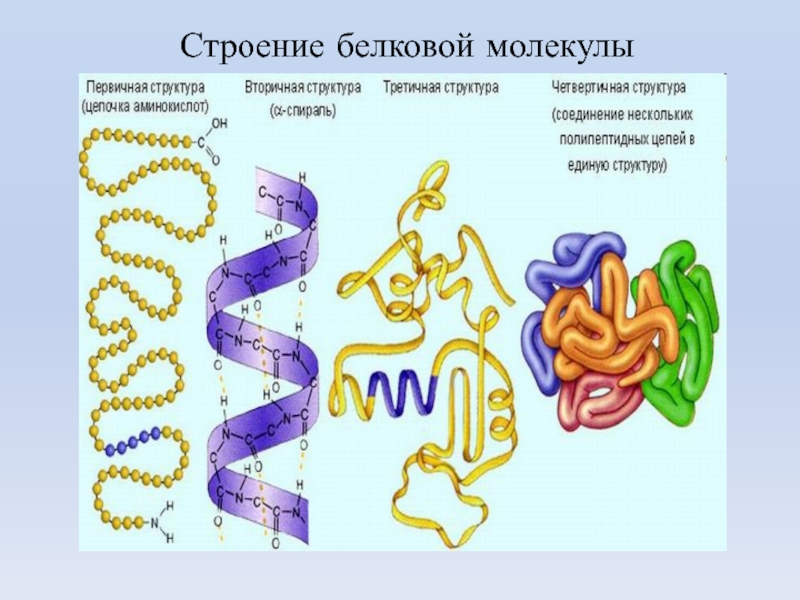
- 25. Строение белковой молекулы
- 28. Первичная структура белка - линейная полипептидная цепь из аминокислот, соединенных между собой пептидными связями. аминокислоты
- 39. БЕЛКИ ПРОТЕИНЫ (простые белки) В
Слайд 3
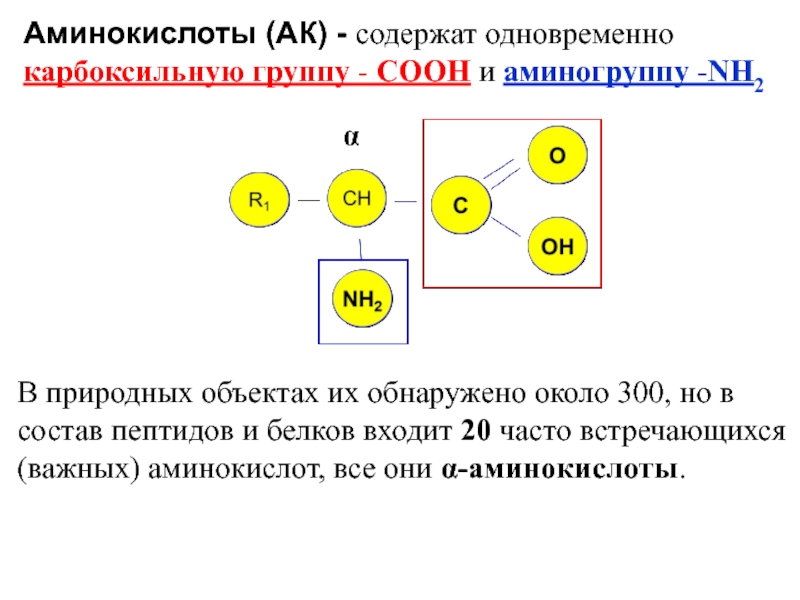
В природных объектах их обнаружено около 300, но в состав пептидов
Аминокислоты (АК) - содержат одновременно карбоксильную группу - СООН и аминогруппу -NН2
Слайд 4Классификация аминокислот
1. Моноаминомонокарбоновые
2. Моноаминодикарбоновые
3. Диаминомонокарбоновые
4. Серусодержащие
5. Имеющие спиртовую группу
6. Циклические
Слайд 8Стереоизомерия.
Все природные a-аминокислоты (кроме глицина)
являются хиральными соединениями. По конфигурации хирального центра в
Природные аминокислоты относятся к L-ряду.
Большинство аминокислот содержат один хиральный центр и имеют два стереоизомера.
Аминокислоты изолейцин, треонин, гидроксипролин, 5-гидроксилизин и цистин содержат два хиральных центра и имеют (кроме цистина) 4 стереоизомера, из которых только один встречается в составе белков.
Слайд 11По кислотно-основным свойствам аминокислоты делят на три группы:
Кислые - с
аспарагиновая и глутаминовая кислоты.
Основные - в боковом радикале имеющие гуанидиновую, имидазольную или аминогруппы:
лизин, аргинин и гистидин.
Все остальные - нейтральные.
Слайд 13Изоэлектрическая точка (ИЭТ) – это значение pH раствора, при
Состояние при котором белок находится в виде диополярного иона (цвиттер-иона), называется изоэлектрическим состоянием (ИЭС).
Слайд 14Биологически важные реакции
α-аминокислот
1.Образование оснований Шиффа
2. Декарбоксилирование
3. Дезаминирование
4. Трансаминирование
5. Образование полипептидов
Слайд 15 Образование оснований Шиффа Образование оснований Шиффа. При взаимодействии аминокислот с альдегидами образуются Образование
По данному механизму осуществляется взаимодействие карбонилсодержащих соединений (стероидных гормонов) с аминогруппами белков рецепторов; образуется связь витамина А (ретиналя) с белковой частью родопсина (светочувствительного пигмента палочек сетчатки глаза).
Слайд 17
-CH2-CH-COOH
NH2
NH
гидроксилирование триптофана
-CH2-CH-COOH
NH2
NH
НО
гидроксилаза
5-гидрокситриптофан
Слайд 18Дезаминирование –
удаления α-АК, которая выделяется в виде NH3 и образования
Дезаминированию не подвергаются
лизин и пролин.
Слайд 21Трансаминирование (переаминирование) - реакция переноса –NH2 с АК на α-кетокислоту, образуются
Подвергаются все АК, кроме
лизина, треонина и пролина.
Слайд 28Первичная структура белка - линейная полипептидная цепь из аминокислот, соединенных между
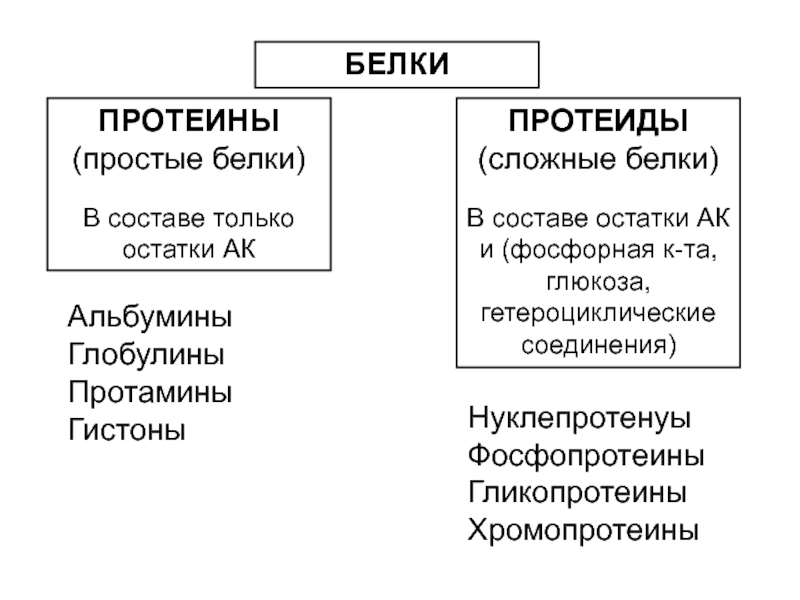
Слайд 39БЕЛКИ
ПРОТЕИНЫ
(простые белки)
В составе только остатки АК
ПРОТЕИДЫ
(сложные белки)
В составе остатки
Альбумины Глобулины
Протамины Гистоны
Нуклепротенyы Фосфопротеины Гликопротеины Хромопротеины