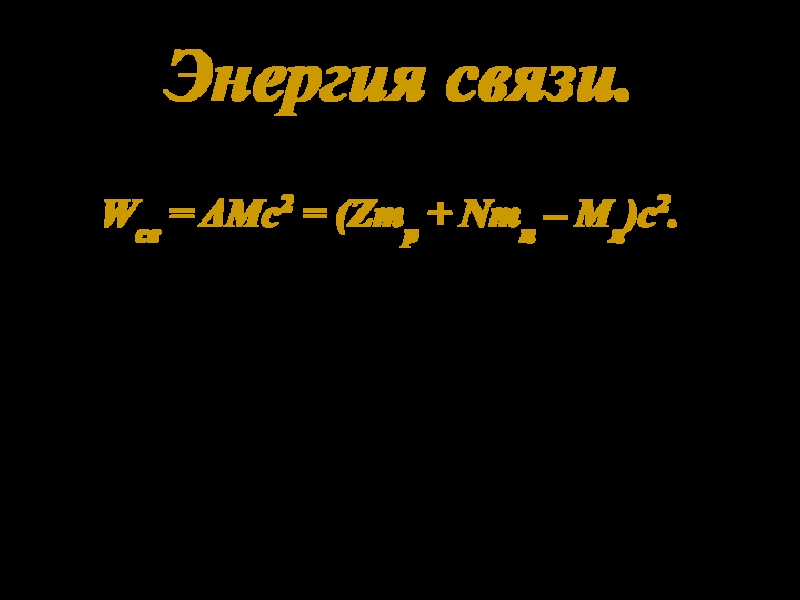- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Строение ядра презентация
Содержание
- 1. Строение ядра
- 2. Условные обзначения X – символ химического элемента,
- 3. Опыт Резерфорда по обнаружению протонов Схема
- 4. Ядерная реакция: - явление
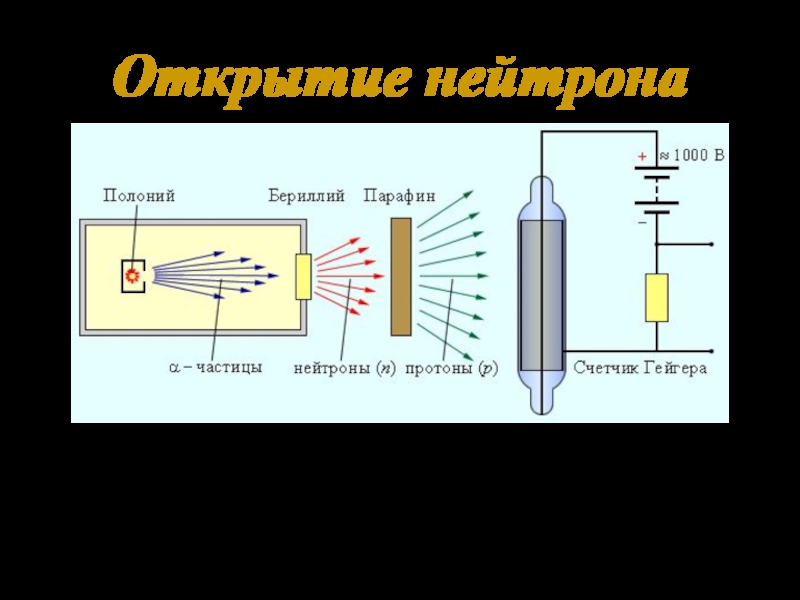
- 5. Открытие нейтрона Схема установки Дж.Чедвика для обнаружения нейтронов
- 6. Ядерная реакция: Нейтрон:
- 7. Протонно-нейтронная модель ядра Д.Д.Иваненко, В.Гейзенберг – 1932
- 8. Изотопы Атомы химического элемента, отличающиеся друг от
- 9. Вопросы Почему в таблице Менделеева относительная атомная
- 10. Опыт: многие атомы являются устойчивыми. Вопрос: Что удерживает протоны и нейтроны в ядре?
- 11. Ядерные силы Игорь Евгеньевич Тамм, Хидеки Юкава
- 12. Ядерные силы Свойства: 1. На расстояниях порядка
- 13. Сравнение фундаментальных взаимодействий
- 14. Энергия связи При плавлении льда на 1
- 15. Энергия связи Для вырывания одного нуклона из
- 16. Дефект массы. Опыт: масса любого ядра
- 17. Энергия связи. Энергия связи: Wсв = ΔMc2 = (Zmp + Nmn – Mя)c2. Удельная энергия связи: Примеры: учебник, стр. 50
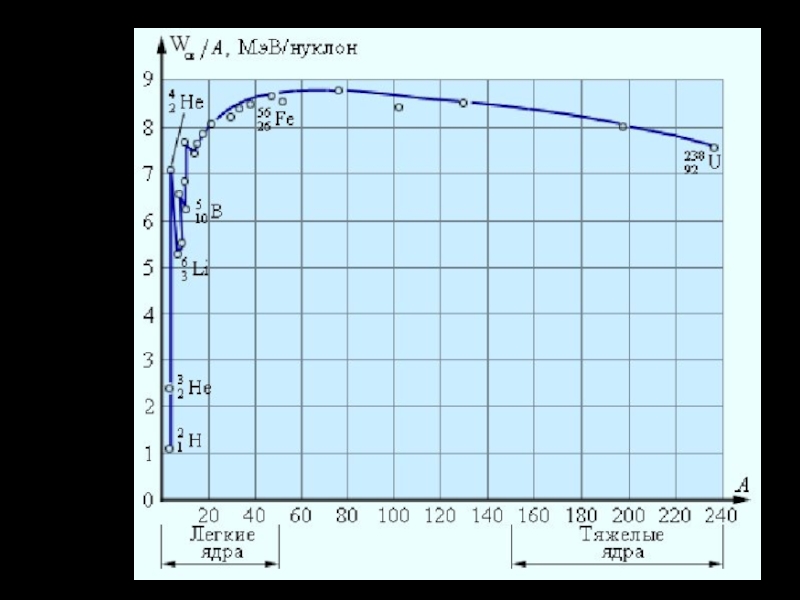
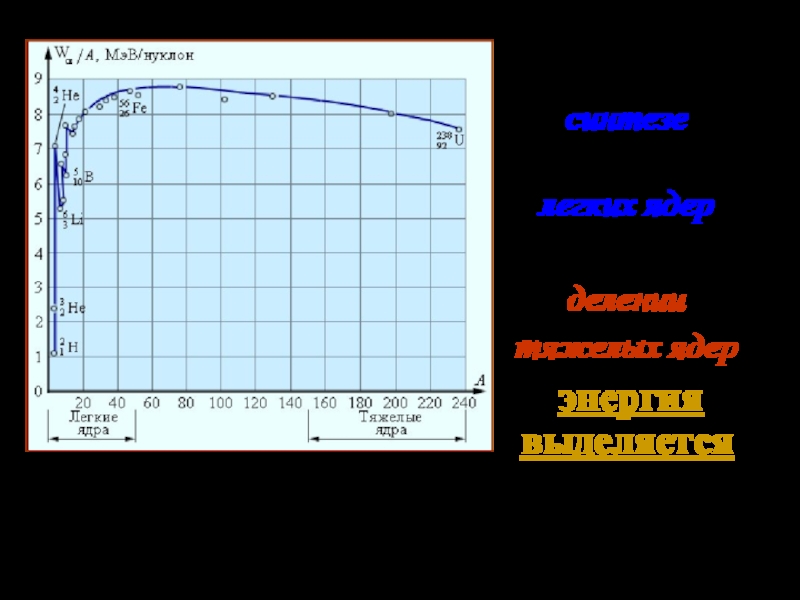
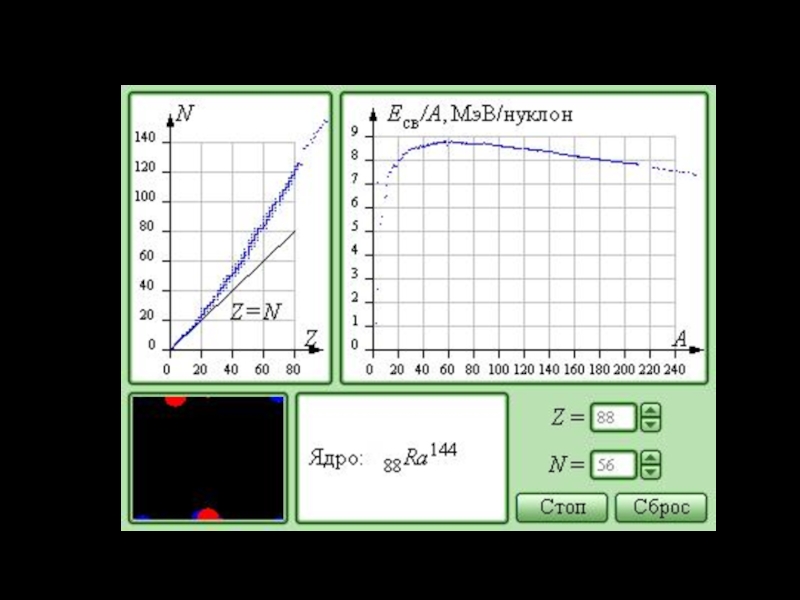
- 18. График зависимости модуля удельной энергии связи от массового числа
- 19. При синтезе (соединении) легких ядер
Слайд 2Условные обзначения
X – символ химического элемента,
Z – атомный номер,
А – массовое
число.
82 Pb
207, 20
свинец
6 C
12, 01
углерод
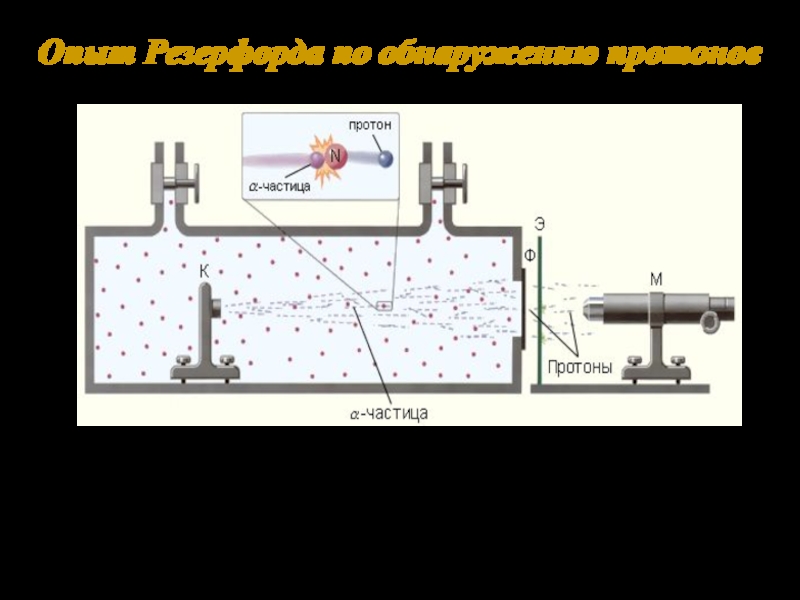
Слайд 3Опыт Резерфорда по обнаружению протонов
Схема опытов в продуктах расщепления ядер:
К – свинцовый контейнер с радиоактивным источником α-частиц, Ф – металлическая фольга, Э – экран, покрытый сульфидом цинка, М – микроскоп.
Слайд 4Ядерная реакция:
- явление расщепления ядер азота при ударах быстрых α-частиц.
Протон:
Протон
Протон, p
mp = 1,67262·10–27 кг
= 1,007276 а. е. м. =1836,1me
qp = 1,60217733·10–19 Кл
= +1е
Участвует в гравитационном, электромагнитном и ядерном (сильном) взаимодействиях.
Слайд 6Ядерная реакция:
Нейтрон:
Нейтрон
Нейтрон, n
mn=1,67493·10-27 кг =
= 1,008665 а. е. м.
=1838,6 me
qn = 0
Участвует в гравитационном и ядерном (сильном) взаимодействиях.
=1838,6 me
qn = 0
Участвует в гравитационном и ядерном (сильном) взаимодействиях.
Слайд 7Протонно-нейтронная модель ядра
Д.Д.Иваненко, В.Гейзенберг – 1932 г.
Z – число протонов в
составе ядра равно порядковому номеру химического элемента в периодической системе Менделеева;
N – число нейтронов в составе ядра атома данного химического элемента;
А = Z + N – массовое число ядра; суммарное количество протонов и нейтронов (называемых общим термином «нуклоны») в ядре.
Ze – заряд ядра (Г. Мозли, 1913).
N – число нейтронов в составе ядра атома данного химического элемента;
А = Z + N – массовое число ядра; суммарное количество протонов и нейтронов (называемых общим термином «нуклоны») в ядре.
Ze – заряд ядра (Г. Мозли, 1913).
Слайд 8Изотопы
Атомы химического элемента, отличающиеся друг от друга числом нейтронов в ядре,
называются изотопами.
У углерода – 2 стабильных изотопов, у кислорода – 3.
Химические элементы в природных условиях обычно представляют собой смесь изотопов.
У углерода – 2 стабильных изотопов, у кислорода – 3.
Химические элементы в природных условиях обычно представляют собой смесь изотопов.
– обычный водород
– дейтерий
– тритий
Учебник, стр.47
Протоны и нейтроны принято называть нуклонами.
Слайд 9Вопросы
Почему в таблице Менделеева относительная атомная масса всех элементов выражена дробным
числом?
Для чего применяются изотопы в науке и технике?
Для чего применяются изотопы в науке и технике?
Слайд 11Ядерные силы
Игорь Евгеньевич Тамм, Хидеки Юкава
Ядерное (сильное) взаимодействие.
R ~ А1/3
ρядра =
2,5.1014 г/см3
Слайд 12Ядерные силы
Свойства:
1. На расстояниях порядка 10-13см сильные взаимодействия соответствуют притяжению, при
уменьшении расстояния – отталкиванию.
2. Независимы от наличия электрического заряда (свойство зарядовой независимости).
3. Взаимодействуют с ограниченным числом нуклонов (свойство насыщения).
4. Короткодействующие: быстро убывают, начиная с r ≈ 2,2.10-15 м.
2. Независимы от наличия электрического заряда (свойство зарядовой независимости).
3. Взаимодействуют с ограниченным числом нуклонов (свойство насыщения).
4. Короткодействующие: быстро убывают, начиная с r ≈ 2,2.10-15 м.
Слайд 14Энергия связи
При плавлении льда на 1 молекулу Wсв=0,06эВ
При парообразовании воды на
1 молекулу Wсв=0,4эВ
Для выбивания одного электрона из Na Wсв=2,3эВ
Для ионизации атома водорода Wсв=13,6эВ
Для выбивания одного электрона из Na Wсв=2,3эВ
Для ионизации атома водорода Wсв=13,6эВ
Слайд 15Энергия связи
Для вырывания одного нуклона из ядра 238U 7,5 МэВ
1 МэВ
= 106 эВ
Энергия связи ядра равна минимальной энергии, которую необходимо затратить для полного расщепления ядра на отдельные частицы (нуклоны).
Энергия связи ядра равна минимальной энергии, которую необходимо затратить для полного расщепления ядра на отдельные частицы (нуклоны).
Слайд 16Дефект массы.
Опыт: масса любого ядра Mя всегда меньше суммы масс
входящих в его состав протонов и нейтронов:
Mя < Zmp + Nmn.
Дефект массы:
ΔM = Zmp + Nmn – Mя
Mя < Zmp + Nmn.
Дефект массы:
ΔM = Zmp + Nmn – Mя