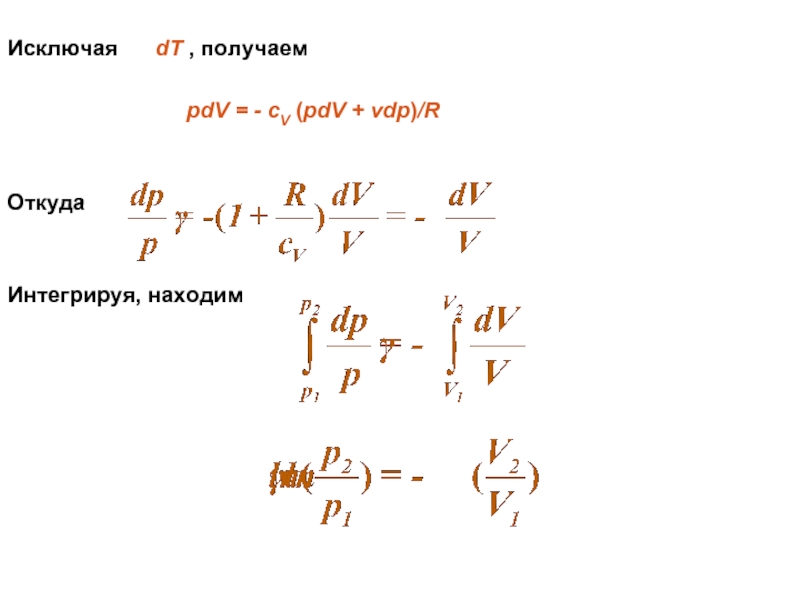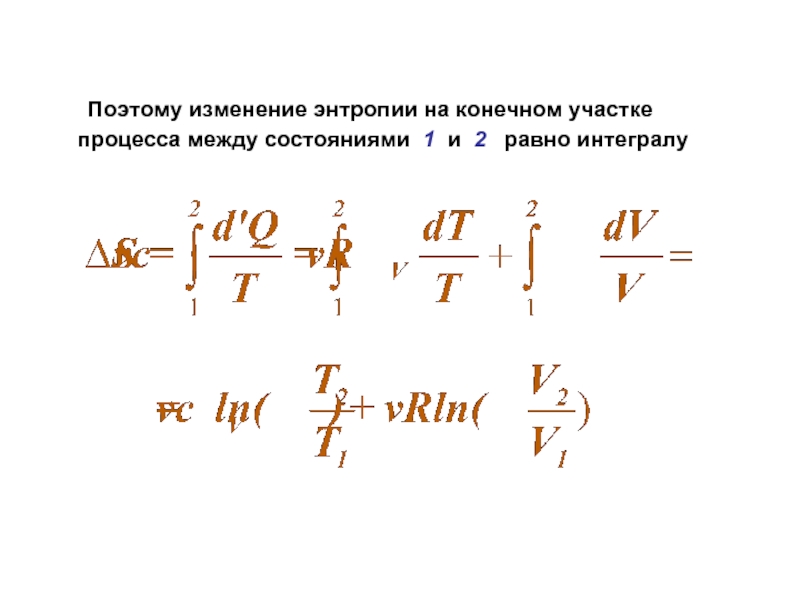из параметров системы остается постоянным.
Изохорический процесс: V = const
Из уравнения состояния идеального
газа для двух температур T1 и T2
следует
откуда
В процессе 1 → 2 происходит нагревание газа
В процессе 1 → 3 происходит охлаждение газа
- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Применение первого начала термодинамики к изопроцессам презентация
Содержание
- 1. Применение первого начала термодинамики к изопроцессам
- 2. Пусть начальное состояние газа отвечает состоянию при
- 3. Изобарический процесс: p = const В
- 4. Перепишем последнее соотношение в виде
- 5. 3) Изотермический процесс: Т = const
- 6. Используя формулу U = νсVT ,
- 7. 4) Адиабатический процесс : d'Q = 0
- 8. Исключая dT , получаем
- 9. Последнюю формулу можно переписать в виде
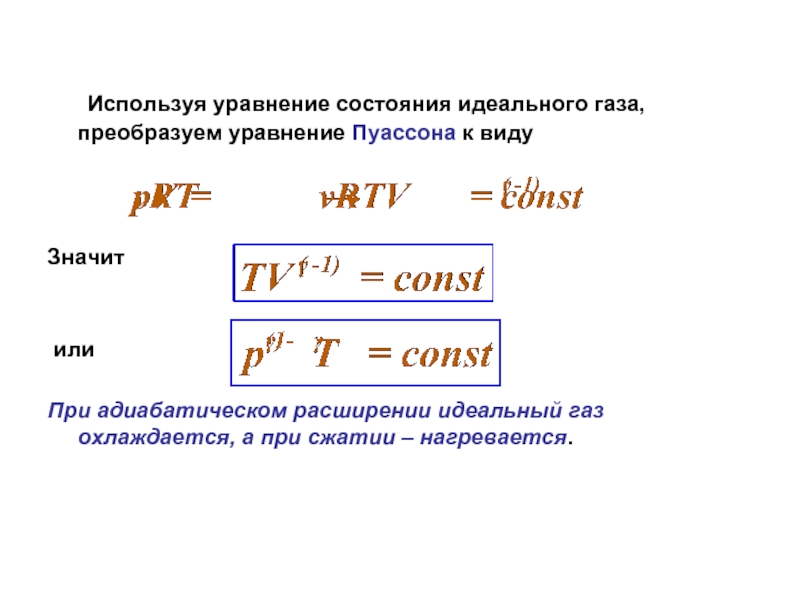
- 10. Используя уравнение состояния идеального газа, преобразуем уравнение
- 11. Найдем работу газа при адиабатическом процессе.
- 12. Тогда Используя
- 13. 11.6 Политропические процессы Политропический процесс –
- 14. С другой стороны, из уравнения состояния идеального
- 15. Обозначим
- 16. Изменение энтропии в неадиабатических процессах идеального газа
- 17. Поэтому изменение энтропии на конечном участке процесса между состояниями 1 и 2 равно интегралу
- 18. Отсюда следует, что 1 ) при
- 19. Изменение энтропии при плавлении и испарении
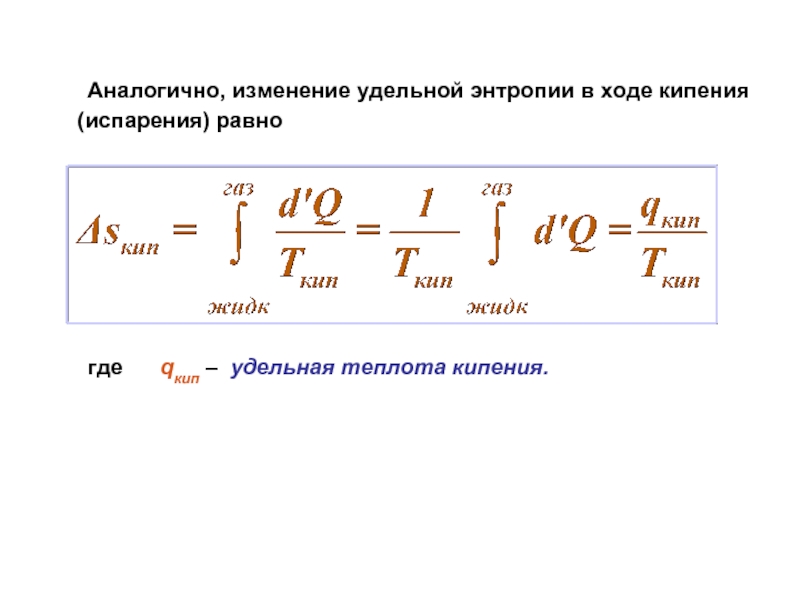
- 20. Аналогично, изменение удельной энтропии в ходе кипения
- 21. В сосуде под поршнем находится масса m=1г
Слайд 1Применение первого начала термодинамики к изопроцессам
Изопроцессом называется процесс, при котором один
Слайд 2 Пусть начальное состояние газа отвечает состоянию при нормальных условиях Т0 =
0°С = 273.15 °К, р0 = 1 атм, тогда для произвольной температуры Т давление в изохорическом процессе находится из уравнения
Давление газа пропорционально его температуре - Закон Шарля
Поскольку d′A = pdV = 0 , то при изохорическом процессе газ не совершает работу над внешними телами.
При этом переданная газу теплота равна d′Q = d′А + dU = dU
То есть при изохорическом процессе вся теплота, передаваемая газу, идет на увеличение его внутренней энергии.
В итоге получаем
Давление газа пропорционально его температуре - Закон Шарля
Поскольку d′A = pdV = 0 , то при изохорическом процессе газ не совершает работу над внешними телами.
При этом переданная газу теплота равна d′Q = d′А + dU = dU
То есть при изохорическом процессе вся теплота, передаваемая газу, идет на увеличение его внутренней энергии.
В итоге получаем
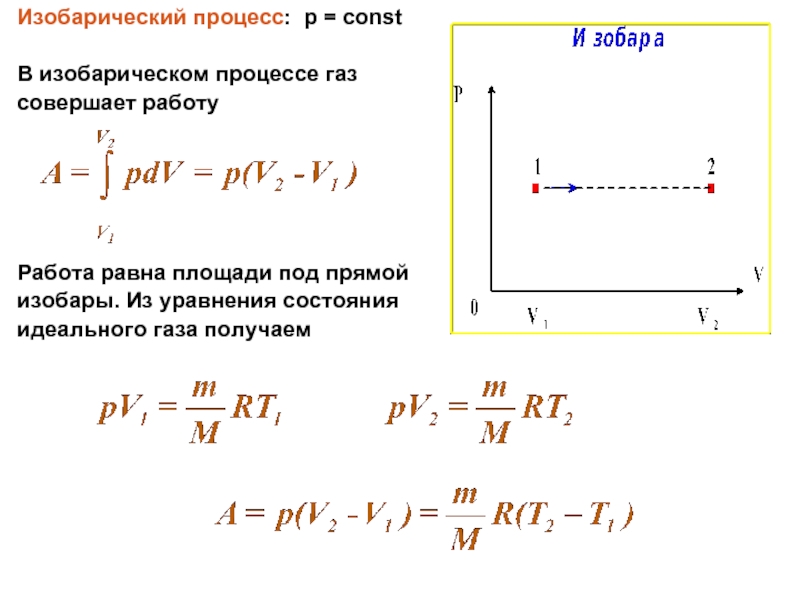
Слайд 3Изобарический процесс: p = const
В изобарическом процессе газ
совершает работу
Работа равна
площади под прямой
изобары. Из уравнения состояния
идеального газа получаем
изобары. Из уравнения состояния
идеального газа получаем
Слайд 4
Перепишем последнее соотношение в виде
Это равенство раскрывает физический смысл газовой
постоянной R - она равна работе 1 моля идеального газа, совершаемой им при нагревании на 1° К в условиях изобарного расширения.
Возьмем в качестве начального состояния - состояние идеального газа при нормальных условиях (Т0, V0), тогда объем газа V при произвольной температуре Т в изобарическом процессе равен
Объем газа при постоянном давлении пропорционален его температуре - закон Гей-Люссака.
Возьмем в качестве начального состояния - состояние идеального газа при нормальных условиях (Т0, V0), тогда объем газа V при произвольной температуре Т в изобарическом процессе равен
Объем газа при постоянном давлении пропорционален его температуре - закон Гей-Люссака.
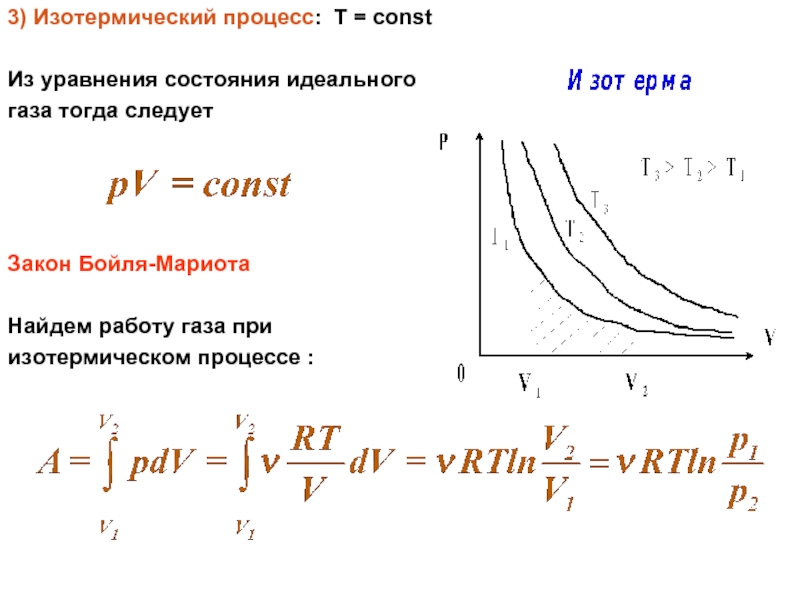
Слайд 53) Изотермический процесс: Т = const
Из уравнения состояния идеального
газа тогда следует
Закон
Бойля-Мариота
Найдем работу газа при
изотермическом процессе :
Найдем работу газа при
изотермическом процессе :
Слайд 6Используя формулу U = νсVT , получаем
dU = νсV dT = 0
Следовательно, внутренняя энергия газа при изотермическом процессе не меняется .
Поэтому d'Q = d'A
Значит, при изотермическом процессе вся теплота, сообщаемая газу, идет на совершение им работы над внешними телами.
Поэтому
Чтобы при расширении газа его температура не понижалась, к газу необходимо подводить количество теплоты, равное его работе над внешними телами.
Следовательно, внутренняя энергия газа при изотермическом процессе не меняется .
Поэтому d'Q = d'A
Значит, при изотермическом процессе вся теплота, сообщаемая газу, идет на совершение им работы над внешними телами.
Поэтому
Чтобы при расширении газа его температура не понижалась, к газу необходимо подводить количество теплоты, равное его работе над внешними телами.
Слайд 7 4) Адиабатический процесс : d'Q = 0
При адиабатическом процессе теплообмен между
газом и окружающей средой отсутствует. Из первого начала термодинамики получаем
d'A = - dU
Поэтому в адиабатическом процессе работа газа над внешними телами совершается за счет убыли его внутренней энергии.
Используя dU = νсVdT ; d'A = рdV
находим рdV = -νсV dT
С другой стороны, из уравнения состояния идеального газа следует
d(рV) = pdV + Vdp = νRdT
d'A = - dU
Поэтому в адиабатическом процессе работа газа над внешними телами совершается за счет убыли его внутренней энергии.
Используя dU = νсVdT ; d'A = рdV
находим рdV = -νсV dT
С другой стороны, из уравнения состояния идеального газа следует
d(рV) = pdV + Vdp = νRdT
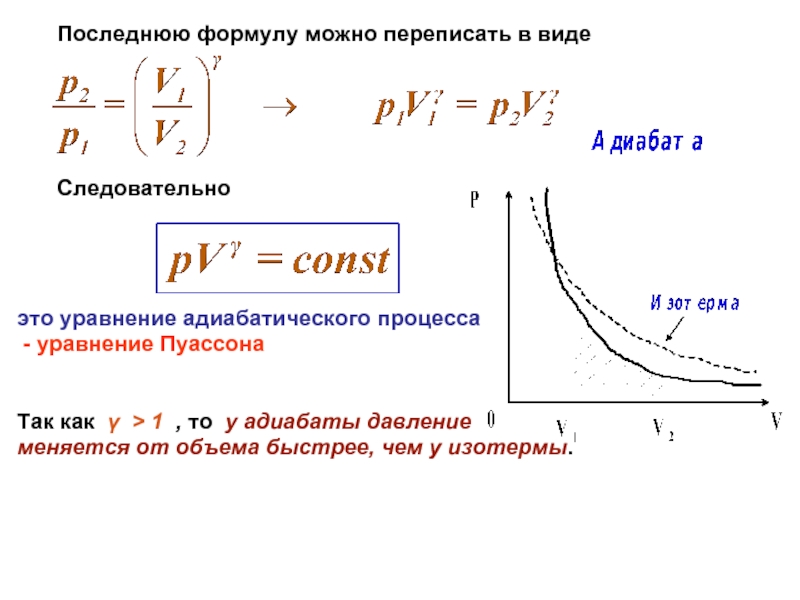
Слайд 9 Последнюю формулу можно переписать в виде
Следовательно
это уравнение адиабатического процесса
- уравнение
Пуассона
Так как γ > 1 , то у адиабаты давление
меняется от объема быстрее, чем у изотермы.
Так как γ > 1 , то у адиабаты давление
меняется от объема быстрее, чем у изотермы.
Слайд 10 Используя уравнение состояния идеального газа, преобразуем уравнение Пуассона к виду
Значит
или
При адиабатическом расширении идеальный газ охлаждается, а при сжатии – нагревается.
При адиабатическом расширении идеальный газ охлаждается, а при сжатии – нагревается.
Слайд 11 Найдем работу газа при адиабатическом процессе.
Из первого начала термодинамики
после
интегрирования, находим
Выразим работу газа через давление и объем. Для этого преобразуем формулу к виду
Выразим работу газа через давление и объем. Для этого преобразуем формулу к виду
Слайд 13 11.6 Политропические процессы
Политропический процесс – это процесс в ходе которого
теплоемкость газа остается постоянной:
cm = const
где cm – молярная теплоемкость.
Найдем уравнение политропы для идеального газа.
Из первого начала термодинамики следует
откуда получаем
cm = const
где cm – молярная теплоемкость.
Найдем уравнение политропы для идеального газа.
Из первого начала термодинамики следует
откуда получаем
Слайд 14С другой стороны, из уравнения состояния идеального газа
Поэтому можно записать
Поскольку
cP = cV + R то
Слайд 15 Обозначим
, получим
Интегрируем
Следовательно
Это - уравнение политропы, n - показатель политропы.
Все предыдущие процессы являются частными случаями политропического процесса:
n = 0 изобара cm = cP
n = 1 изотерма cm = ∞
n = ∞ изохора cm = cV
n = γ адиабата cm = 0
Интегрируем
Следовательно
Это - уравнение политропы, n - показатель политропы.
Все предыдущие процессы являются частными случаями политропического процесса:
n = 0 изобара cm = cP
n = 1 изотерма cm = ∞
n = ∞ изохора cm = cV
n = γ адиабата cm = 0
Слайд 16Изменение энтропии в неадиабатических процессах идеального газа
В неадиабатических процессах между идеальным
газом и внешними телами происходит обмен теплотой. Эти процессы являются обратимыми, поэтому для их описания можно использовать формулу, связывающую теплоту и энтропию. Для малого участка процесса теплота, переданная газу внешними телами, равна
С другой стороны, согласно первому началу термодинамики, эту теплоту можно представить в виде
С другой стороны, согласно первому началу термодинамики, эту теплоту можно представить в виде
Слайд 17 Поэтому изменение энтропии на конечном участке процесса между состояниями 1 и
2 равно интегралу
Слайд 18Отсюда следует, что
1 ) при изотермическом процессе ( Т2 =
Т1 )
2 ) при изохорическом процессе ( V2 = V1 )
3 ) при изобарическом процессе ( p2 = p1 , )
2 ) при изохорическом процессе ( V2 = V1 )
3 ) при изобарическом процессе ( p2 = p1 , )
Слайд 19Изменение энтропии при плавлении и испарении
Если при плавлении или испарении давление
не меняется, то как показывает опыт, в таких процессах у большинства веществ температура тоже остается постоянной. Поэтому изменение удельной энтропии (для единицы массы вещества) в ходе плавления равно
где qпл – удельная теплота плавления.
где qпл – удельная теплота плавления.
Слайд 20 Аналогично, изменение удельной энтропии в ходе кипения (испарения) равно
где qкип – удельная теплота кипения.
Слайд 21В сосуде под поршнем находится масса m=1г азота. Какое количество теплоты
Q надо затратить, чтобы нагреть азот на ΔТ=10К? На сколько при этом поднимется поршень? Масса поршня М=1 кг, площадь его поперечного сечения S=10 см2. Давление под поршнем p=100 кПа.
Согласно первому началу термодинамики
Q=ΔU+A i=5
Тогда Q=10.39 Дж.
При расширении газ совершает работу против сил тяжести и против сил атмосферного давления, тогда
Δh=2.7 см.