- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Предмет физической химии презентация
Содержание
- 1. Предмет физической химии
- 2. Учебная литература Курс физической химии: В
- 3. Методическая и справочная литература Краткий справочник
- 4. Физическая химия (ФХ) – наука о применении
- 5. Основные разделы ФХ
- 6. Химическая термодинамика Основные понятия химической термодинамики
- 7. ХТД изучает взаимные превращения массы и энергии
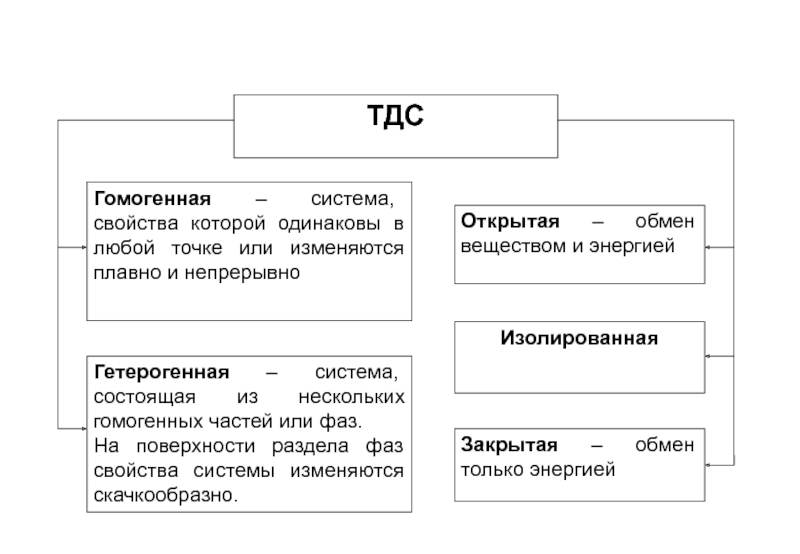
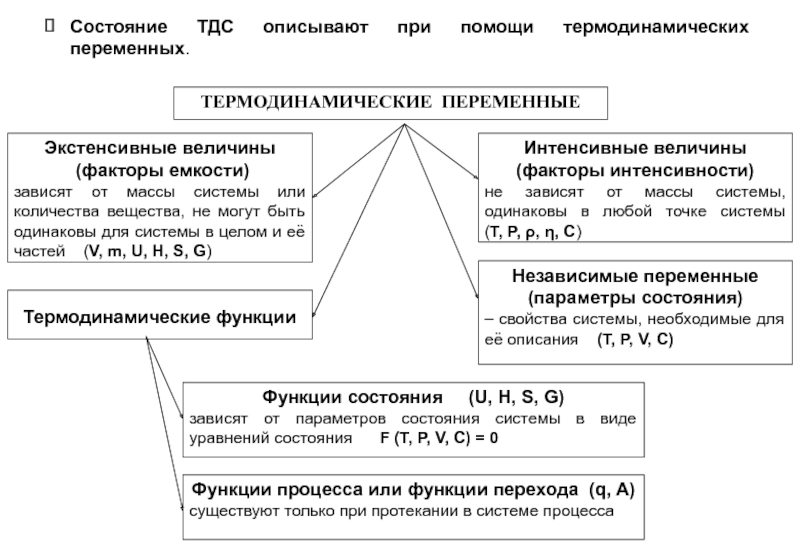
- 9. Состояние ТДС описывают при помощи термодинамических переменных.
- 10. Свойства функций состояния и функций процесса Бесконечно
- 11. Теплота и работа – два способа передачи
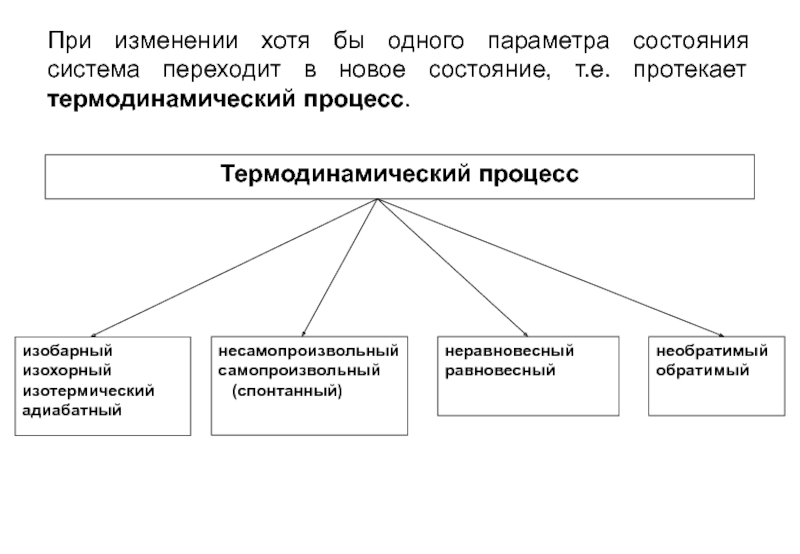
- 12. При изменении хотя бы одного параметра состояния
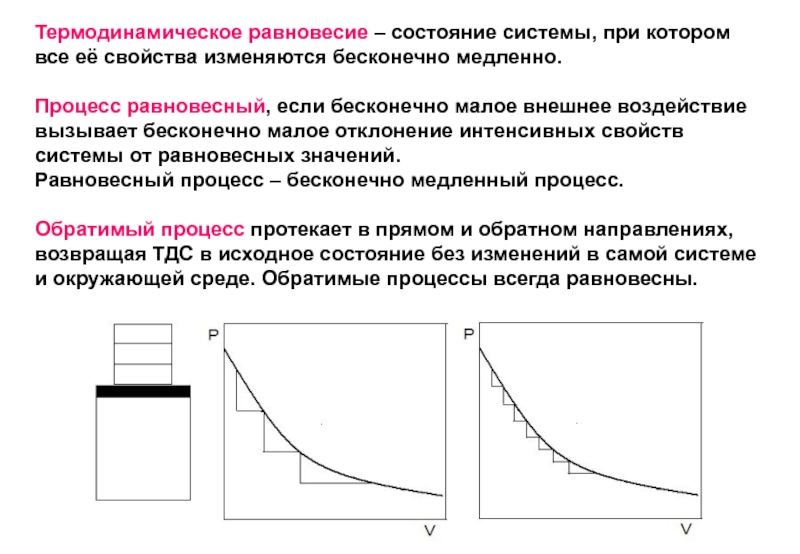
- 13. Термодинамическое равновесие – состояние системы, при котором
- 14. Первое начало термодинамики I
- 15. dU = δq – δA −
- 16. Теплота и работа в различных процессах dU = δQ – PdV (5)
- 17. dU = δQ – PdV (5)
- 18. dU = δQ – PdV (5)
- 19. dU = δQ – PdV (5)
- 20. Работа расширения (сжатия) газа в различных процессах
- 21. Разминка В процессе дыхания при расширении и
- 22. Такую работу выполняет Ваш организм даже когда Вы «отдыхаете»!
Слайд 2Учебная литература
Курс физической химии: В 2-х т. Т 1./ Под ред.
Стромберг А.Б., Семченко Д.П. Физическая химия. М.: Высшая школа. 1999 (1988).
Зимон А. Д. Физическая химия. М. : Агар, 2006.
Горшков В. И. Основы физической химии / В. И. Горшков, И. А. Кузнецов. - М.: БИНОМ. Лаборатория знаний, 2011.
Белик В.В., Киенская К.И. Физическая и коллоидная химия. М. : Академия, 2007.
Слайд 3 Методическая и справочная литература
Краткий справочник физико-химических величин / Под ред.
Калинина Л.А. Лабораторный практикум по физической химии. Методические указания к лабораторным работам. Часть 1. ВятГУ, 2003.
Калинина Л.А. Лабораторный практикум по физической химии. Часть 2. Уч. Пособие, ВятГУ, 2008.
Фоминых Е.Г. Физическая химия: Уч. Пособие, ВятГУ, 2014.
Слайд 4Физическая химия (ФХ) – наука о применении теоретических и экспериментальных методов
Химические превращения сопровождаются или инициируются физическими явлениями.
ФХ рассматривает химические процессы в неразрывной связи с физическими явлениями.
Задача ФХ – установить эти взаимосвязи и дать их количественное описание.
Слайд 5
Основные разделы ФХ
Химическая термодинамика (ХТД)
Практические приложения ХТД:
Термохимия
Учение о химическом равновесии
Учение о фазовых равновесиях
Учение о растворах
Электрохимия
Химическая кинетика и катализ
Квантовая химия и строение вещества
Слайд 7ХТД изучает взаимные превращения массы и энергии (в форме теплоты и
Термодинамический подход к описанию реакций позволяет
установить возможность (невозможность) осуществления химической реакции в заданных условиях;
предсказать направление самопроизвольного протекания процесса;
3) определить предел протекания процесса (условия достижения химического равновесия).
Объект изучения термодинамики – термодинамическая система (ТДС). ХТД рассматривает только макроскопические системы.
ТДС – тело или группа тел, отделенные от окружающего мира реальной или мысленной поверхностью.
Слайд 10Свойства функций состояния и функций процесса
Бесконечно малое изменение функции состояния есть
Изменение функции состояния не зависит от пути протекания процесса:
В циклическом процессе функция состояния не изменяется:
Бесконечно малое изменение функции процесса есть приращение δq, δA.
Изменение функции процесса зависит от пути его протекания:
В циклическом процессе функция процесса изменяется:
Слайд 11Теплота и работа – два способа передачи энергии.
Теплота – энергия передается
q > 0 – теплота поглощается системой – эндотермический процесс
q < 0 – теплота выделяется из системы – экзотермический процесс
Работа (A или W)– энергия передается за счет направленного движения макрообъектов.
А < 0 – работа совершается внешними силами над системой
А > 0 – работу совершает сама система
А = АМЕХ + АПОЛ
АМЕХ = PΔV – механическая работа, т. е. работа расширения или сжатия газа
АПОЛ – полезная работа (химическая, электрическая, магнитная, сил поверхностного натяжения и др.)
Слайд 12При изменении хотя бы одного параметра состояния система переходит в новое
Слайд 13Термодинамическое равновесие – состояние системы, при котором все её свойства изменяются
Слайд 14Первое начало термодинамики
I закон термодинамики - закон сохранения
Вечный двигатель первого рода не существует.
В изолированной системе различные формы энергии переходят друг в друга в строго эквивалентных количествах, т. е. внутренняя энергия изолированной системы постоянна.
Внутренняя энергия – суммарная энергия ТДС, включающая кинетическую энергию движения всех видов частиц и потенциальную энергию их взаимодействия.
Внутренняя энергия закрытой системы есть разность теплоты, подводимой к системе, и работы, которую совершает система U = q – A .
Слайд 15
dU = δq – δA − дифференциальная форма (1)
∆U = q – A − интегральная форма (2)
∆U = q – Aпол− Амех = q – Aпол− PΔV = Q − PΔV (3)
Q = q – Aпол − тепловой эффект реакции по Кирееву (4)
Aпол = 0 → Q = q
dU = δQ – PdV − дифференциальная форма (5)
∆U = Q – PΔV − интегральная форма (6)
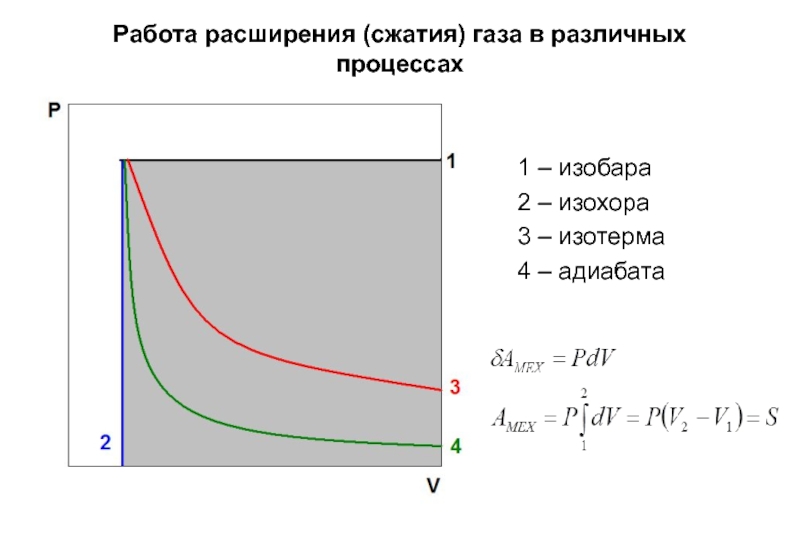
Слайд 20Работа расширения (сжатия) газа в различных процессах
1 – изобара
2 – изохора
3
4 – адиабата
Слайд 21Разминка
В процессе дыхания при расширении и сжатии легких человек затрачивает энергию.
Оцените величину работы, совершаемой при дыхании человека в течение 24 часов.
Чтобы почувствовать, насколько велика эта работа, представьте, что такая же работа совершается при подъеме груза массой m (кг) на высоту 30-этажного небоскреба, примерно 100 метров. Рассчитайте массу груза.