900igr.net
- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Открытие нейтрона и протона презентация
Содержание
- 1. Открытие нейтрона и протона
- 2. Открытие протона После создания ядерной модели атома
- 3. Первую частицу, входящую в состав атомных ядер,
- 4. Вывод: α-частицы из
- 5. Продолжая опыты с бором, фтором,
- 6. В 1930 г. немецкие ученые В. Боте
- 7. В том же 1932 году, английский
- 8. Строение атомного ядра Советский физик Д.Д.Иваненко и
- 9. Изотопы Изучения атомных ядер показали, что большинство
- 10.
- 11. Атомные массы химических элементов в таблице
- 12. Применение изотопов Как способ контроля износа поршневых
- 13. Одним из наиболее выдающихся исследований явилось исследование
- 14. Облучение семян растений приводит к заметному увеличению
- 15. В археологии: Для определения возраста древних предметов органического происхождения.
- 16. Метод «меченых атомов»: Основан на том, что
Слайд 1Открытие нейтрона и протона
Автор: Фомичева С.Е., учитель физики МБОУ «Средняя школа
Слайд 2Открытие протона
После создания ядерной модели атома вопрос о составе атомного ядра
Одна из основных характеристик атомного ядра — его электрический заряд. Точные измерения электрического заряда атомных ядер были выполнены в 1913 году Г. Мозли.
Генри Гвин Джефрис Мозли
Электрический заряд ядра атома q равен произведению элементарного электрического заряда е на порядковый номер Z химического элемента в таблице Д.И. Менделеева: q = Z·e.
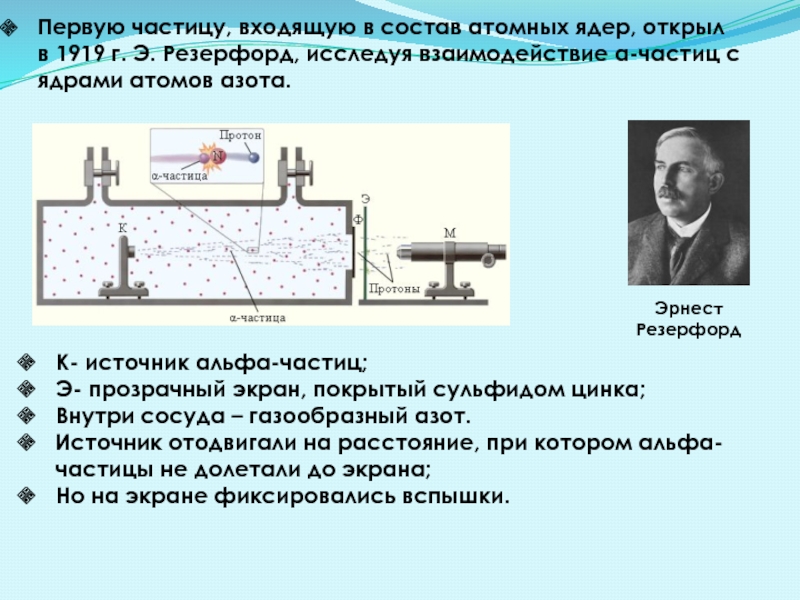
Слайд 3Первую частицу, входящую в состав атомных ядер, открыл в 1919 г.
Эрнест Резерфорд
К- источник альфа-частиц;
Э- прозрачный экран, покрытый сульфидом цинка;
Внутри сосуда – газообразный азот.
Источник отодвигали на расстояние, при котором альфа-частицы не долетали до экрана;
Но на экране фиксировались вспышки.
Слайд 4
Вывод:
α-частицы из ядер азота выбивали какие-то другие заряженные частицы.
Исследования действия
q=+1e, m=1а.е.м
Слайд 5
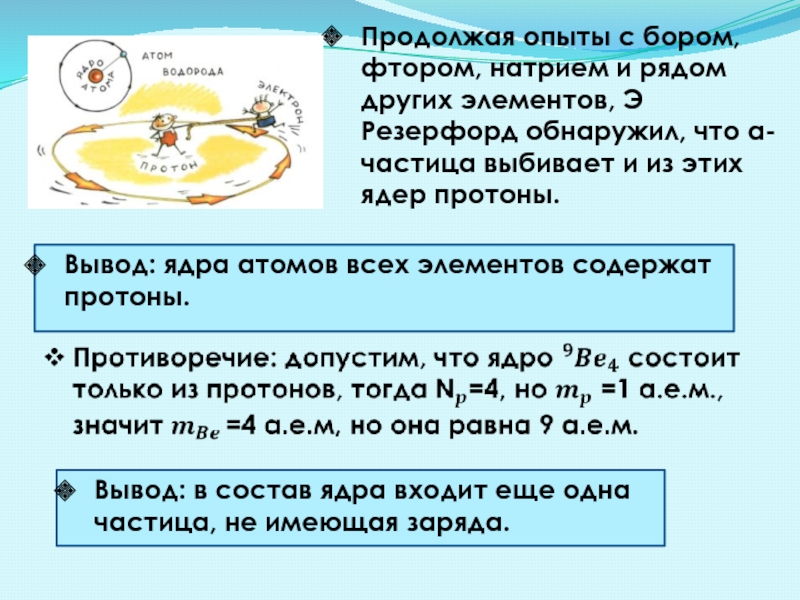
Продолжая опыты с бором, фтором, натрием и рядом других элементов, Э
Вывод: ядра атомов всех элементов содержат протоны.
Вывод: в состав ядра входит еще одна частица, не имеющая заряда.
Слайд 6В 1930 г. немецкие ученые В. Боте и Г. Беккер обнаружили,
Доказательство существования нейтрона.
В 1932 г. французские ученые Ф. и И. Жолио-Кюри выяснили, что эти лучи почти не ионизуют воздух, через который проходят. Но если на их пути поместить парафин, то ионизирующая способность лучей резко возрастает. Они предположили, что это излучение выбивает из парафиновой пластины протоны.
Слайд 7
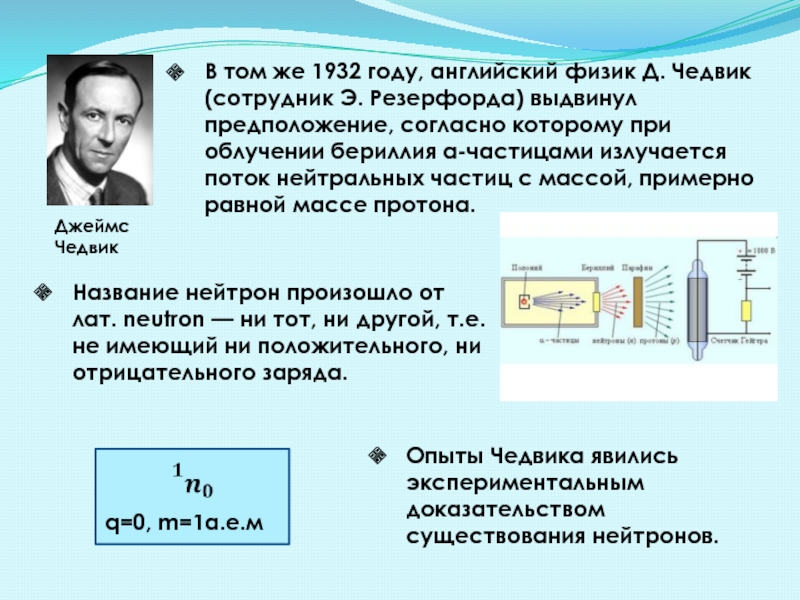
В том же 1932 году, английский физик Д. Чедвик (сотрудник Э.
Название нейтрон произошло от лат. neutron — ни тот, ни другой, т.е. не имеющий ни положительного, ни отрицательного заряда.
Джеймс Чедвик
Опыты Чедвика явились экспериментальным доказательством существования нейтронов.
q=0, m=1а.е.м
Слайд 8Строение атомного ядра
Советский физик Д.Д.Иваненко и В.Гейзенберг предложили протонно-нейтронную модель ядра
Согласно
Протон и нейтрон – два зарядовых состояния ядерной частицы, называемой нуклоном.
Число протонов в ядре равняется числу электронов в атоме;
Слайд 9Изотопы
Изучения атомных ядер показали, что большинство химических элементов представляют собой смесь
Атомы с одинаковыми зарядами ядра, но с различными массами назвали изотопами элемента.
Название изотоп произошло от греч. isos — одинаковый, topos — место, т.е. это химические вещества, занимающие одно и то же место в таблице Д.И. Менделеева.
Слайд 11
Атомные массы химических элементов в таблице Менделеева выражены дробными числами из-за
Например: в среднем на 100 атомов хлора приходится 75 атомов с массой 35 а.е.м. и 25 атомов с массой 37 а.е.м, поэтому средняя масса:
Слайд 12Применение изотопов
Как способ контроля износа поршневых колец в двигателях внутреннего сгорания.
Мощное гамма-излучение радиоактивных препаратов используют для исследования внутренней структуры металлических отливок с целью обнаружения в них дефектов.
В промышленности:
Слайд 13Одним из наиболее выдающихся исследований явилось исследование обмена веществ в организмах.
Радиоактивные изотопы применяются в медицине как для постановки диагноза, так и для терапевтических целей. Радиоактивный натрий, вводимый в небольших количествах в кровь, используется для исследования кровообращения, йод интенсивно отлагается в щитовидной железе, особенно при базедовой болезни.
Интенсивное гамма-излучение кобальта используется при лечении раковых заболеваний (кобальтовая пушка).
В медицине:
Слайд 14Облучение семян растений приводит к заметному увеличению урожайности.
Вызывают мутации у
Получены микроорганизмы, применяемые в производстве антибиотиков.
Для борьбы с вредными насекомыми и для консервации пищевых продуктов.
Для выясния, какое из фосфорных удобрений лучше усваивается растением.
В сельском хозяйстве: