- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Основы термодинамики презентация
Содержание
- 1. Основы термодинамики
- 2. На первый план выступают тепловые процессы и энергетические преобразования
- 3. ИЗ ИСТОРИИ РАЗВИТИЯ ТЕРМОДИНАМИКИ
- 4. ИЗ ИСТОРИИ РАЗВИТИЯ ТЕРМОДИНАМИКИ
- 5. ТЕРМОДИНАМИЧЕСКАЯ СИСТЕМА Любая совокупность макроскопических
- 6. ЧТО ИЗУЧАЕТ ТЕРМОДИНАМИКА? √ Возникла как
- 7. ГРАНИЦЫ ПРИМЕНИМОСТИ ТЕРМОДИНАМИКИ Неприменима к системе из
- 8. ТЕРМОДИНАМИЧЕСКИЕ ПАРАМЕТРЫ Совокупность физических величин, характеризующих свойства термодинамической системы.
- 9. Внутренняя энергия Определение: Внутренняя энергия
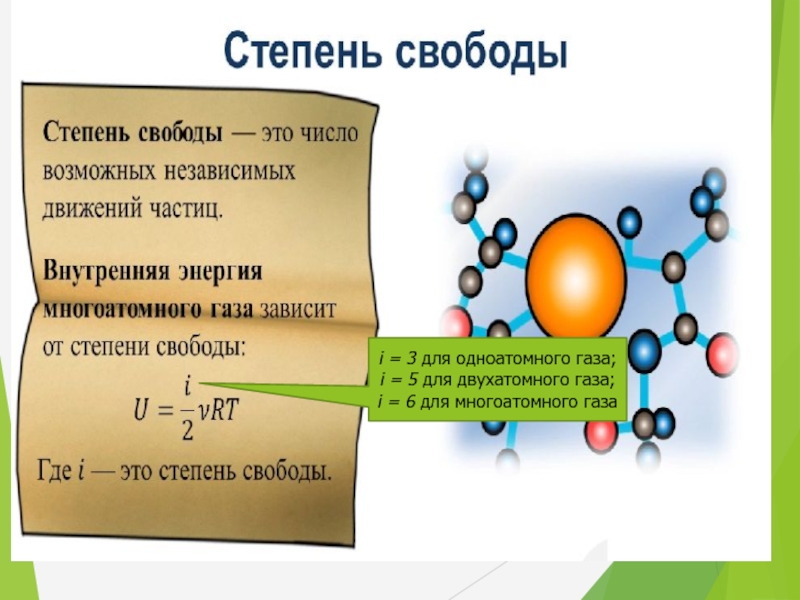
- 12. i = 3 для одноатомного газа;
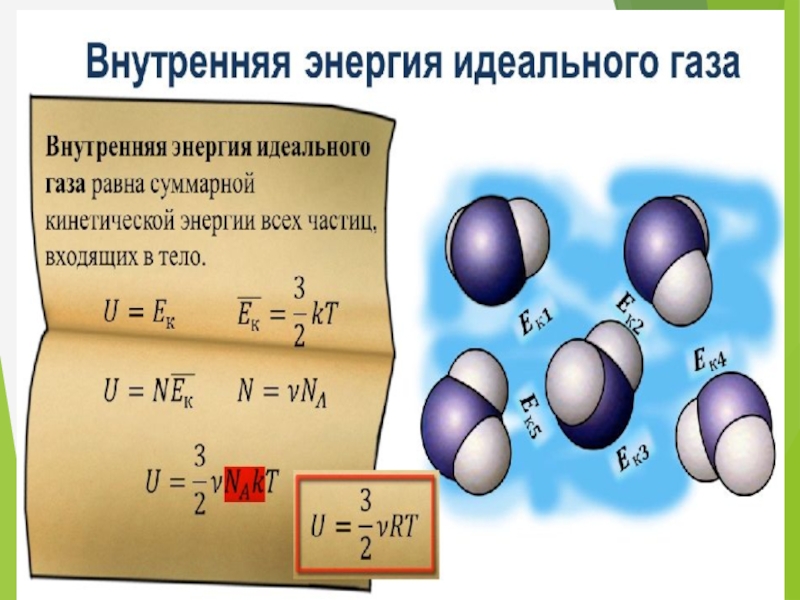
- 13. Внутренняя энергия идеального одноатомного газа
- 14. Внутренняя энергия идеального двухатомного газа
- 15. Так как - уравнение Менделеева–Клапейрона,
- 16. В общем виде: где i – число
- 18. Изменение внутренней энергии тела ΔU Совершение работы
- 19. Работа в термодинамике Работа газа:
- 28. I ЗАКОН ТЕРМОДИНАМИКИ Изменение внутренней энергии ΔU
- 29. Первый закон термодинамики Изменение внутренней энергии системы
- 30. ТЕРМОДИНАМИКА ИЗОПРОЦЕССОВ. Процессы, происходящие при постоянном значении
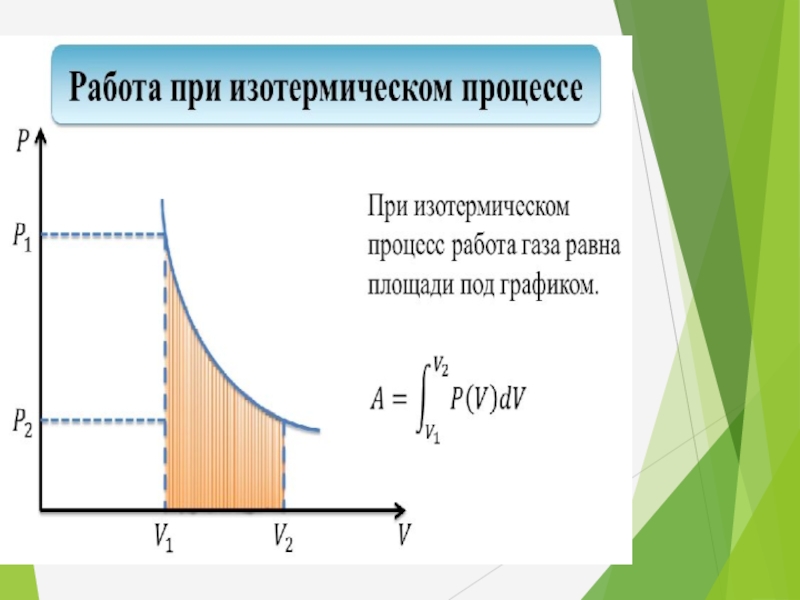
- 31. ИЗОТЕРМИЧЕСКИЙ ПРОЦЕСС Процесс, происходящий при постоянной температуре.
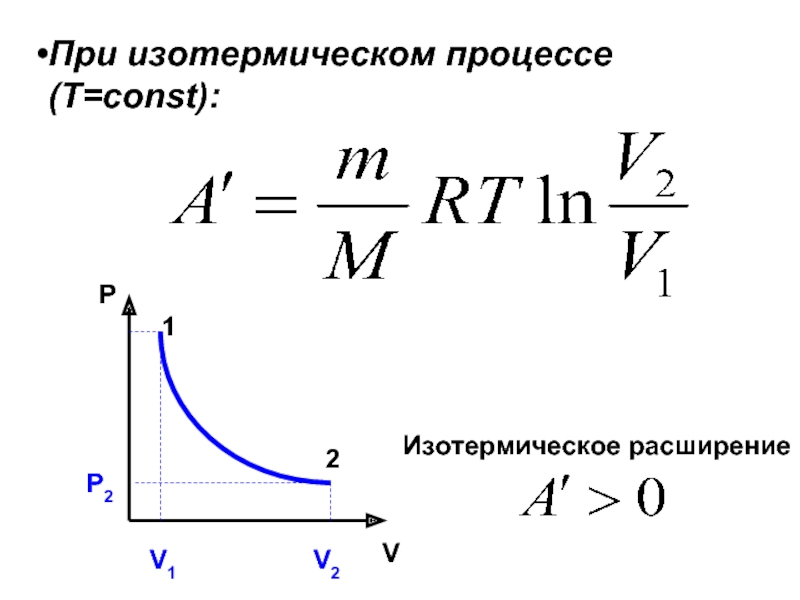
- 32. При изотермическом процессе (Т=const): P V
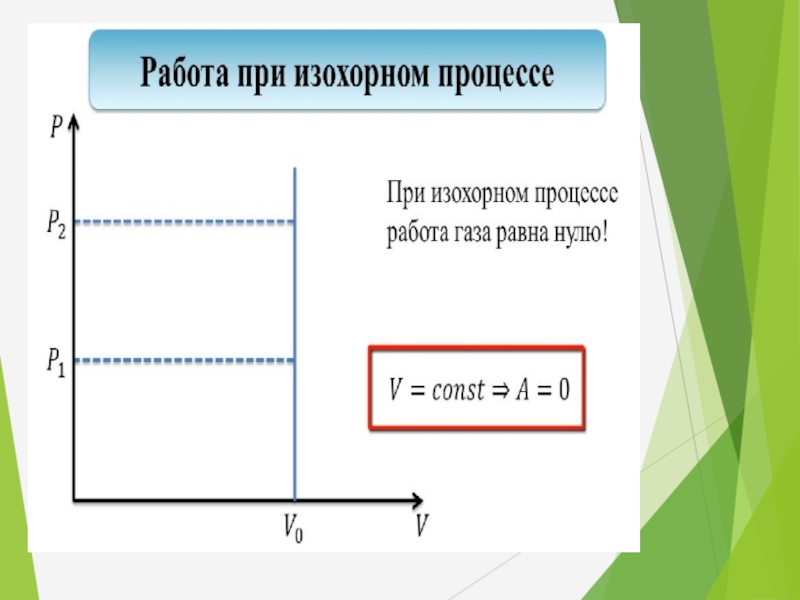
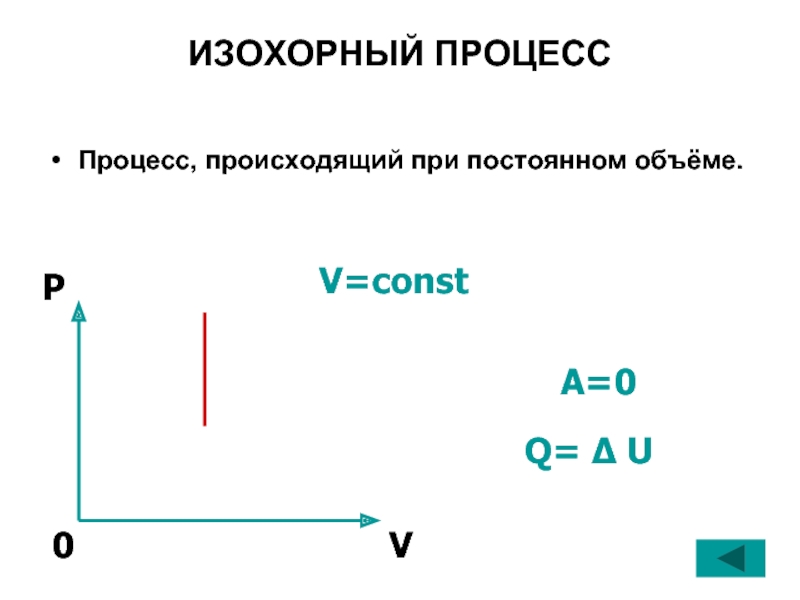
- 33. ИЗОХОРНЫЙ ПРОЦЕСС Процесс, происходящий при постоянном объёме. V=const Q= Δ U A=0
- 34. Работа газа при изопроцессах При изохорном процессе
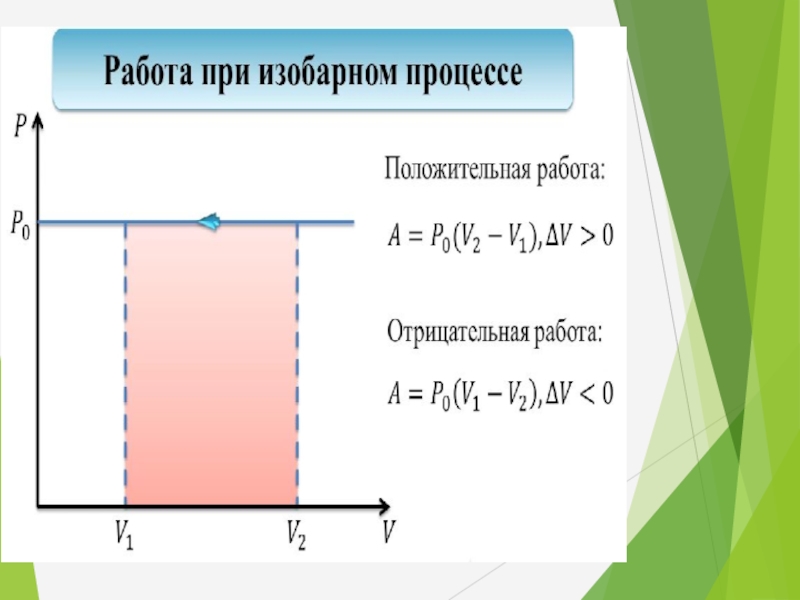
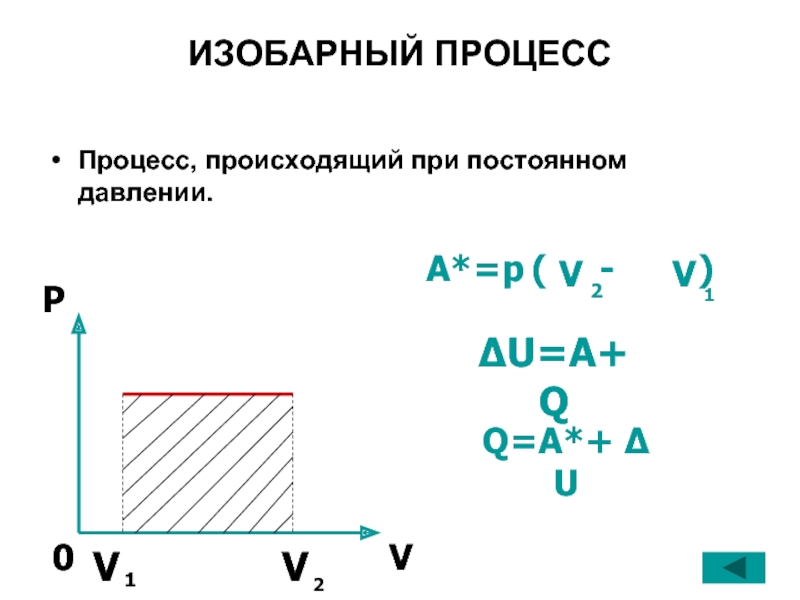
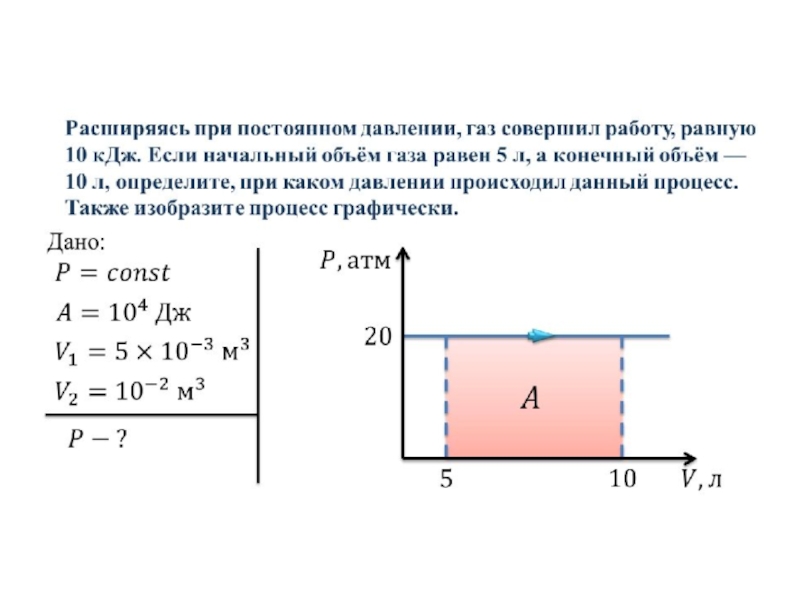
- 35. ИЗОБАРНЫЙ ПРОЦЕСС Процесс, происходящий при постоянном
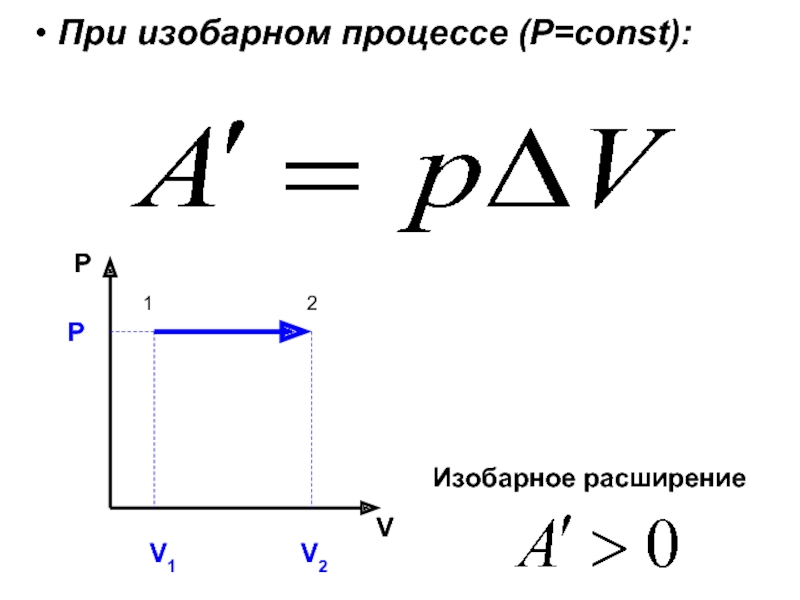
- 36. При изобарном процессе (Р=const):
- 37. АДИАБАТНЫЙ ПРОЦЕСС Процесс, происходящий без теплообмена с
- 38. Геометрическое истолкование работы: Работа, совершаемая газом в
- 39. Количество теплоты – часть внутренней энергии, которую тело получает или теряет при теплопередаче
- 40. Применение первого закона термодинамики к различным процессам
- 41. II ЗАКОН ТЕРМОДИНАМИКИ Тепловые процессы необратимы.
- 42. Тепловые
- 43. ТЕПЛОВОЙ ДВИГАТЕЛЬ – ГЛАВНЫЙ ДВИГАТЕЛЬ СОВРЕМЕННОЙ
- 44. Принцип действия тепловых двигателей Т1 – температура
- 45. Коэффициент полезного действия (КПД) теплового двигателя –
- 46. где работа, совершаемая двигателем тогда
- 47. Максимальное значение КПД тепловых двигателей (цикл Карно):
- 48. Отрицательные последствия использования тепловых двигателей: Потепление
- 49. ВЕЧНЫЙ ДВИГАТЕЛЬ Первого рода Второго рода
- 50. ТЕРМОДИНАМИКА И ПРИРОДА В окружающей нас природе
- 51. Тест по ТЕРМОДИНАМИКЕ На сколько отделов делится
- 52. Тест по ТЕРМОДИНАМИКЕ (продолжение) При каком изопроцессе
- 56. Литература Мякишев Г.Я., Буховцев Б.Б.,Сотский Н.Н. Физика
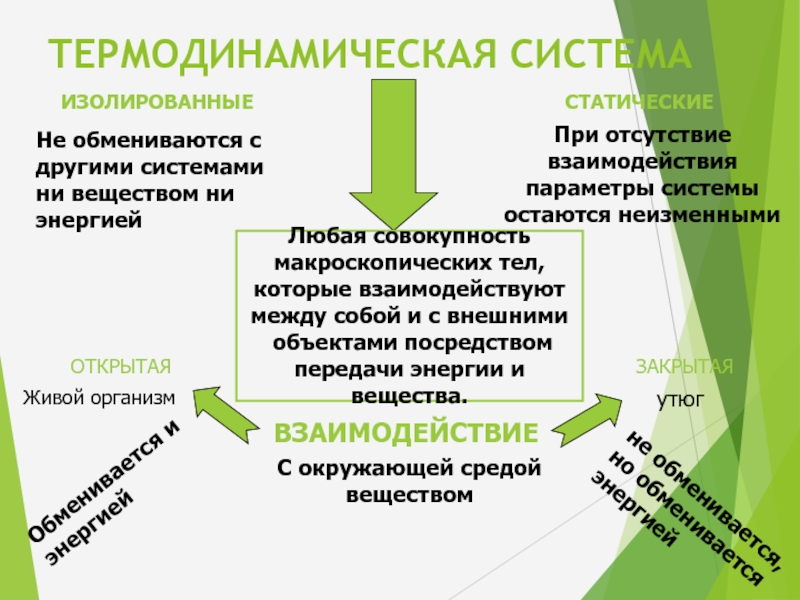
Слайд 5ТЕРМОДИНАМИЧЕСКАЯ СИСТЕМА
Любая совокупность
макроскопических тел,
которые взаимодействуют
между собой и с
ИЗОЛИРОВАННЫЕ
СТАТИЧЕСКИЕ
Не обмениваются с другими системами ни веществом ни энергией
При отсутствие взаимодействия параметры системы остаются неизменными
ВЗАИМОДЕЙСТВИЕ
ОТКРЫТАЯ
ЗАКРЫТАЯ
С окружающей средой веществом
не обменивается, но обменивается энергией
Обменивается и энергией
Живой организм
утюг
Слайд 6ЧТО ИЗУЧАЕТ ТЕРМОДИНАМИКА?
√ Возникла как наука тепловых процессов, рассматриваемых с
√ Не рассматривает явления с точки зрения движения молекул.
√ Изучает наиболее общие свойства макроскопических систем, находящихся в равновесном состоянии, и процессы их перехода из одного состояния в другое.
√ Термодинамический метод широко используется в других разделах физики, химии, биологии.
√ Как и любая физическая теория или раздел физики, имеет свои границы применимости.
Слайд 7ГРАНИЦЫ ПРИМЕНИМОСТИ ТЕРМОДИНАМИКИ
Неприменима к системе из нескольких молекул.
Не может быть применима
Слайд 8ТЕРМОДИНАМИЧЕСКИЕ ПАРАМЕТРЫ
Совокупность физических величин, характеризующих свойства термодинамической системы.
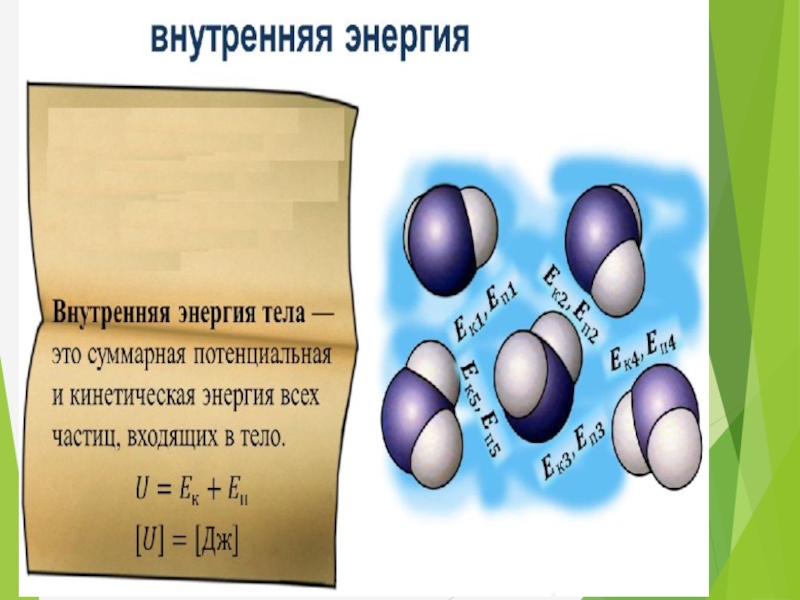
Слайд 9Внутренняя энергия
Определение:
Внутренняя энергия тела – это сумма кинетической энергии хаотического теплового
Обозначение:
U
Единицы измерения:
[Дж]
Слайд 15
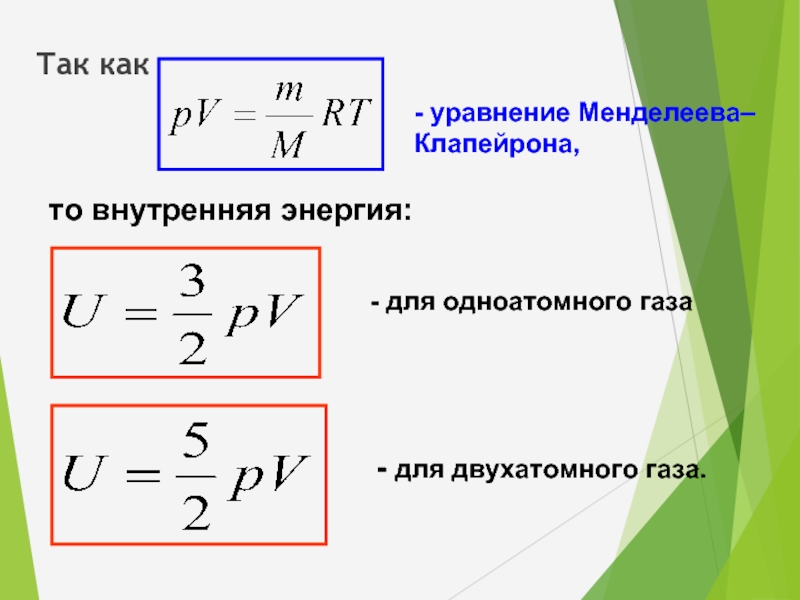
Так как
- уравнение Менделеева–Клапейрона,
то внутренняя энергия:
- для одноатомного газа
- для
Слайд 16В общем виде:
где i – число степеней свободы молекул газа (i
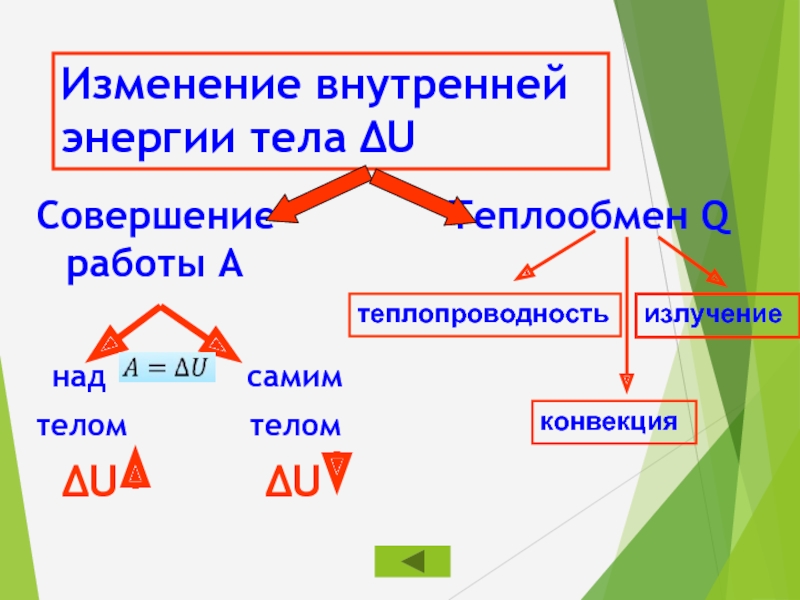
Слайд 18Изменение внутренней энергии тела ΔU
Совершение работы А
над
телом телом
ΔU ΔU
Теплообмен Q
теплопроводность
конвекция
излучение
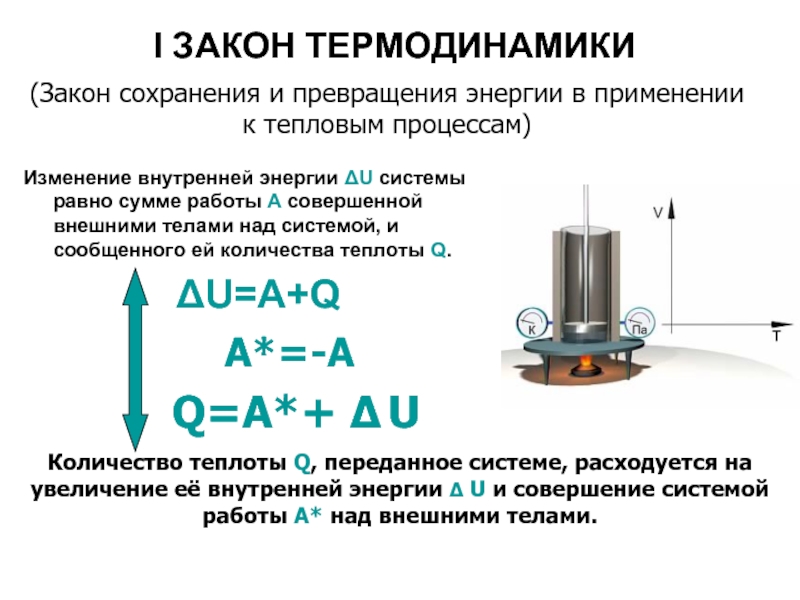
Слайд 28I ЗАКОН ТЕРМОДИНАМИКИ
Изменение внутренней энергии ΔU системы равно сумме работы A
ΔU=A+Q
A*=-A
Q=A*+ Δ U
Количество теплоты Q, переданное системе, расходуется на увеличение её внутренней энергии Δ U и совершение системой работы A* над внешними телами.
(Закон сохранения и превращения энергии в применении к тепловым процессам)
Слайд 29Первый закон термодинамики
Изменение внутренней энергии системы при переходе её из одного
Количество теплоты, переданное системе, идёт на изменение её внутренней энергии и на совершение системой работы над внешними телами
Слайд 30ТЕРМОДИНАМИКА ИЗОПРОЦЕССОВ.
Процессы, происходящие при постоянном значении одного из параметров состояния (T,V
ИЗОТЕРМИЧЕСКИЙ
ИЗОХОРНЫЙ
ИЗОБАРНЫЙ
АДИАБАТНЫЙ
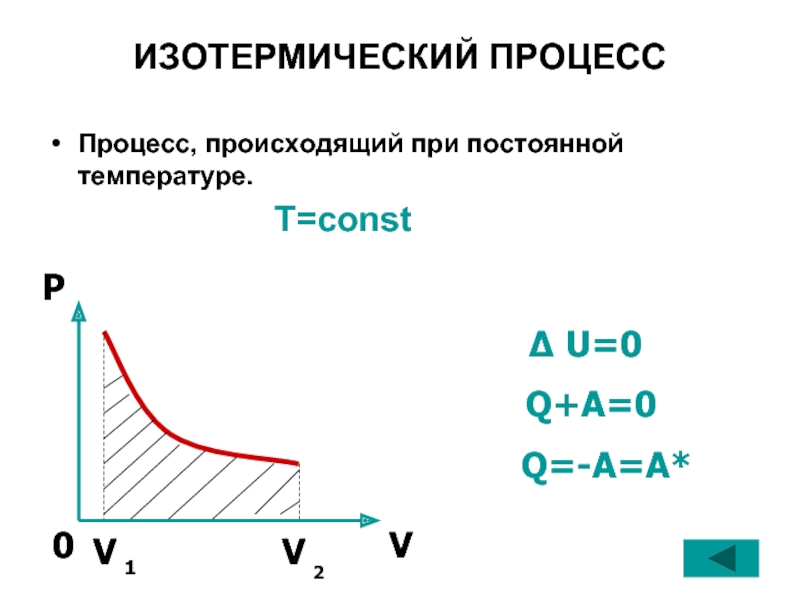
Слайд 31ИЗОТЕРМИЧЕСКИЙ ПРОЦЕСС
Процесс, происходящий при постоянной температуре.
Δ U=0
Q+A=0
Q=-A=A*
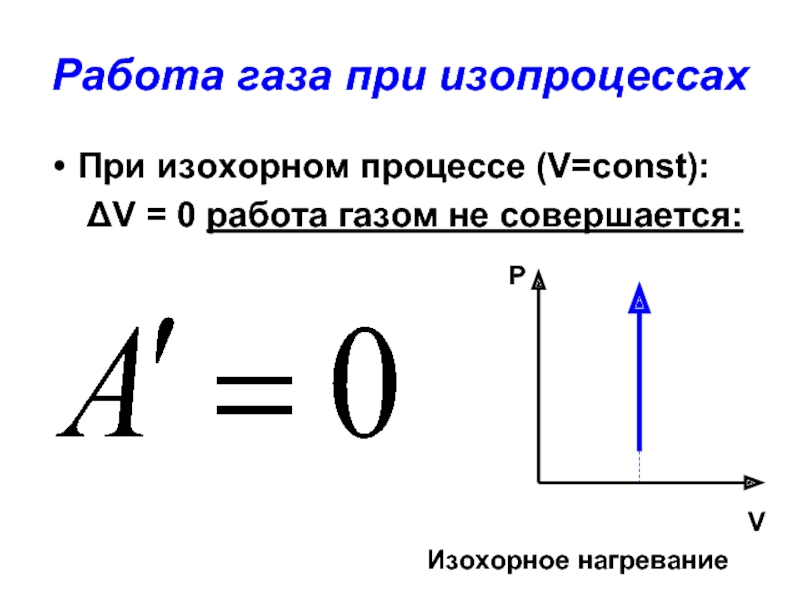
Слайд 34Работа газа при изопроцессах
При изохорном процессе (V=const):
ΔV =
P
V
Изохорное нагревание
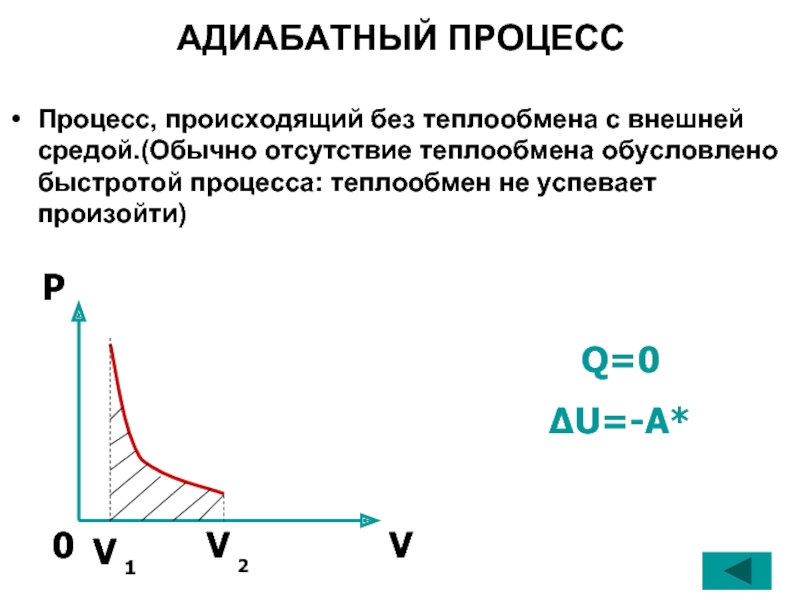
Слайд 37АДИАБАТНЫЙ ПРОЦЕСС
Процесс, происходящий без теплообмена с внешней средой.(Обычно отсутствие теплообмена обусловлено
Q=0
ΔU=-A*
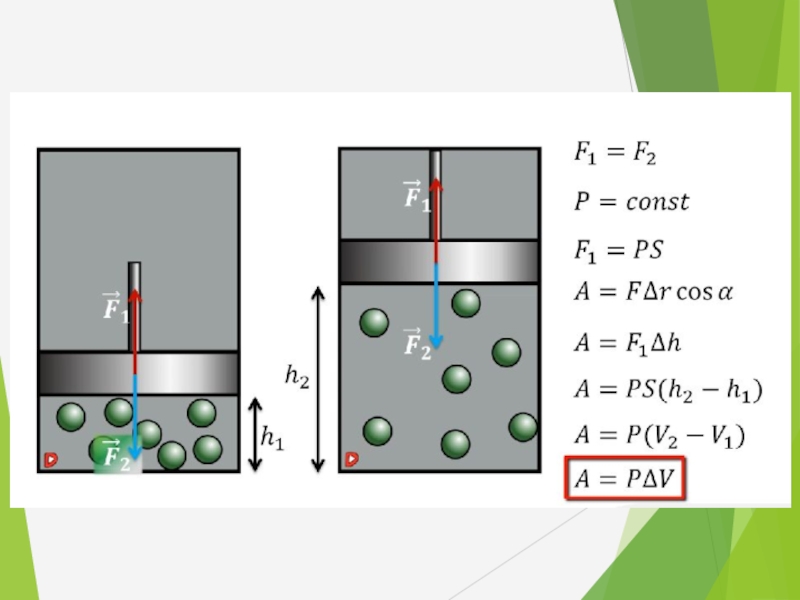
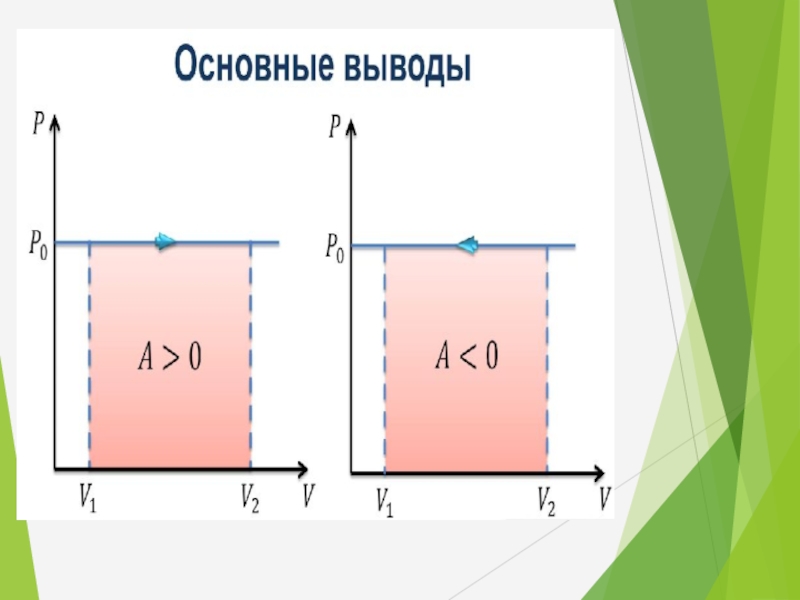
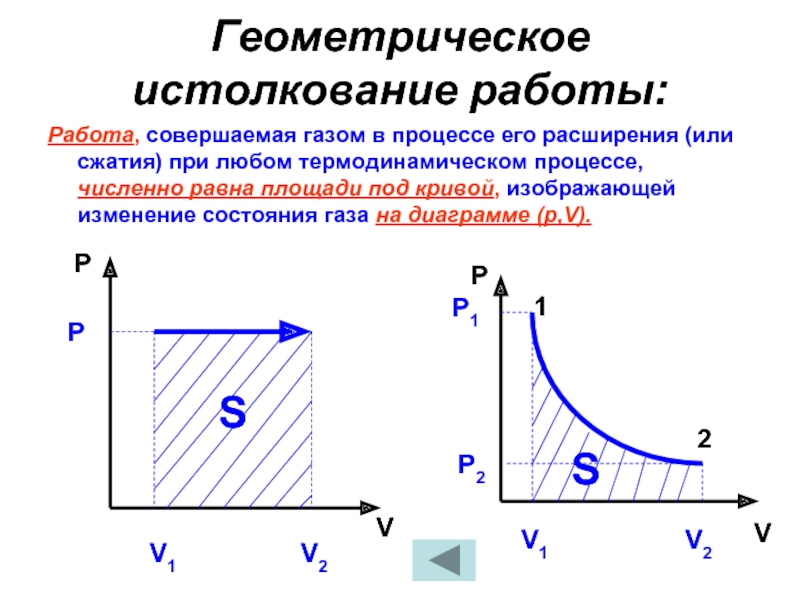
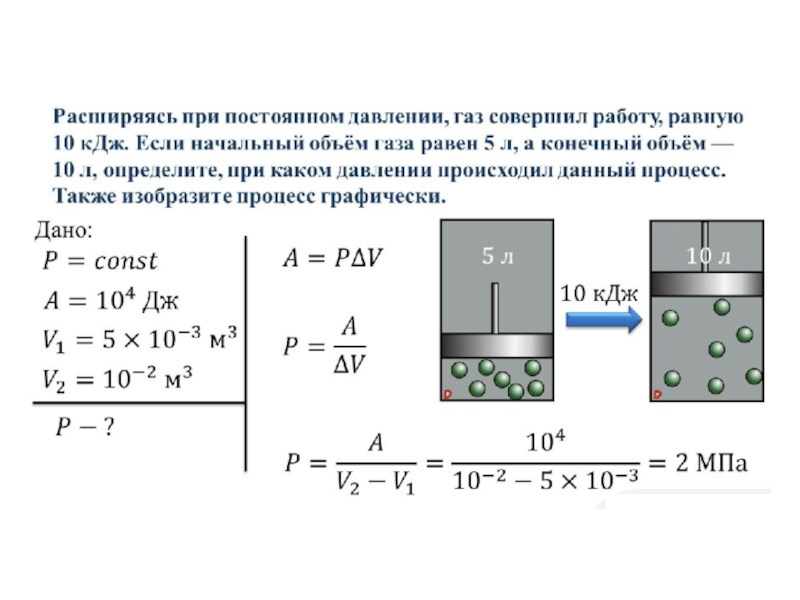
Слайд 38Геометрическое истолкование работы:
Работа, совершаемая газом в процессе его расширения (или сжатия)
P
V
V1
V2
P
P
V
Р2
1
2
V1
V2
S
S
Р1
Слайд 39Количество теплоты – часть внутренней энергии, которую тело получает или теряет
Слайд 41II ЗАКОН ТЕРМОДИНАМИКИ
Тепловые процессы необратимы.
Не возможно перевести теплоту от более
Не возможен круговой процесс, единственным результатом которого было бы производство работы за счет охлаждения теплового резервуара.
Не возможен круговой процесс, единственным результатом которого является передача теплоты от менее нагретого тела более нагретому.
Слайд 42 Тепловые двигатели –
устройства, превращающие
Виды тепловых двигателей
Слайд 43ТЕПЛОВОЙ ДВИГАТЕЛЬ –
ГЛАВНЫЙ ДВИГАТЕЛЬ СОВРЕМЕННОЙ ЭНЕРГЕТИКИ
Периодически действующий двигатель, совершающий работу
НАГРЕВАТЕЛЬ (Т1)
РАБОЧЕЕ ТЕЛА
ХОЛОДИЛЬНИК (Т2)
Q1
Q2
A*
A*=Q1 – Q2
Виды двигателей:
Паровая и газовая турбины
Карбюраторный двс
Дизель двс
Ракетный двигатель
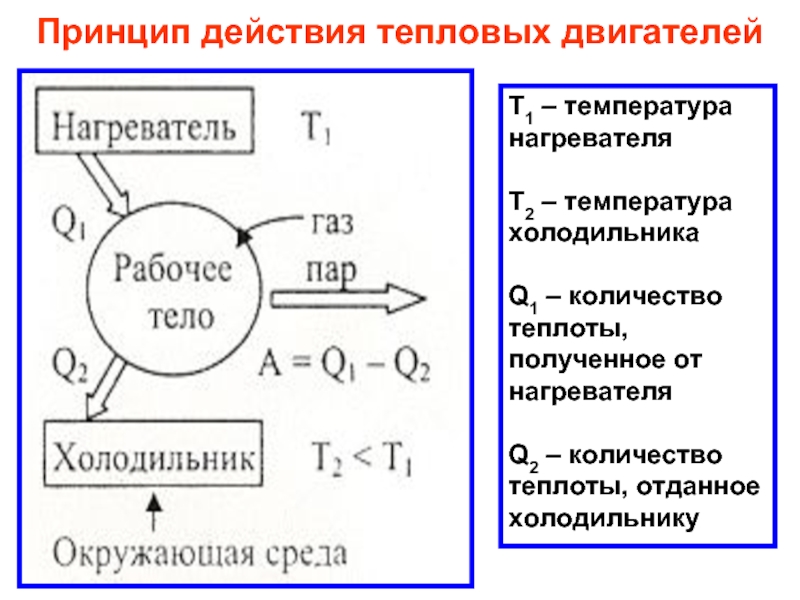
Слайд 44Принцип действия тепловых двигателей
Т1 – температура нагревателя
Т2 – температура холодильника
Q1 –
Q2 – количество теплоты, отданное холодильнику
Слайд 45Коэффициент полезного действия (КПД) теплового двигателя –
отношение работы А’, совершаемой
Слайд 46где
работа, совершаемая
двигателем
тогда
КПД всегда меньше единицы, так как у всех двигателей
передаётся холодильнику
При
двигатель не может работать
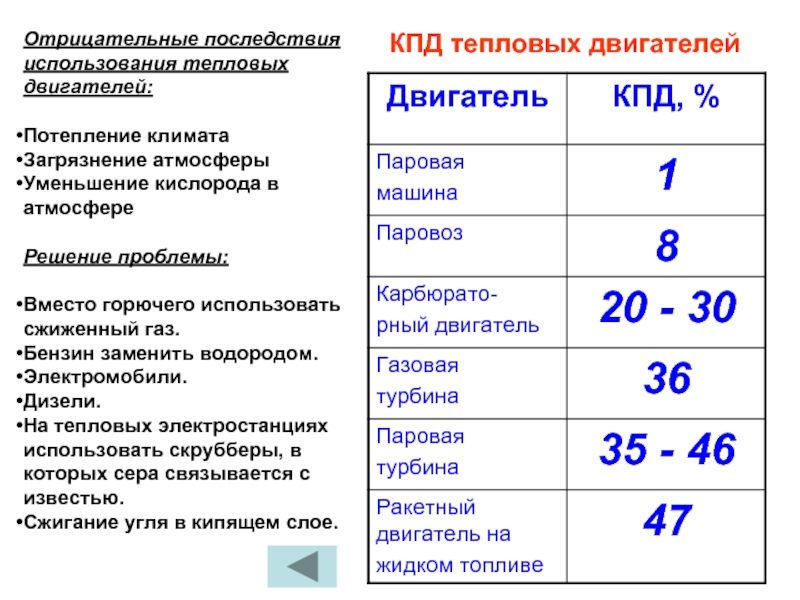
Слайд 48Отрицательные последствия использования тепловых двигателей:
Потепление климата
Загрязнение атмосферы
Уменьшение кислорода в
Решение проблемы:
Вместо горючего использовать сжиженный газ.
Бензин заменить водородом.
Электромобили.
Дизели.
На тепловых электростанциях использовать скрубберы, в которых сера связывается с известью.
Сжигание угля в кипящем слое.
КПД тепловых двигателей
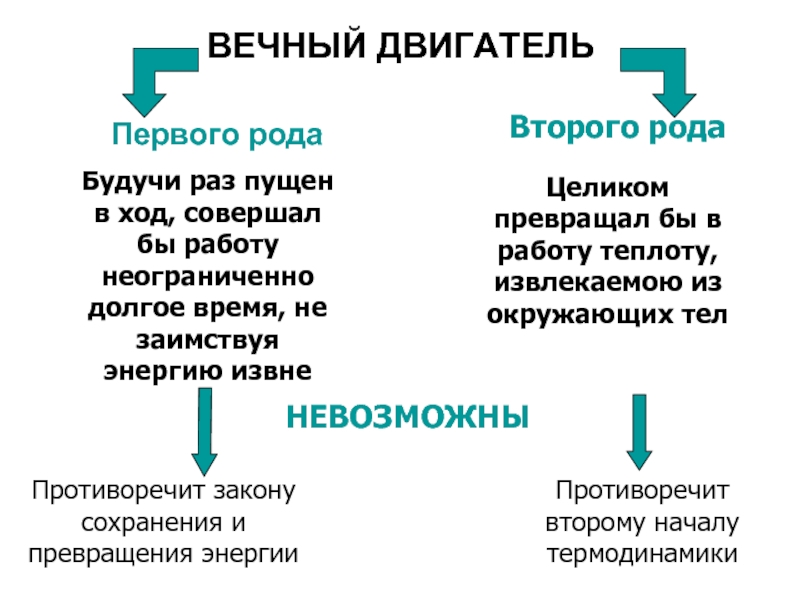
Слайд 49ВЕЧНЫЙ ДВИГАТЕЛЬ
Первого рода
Второго рода
Целиком превращал бы в работу теплоту, извлекаемою из
Будучи раз пущен в ход, совершал бы работу неограниченно долгое время, не заимствуя энергию извне
НЕВОЗМОЖНЫ
Противоречит закону сохранения и превращения энергии
Противоречит второму началу термодинамики
Слайд 50ТЕРМОДИНАМИКА И ПРИРОДА
В окружающей нас природе термодинамически обратимых процессов нет.
Энтропия в
По определению А. Эддингтона, возрастание энтропии, определяющей необратимые процессы есть «стрела времени»:чем выше энтропия системы, тем больше временной промежуток прошла система в своей эволюции.
Возрастание энтропии вселенной должно привести к тому, что температура всех тел сравняется т. е. наступит тепловое равновесие и все процессы прекратятся, наступит «тепловая смерть Вселенной». (Выводы второго закона термодинамики не всегда имеют место в природе и его нельзя применить ко всем существующим процессам).
Слайд 51Тест по ТЕРМОДИНАМИКЕ
На сколько отделов делится термодинамика как предмет?
а) на три в)
б) на четыре г) на шесть
Кем была предложена температурная шкала, которой мы пользуемся в повседневной жизни?
а) Кельвином в) Карно
б) Цельсием г) Джоулем
Что изучает термодинамика?
а) тепловые процессы в) звуковые явления
б) движение молекул г) механические явления
Термодинамическая система, которая не взаимодействует с другими системами называется:
а) закрытой в) статической
б) изолированной г) открытой
Процессы, происходящие при постоянной температуре называются:
а) адиабатными в) изобарными
б) изотермическими г) изохорными
Слайд 52Тест по ТЕРМОДИНАМИКЕ
(продолжение)
При каком изопроцессе работа не совершается?
а) при изотермическом в) адиабатном
б)
7. Согласно второму началу термодинамики тепловые процессы:
а) обратимы в) необратимы
б) изолированы г) закрыты
8. Какой двигатель не является тепловым?
а) паровая турбина в) ракетный двигатель
б) водяная турбина г) дизель
9. Энтропия в термодинамически необратимых процессах:
а) возрастает в) не изменяется
б) уменьшатся г) равна нулю
10. Тепловая смерть Вселенной наступит, если:
а) температура всех тел сравняется;
б) температура всех тел станет равной нулю;
в) температура всех тел будет повышаться;
г) температура всех тел будет понижаться.
Слайд 56Литература
Мякишев Г.Я., Буховцев Б.Б.,Сотский Н.Н. Физика 10 класс. – М.: Просвещение.
Касьянов
Волков В.А. Поурочные разработки по физике. 10 класс. – М: Вако, 2006. – 400 с.
Касаткина И.Л., Ларцева Н.А., Шкиль Т.В. Репетитор по физике. В 2-х томах. Том 1. – Ростов-на-Дону: Феникс, 1995. – 863 с.
www: fiz.1september.ru