- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Основные положения молекулярно-кинетической теории. Размеры молекул презентация
Содержание
- 1. Основные положения молекулярно-кинетической теории. Размеры молекул
- 2. Молекулярная физика – раздел физики, изучающий внутреннее
- 3. Молекула – наименьшая устойчивая частица вещества, обладающая
- 4. Тепловое движение. Макроскопические тела. Тепловые явления.
- 5. Основные положения молекулярно-кинетической теории.
- 6. положение № 1 –
- 7. положение № 1 –
- 8. положение № 2 –
- 9. 3. Броуновское движение (хаотическое
- 10. положение № 3 –
- 13. Агрегатные состояния вещества
- 15. Агрегатные состояния вещества
- 16. Масса молекул. Количество вещества.
- 17. Количество вещества Один моль -
- 18. Число Авогадро (NA) В моле любого вещества NA = 6,02*1023 1/моль
- 22. Д.З. §1.24, повторить записи Учебник Упр.4 № 8, 10, 12.
Слайд 2Молекулярная физика – раздел физики, изучающий внутреннее строение тел, а также
тепловые процессы, происходящие внутри вещества
Слайд 3Молекула – наименьшая устойчивая частица вещества, обладающая его химиченскими свойствами. Молекулы
образуются из атомов.
Атом – наименьшая частица химического элемента, носитель его свойств.
Атом – наименьшая частица химического элемента, носитель его свойств.
Слайд 6
положение № 1 – все вещества состоят из частиц (молекул,
атомов, ионов …) между которыми есть промежутки. положение № 2 – частицы находятся в постоянном, беспорядочном (хаотичном движении (тепловое движение).
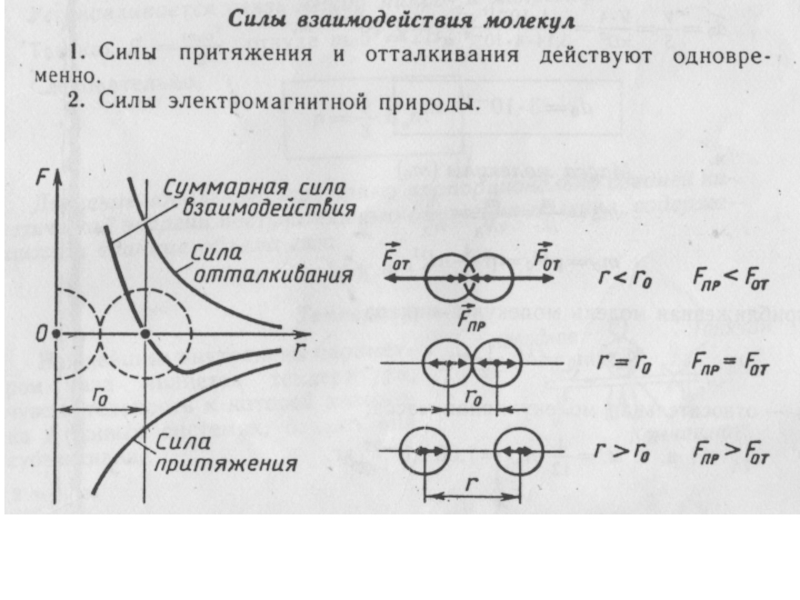
положение № 3 – между молекулами существует межмолекулярное взаимодействие (притяжение и отталкивание).
положение № 3 – между молекулами существует межмолекулярное взаимодействие (притяжение и отталкивание).
Слайд 7
положение № 1 – все вещества состоят из частиц (молекул,
атомов, ионов …) между которыми есть промежутки.
Опытные обоснования:
Крошение вещества
Испарение жидкостей
Смешивание веществ; диффузия
Фотографии туннельного микроскопа
Растворимость
Сжимаемость веществ
Опытные обоснования:
Крошение вещества
Испарение жидкостей
Смешивание веществ; диффузия
Фотографии туннельного микроскопа
Растворимость
Сжимаемость веществ
Слайд 8
положение № 2 – частицы находятся в постоянном, беспорядочном (хаотичном
движении (тепловое движение).
Опытные обоснования:
1. Испарение
2. Диффузия (самопроизвольное проникновение частиц одного вещества между частицами другого вещества. Скорость диффузии зависит от температуры и агрегатного состояния вещества).
Опытные обоснования:
1. Испарение
2. Диффузия (самопроизвольное проникновение частиц одного вещества между частицами другого вещества. Скорость диффузии зависит от температуры и агрегатного состояния вещества).
Слайд 9
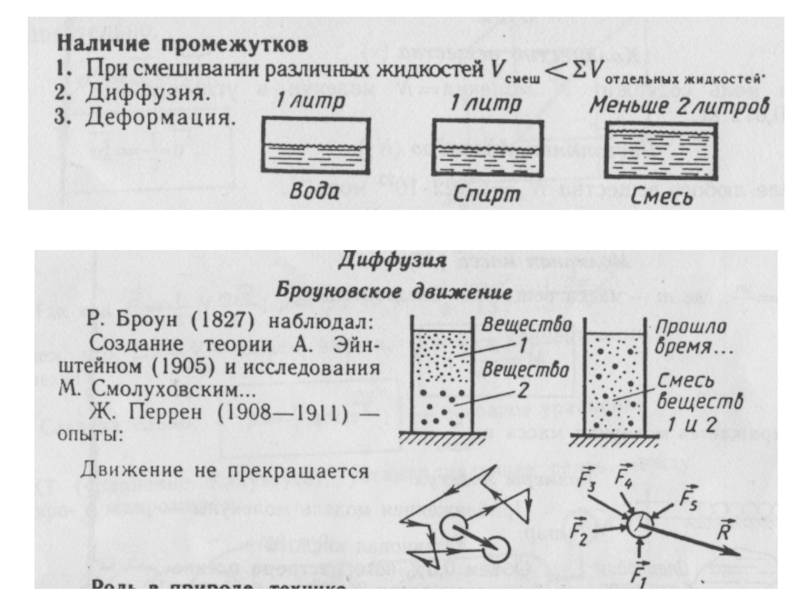
3. Броуновское движение (хаотическое движение взвешенных частиц в жидкости или
газе частиц под действием нескомпенсированных ударов молекул жидкости или газа).
4. Давление газа на стенки сосуда.
5. Стремление газа занять любой объем.
4. Давление газа на стенки сосуда.
5. Стремление газа занять любой объем.
Слайд 10
положение № 3 – между молекулами существует межмолекулярное взаимодействие (притяжение
и отталкивание).
Опытные обоснования:
1. Деформация тела
2. Сохранение формы твердого тела
3. Существование жидкостей.
4. Наличие промежутков между частицами.
5. Смачивание.
6. Молекулярное сцепление.
Опытные обоснования:
1. Деформация тела
2. Сохранение формы твердого тела
3. Существование жидкостей.
4. Наличие промежутков между частицами.
5. Смачивание.
6. Молекулярное сцепление.
Слайд 17Количество вещества
Один моль - это количество вещества, в котором содержится
столько же частиц, сколько атомов в в углероде массой 0,012 кг.
N молекул = N молекул в углероде массой 0,012 кг
N молекул = N молекул в углероде массой 0,012 кг