- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Коррозионные процессы презентация
Содержание
- 1. Коррозионные процессы
- 2. Коррозия Коррозия – необратимый процесс постепенного разрушения
- 3. Классификация видов коррозии физическая По механизму процессов
- 4. Коррозия металлических конструкций
- 5. Химическая коррозия металлов При химической коррозии идет
- 6. дымоход прогорел
- 7. Электрохимическая коррозия металлов При электрохимической коррозии возникает
- 8. Коррозия металлов в контакте
- 9. Контактная коррозия Способность перехода иона металла в
- 10. Коррозия металлов в контакте Цинк защищает железо
- 11. Атмосферная коррозия Конденсация на поверхности конструкции водяных
- 12. Шуховская радиобашня на Шаболовке Все почтенные девяносто
- 13. Шуховская радиобашня на Шаболовке
- 14. Шуховская радиобашня на Шаболовке
- 15. Шуховская радиобашня на Шаболовке
- 16. Шуховская радиобашня на Шаболовке Коррозия элементов в
- 17. Шуховская радиобашня на Шаболовке
- 18. Шуховская радиобашня на Шаболовке
- 19. Шуховская радиобашня на Шаболовке Стержни, образующие вертикальную
- 20. Шаболовская башня – щелевая коррозия Щелевая коррозия
- 21. Шаболовская башня – щелевая коррозия Постепенно внутри
- 22. Шаболовская башня – щелевая коррозия Этого типа
- 23. Пробные расчистки методами мягкого бластинга выявили хорошее
- 24. Сталь фабрики германского концерна KRUPP в бывшем
- 25. Почвенная (подземная) коррозия Неоднородность среды Неравномерный доступ
- 26. Коррозия винтовых свай Для обычной почвы средняя
- 27. Электрохимическая защита от коррозии 1) Протекторная защита
- 28. Электрохимическая защита от коррозии 2) Катодная защита
- 29. Коррозия блуждающими токами Схема возникновения блуждающего
- 30. Коррозия от действия блуждающих токов Блуждающие токи
- 31. Способы снижения коррозии блуждающими токами Дренаж -
- 32. Коррозия арматуры в бетоне
- 33. Карбонизация бетона Карбонизация (нейтрализация) бетона – процесс
- 34. Коррозия
- 35. Определение глубины карбонизации бетона
- 36. Определение глубины карбонизации бетона
- 37. Коррозия
- 38. Коррозия арматуры в бетоне Стальная арматура в
- 39. Коррозия арматуры в бетоне Хлориды могут попасть
- 40. Коррозия арматуры в бетоне Для высокопрочных сталей
- 41. Отколы защитного слоя бетона вследствие давления продуктов коррозии
- 42. Пятна ржавчины на поверхности бетона вдоль расположения стержней
- 43. Коррозия
- 44. Разрушение защитного слоя бетона, коррозия арматуры до 70% из-за нарушения температурно-влажностных условий эксплуатации
- 45. Разрушение защитного слоя, коррозия арматуры до 30% вследствие действия агрессивных факторов
- 46. Коррозия арматуры в зоне трещин Время депассивации
- 47. Коррозия бетона в жидких средах
- 48. Коррозия бетона в жидких средах Выщелачивание гидроксида
- 49. Коррозия выщелачивания (коррозия 1-го вида) этот вид
- 50. Кислотная коррозия (коррозия 2-го вида) очень часто
- 51. Коррозия мостовых конструкций
- 52. Сульфатная коррозия (коррозия 3-го вида) Сильным разрушениям
- 53. Коррозия мостовых конструкций
- 54. Методы защиты железобетонных конструкций
- 55. Учёт требований долговечности при проектировании железобетонных конструкций
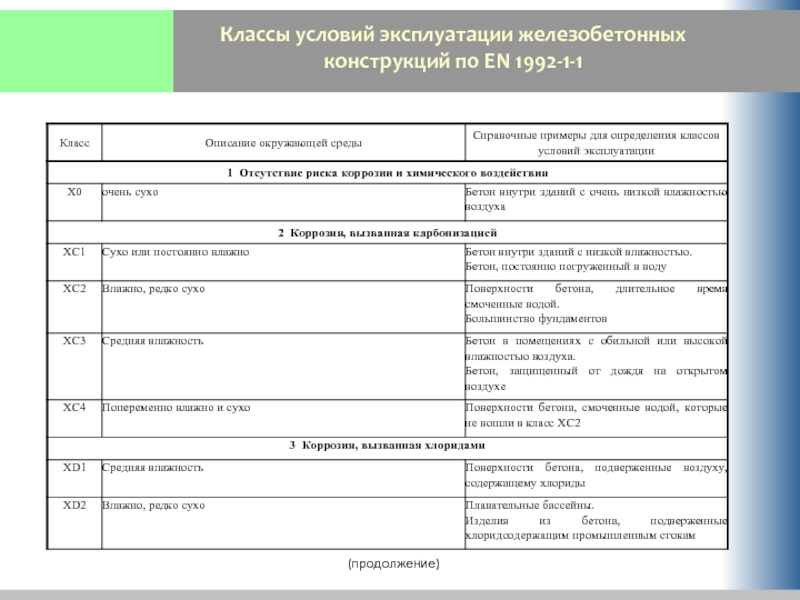
- 56. Классы условий эксплуатации железобетонных конструкций по EN 1992-1-1 (продолжение)
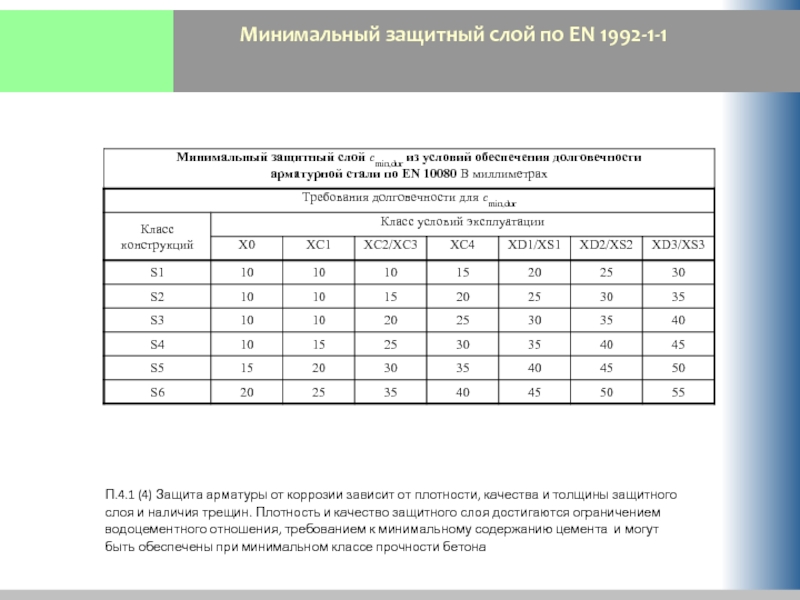
- 57. Минимальный защитный слой по EN 1992-1-1 П.4.1
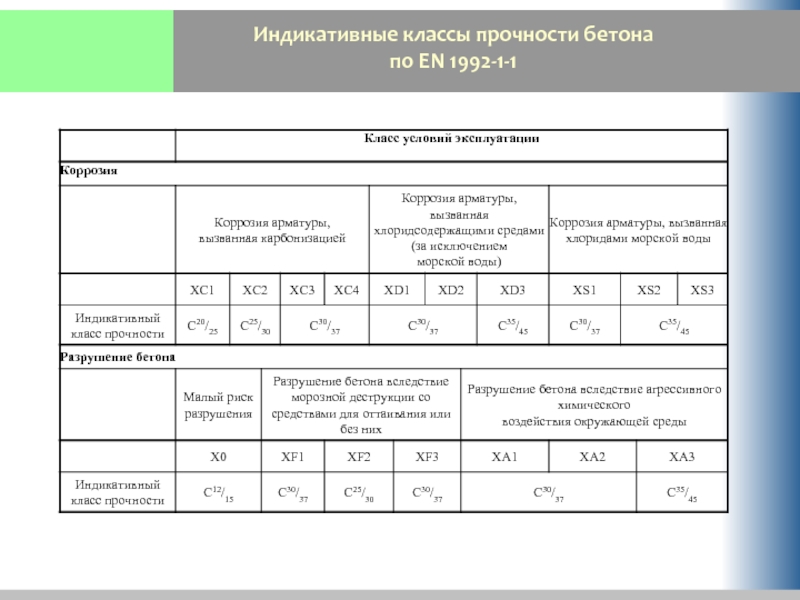
- 58. Индикативные классы прочности бетона по EN 1992-1-1
- 59. Коррозия мостовых конструкций
- 60. Коррозия мостовых конструкций
- 61. Коррозия мостовых конструкций
- 62. Коррозия мостовых конструкций
- 63. Коррозия мостовых конструкций
- 64. Коррозия зоны опирания опоры освещения
- 65. дефект
- 66. Протечки
- 67. Разрушение бетона пролетного строения
- 68. Разрушение бетона маломассивной опоры с оголением и коррозией арматуры
- 69. Коррозия
- 70. Коррозия
- 71. Коррозия
- 72. Коррозия
- 73. Коррозия
- 74. Уменьшение глубины опирания ребра плиты перекрытия с
- 75. Следы замачивания несущих конструкций вследствие неудовлетворительного состояния кровли
Слайд 2Коррозия
Коррозия – необратимый процесс постепенного разрушения материала под действием агрессивных сред.
Количественные
Фронт коррозии – поверхность, отделяющая повреждённый материал от неповреждённого.
Степень агрессивности среды оценивается только по отношению к конкретному материалу.
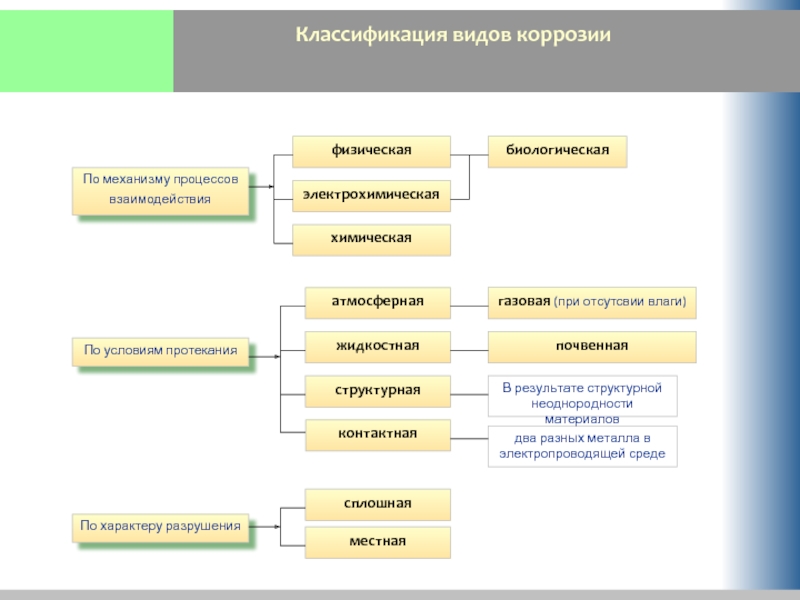
Слайд 3Классификация видов коррозии
физическая
По механизму процессов взаимодействия
электрохимическая
химическая
биологическая
По условиям протекания
атмосферная
газовая (при отсутсвии влаги)
жидкостная
почвенная
структурная
контактная
По
сплошная
местная
два разных металла в электропроводящей среде
В результате структурной неоднородности материалов
Слайд 5Химическая коррозия металлов
При химической коррозии идет окисление металла без возникновения цепи
4Al + 3O2 = 2Al2O3.
Для алюминия этот процесс благоприятен, т.к. оксидная пленка плотно прилегает к поверхности металла и не дает дальнейшего доступа кислорода к металлу (пассивация).
Железо окисляется только при высокой температуре (свыше 100оС)
2Fe + O2 = FeO, 4FeO + 3O2 = 2Fe2O3
Окисление металлов, соприкасающихся с газовой средой, происходит в котлах, дымовых трубах и т.д.
При нагревании стальных конструкций поверхностный слой обезуглероживается, становится мягким, сталь приобретает свойство текучести:
2Fe3C + O2 = 6Fe + 2CO
Fe3C + CO2 = 3Fe + 2CO
Fe3C + H2O = 3Fe + CO + H2
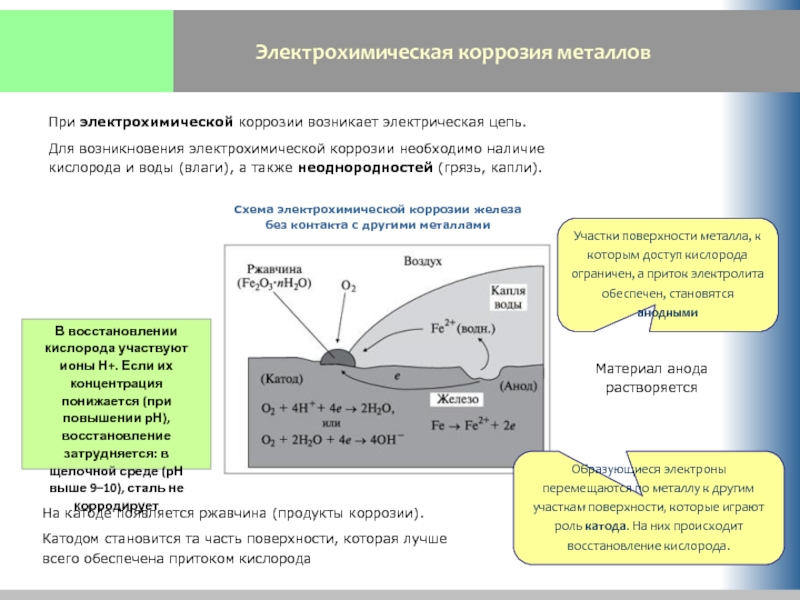
Слайд 7Электрохимическая коррозия металлов
При электрохимической коррозии возникает электрическая цепь.
Для возникновения электрохимической коррозии
Материал анода растворяется
На катоде появляется ржавчина (продукты коррозии).
Катодом становится та часть поверхности, которая лучше всего обеспечена притоком кислорода
Схема электрохимической коррозии железа без контакта с другими металлами
Участки поверхности металла, к которым доступ кислорода ограничен, а приток электролита обеспечен, становятся анодными
Образующиеся электроны перемещаются по металлу к другим участкам поверхности, которые играют роль катода. На них происходит восстановление кислорода.
В восстановлении кислорода участвуют ионы Н+. Если их концентрация понижается (при повышении рН), восстановление затрудняется: в щелочной среде (рН выше 9–10), сталь не корродирует
Слайд 9Контактная коррозия
Способность перехода иона металла в электролит характеризуется электродным потенциалом –
Величина электродного потенциала зависит от природы металла, электролита и от температуры
Контактная коррозия: менее благородный металл становится анодом, более благородный – катодом.
Чем больше отношение площади катода к площади анода, тем интенсивнее протекает разрушение элементов конструкций из менее благородного материала.
при контакте низколегированной стали различных марок (в том числе в сварных швах), если одна из них легирована медью или никелем;
при воздействии на конструкции пыли, содержащей тяжелые металлы или их оксиды, гидрооксиды, соли;
при попадании на конструкции потеков воды с корродирующих медных деталей;
при попадании на поверхность конструкций из оцинкованной стали или алюминиевых сплавов графитовой либо железорудной пыли, коксовой крошки
Примеры контактной коррозии:
Нержавеющая сталь
Алюминиевые сплавы
Углеродистая или низколегорованная сталь
Оцинкованная сталь
Слайд 10Коррозия металлов в контакте
Цинк защищает железо от коррозии даже после нарушения
цинк играет роль анода и корродирует вместо железа.
Наиболее сильно разрушение наблюдается в местах несплошности покрытия (на кромках).
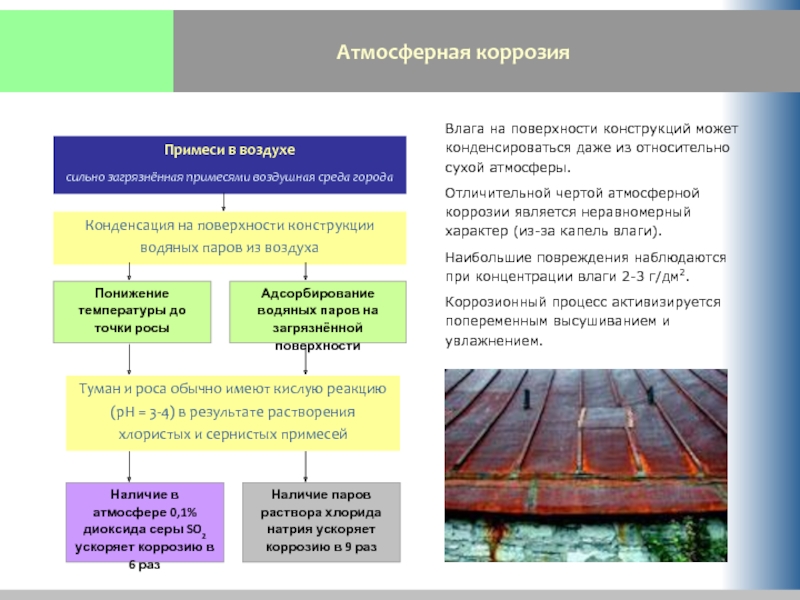
Слайд 11Атмосферная коррозия
Конденсация на поверхности конструкции водяных паров из воздуха
Туман и роса
Понижение температуры до точки росы
Адсорбирование водяных паров на загрязнённой поверхности
Примеси в воздухе
сильно загрязнённая примесями воздушная среда города
Наличие в атмосфере 0,1% диоксида серы SO2 ускоряет коррозию в 6 раз
Наличие паров раствора хлорида натрия ускоряет коррозию в 9 раз
Влага на поверхности конструкций может конденсироваться даже из относительно сухой атмосферы.
Отличительной чертой атмосферной коррозии является неравномерный характер (из-за капель влаги).
Наибольшие повреждения наблюдаются при концентрации влаги 2-3 г/дм2.
Коррозионный процесс активизируется попеременным высушиванием и увлажнением.
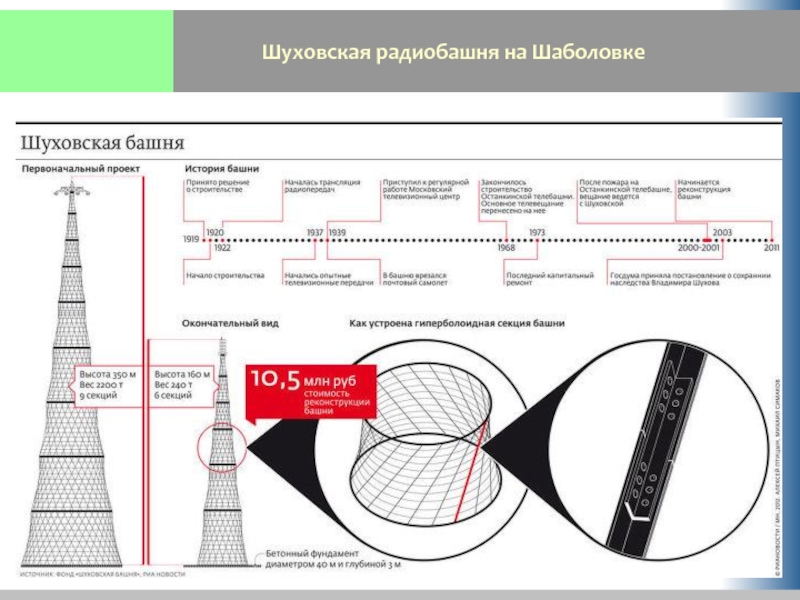
Слайд 12Шуховская радиобашня на Шаболовке
Все почтенные девяносто лет своего существования Шуховская башня
Слайд 16Шуховская радиобашня на Шаболовке
Коррозия элементов в основном поразила горизонтальные пояса. Это
Слайд 19Шуховская радиобашня на Шаболовке
Стержни, образующие вертикальную конструкцию, были менее подвержены коррозии
Слайд 20Шаболовская башня – щелевая коррозия
Щелевая коррозия возникает в случае, когда плотное
Слайд 21Шаболовская башня – щелевая коррозия
Постепенно внутри щели или зазора скапливаются продукты
Слайд 22Шаболовская башня – щелевая коррозия
Этого типа коррозии можно было бы избежать,
Слайд 23Пробные расчистки методами мягкого бластинга выявили хорошее состояние металла
особенность мягкого
Слайд 24Сталь фабрики германского концерна KRUPP в бывшем городе Friedenshütte (ныне в
Анализ металла, использованного при строительстве Шаболовской башни, показал, что по содержанию примесей (углерода от 0,05 до 0,36%; серы от 0,018 до 0,065%; фосфора) превышает норму в двух третях элементов башни. Сталь подобного типа не подлежит сварке, но зато она покрылась естественно образовавшейся оксидной плёнкой, играющей защитную роль (пассивирование) для основного объёма металла.
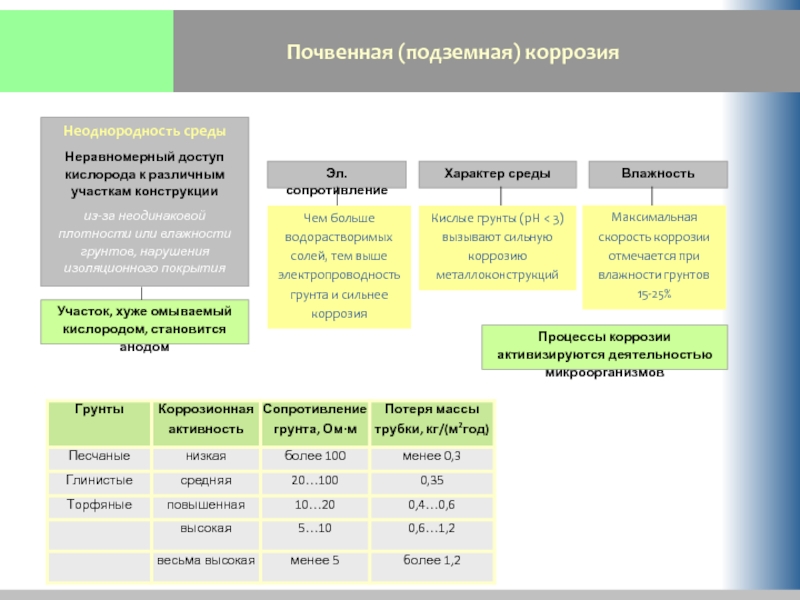
Слайд 25Почвенная (подземная) коррозия
Неоднородность среды
Неравномерный доступ кислорода к различным участкам конструкции
из-за неодинаковой
Участок, хуже омываемый кислородом, становится анодом
Кислые грунты (рН < 3) вызывают сильную коррозию металлоконструкций
Чем больше водорастворимых солей, тем выше электропроводность грунта и сильнее коррозия
Максимальная скорость коррозии отмечается при влажности грунтов 15-25%
Эл. сопротивление
Характер среды
Влажность
Процессы коррозии активизируются деятельностью микроорганизмов
Слайд 26Коррозия винтовых свай
Для обычной почвы средняя величина коррозии составляет 0,03 мм
В большинстве случаев срок службы свай устанавливается 50 лет
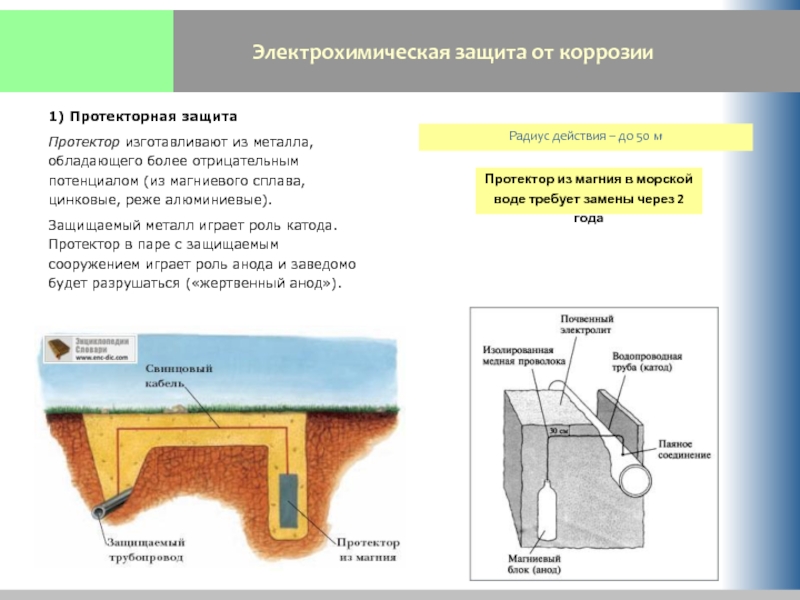
Слайд 27Электрохимическая защита от коррозии
1) Протекторная защита
Протектор изготавливают из металла, обладающего более
Защищаемый металл играет роль катода. Протектор в паре с защищаемым сооружением играет роль анода и заведомо будет разрушаться («жертвенный анод»).
Радиус действия – до 50 м
Протектор из магния в морской воде требует замены через 2 года
Слайд 28Электрохимическая защита от коррозии
2) Катодная защита
Конструкция соединяется с электродом (обычно чугунный
При этом защищаемую конструкцию подключают к (-), а электрод – к (+) источника тока. В этом случае электроны отнимаются от анода источником тока, анод разрушается, а на катоде (защищаемой конструкции) происходит восстановление окислителя.
Радиус действия – до 2 км
Засыпка (гипс + хлорид натрия) – снижает локальное сопротивление слоя почвы, находящегося вблизи анода, а также пассивирующего слоя на поверхности анода
Чем больше скорость коррозии, тем больше должна быть плотность тока
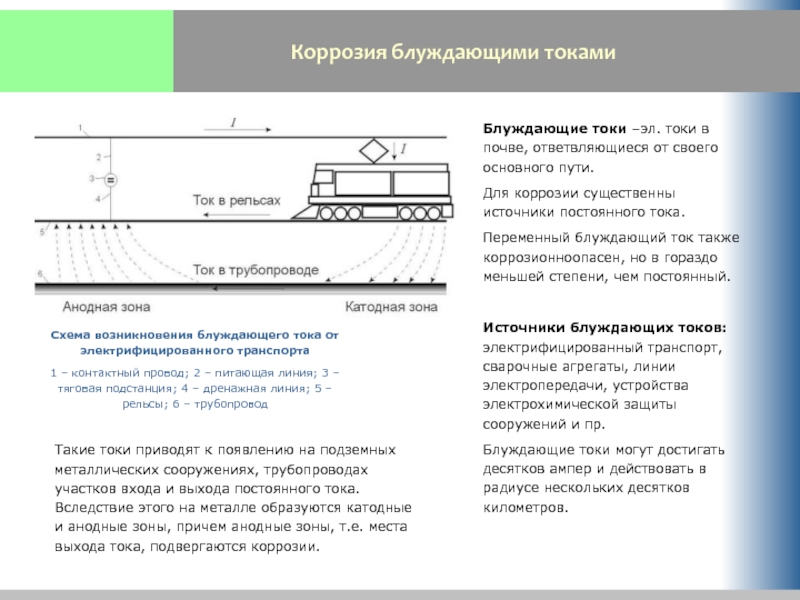
Слайд 29Коррозия блуждающими токами
Схема возникновения блуждающего тока от электрифицированного транспорта
1 –
Блуждающие токи –эл. токи в почве, ответвляющиеся от своего основного пути.
Для коррозии существенны источники постоянного тока.
Переменный блуждающий ток также коррозионноопасен, но в гораздо меньшей степени, чем постоянный.
Источники блуждающих токов: электрифицированный транспорт, сварочные агрегаты, линии электропередачи, устройства электрохимической защиты сооружений и пр.
Блуждающие токи могут достигать десятков ампер и действовать в радиусе нескольких десятков километров.
Такие токи приводят к появлению на подземных металлических сооружениях, трубопроводах участков входа и выхода постоянного тока. Вследствие этого на металле образуются катодные и анодные зоны, причем анодные зоны, т.е. места выхода тока, подвергаются коррозии.
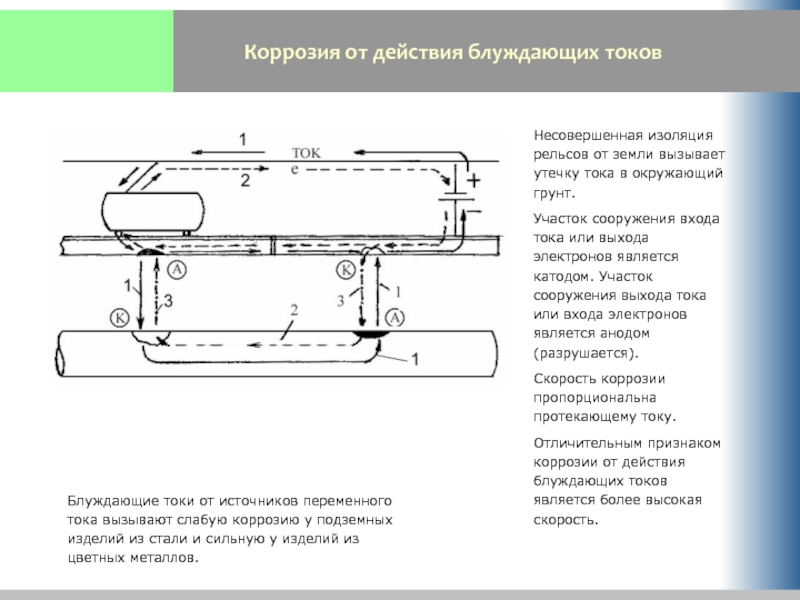
Слайд 30Коррозия от действия блуждающих токов
Блуждающие токи от источников переменного тока вызывают
Несовершенная изоляция рельсов от земли вызывает утечку тока в окружающий грунт.
Участок сооружения входа тока или выхода электронов является катодом. Участок сооружения выхода тока или входа электронов является анодом (разрушается).
Скорость коррозии пропорциональна протекающему току.
Отличительным признаком коррозии от действия блуждающих токов является более высокая скорость.
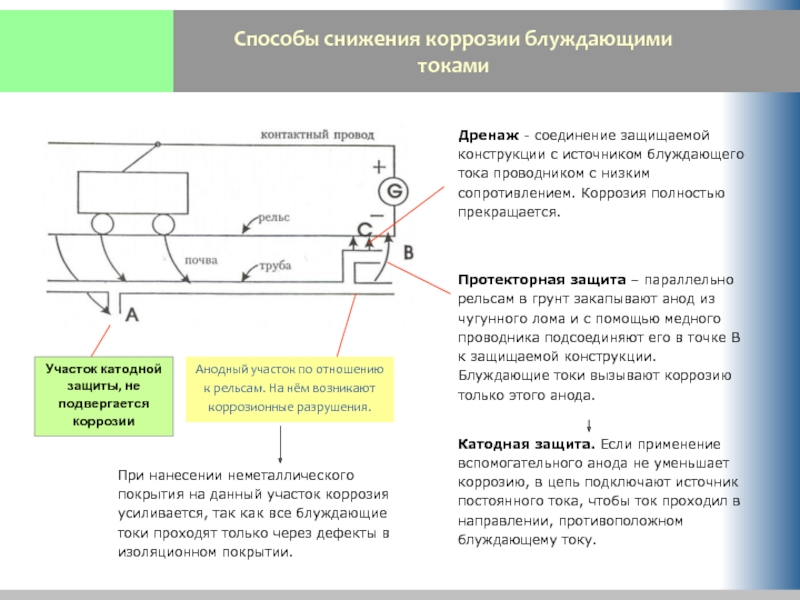
Слайд 31Способы снижения коррозии блуждающими токами
Дренаж - соединение защищаемой конструкции с источником
Протекторная защита – параллельно рельсам в грунт закапывают анод из чугунного лома и с помощью медного проводника подсоединяют его в точке В к защищаемой конструкции. Блуждающие токи вызывают коррозию только этого анода.
Катодная защита. Если применение вспомогательного анода не уменьшает коррозию, в цепь подключают источник постоянного тока, чтобы ток проходил в направлении, противоположном блуждающему току.
Анодный участок по отношению к рельсам. На нём возникают коррозионные разрушения.
Участок катодной защиты, не подвергается коррозии
При нанесении неметаллического покрытия на данный участок коррозия усиливается, так как все блуждающие токи проходят только через дефекты в изоляционном покрытии.
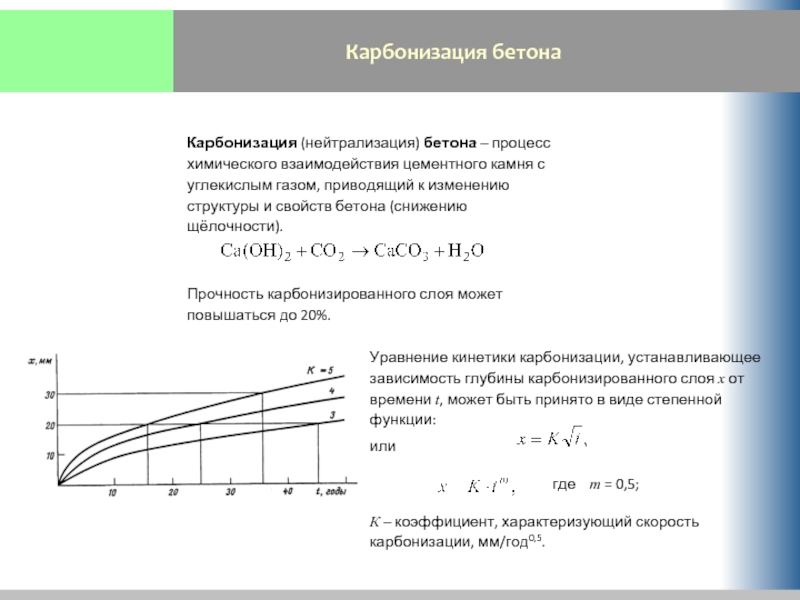
Слайд 33Карбонизация бетона
Карбонизация (нейтрализация) бетона – процесс химического взаимодействия цементного камня с
Прочность карбонизированного слоя может повышаться до 20%.
Уравнение кинетики карбонизации, устанавливающее зависимость глубины карбонизированного слоя x от времени t, может быть принято в виде степенной функции:
или
где m = 0,5;
К – коэффициент, характеризующий скорость карбонизации, мм/год0,5.
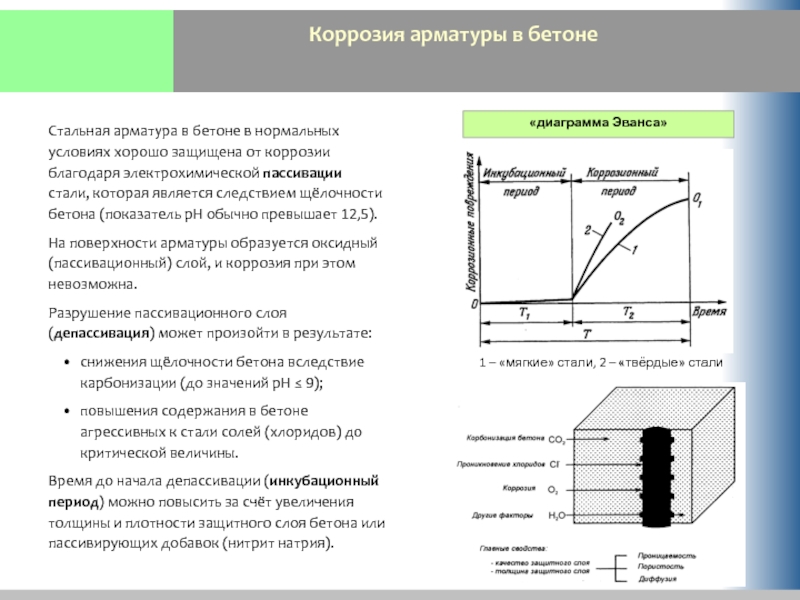
Слайд 38Коррозия арматуры в бетоне
Стальная арматура в бетоне в нормальных условиях хорошо
На поверхности арматуры образуется оксидный (пассивационный) слой, и коррозия при этом невозможна.
Разрушение пассивационного слоя (депассивация) может произойти в результате:
снижения щёлочности бетона вследствие карбонизации (до значений рН ≤ 9);
повышения содержания в бетоне агрессивных к стали солей (хлоридов) до критической величины.
Время до начала депассивации (инкубационный период) можно повысить за счёт увеличения толщины и плотности защитного слоя бетона или пассивирующих добавок (нитрит натрия).
«диаграмма Эванса»
1 – «мягкие» стали, 2 – «твёрдые» стали
Слайд 39Коррозия арматуры в бетоне
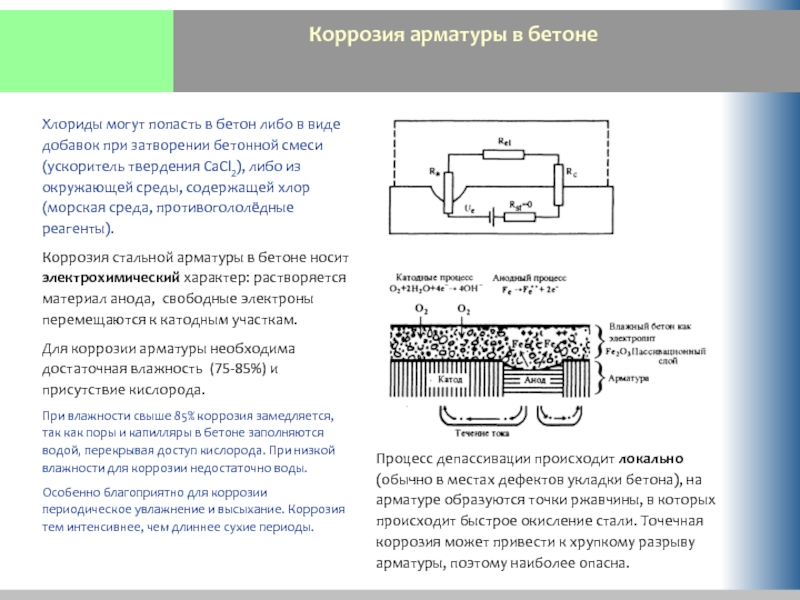
Хлориды могут попасть в бетон либо в виде
Коррозия стальной арматуры в бетоне носит электрохимический характер: растворяется материал анода, свободные электроны перемещаются к катодным участкам.
Для коррозии арматуры необходима достаточная влажность (75-85%) и присутствие кислорода.
При влажности свыше 85% коррозия замедляется, так как поры и капилляры в бетоне заполняются водой, перекрывая доступ кислорода. При низкой влажности для коррозии недостаточно воды.
Особенно благоприятно для коррозии периодическое увлажнение и высыхание. Коррозия тем интенсивнее, чем длиннее сухие периоды.
Процесс депассивации происходит локально (обычно в местах дефектов укладки бетона), на арматуре образуются точки ржавчины, в которых происходит быстрое окисление стали. Точечная коррозия может привести к хрупкому разрыву арматуры, поэтому наиболее опасна.
Слайд 40Коррозия арматуры в бетоне
Для высокопрочных сталей характерно коррозионное растрескивание – межкристаллитная
Точечная коррозия арматуры характеризуется значительной глубиной проникания и проходит без достаточно явных признаков, так как при малых по площади участках поражения продукты коррозии не могут оказать давления, достаточного для разрыва защитного слоя бетона.
Внешние признаки коррозионного повреждения арматуры в бетоне:
Пятна ржавчины на поверхности бетона вдоль расположения стержней;
Трещины, ориентированные по направлению арматуры;
Отколы защитного слоя бетона вследствие давления продуктов коррозии.
Стремление уменьшить диаметр арматуры приводит к более существенным коррозионным потерям её поперечного сечения.
Слайд 44Разрушение защитного слоя бетона, коррозия арматуры до 70% из-за нарушения температурно-влажностных
Слайд 45Разрушение защитного слоя, коррозия арматуры до 30% вследствие действия агрессивных факторов
Слайд 46Коррозия арматуры в зоне трещин
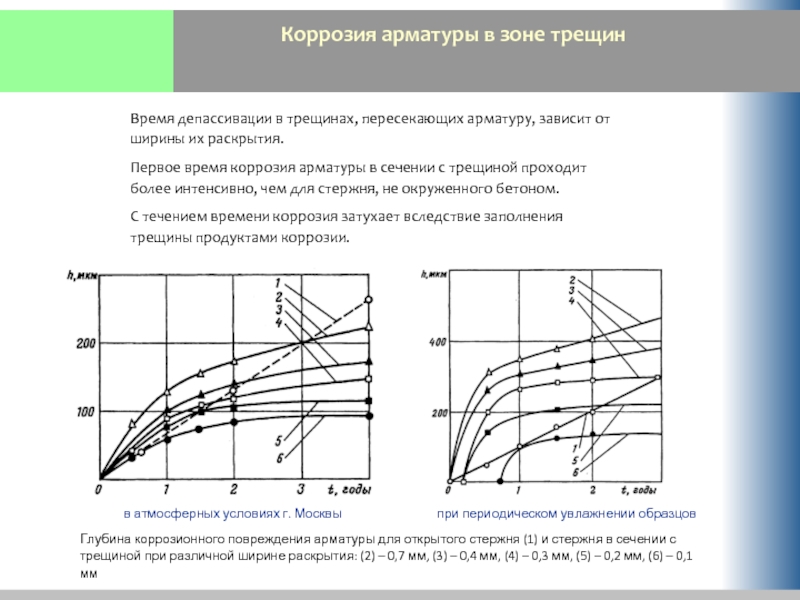
Время депассивации в трещинах, пересекающих арматуру, зависит
Первое время коррозия арматуры в сечении с трещиной проходит более интенсивно, чем для стержня, не окруженного бетоном.
С течением времени коррозия затухает вследствие заполнения трещины продуктами коррозии.
Глубина коррозионного повреждения арматуры для открытого стержня (1) и стержня в сечении с трещиной при различной ширине раскрытия: (2) – 0,7 мм, (3) – 0,4 мм, (4) – 0,3 мм, (5) – 0,2 мм, (6) – 0,1 мм
в атмосферных условиях г. Москвы
при периодическом увлажнении образцов
Слайд 48Коррозия бетона в жидких средах
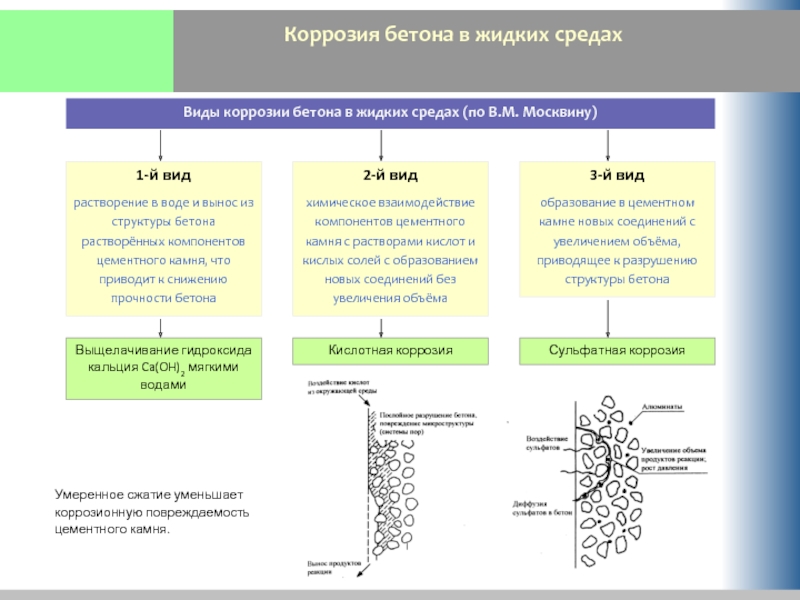
Выщелачивание гидроксида кальция Ca(OH)2 мягкими водами
1-й вид
растворение
Виды коррозии бетона в жидких средах (по В.М. Москвину)
2-й вид
химическое взаимодействие компонентов цементного камня с растворами кислот и кислых солей с образованием новых соединений без увеличения объёма
3-й вид
образование в цементном камне новых соединений с увеличением объёма, приводящее к разрушению структуры бетона
Кислотная коррозия
Сульфатная коррозия
Умеренное сжатие уменьшает коррозионную повреждаемость цементного камня.
Слайд 49Коррозия выщелачивания (коррозия 1-го вида)
этот вид коррозии наблюдается с наружной стороны
Выщелачивание – процесс растворения и выноса гидроокиси кальция Са(ОН)2 из тела бетона фильтрующейся через его толщину водой.
Наиболее опасно, когда вода фильтруется через тело бетона под напором.
Снижается плотность бетона, а следовательно, и его прочность.
При бетонах нормальной плотности, высокой жесткости воды, медленном ее поступлении к открытой поверхности конструкции в бетоне часто происходит постепенное затухание процесса фильтрации из-за и отложения в его порах мельчайших взвешенных в воде минеральных частиц (кальматации пор).
Характерные признаки коррозии выщелачивания - образование белых потеков, хлопьев или сталактитов на внутренней, не соприкасающейся с водой поверхности бетона.
Слайд 50Кислотная коррозия (коррозия 2-го вида)
очень часто интенсивной кислотной коррозии подвергаются конструкции
Между кислотами и кислыми солями, содержащимися в агрессивной среде, и цементным камнем протекают химические реакции, в результате которых образуются легкорастворимые соли и аморфные малорастворимые продукты. И те и другие не обладают вяжущей способностью, нарушается сцепление между компонентами бетона, последний становится рыхлым, теряет свою прочность.
Сульфаты и особенно хлористый кальций, образующиеся при воздействии на цементный камень соответственно серной и соляной кислот, рыхлые, нестойкие и легко вымываемые водой продукты, значительно ослабляют бетон и способствуют его быстрому разрушению.
Визуально пораженный кислотами бетон имеет шероховатую и рыхлую структуру вследствие потери вяжущих свойств, чаще всего бурого или грязно-белого цвета. Наружные поверхности конструкций шелушатся и отслаиваются от основной массы бетона кусками или лещадками
Слайд 52Сульфатная коррозия (коррозия 3-го вида)
Сильным разрушениям от этого вида коррозии подвергаются
В бетоне под действием агрессивных вод, содержащих сульфаты - сернокислые соединения (CaSО4, Nа2SO4, MgSO4 и др.), разрушение проявляется в виде разбухания и искривления конструктивных элементов.
В этом случае не только не происходит удаления составляющих из объема цементного камня, а наоборот, в результате химических реакций между ним и веществами, поступающими из внешней среды, образуются новые соединения, объем которых превышает объем твердой фазы компонентов цементного камня.
Типичный пример такой коррозии - образование "цементной бациллы" - гидросульфоалюмината кальция. Гидросульфоалюминаты кальция занимают объем, в два с половиной раза больший, чем исходный алюминат кальция. В результате появляются внутренние напряжения, которые могут превысить предел прочности бетона при растяжении и тем самым вызвать появление трещин
Результатом этого вида коррозии иногда бывают образования на поверхности бетона пузырей - явление местного расслаивания. Оно состоит в том, что от бетона начинают отскакивать плоские круглые осколки
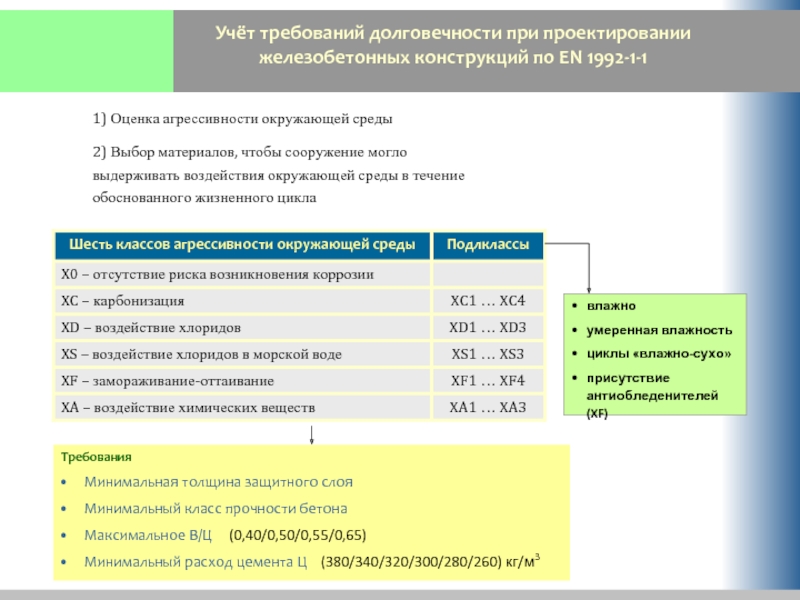
Слайд 55Учёт требований долговечности при проектировании железобетонных конструкций по EN 1992-1-1
1) Оценка
2) Выбор материалов, чтобы сооружение могло выдерживать воздействия окружающей среды в течение обоснованного жизненного цикла
влажно
умеренная влажность
циклы «влажно-сухо»
присутствие антиобледенителей (XF)
Требования
Минимальная толщина защитного слоя
Минимальный класс прочности бетона
Максимальное В/Ц (0,40/0,50/0,55/0,65)
Минимальный расход цемента Ц (380/340/320/300/280/260) кг/м3
Слайд 57Минимальный защитный слой по EN 1992-1-1
П.4.1 (4) Защита арматуры от коррозии
Слайд 74Уменьшение глубины опирания ребра плиты перекрытия с разрушением бетона, не заполнены
Несоблюдение проектных температурно-влажностных условий эксплуатации, неудовлетворительное состояние кровли