- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Физико-химические методы анализа. Хроматография презентация
Содержание
- 1. Физико-химические методы анализа. Хроматография
- 2. Аналитическая химия - 1 План лекций
- 3. Аналитическая химия - 1 Рекомендуемые учебники
- 4. Аналитическая химия - 1 УНИВЕРСАЛЬНОСТЬ, ЭКСПРЕССНОСТЬ, ЧУВСТВИТЕЛЬНОСТЬ
- 5. Аналитическая химия - 1 Основные понятия Хроматография
- 6. Аналитическая химия - 1 Основные понятия НФ:
- 7. Аналитическая химия - 1 Хроматограмма – внутренняя
- 8. Аналитическая химия - 1 Классификация По способу
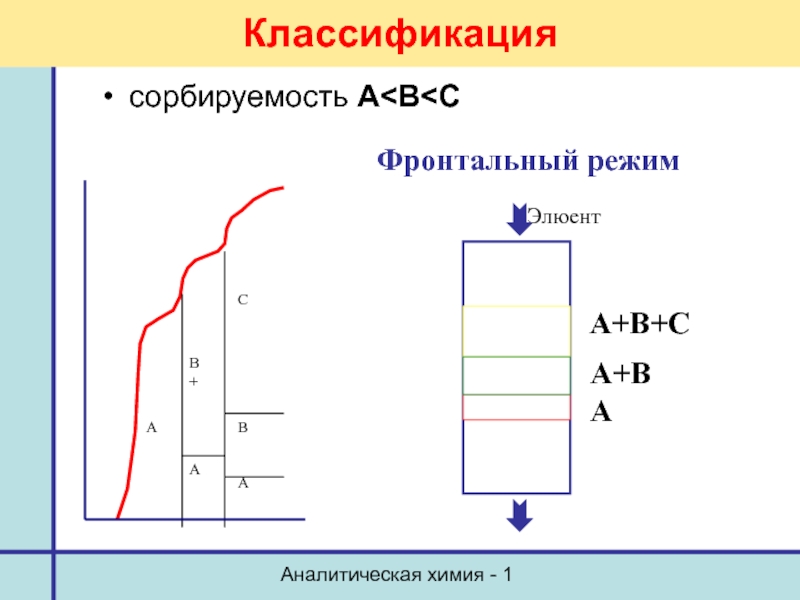
- 9. Аналитическая химия - 1 Классификация сорбируемость А
- 10. Аналитическая химия - 1 Классификация сорбируемость А
- 11. Аналитическая химия - 1 Классификация сорбируемость А
- 12. Аналитическая химия - 1 Классификация По природе
- 13. Аналитическая химия - 1 Классификация По природе
- 14. Аналитическая химия - 1 Классификация По технике
- 15. Аналитическая химия - 1 Классификация По цели
- 16. Аналитическая химия - 1 Классификация По агрегатному состоянию ПФ и НФ
- 17. Аналитическая химия - 1 История 1903 -
- 18. Аналитическая химия - 1 Общие принципы хроматографического
- 19. Аналитическая химия - 1 Хроматографические параметры Хроматограмма
- 20. Аналитическая химия - 1 Хроматографические параметры Время
- 21. Аналитическая химия - 1 Хроматографические параметры Удерживаемый
- 22. Аналитическая химия - 1 Хроматографические параметры Коэффициент
- 23. Аналитическая химия - 1 Хроматографические параметры Коэффициент
- 24. Аналитическая химия - 1 ЭФФЕКТИВНОСТЬ Теоретическая тарелка
- 25. Аналитическая химия - 1 Эффективность и селективность
- 26. Аналитическая химия - 1 Разделение пиков
- 27. Аналитическая химия - 1 Эффективность и селективность
- 28. Аналитическая химия - 1 Эффективность и селективность 1 2 3
- 29. Аналитическая химия - 1 Качественный анализ Времена
- 30. Аналитическая химия - 1 Качественный анализ Индекс
- 31. Аналитическая химия - 1 Качественный анализ Индекс
- 32. Аналитическая химия - 1 Количественный анализ По
- 33. Аналитическая химия - 1 Количественный анализ Методы
- 34. Аналитическая химия - 1 Количественный анализ Градуировка
- 35. Аналитическая химия - 1 Количественный анализ
- 36. Аналитическая химия - 1 Физическая адсорбция.
- 37. Аналитическая химия - 1 Неполярный на неполярном
- 38. Аналитическая химия - 1 Сорбционные свойства
- 39. Аналитическая химия - 1 Теории хроматографии Изотерма
- 40. Аналитическая химия - 1 Теории хроматографии CS CM
- 41. Аналитическая химия - 1 Теории хроматографии ТЕОРИЯ
- 42. Аналитическая химия - 1 Кинетическая теория Кинетические
- 43. Аналитическая химия - 1 Теории хроматографии. Кинетическая
- 44. Аналитическая химия - 1
- 45. Аналитическая химия - 1 КИНЕТИЧЕСКАЯ ТЕОРИЯ vоптим Нmin
Слайд 1Аналитическая химия - 1
Аналитическая химия
II. Физико-химические методы анализа
ХРОМАТОГРАФИЯ
Слайд 2Аналитическая химия - 1
План лекций
Основные понятия
Классификация методов
История
Хроматографические
Теоретические основы
Основные виды хроматографии
Слайд 3Аналитическая химия - 1
Рекомендуемые учебники
КАЗАНСКИЙ (ПРИВОЛЖСКИЙ) ФЕДЕРАЛЬНЫЙ УНИВЕРСИТЕТ
------------------------------------------------
Химический институт им.А.М.Бутлерова
ОСНОВЫ
Стойков И.И., Стойкова Е.Е.
Казань – 2010
Слайд 5Аналитическая химия - 1
Основные понятия
Хроматография (Х) – динамический метод разделения и
……. основанный на различии между константами равновесия распределения компонентов разделяемой смеси между НФ с большой удельной поверхностью и ПФ, которая протекает через неподвижную.
Слайд 6Аналитическая химия - 1
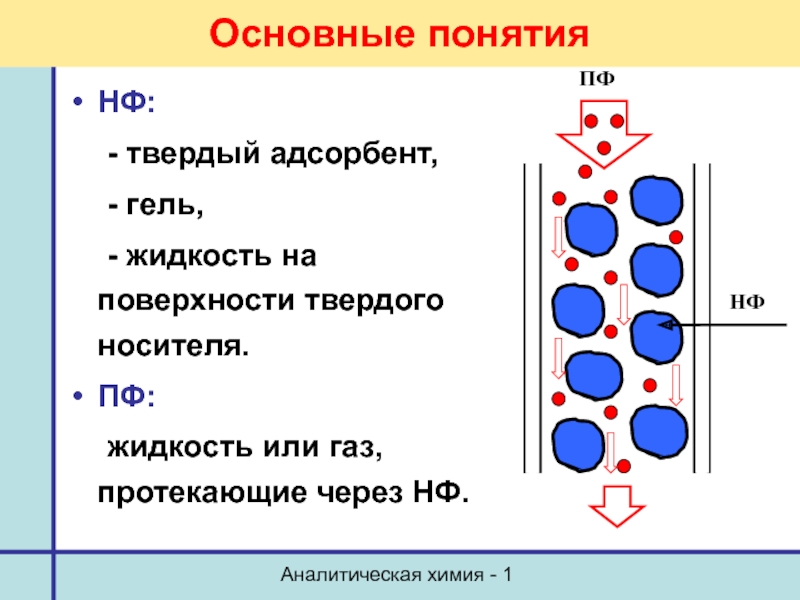
Основные понятия
НФ:
- твердый адсорбент,
- гель,
- жидкость
ПФ:
жидкость или газ, протекающие через НФ.
Слайд 7Аналитическая химия - 1
Хроматограмма – внутренняя (полосы вдоль колонки) и внешняя
Сорбат – анализируемая проба в ПФ (сорбент – НФ)
Элюент – ПФ на входе
Элюат – ПФ на выходе
Основные понятия
Слайд 8Аналитическая химия - 1
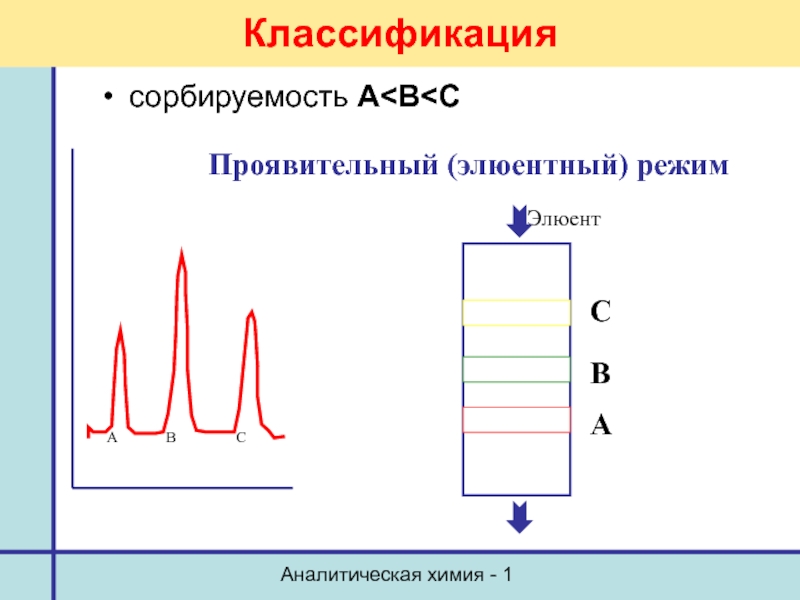
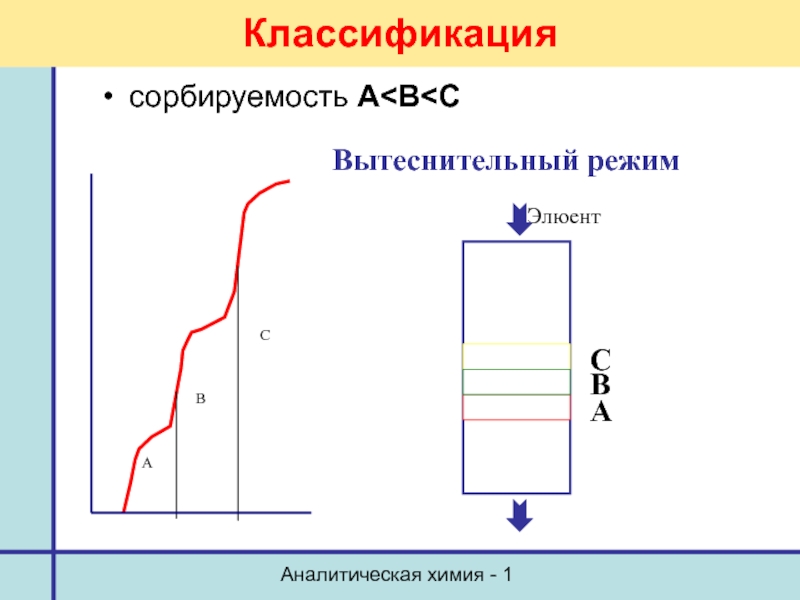
Классификация
По способу перемещения сорбатов вдоль слоя сорбента:
элюентный (проявительный)
вытеснительный
фронтальный
электрохроматография
Слайд 12Аналитическая химия - 1
Классификация
По природе процесса, обусловливающего
распределение сорбатов между ПФ и
Адсорбционная - разделение основано на различии в адсорбируемости компонентов смеси на данном адсорбенте
Распределительная - ─ // ─ в растворимости сорбатов в ПФ и НФ или на различии в стабильности образующихся комплексов
Ионообменная - ─ // ─ констант ионообменного равновесия
Осадочная - ─ // ─ в растворимости осадков в ПФ
Эксклюзионная - ─ // ─ в проницаемости молекул разделяемых веществ в НФ и обусловлено размерами этих молекул
Аффинная - разделение основано на биоспецифическом взаимодействии компонентов с аффинным лигандом
Слайд 13Аналитическая химия - 1
Классификация
По природе исследуемых объектов:
молекулярная
ионная (ионообменная)
хроматография надмолекулярных
Слайд 14Аналитическая химия - 1
Классификация
По технике выполнения:
колоночная
препаративная
насадочная
капиллярная
плоскостная
бумажная
тонкослойная
Слайд 15Аналитическая химия - 1
Классификация
По цели хроматографирования:
аналитическая - качественный и
количественный анализ
неаналитическая
физико-химических характеристик
веществ на основании
хроматографических параметров удерживания
препаративная - для получения особо чистых веществ,
для выделения и концентрирования
микропримесей
промышленная - для автоматического
контроля и управления
производственным процессом
Слайд 17Аналитическая химия - 1
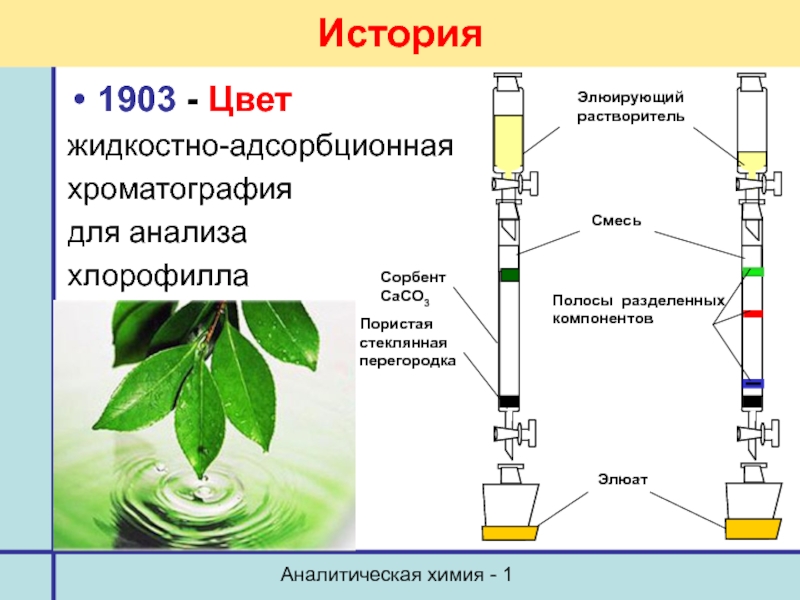
История
1903 - Цвет
жидкостно-адсорбционная
хроматография
для анализа
хлорофилла
Элюирующий растворитель
Полосы
Пористая стеклянная перегородка
Сорбент
CaCO3
Смесь
Элюат
Слайд 18Аналитическая химия - 1
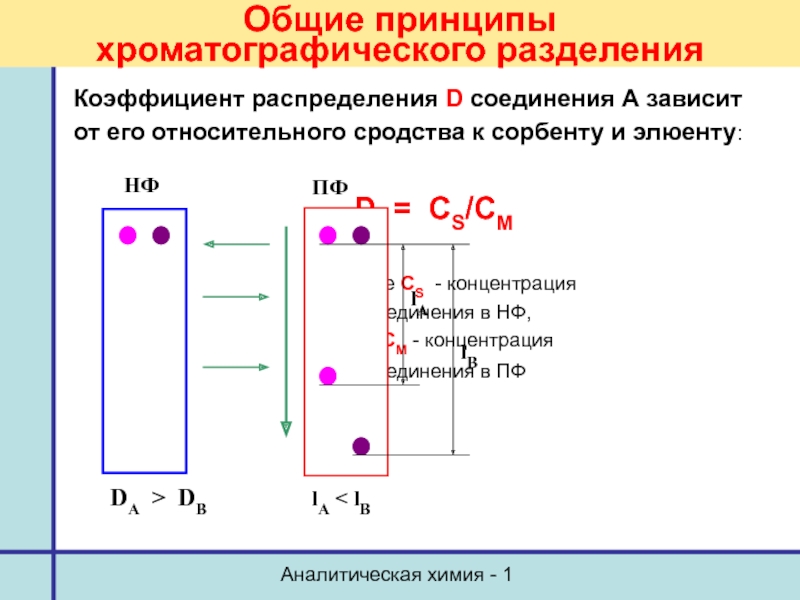
Общие принципы хроматографического разделения
Коэффициент распределения D соединения А
от его относительного сродства к сорбенту и элюенту:
D = CS/CМ
где CS - концентрация
соединения в НФ,
а CM - концентрация
соединения в ПФ
Слайд 19Аналитическая химия - 1
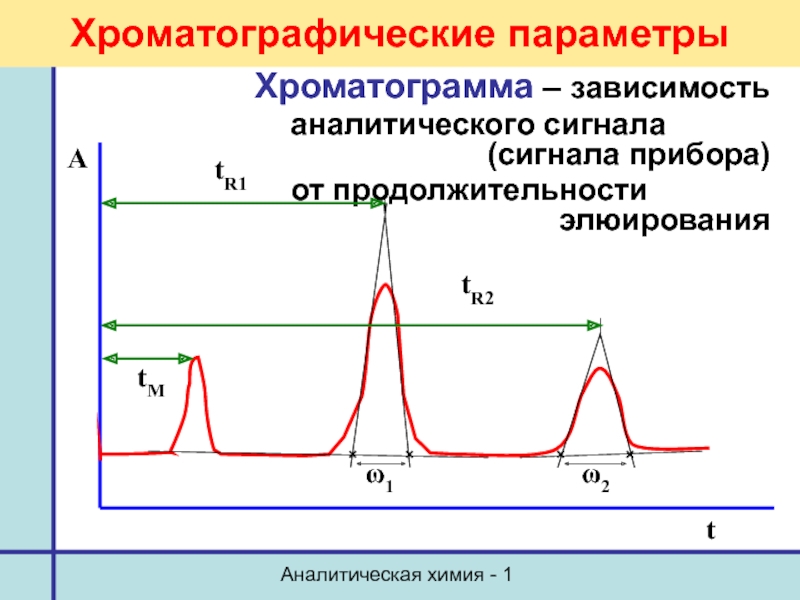
Хроматографические параметры
Хроматограмма – зависимость
аналитического сигнала (сигнала прибора)
от
Слайд 20Аналитическая химия - 1
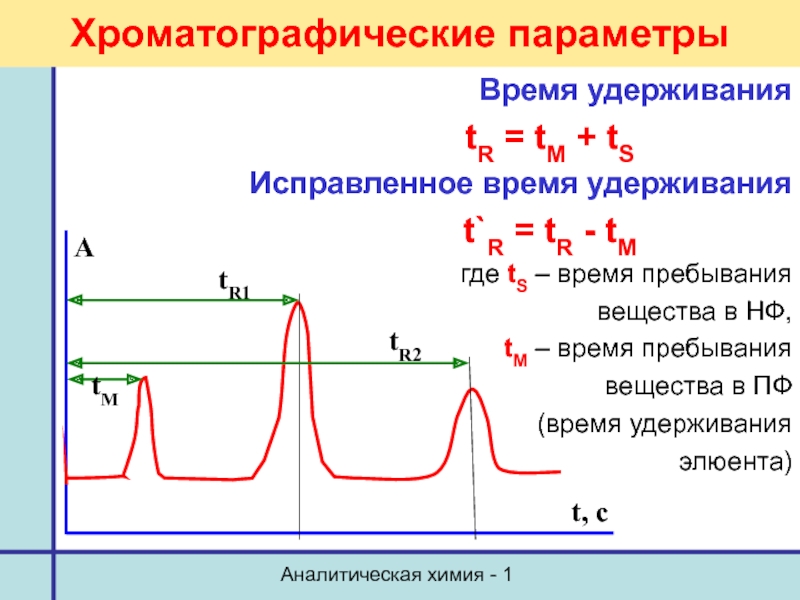
Хроматографические параметры
Время удерживания
tR = tM + tS
Исправленное
t`R = tR - tM
где tS – время пребывания
вещества в НФ,
tM – время пребывания
вещества в ПФ
(время удерживания
элюента)
Слайд 21Аналитическая химия - 1
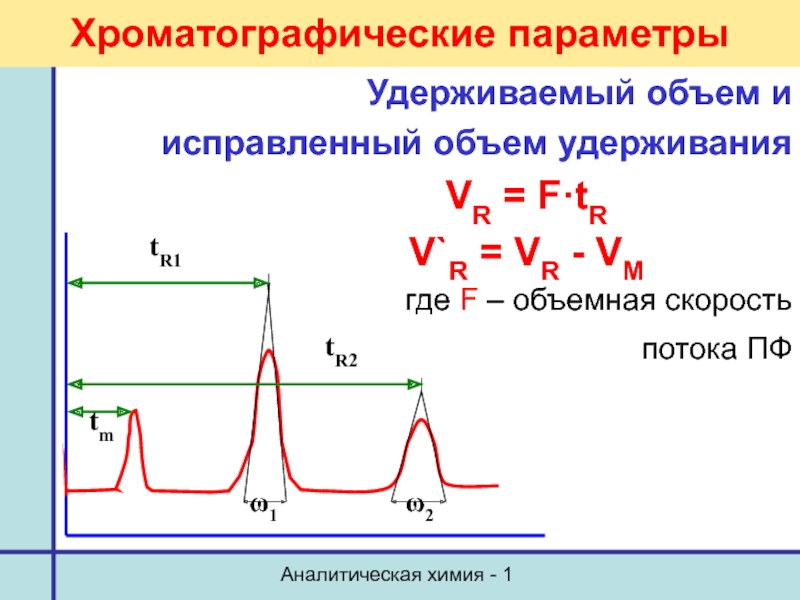
Хроматографические параметры
Удерживаемый объем и
исправленный объем удерживания
V`R = VR - VМ
где F – объемная скорость
потока ПФ
Слайд 22Аналитическая химия - 1
Хроматографические параметры
Коэффициент удерживания (замедления)
R = tM/tR = 1/(1+
Слайд 23Аналитическая химия - 1
Хроматографические параметры
Коэффициент ёмкости
k` = t`R/tM = DVS/VM
1.5 < k` < 4
Слайд 25Аналитическая химия - 1
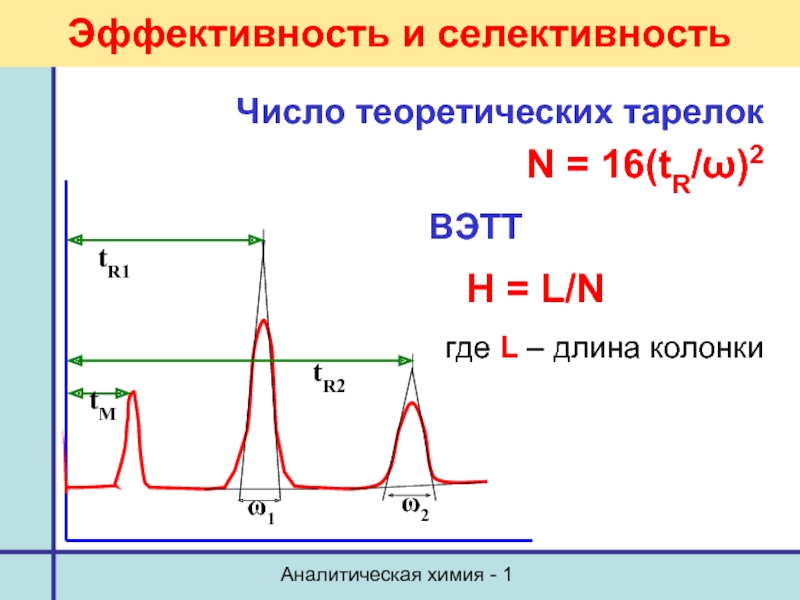
Эффективность и селективность
Число теоретических тарелок
N = 16(tR/ω)2
ВЭТТ
Н = L/N
где L – длина колонки
Слайд 26Аналитическая химия - 1
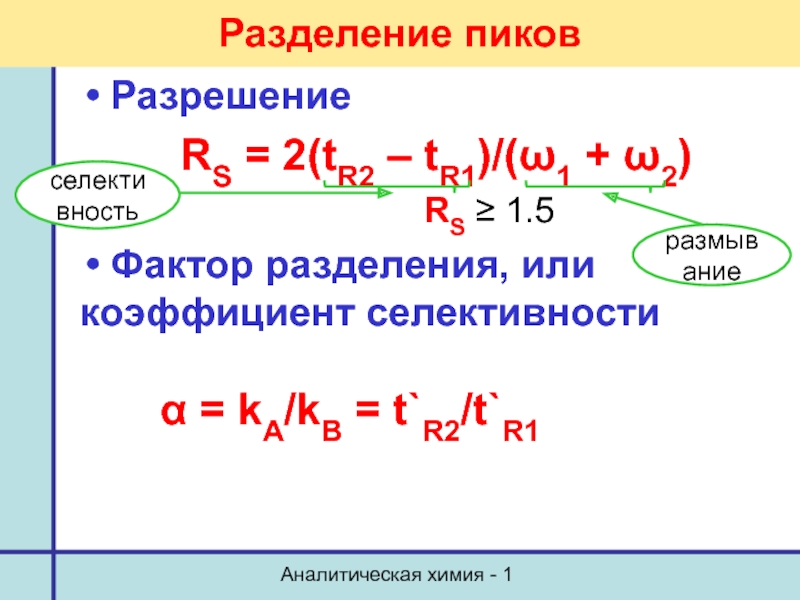
Разделение пиков
Разрешение
RS = 2(tR2 – tR1)/(ω1 +
RS ≥ 1.5
Фактор разделения, или
коэффициент селективности
α = kА/kB = t`R2/t`R1
селективность
размывание
Слайд 27Аналитическая химия - 1
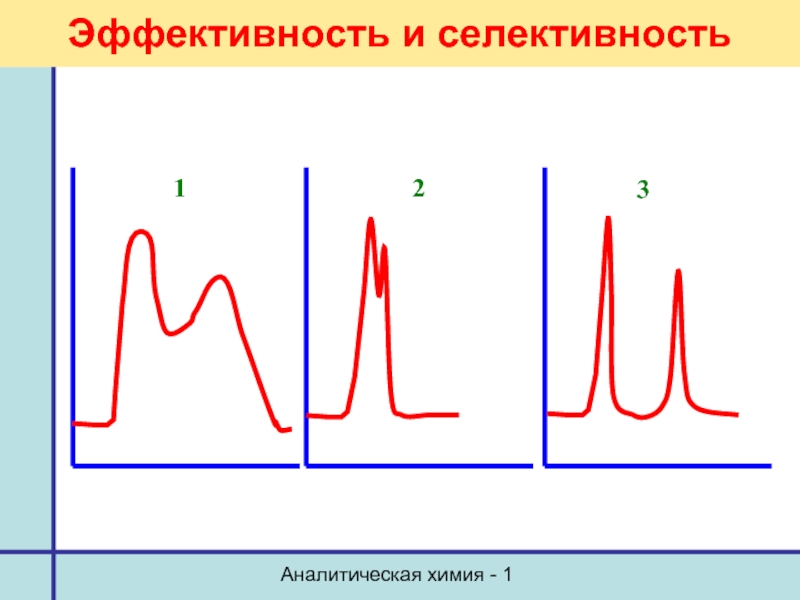
Эффективность и селективность
Зависимость разрешения от коэффициента ёмкости, селективности
RS = 0.25√N[(α – 1)/α][k'/(1 + k')]
Необходимое для разделения число теоретических тарелок
N = 16RS2[(1 + k')/k']2[α/(α – 1)]2
Слайд 29Аналитическая химия - 1
Качественный анализ
Времена удерживания
Корреляционные зависимости параметров удерживания
-
- зависимости времён удерживания на колонках с разными НФ
- индекс удерживания Ковача
Слайд 30Аналитическая химия - 1
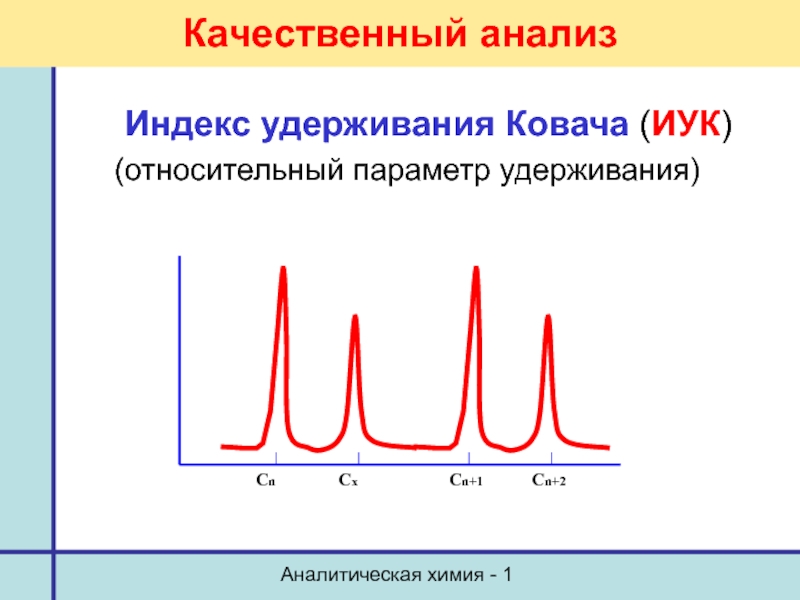
Качественный анализ
Индекс удерживания Ковача (ИУК)
(относительный
Слайд 31Аналитическая химия - 1
Качественный анализ
Индекс удерживания Ковача (ИУК)
In = 100n
t`Rn
(lgt`Rx – lgt`Rn)
Ix = 100n + 100 ————————
(lgt`R(n+1) – lgt`Rn)
Слайд 32Аналитическая химия - 1
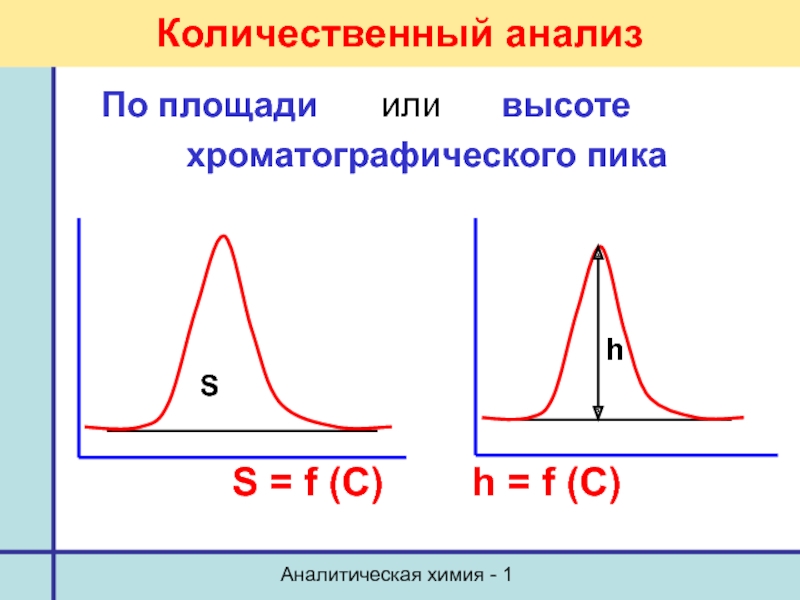
Количественный анализ
По площади или высоте
хроматографического пика
S = f
Слайд 33Аналитическая химия - 1
Количественный анализ
Методы количественного анализа
Метод нормировки
Метод абсолютной калибровки
Метод внутреннего стандарта
Слайд 34Аналитическая химия - 1
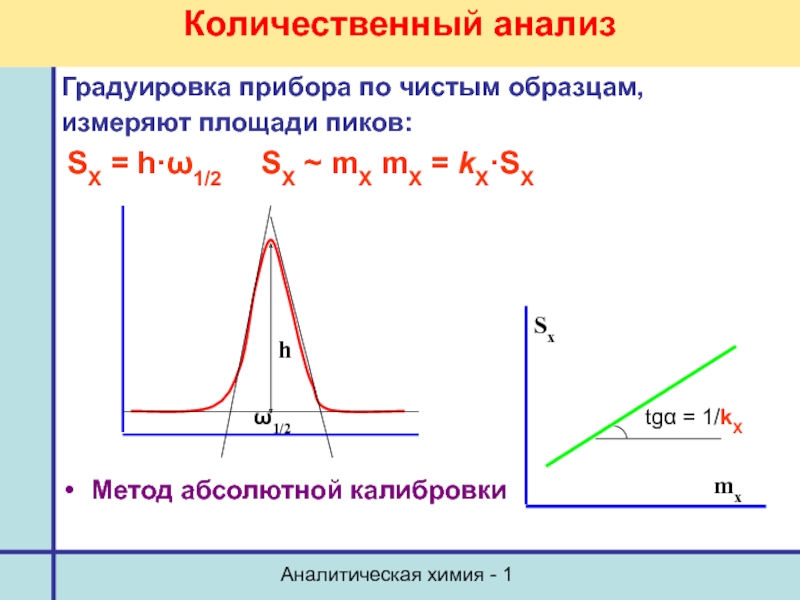
Количественный анализ
Градуировка прибора по чистым образцам,
измеряют площади пиков:
SX = h·ω1/2 SX ~ mX mX = kX·SX
Метод абсолютной калибровки
Слайд 35Аналитическая химия - 1
Количественный анализ
Метод внутренней нормализации (нормировки)
Х% = 100·SX/ST
Метод
mX = kX·SX mX/mM = KX·SX/SM, KX = kX/kМ
mМ = kМ·SМ mX = mM·KX·SX/SM
Слайд 36Аналитическая химия - 1
Физическая адсорбция.
Происходит за счет
- водородных связей,
- электростатических взаимодействий.
Характеризуется:
- большой скоростью,
- обратимостью,
- уменьшением количества поглощенного
адсорбата с повышением температуры.
Теории хроматографии. Сорбция.
Слайд 37Аналитическая химия - 1
Неполярный на неполярном – за счет дисперсионных сил
Полярный на неполярном (и наоборот) – за счет индукционных взаимодействий
Полярный на полярном – за счет ориентационных диполь-дипольных взаимодействий или водородного связывания
Теории хроматографии. Сорбция.
Слайд 38Аналитическая химия - 1
Сорбционные свойства сорбента
зависят от:
- удельной поверхности,
- пористости,
- структуры пор,
- природы сорбента и среды, из которой происходит сорбция
Теории хроматографии. Сорбция.
Слайд 39Аналитическая химия - 1
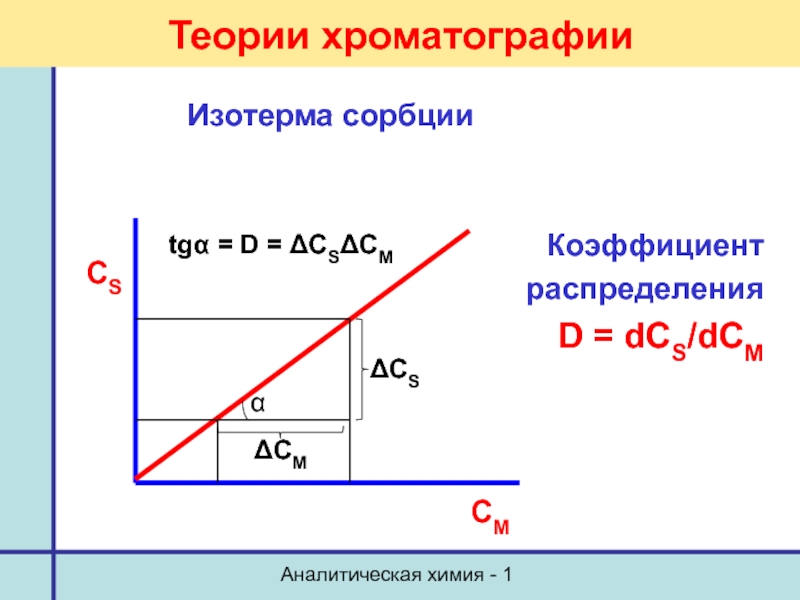
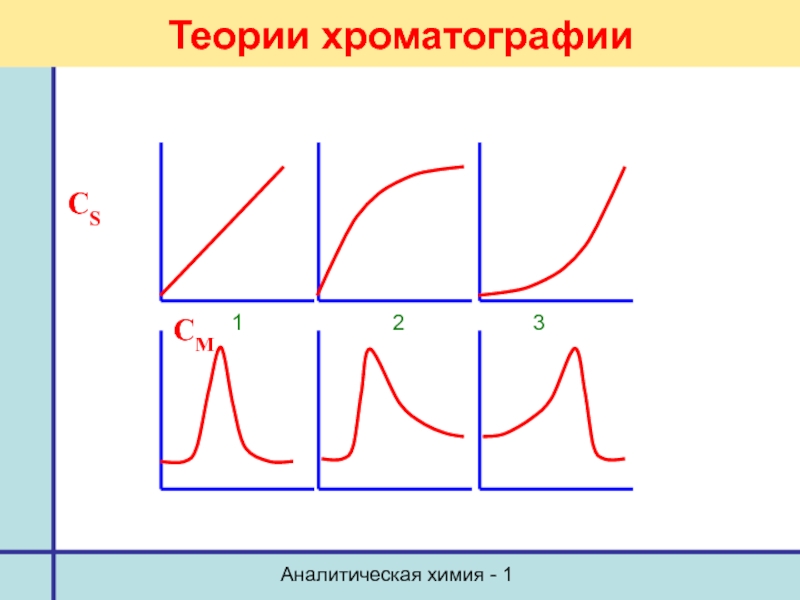
Теории хроматографии
Изотерма сорбции
Коэффициент
распределения
D = dCS/dCM
tgα =
CS
CM
ΔCM
ΔCS
α
Слайд 41Аналитическая химия - 1
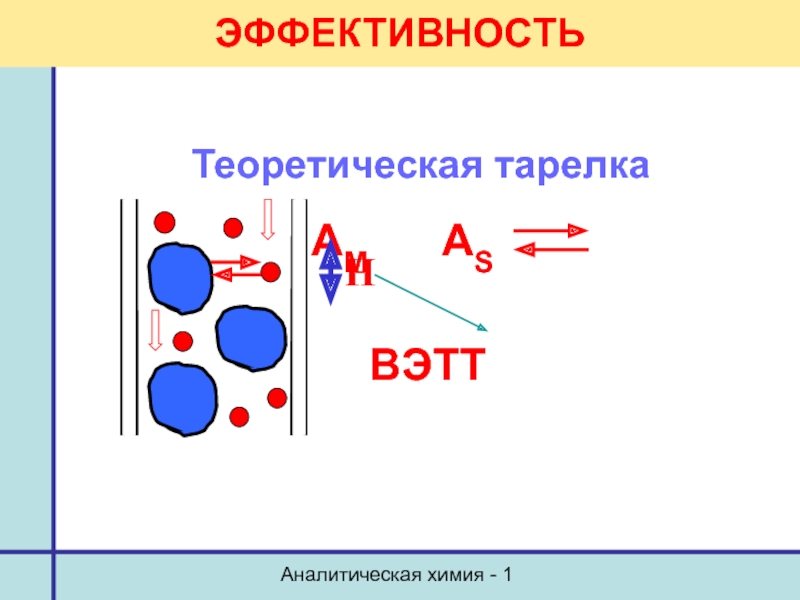
Теории хроматографии
ТЕОРИЯ ТЕОРЕТИЧЕСКИХ ТАРЕЛОК
- колонка состоит из определенного
- равновесие на каждой ТТ считается достигнутым до того, как ПФ переместится на следующую ТТ (т.е. мгновенно)
- на каждой ТТ число сорбируемых частиц веществ < числа сорбируемых частиц элюента
- все процессы в колонке независимы друг от друга
Слайд 42Аналитическая химия - 1
Кинетическая теория
Кинетические параметры:
- объемная скорость
- диаметр частиц сорбента,
- геометрия частиц,
- коэффициент диффузии.
Теории хроматографии
Слайд 43Аналитическая химия - 1
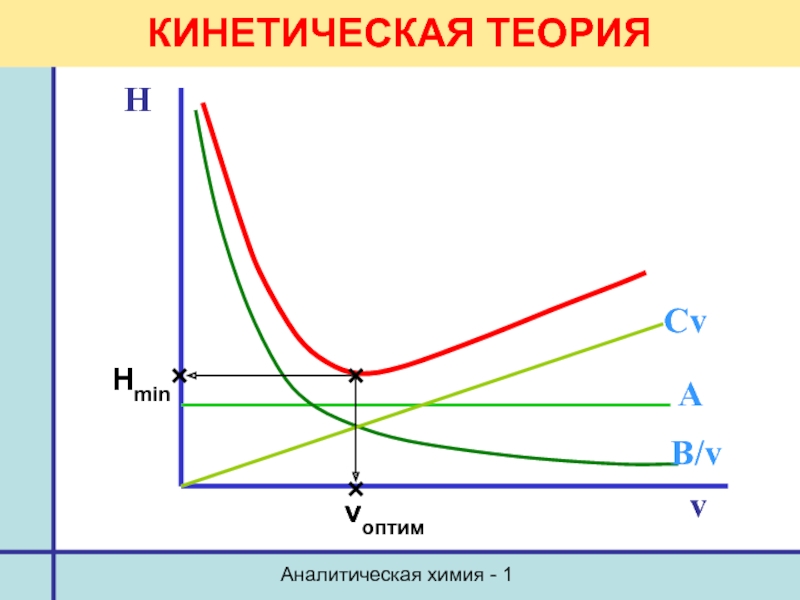
Теории хроматографии. Кинетическая
Уравнение Ван-Деемтера
H = A
где А –вихревая диффузия,
B/v – молекулярная диффузия,
Cv – отклонение от сорбционного равновесия (сопротивление массопереносу),
v – скорость потока
Слайд 44Аналитическая химия - 1
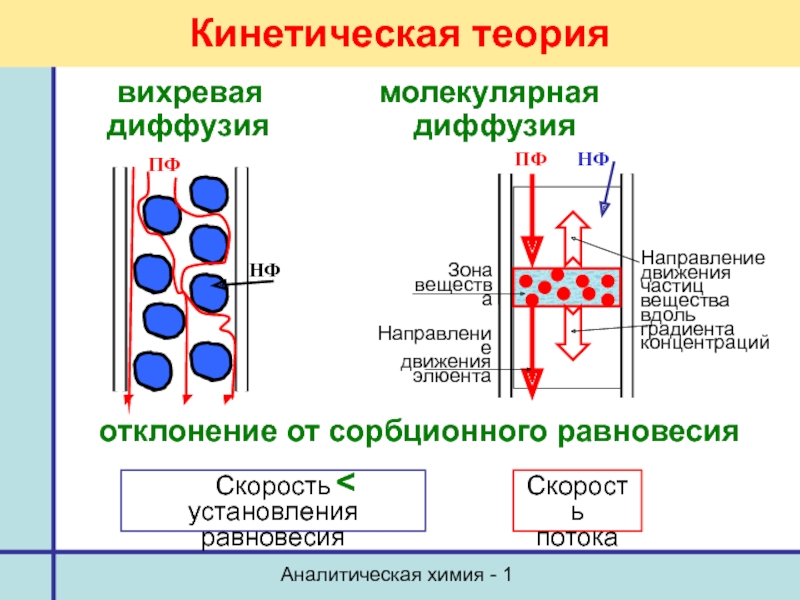
вихревая молекулярная
диффузия диффузия
отклонение от сорбционного равновесия
<
Кинетическая теория
Скорость
установления равновесия
Скорость
потока