- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Биофизика мембранных процессов. Мембранный транспорт презентация
Содержание
- 1. Биофизика мембранных процессов. Мембранный транспорт
- 2. Виды мембранного транспорта (МТ) Мембранный транспорт (МТ)
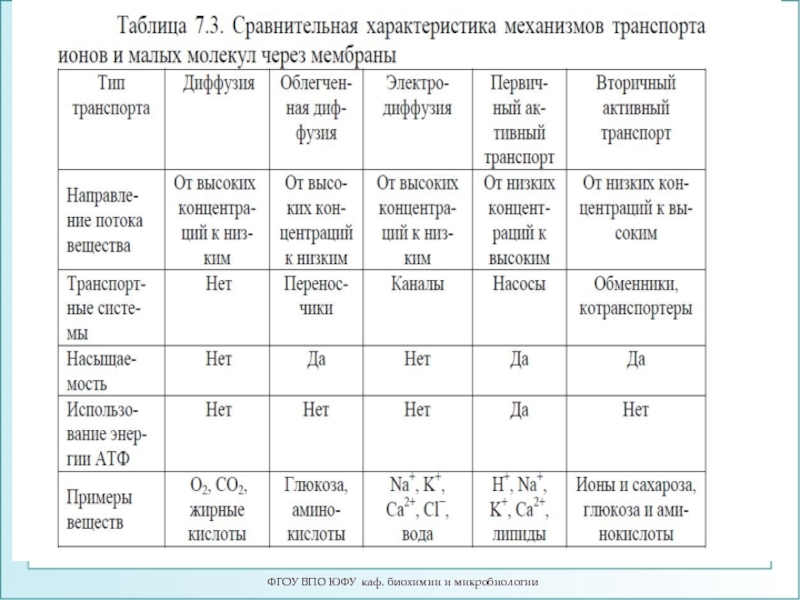
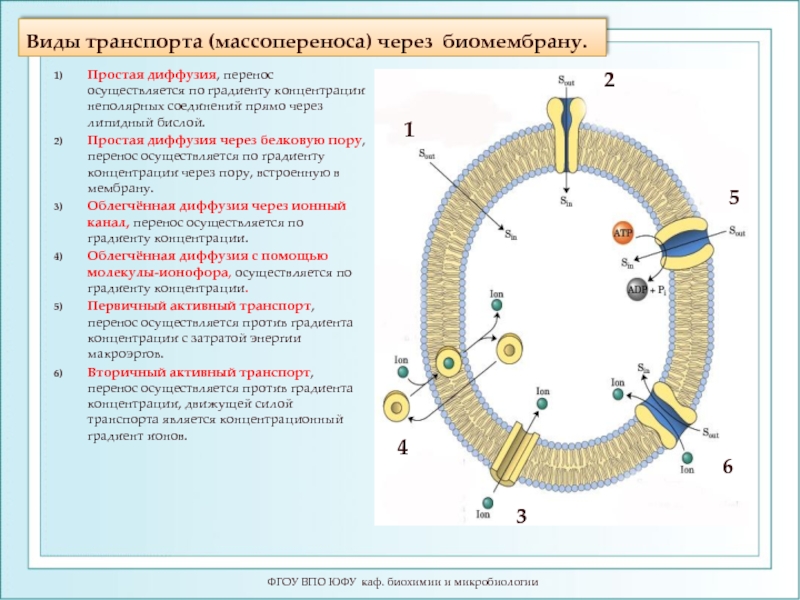
- 3. Виды транспорта (массопереноса) через биомембрану. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
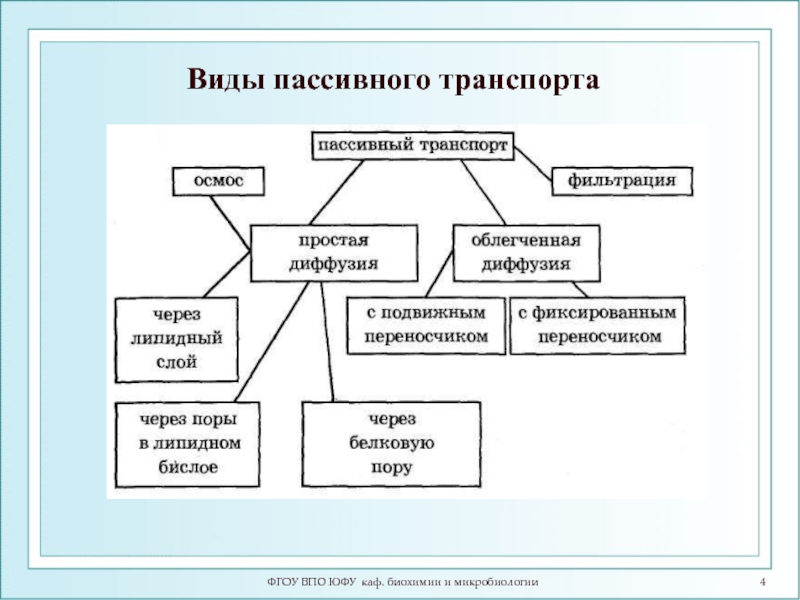
- 4. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии Виды пассивного транспорта
- 5. Энергия пассивного транспорта создается различными градиентами: концентрационным
- 6. Виды пассивного транспорта Диффузия Осмос Фильтрация Облегченная
- 7. Диффузия – это самопроизвольный процесс проникновения
- 8. Простая диффузия описывается уравнением Фика : скорость
- 9. Скорость диффузии - это количество вещества,
- 10. Осмос - движение молекулы воды через
- 11. Уравнение, описывающее осмотический перенос воды. где
- 12. Фильтрация – это движение раствора через
- 13. Фильтрация – движение жидкости через поры
- 14. Уравнение Коллендера-Бернульда описывает транспорт веществ через липидный
- 15. Различные виды транспорта ФГОУ ВПО ЮФУ каф. биохимии и микробиологии Переносчик Канал
- 16. Облегчённая диффузия. ФГОУ ВПО ЮФУ каф.
- 17. Виды мембранного транспорта по направлению и количеству
- 18. Активный транспорт. Виды активного транспорта.
- 19. Активный транспорт: типы насосов (транспортных АТФаз) Семейство
- 20. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
- 21. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии АВС-транспортер, «выкачивающий» липофильные вещества из клетки
- 22. АТФ-синтаза/АТФ-аза: «вальсирующий» комплекс Структура: Две субъединицы: F0
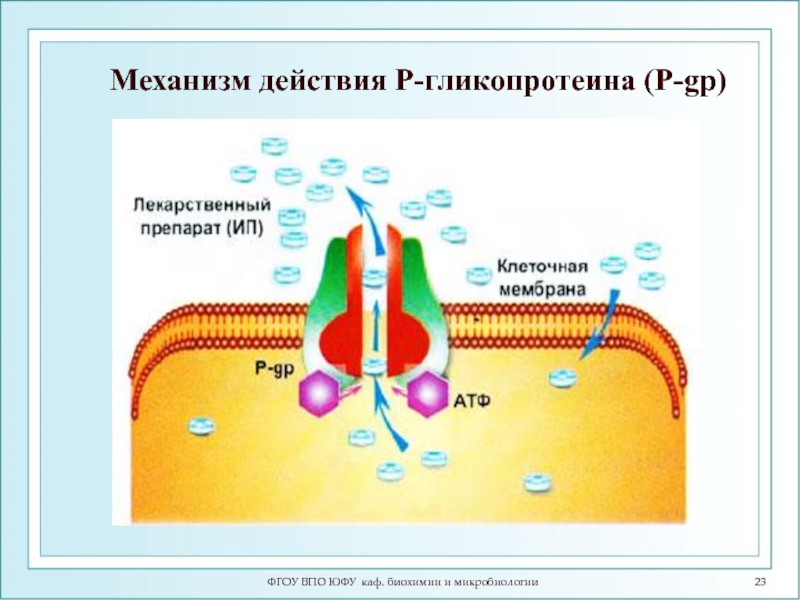
- 23. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии Механизм действия Р-гликопротеина (P-gp)
- 24. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
- 25. Роль онкотического и гидростатического давления в транспорте
- 26. Строение Na+/K+-ATФазы ФГОУ ВПО ЮФУ каф.
- 27. Реакционный цикл Na+/K+-ATФазы ФГОУ ВПО ЮФУ
- 28. Связывание ионов Na+ и K+ в ионных
- 29. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
- 30. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии Биопотенциалы
- 31. Генерация и распространение биоэлектрических потенциалов - важнейшее
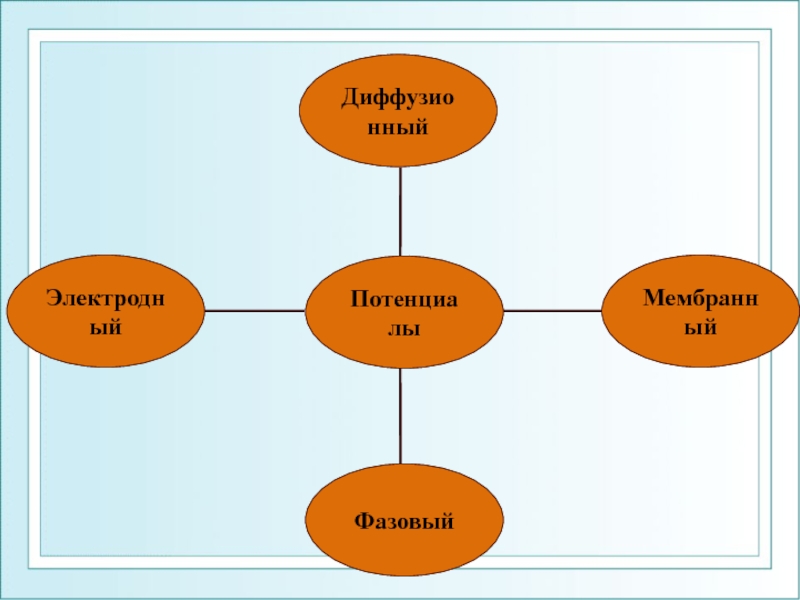
- 32. Для возникновения биопотенциалов решающее значение имеют потенциалы, обусловленные асимметричным, неравномерным распределением ионов.
- 34. Диффузионный потенциал возникает на границе раздела
- 35. Диффузионный потенциал
- 36. Мембранный потенциал возникает на границе раздела
- 37. Мембранный потенциал определяют из уравнения Нернста Где
- 38. Фазовые потенциалы возникают на границе
- 39. Электродный потенциал возникает в результате
- 40. В 1902 году Бернштейном была выдвинута мембранная
- 41. Сущность мембранной теории биопотенциалов
- 42. Мембранным потенциалом называется разность потенциалов между внутренней и наружной поверхностями мембраны.
- 43. Потенциал покоя – стационарная разность электрических потенциалов,
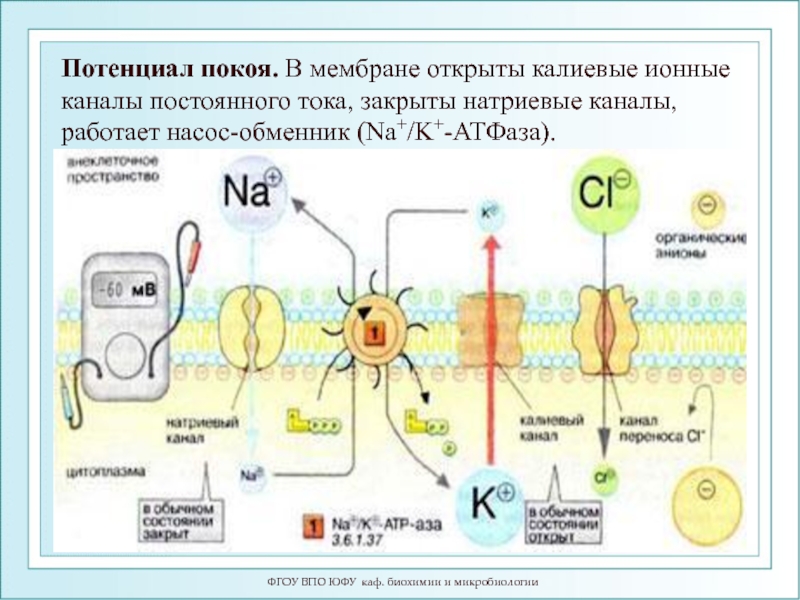
- 44. Потенциал покоя. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
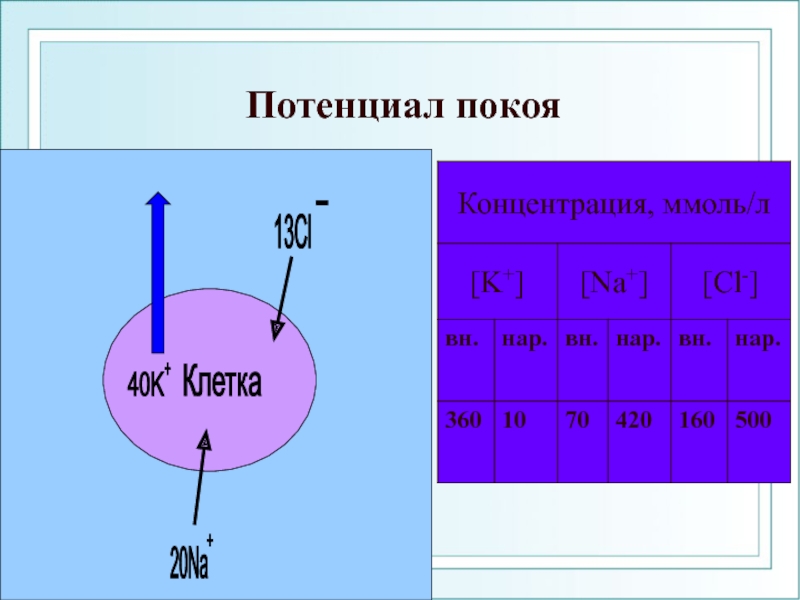
- 45. Потенциал покоя
- 46. При образовании потенциала покоя мембрана внутри заряжена
- 47. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
- 48. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
- 49. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
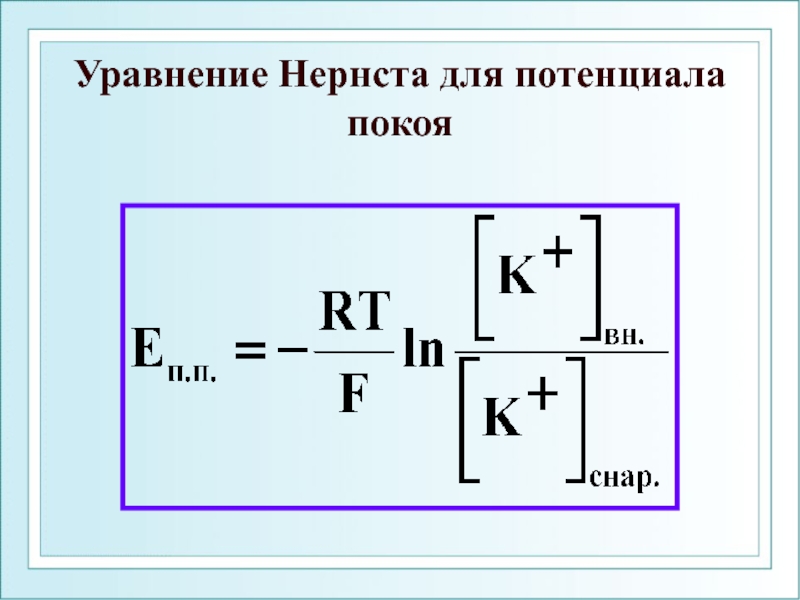
- 50. Уравнение Нернста для потенциала покоя
- 51. Уравнение Гольдмана для потенциала покоя
- 52. Отношение коэффициентов проницаемости для состояния покоя PК
- 53. С учетом работы электрогенных ионных насосов для
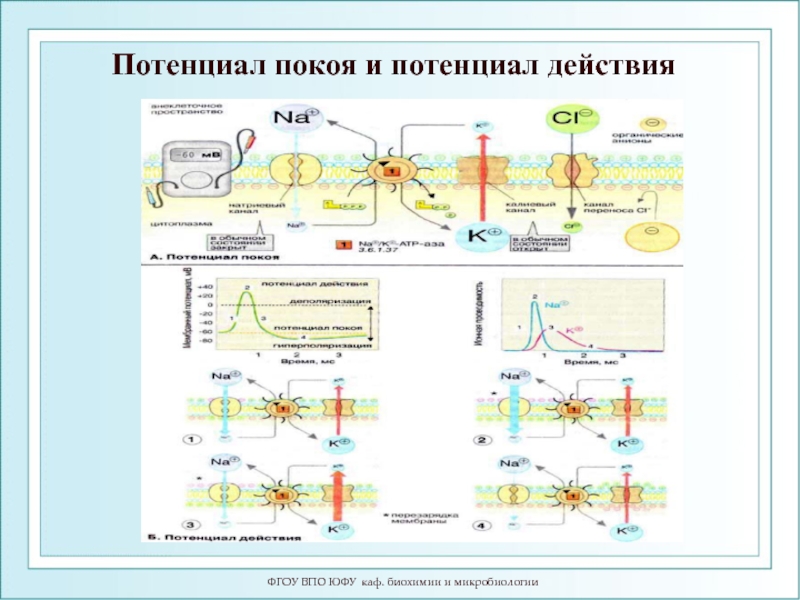
- 54. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии Потенциал покоя и потенциал действия
- 55. Потенциал действия (ПД) – это последовательность изменений,
- 56. Потенциалом действия называется электрический импульс, обусловленный изменением
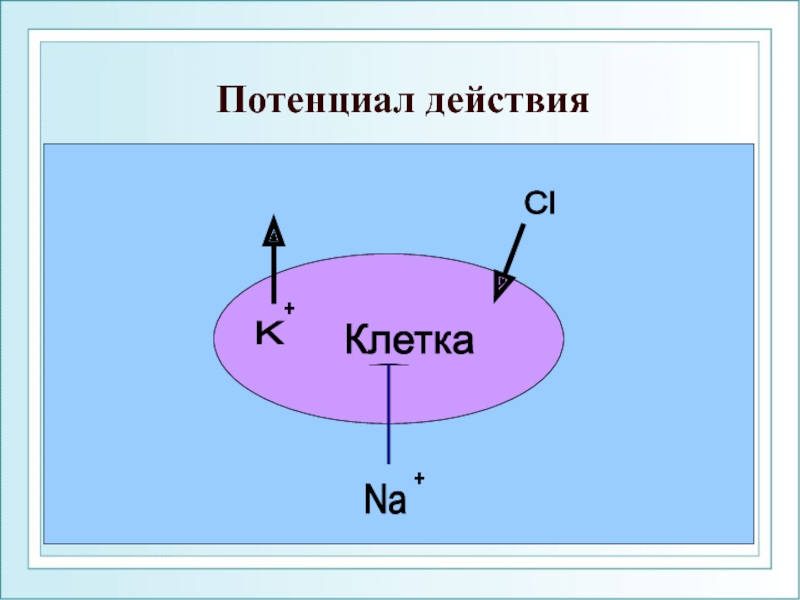
- 57. Потенциал действия
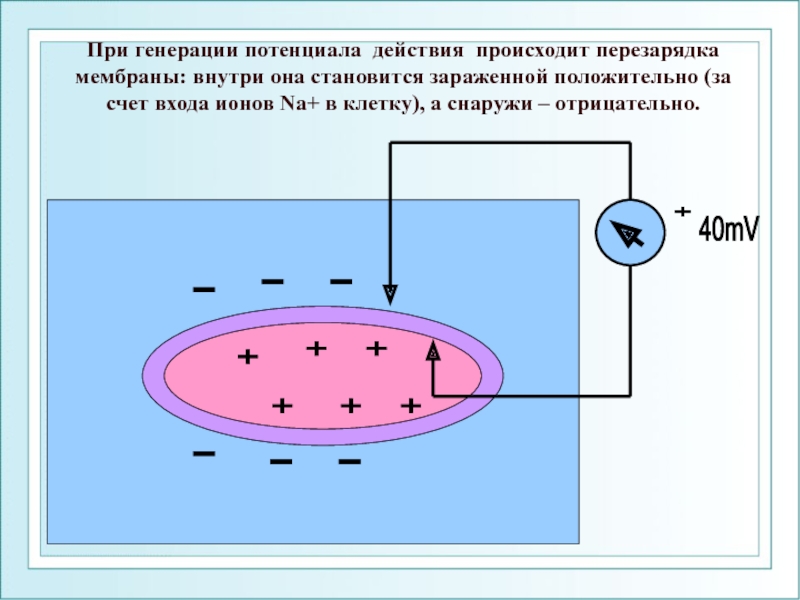
- 58. При генерации потенциала действия происходит перезарядка мембраны:
- 59. Возбудимость – это способность клеток к быстрому
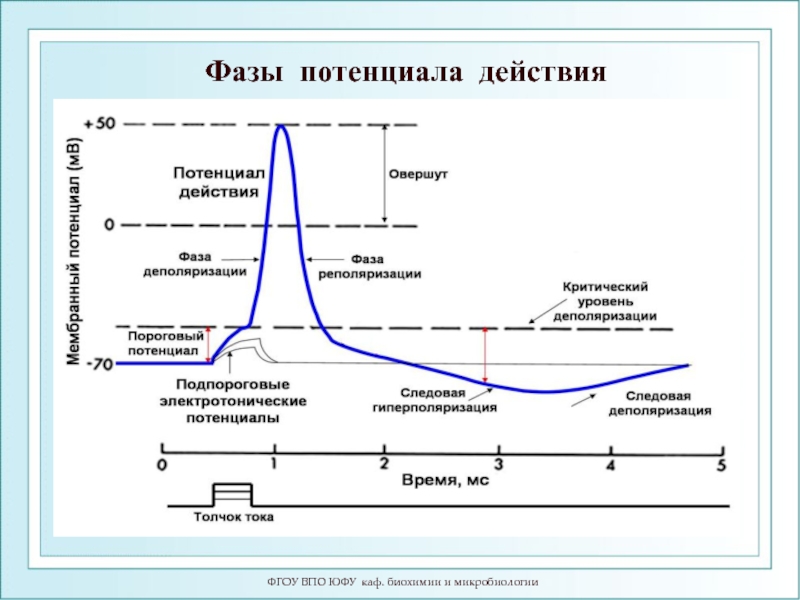
- 60. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии Фазы потенциала действия
- 61. Стимуляция нервной клетки достигает порога возбудимости, необходимого
- 62. Поскольку деполяризация в клетке продолжается, открывается больше
- 63. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
- 64. Физический механизм деполяризации
- 65. Отношение коэффициентов проницаемости ионов для фазы деполяризации
- 66. Физический механизм реполяризации Выход К+ в
- 67. Формирование потенциала действия обусловлено двумя ионными потоками
- 68. МЕХАНИЗМ ВОЗНИКНОВЕНИЯ ПОТЕНЦИАЛА ДЕЙСТВИЯ
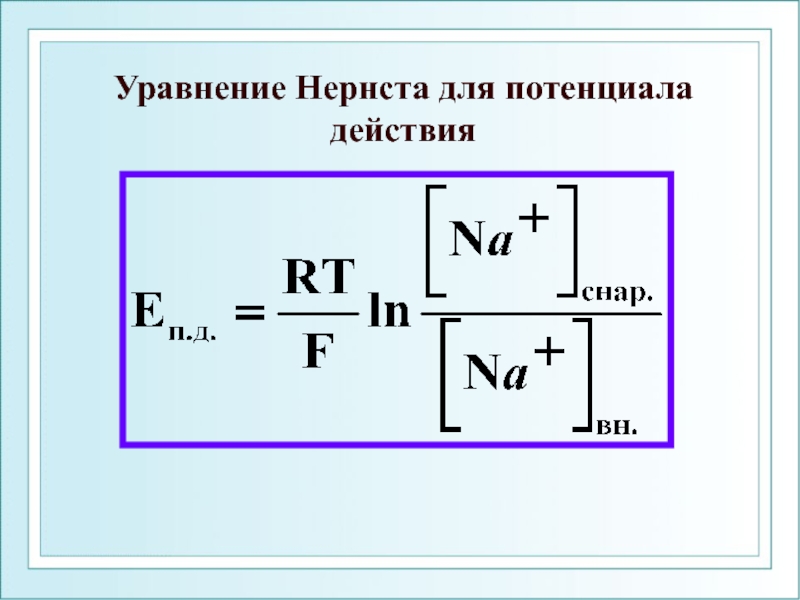
- 69. Уравнение Нернста для потенциала действия
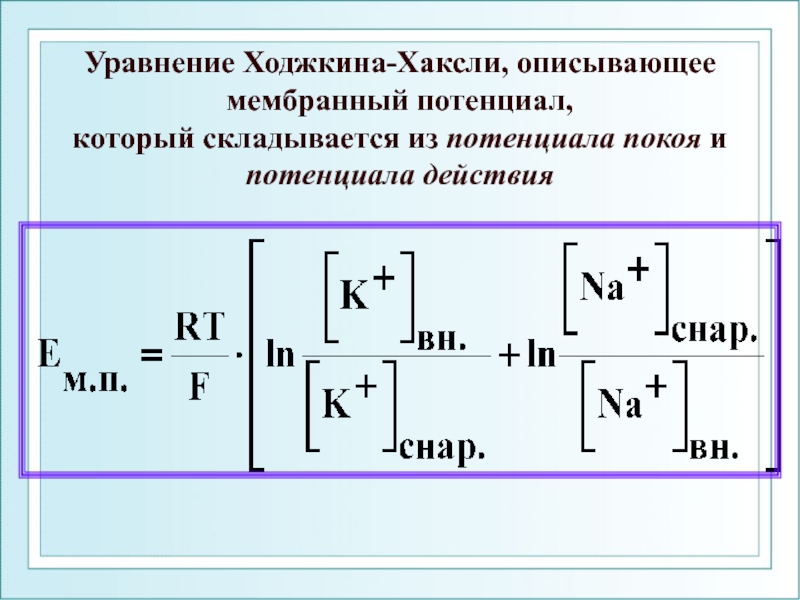
- 70. Уравнение Ходжкина-Хаксли, описывающее мембранный потенциал,
- 71. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии Ионные каналы
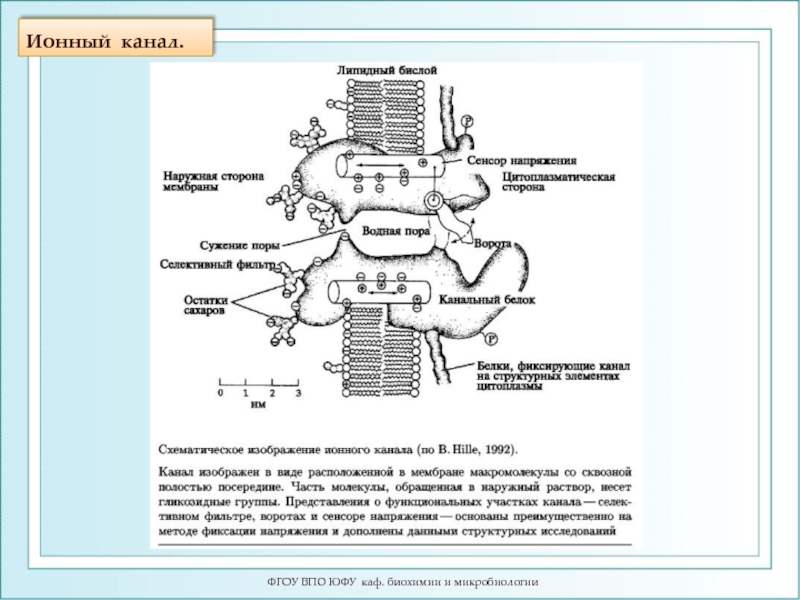
- 72. Ионный канал. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
- 73. Ионный транспорт ФГОУ ВПО ЮФУ каф. биохимии
- 74. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
- 75. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
- 76. Свойства ионных каналов Селективность Независимость работы отдельных
- 77. Свойства ионных каналов 1.Селективность – способность пропускать
- 78. 2.Независимость работы отдельных каналов
- 79. 3.Дискретный характер проводимости
- 80. 4.Зависимость параметров каналов от мембранного потенциала
- 81. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
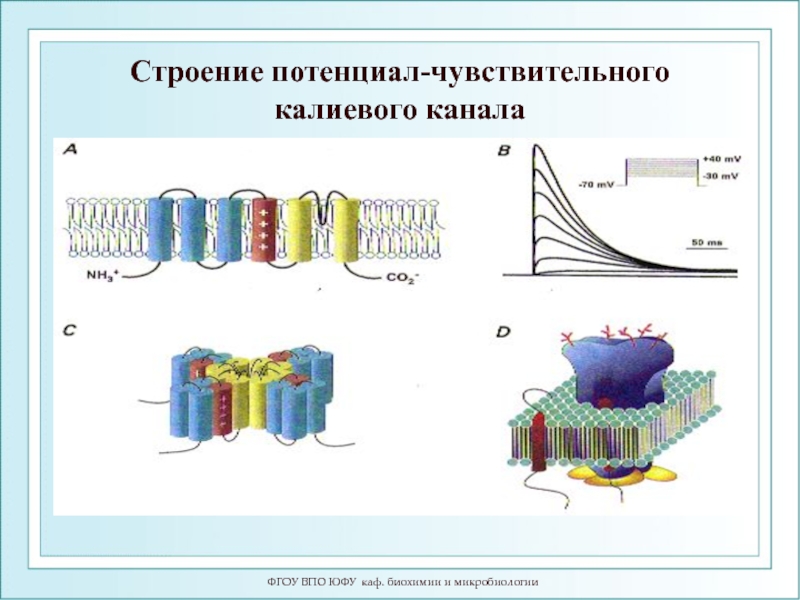
- 82. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии Строение потенциал-чувствительного калиевого канала
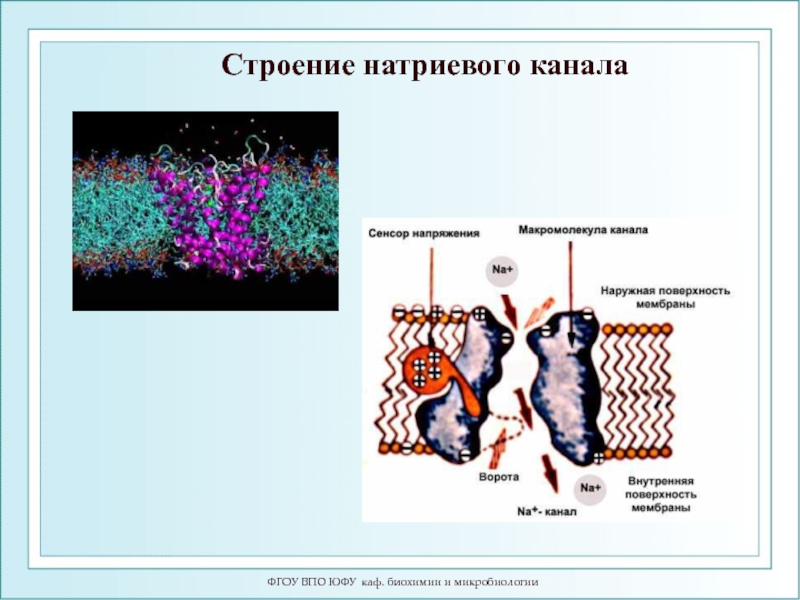
- 83. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии Строение натриевого канала
- 84. Потенциал-чувствительный натриевый канал
- 85. Сравнение параметров ионных каналов ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
- 86. Строение калиевого канала. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
- 87. Энергетические профили ионных каналов. ФГОУ ВПО
- 88. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
- 89. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
- 90. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
- 91. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
- 92. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
- 93. Действие местных анестетиков. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
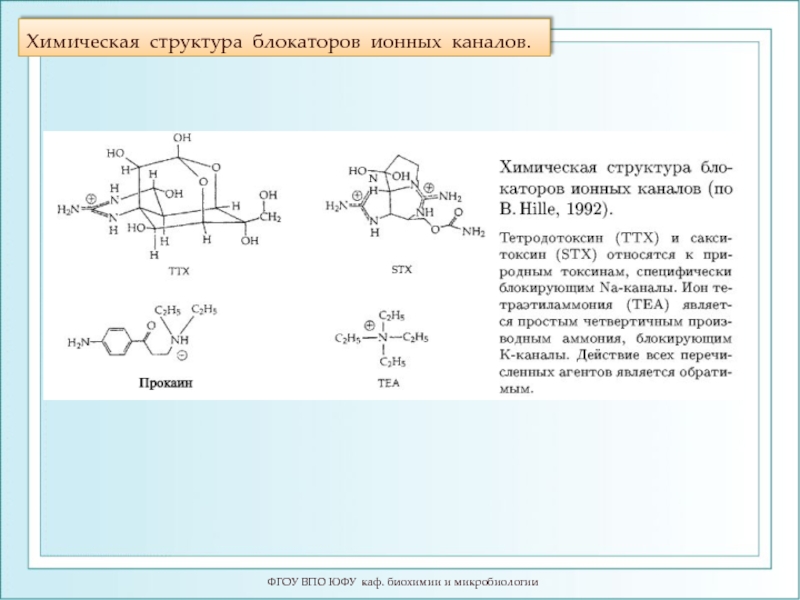
- 94. Химическая структура блокаторов ионных каналов. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
- 95. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
- 96. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
- 97. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
- 98. Индуцированный ионный транспорт осуществляется ионофорами, которые
- 99. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
- 100. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
- 101. Ионофоры. Валиномицин. ФГОУ ВПО ЮФУ
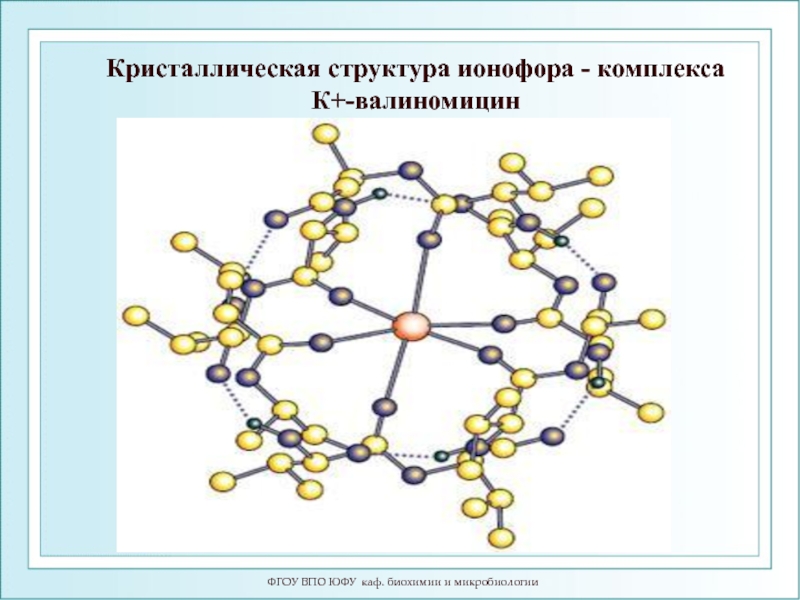
- 102. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии Кристаллическая структура ионофора - комплекса К+-валиномицин
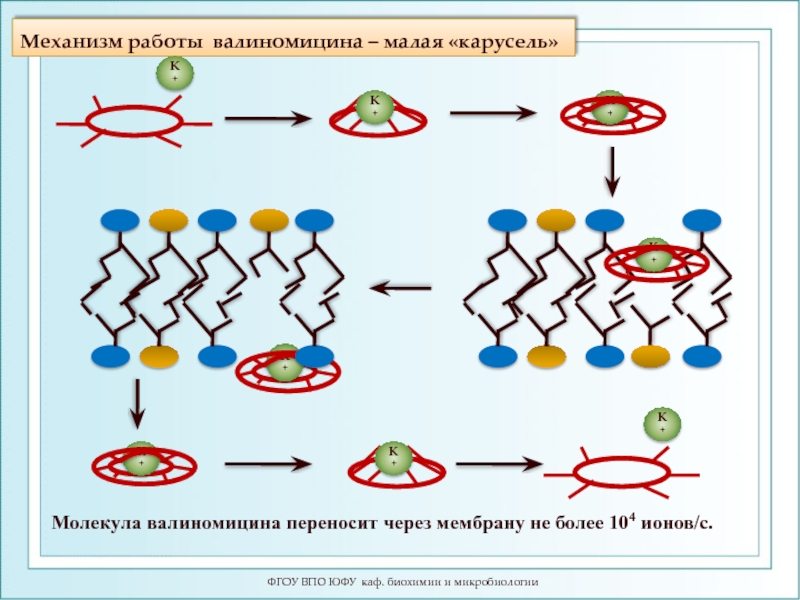
- 103. Механизм работы валиномицина – малая «карусель»
- 104. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
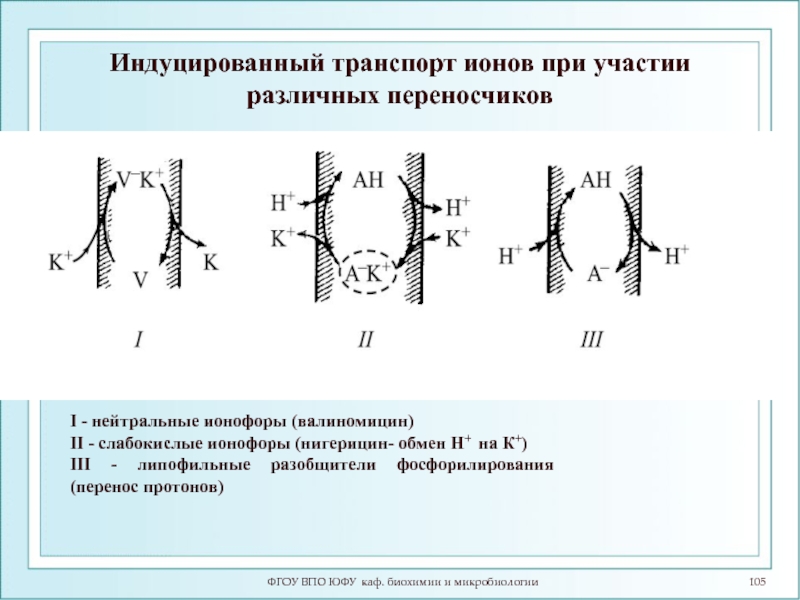
- 105. Индуцированный транспорт ионов при участии различных переносчиков
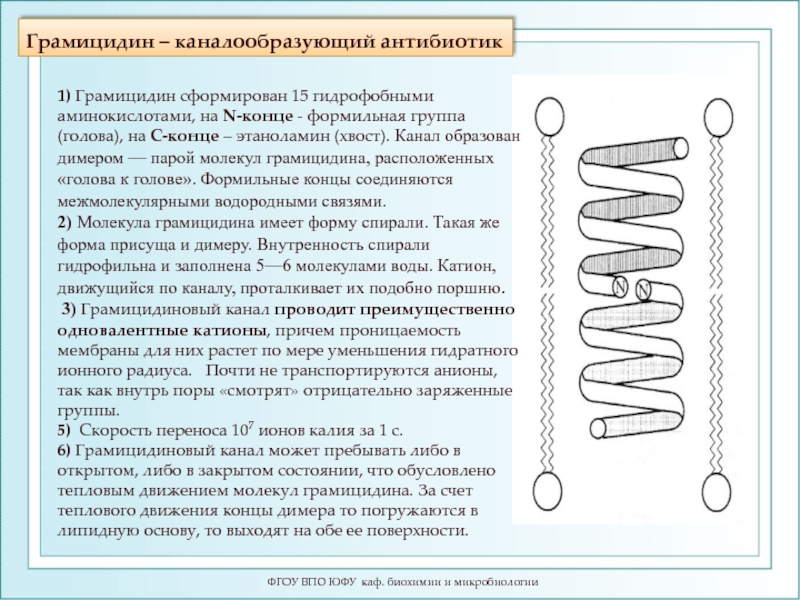
- 106. Грамицидин – каналообразующий антибиотик ФГОУ ВПО
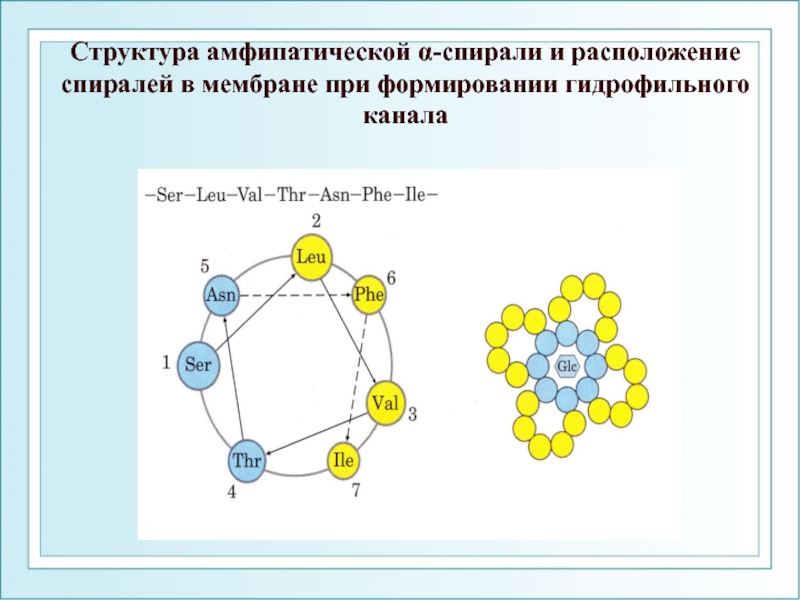
- 107. Структура амфипатической α-спирали и расположение спиралей в мембране при формировании гидрофильного канала
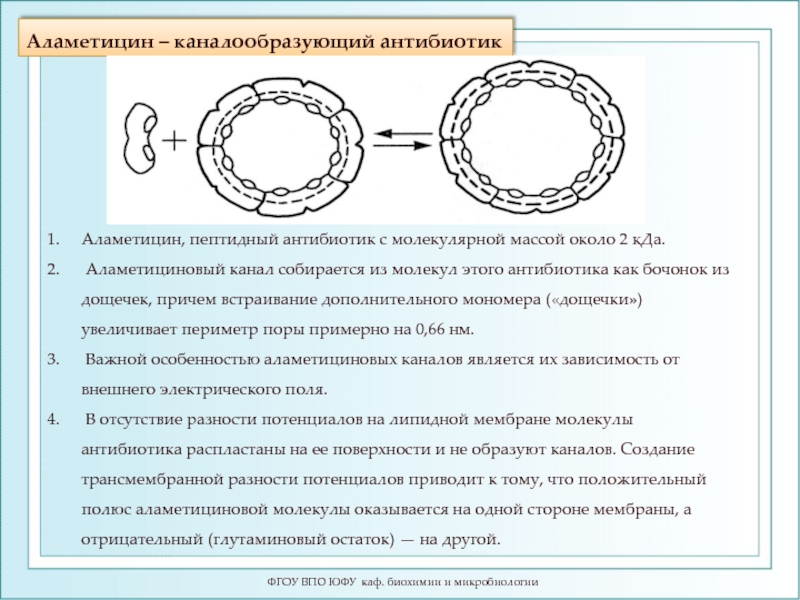
- 108. Аламетицин – каналообразующий антибиотик ФГОУ ВПО
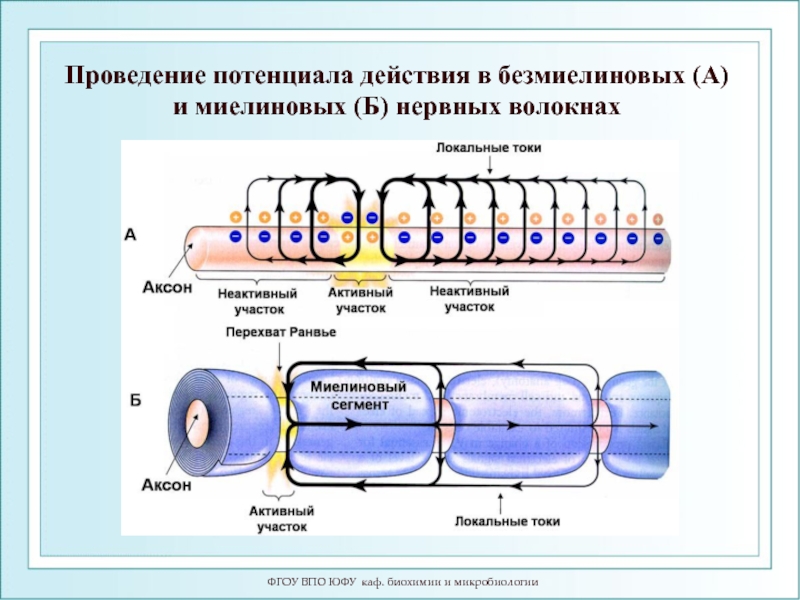
- 109. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
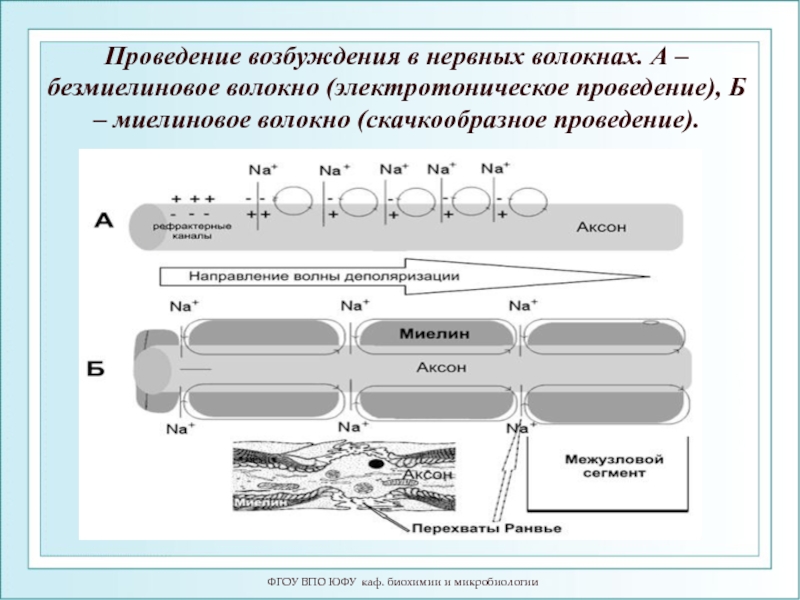
- 110. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
- 111. Передача нервного импульса Выделяют 2 способа повышения
Слайд 2Виды мембранного транспорта (МТ)
Мембранный транспорт (МТ)
1.Пассивный транспорт
1.1.Простая диффузия ионная
1.1.1. Осмос
1.1.2. Через поры
1.1.3. Через липидный бислой
1.2.Фильтрация
1.3. Облегченная диффузия
2.Активный транспорт
2.1.Первичный активный транспорт
2.2. Вторичный активный транспорт
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
Слайд 5Энергия пассивного транспорта создается различными градиентами:
концентрационным
осмотическим
электрическим
градиентом гидростатического давления жидкости
электрохимическим (совокупность концентрационного
Слайд 6Виды пассивного транспорта
Диффузия
Осмос
Фильтрация
Облегченная диффузия
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
Слайд 7Диффузия –
это самопроизвольный процесс проникновения вещества из области большей в
Слайд 8Простая диффузия описывается уравнением Фика : скорость диффузии dm/dt
Слайд 9 Скорость диффузии - это количество вещества, диффундирующего в единицу времени
Градиент концентрации - это изменение концентрации вещества, приходящееся на единицу длины, в направлении диффузии.
Знак «-» показывает, что диффузия идет из области большей в область меньшей концентрации.
D - коэффициент диффузии.
Слайд 10 Осмос - движение молекулы воды через полупроницаемые мембраны из места
Слайд 11Уравнение, описывающее осмотический перенос воды.
где
- количество
Р1 и Р2 – осмотическое давление растворов по обе стороны мембраны;
k – коэффициент проницаемости.
Слайд 12Фильтрация – это движение раствора через поры в мембране под действием
Слайд 13Фильтрация – движение жидкости через поры какой-либо перегородки под действием гидростатического
где
r – радиус поры
l – длина поры
η – вязкость жидкости
Р1-Р2 – разность давления между началом и концом поры
V – объем фильтрованной жидкости
Слайд 14Уравнение Коллендера-Бернульда описывает транспорт веществ через липидный бислой
где
С1 и С2 –
Р – коэффициент проницаемости мембраны
S – площадь, через которую идет перенос
Р = DK/L (С1 - С2)
D – коэффициент диффузии
К – коэффициент распределения
вещества между мембраной и средой
L – толщина мембраны
Слайд 16Облегчённая диффузия.
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
I = Imax [C]/Kt
I - скорость облегченной диффузии
С - концентрация переносимого вещества
Kt - константа транспорта, аналогичная КМ
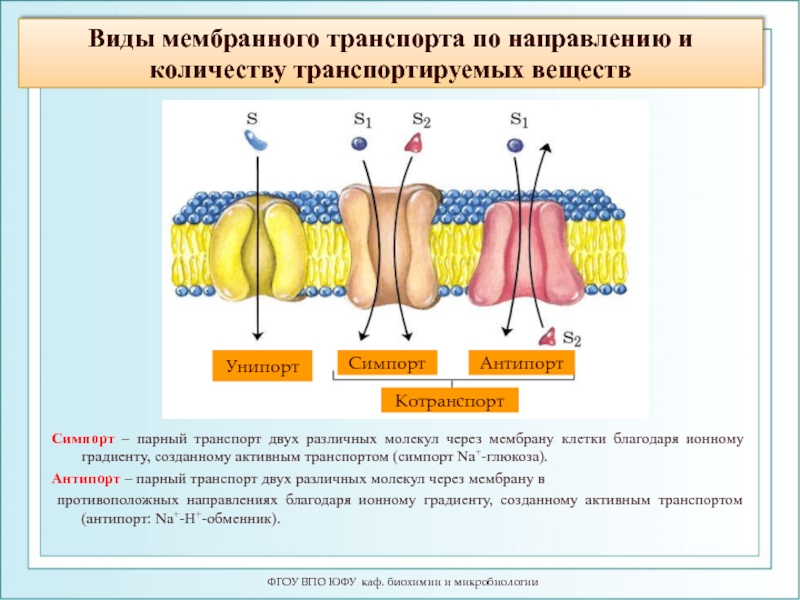
Слайд 17Виды мембранного транспорта по направлению и количеству транспортируемых веществ
ФГОУ ВПО ЮФУ
Симпорт – парный транспорт двух различных молекул через мембрану клетки благодаря ионному градиенту, созданному активным транспортом (симпорт Na+-глюкоза).
Антипорт – парный транспорт двух различных молекул через мембрану в
противоположных направлениях благодаря ионному градиенту, созданному активным транспортом (антипорт: Na+-Н+-обменник).
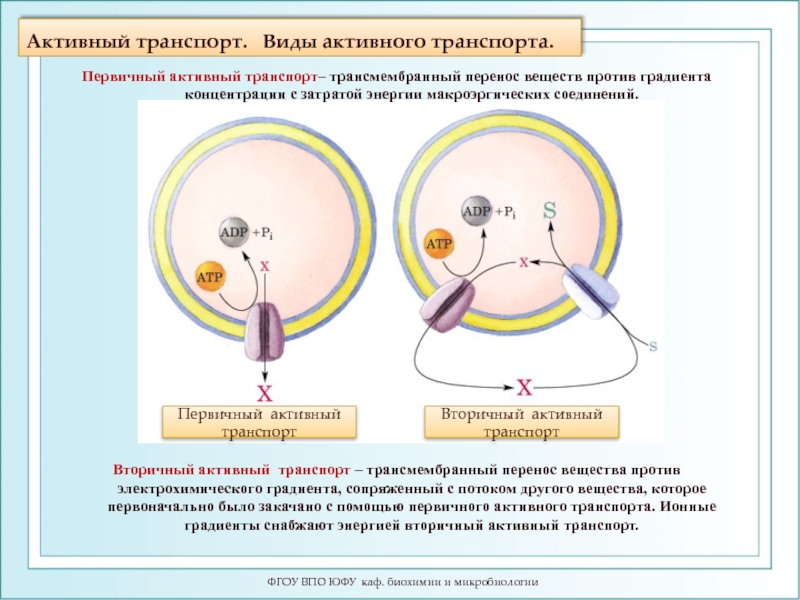
Слайд 18Активный транспорт. Виды активного транспорта.
ФГОУ ВПО ЮФУ каф. биохимии и
Вторичный активный транспорт – трансмембранный перенос вещества против электрохимического градиента, сопряженный с потоком другого вещества, которое первоначально было закачано с помощью первичного активного транспорта. Ионные градиенты снабжают энергией вторичный активный транспорт.
Первичный активный транспорт– трансмембранный перенос веществ против градиента концентрации с затратой энергии макроэргических соединений.
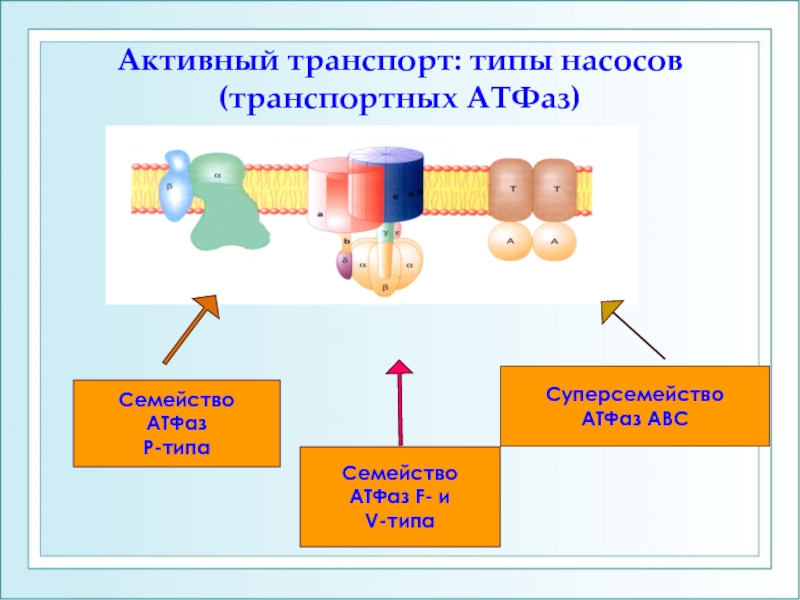
Слайд 19Активный транспорт: типы насосов (транспортных АТФаз)
Семейство
АТФаз
Р-типа
Семейство
АТФаз F- и
V-типа
Суперсемейство
АТФаз АВС
Слайд 20ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
1. АТФ-азы Р-типа –
АТФ-азы F- типа – это обратимы АТФ-зависимые протонные насосы, катализируют трансмембранный перенос протонов против градиента за счет гидролиза АТФ («F- тип» происходит из определения этих АТФ-аз как энергосопрягающих факторов) (Н-АТФ-аза/АТФ-синтаза).
АТФ-азы V-типа - протон-транспортирующие АТФ-азы, обеспечивающие закисление вакуолей, лизосом, эндосом, комплекса Гольджи (сходны с АТФ-азами F-типа).
АВС-транспортеры – используют АТФ для запуска активного транспорта множества субстратов (выкачивают аминокислоты, пептиды, белки, ионы металлов, липиды, желчные кислоты, лекарства и др. из клетки против градиента концентрации) (Р-гликопротеин – мультилекарственный транспортер отвечает за устойчивость опухолей к протовоопухолевым препаратам).
Типы насосов (транспортных АТФ-аз)
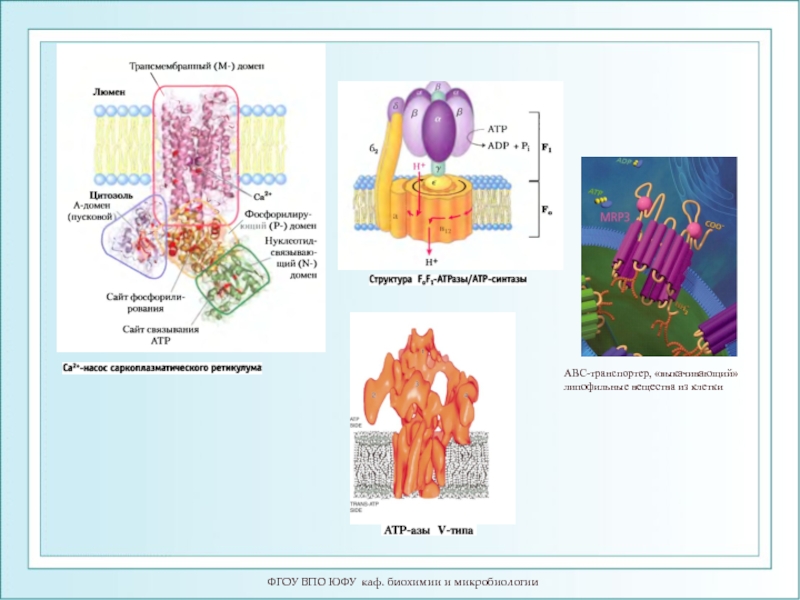
Слайд 21ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
АВС-транспортер, «выкачивающий» липофильные вещества из
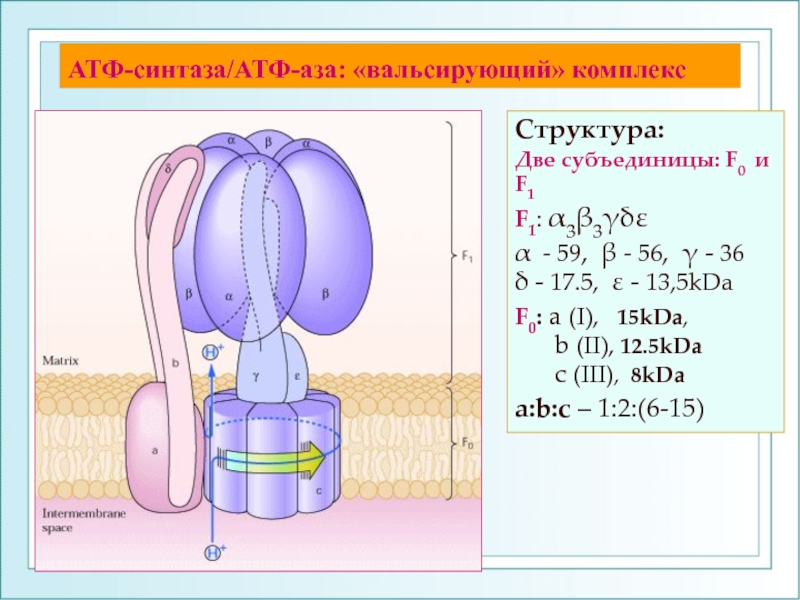
Слайд 22АТФ-синтаза/АТФ-аза: «вальсирующий» комплекс
Структура:
Две субъединицы: F0 и F1
F1: α3β3γδε
α - 59, β
δ - 17.5, ε - 13,5kDa
F0: а (I), 15kDa,
b (II), 12.5kDa
c (III), 8kDa
а:b:с – 1:2:(6-15)
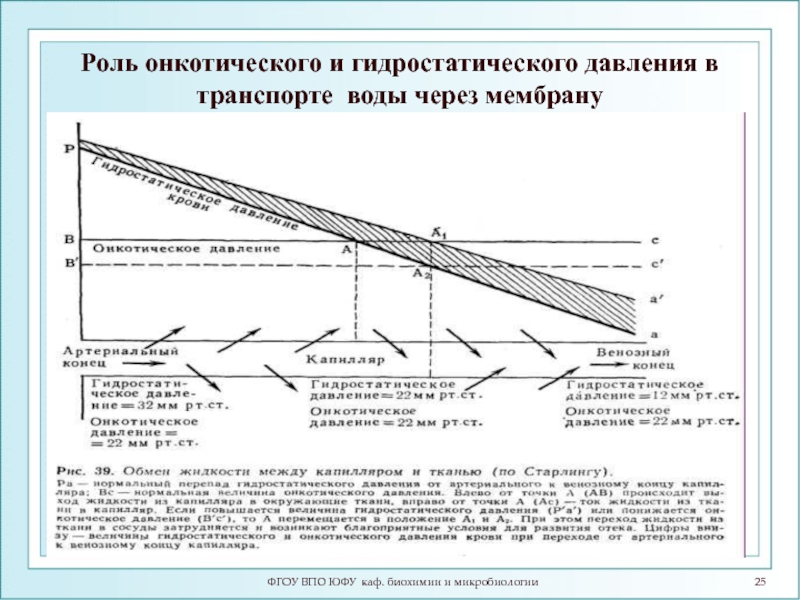
Слайд 25Роль онкотического и гидростатического давления в транспорте воды через мембрану
ФГОУ ВПО
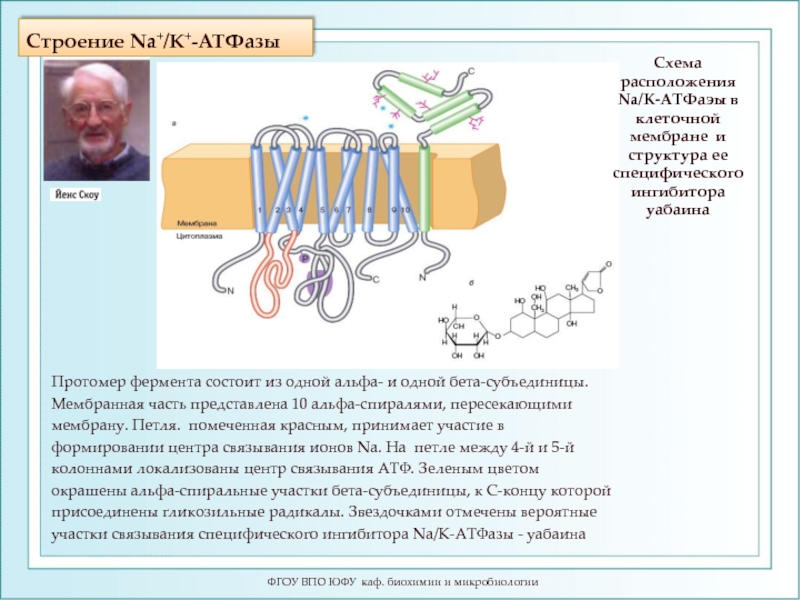
Слайд 26Строение Na+/K+-ATФазы
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
Протомер фермента состоит из
Мембранная часть представлена 10 альфа-спиралями, пересекающими
мембрану. Петля. помеченная кpacным, принимает участие в
формировании центра связывания ионов Nа. На петле между 4-й и 5-й
колоннами локализованы центр связывания АТФ. Зеленым цветом
окрашены альфа-спиральные участки бета-субъединицы, к С-концу которой
присоединены гликозильные радикалы. Звездочками отмечены вероятные
участки связывания специфического ингибитора Na/K-АТФазы - уабаина
Схема расположения Na/K-АТФаэы в клеточной мембране и структура ее специфического ингибитора уабаина
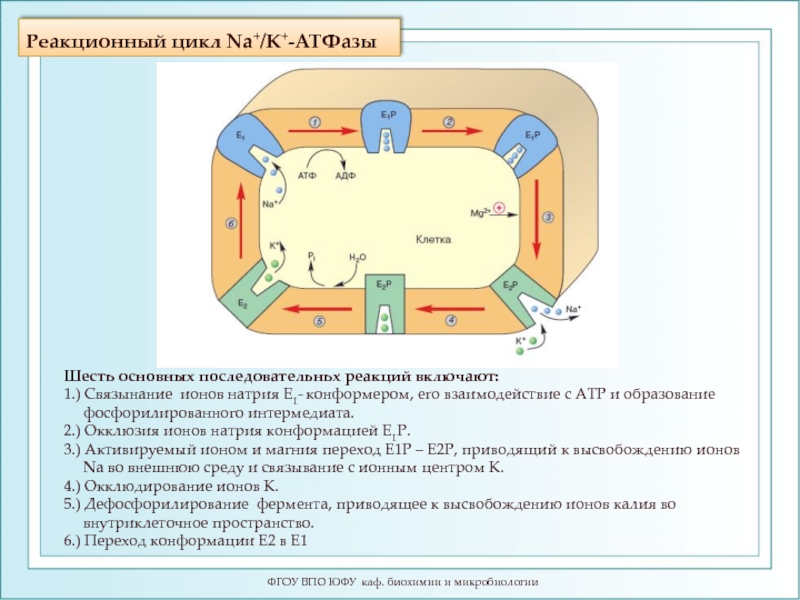
Слайд 27Реакционный цикл Na+/K+-ATФазы
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
Шесть основных последовательньх
1.) Связынание ионов натрия Е1- конформером, его взаимодействие с АТР и образование
фосфорилированного интермедиата.
2.) Окклюзия ионов натрия конформацией Е1Р.
3.) Активируемый ионом и магния переход Е1Р – Е2Р, приводящий к высвобождению ионов
Na во внешнюю среду и связывание с ионным центром K.
4.) Окклюдирование ионов K.
5.) Дефосфорилирование фермента, приводящее к высвобождению ионов калия во
внутриклеточное пространство.
6.) Переход конформации E2 в E1
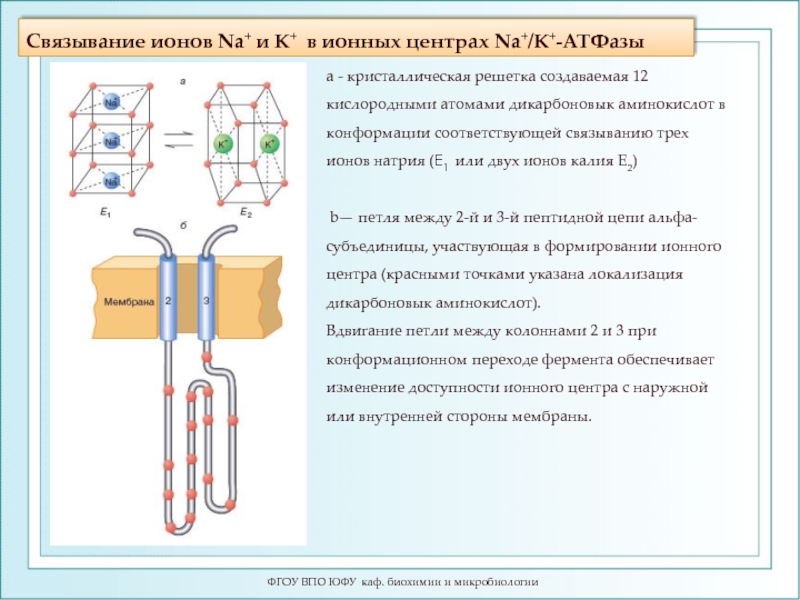
Слайд 28Связывание ионов Na+ и K+ в ионных центрах Na+/K+-ATФазы
ФГОУ ВПО ЮФУ
а - кристаллическая решетка создаваемая 12 кислородными атомами дикарбоновык аминокислот в конформации соответствующей связыванию трех ионов натрия (Е1 или двух ионов калия Е2)
b— петля между 2-й и 3-й пептидной цепи альфа-субъединицы, участвующая в формировании ионного центра (красными точками указана локализация дикарбоновык аминокислот).
Вдвигание петли между колоннами 2 и 3 при конформационном переходе фермента обеспечивает изменение доступности ионного центра с наружной или внутренней стороны мембраны.
Слайд 29ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
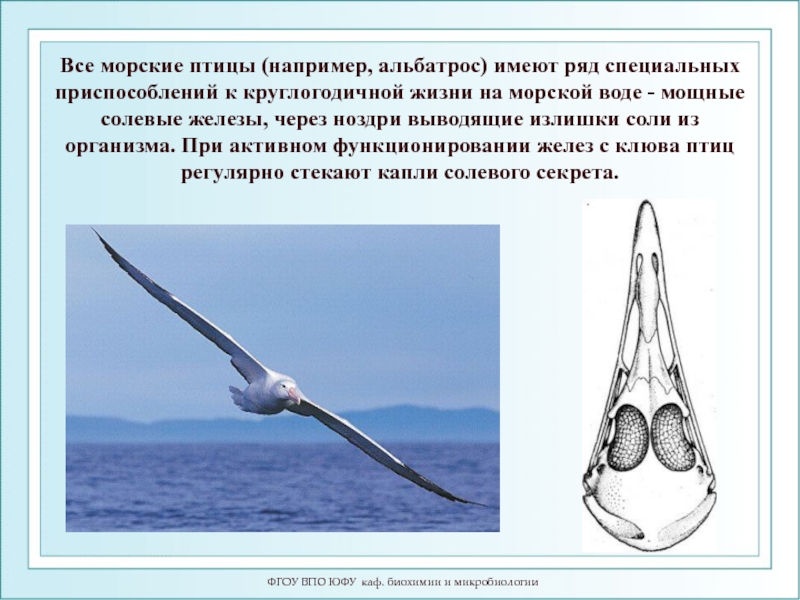
Все морские птицы (например, альбатрос)
Слайд 31Генерация и распространение биоэлектрических потенциалов - важнейшее физическое явление в живых
Слайд 32Для возникновения биопотенциалов решающее значение имеют потенциалы, обусловленные асимметричным, неравномерным распределением
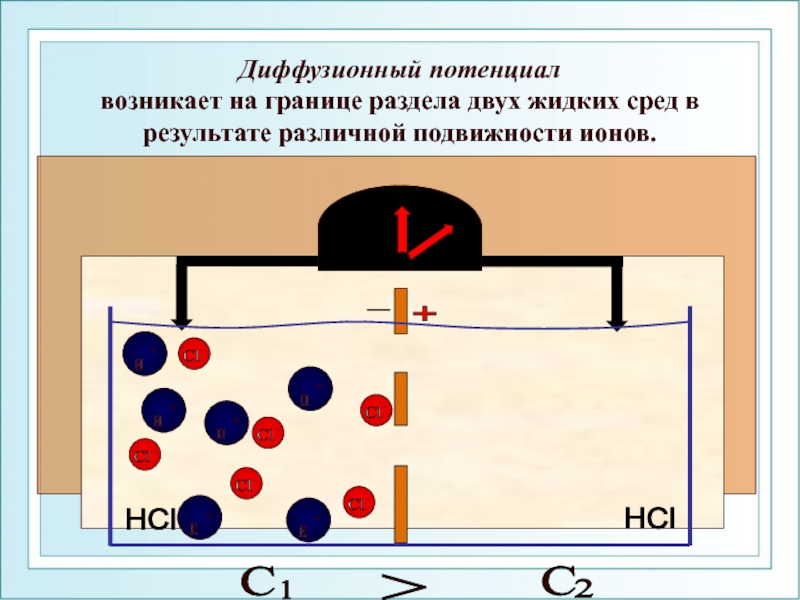
Слайд 34Диффузионный потенциал возникает на границе раздела двух жидких сред в результате
0
1
1
С
>
1
2
С
HCl
HCl
+
-
Слайд 35 Диффузионный потенциал определяется из уравнения Гендерсона
Где
U
V – подвижность анионов
R – универсальная газовая постоянная
Т – абсолютная температура
n – валентность
F – число Фарадея
а1 – активность ионов в области, откуда идет диффузия
а2 – активность ионов в области, куда идет диффузия
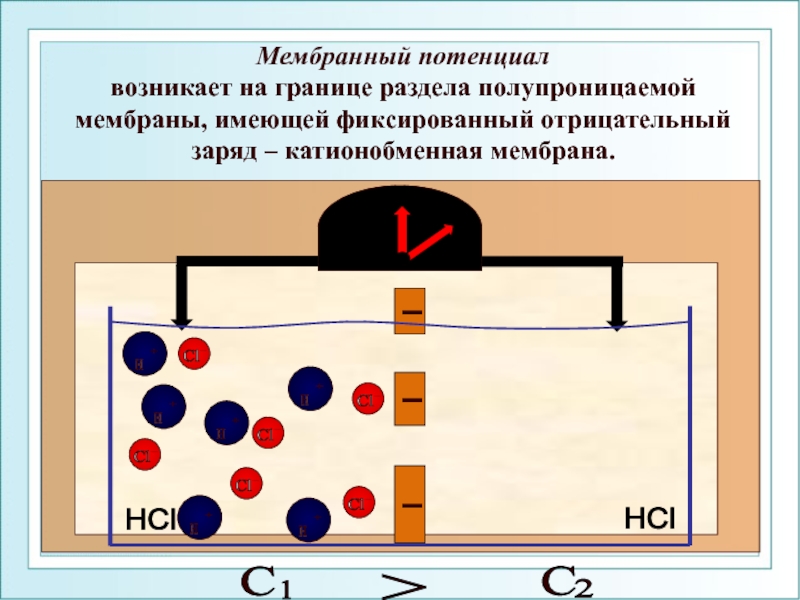
Слайд 36Мембранный потенциал возникает на границе раздела полупроницаемой мембраны, имеющей фиксированный отрицательный
▬
▬
0
1
1
С
>
1
2
С
HCl
HCl
▬
Слайд 37Мембранный потенциал определяют из уравнения Нернста
Где
R – универсальная газовая постоянная
Т –
n – валентность
F – число Фарадея
а1 – активность ионов в области, откуда идет диффузия
а2 – активность ионов в области, куда идет диффузия
Слайд 38
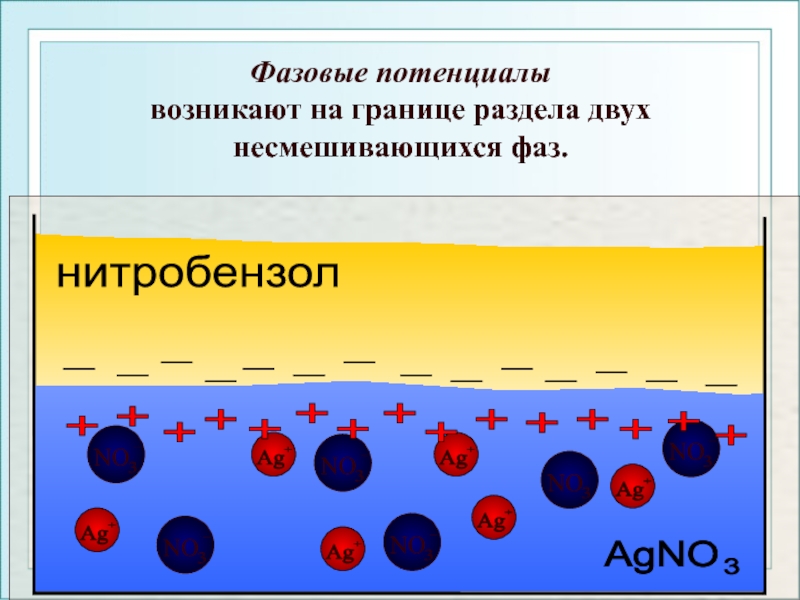
Фазовые потенциалы
возникают на границе раздела двух несмешивающихся фаз.
нитробензол
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
-
-
-
-
-
-
-
-
-
-
-
-
-
-
Слайд 39
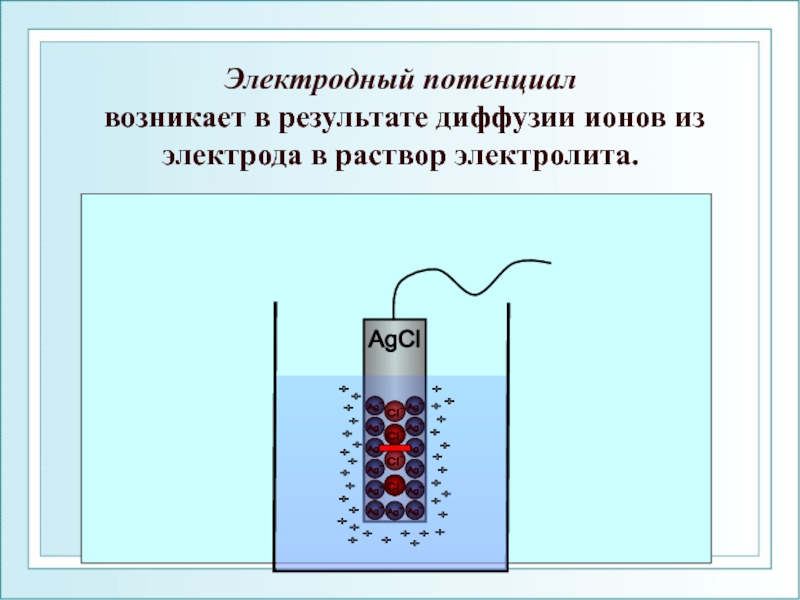
Электродный потенциал
возникает в результате диффузии ионов из электрода в раствор
AgCl
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
Слайд 40В 1902 году Бернштейном была выдвинута мембранная теория биопотенциалов. В 50-60-х
Слайд 41Сущность мембранной теории биопотенциалов
Потенциал
2)неравномерным распределением ионов между клеткой и средой, которое поддерживается механизмами активного транспорта, локализованными в самой мембране.
Слайд 42Мембранным потенциалом
называется разность потенциалов между внутренней и наружной поверхностями мембраны.
Слайд 43Потенциал покоя – стационарная разность электрических потенциалов, регистрируемых между внутренней и
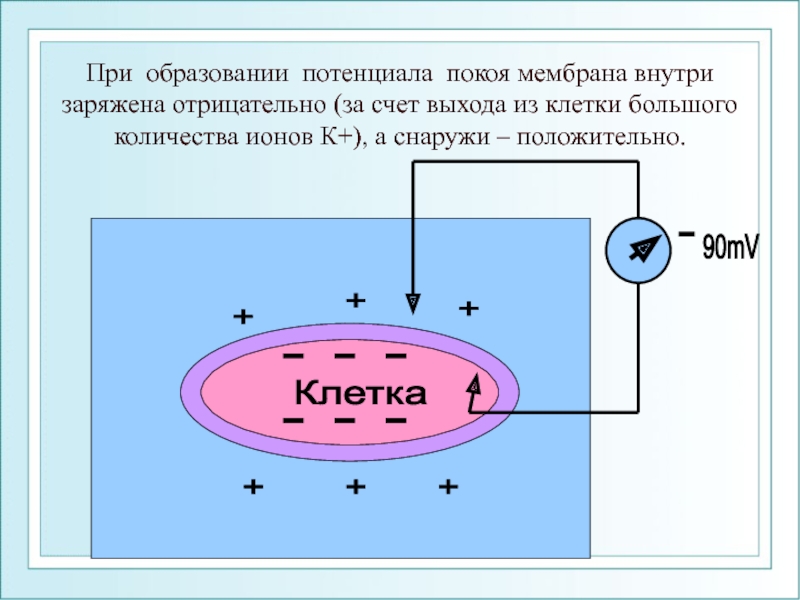
Слайд 46При образовании потенциала покоя мембрана внутри заряжена отрицательно (за счет выхода
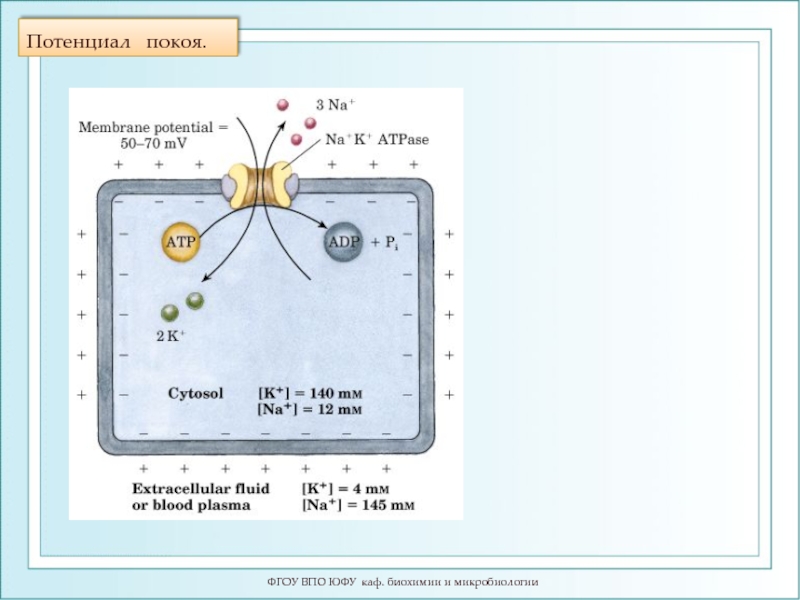
Слайд 47ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
Потенциал покоя. В мембране открыты калиевые
Слайд 48ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
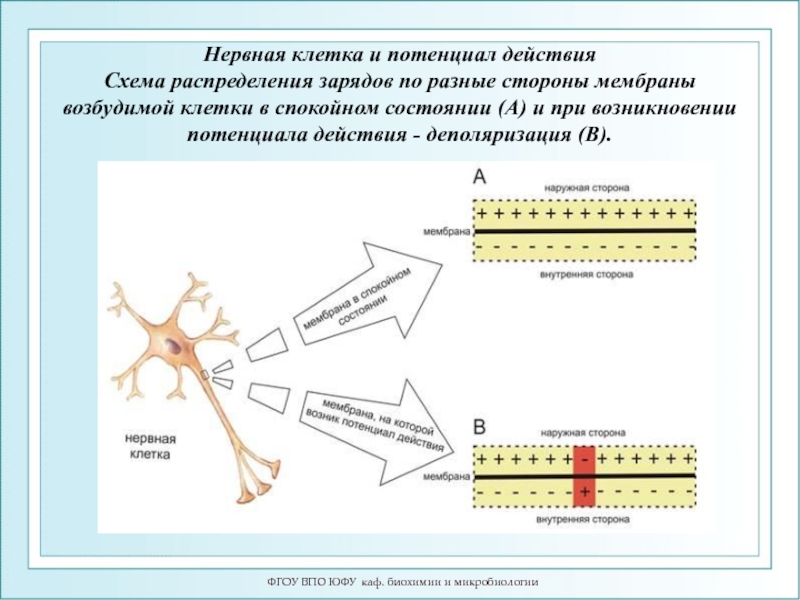
Нервная клетка и потенциал действия
Схема
Слайд 49ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
Причины отрицательности мембранного потенциала покоя:
•
• Электорогенный Na/К- насос в мембране покоящейся клетки остается активен и также участвует в создании отрицательного заряда внутренней поверхности мембраны.
Его вклад: -10 мВ. В сумме это дает -70мВ.
Слайд 53С учетом работы электрогенных ионных насосов для мембранного потенциала было получено
Где m =3/2 - отношение количества ионов натрия к количеству ионов калия, перекачиваемых Na+ - K+-насосом.
Слайд 55Потенциал действия (ПД) – это последовательность изменений, мембранного потенциала, которая запускается
Слайд 56Потенциалом действия называется электрический импульс, обусловленный изменением ионной проницаемости мембраны и
Слайд 58При генерации потенциала действия происходит перезарядка мембраны: внутри она становится зараженной
Слайд 59Возбудимость – это способность клеток к быстрому ответу на раздражение, проявляющемуся
Слайд 61Стимуляция нервной клетки достигает порога возбудимости, необходимого для возникновения потенциала действия.
Начальное
Слайд 62Поскольку деполяризация в клетке продолжается, открывается больше потенциал-зависимых К+-каналов, и К+
После восстановления исходного уровня мембранного потенциала Na+ и К+ каналы возвращаются в состояние покоя.
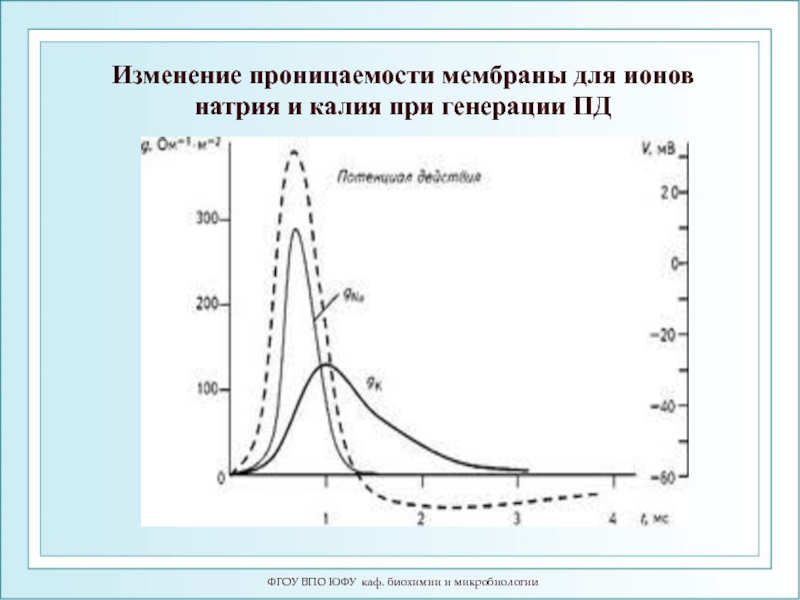
Слайд 63ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
Изменение проницаемости мембраны для ионов
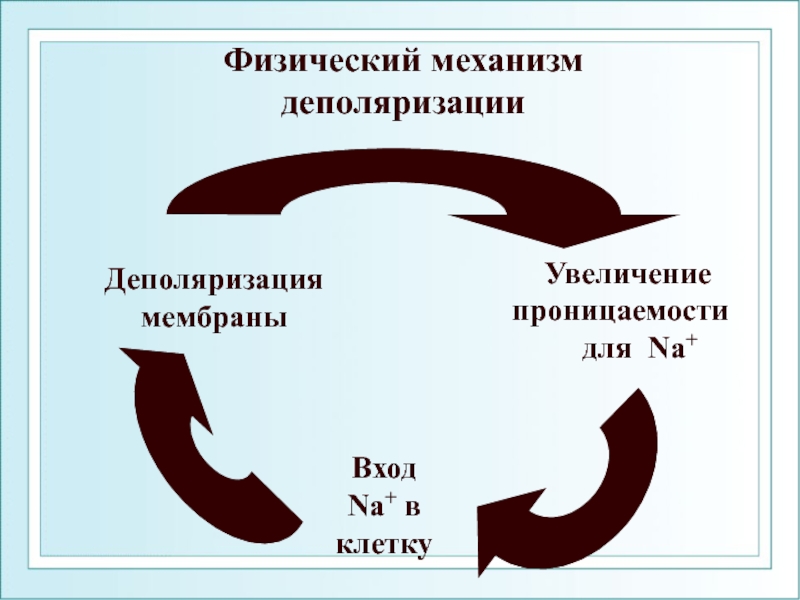
Слайд 64Физический механизм деполяризации
Увеличение
проницаемости
для
Вход
Na+ в
клетку
Деполяризация
мембраны
Слайд 65Отношение коэффициентов проницаемости ионов для фазы деполяризации
PК : РNa : PCl
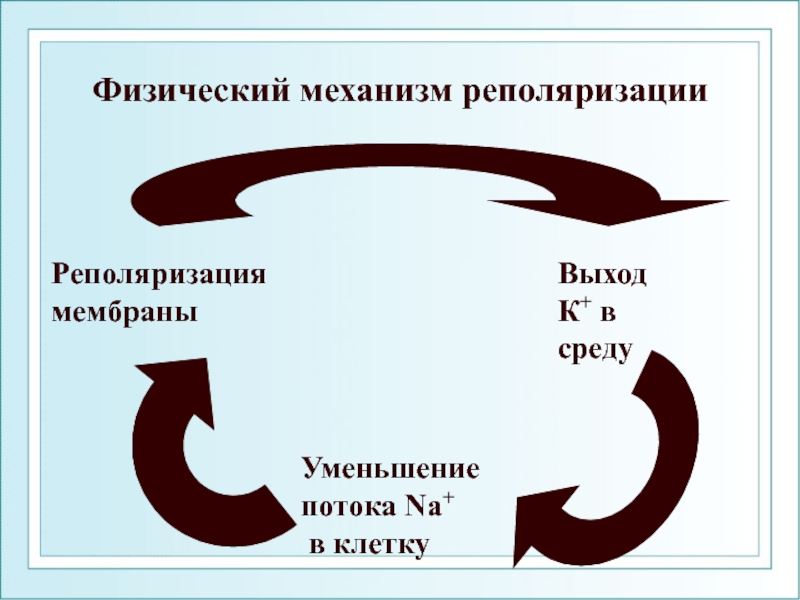
Слайд 66Физический механизм реполяризации
Выход
К+ в
среду
Уменьшение
потока Na+
в клетку
Реполяризация
мембраны
Слайд 67Формирование потенциала действия обусловлено двумя ионными потоками через мембрану: поток ионов
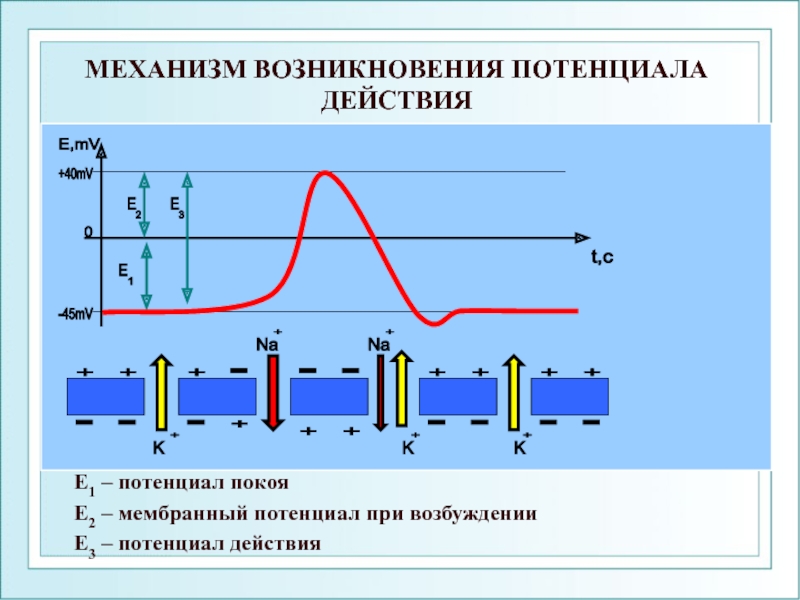
Слайд 68МЕХАНИЗМ ВОЗНИКНОВЕНИЯ ПОТЕНЦИАЛА ДЕЙСТВИЯ
Е1 – потенциал покоя
Е2 – мембранный потенциал при
Е3 – потенциал действия
Слайд 70Уравнение Ходжкина-Хаксли, описывающее мембранный потенциал, который складывается из потенциала покоя и
Слайд 73Ионный транспорт
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
Где
z - валентность иона
e
r - радиус иона
εM - диэлектрическая проницаемость мембраны
εв - диэлектрическая проницаемость воды
Затраты энергии, необходимые для проникновения иона в неполярную фазу, оценивают по формуле Борна. Энергия, затрачиваемая на перемещение иона из воды в мембрану, зависит от:
1)радиуса иона
2)диэлектрических проницаемостей воды и мембраны.
Слайд 74ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
Вероятность перехода иона из воды
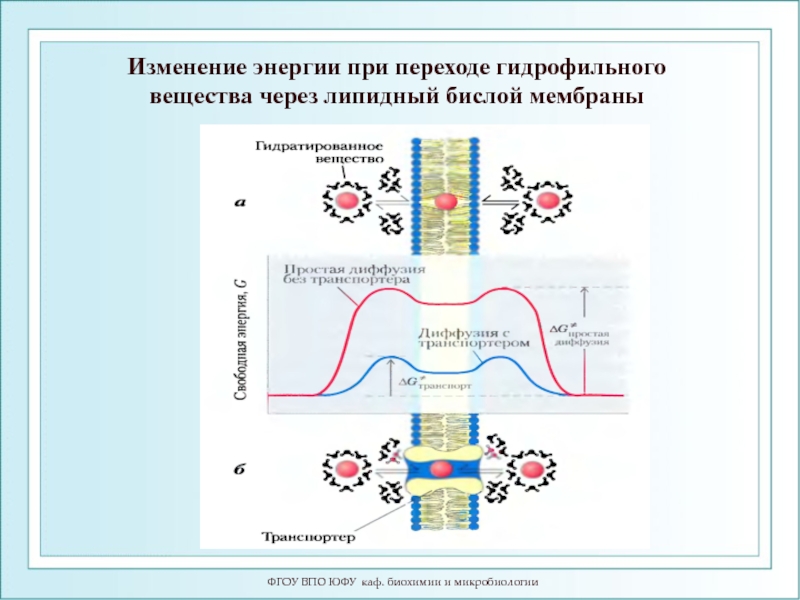
Непосредственный перенос ионов через липидный бислой за счет диффузии маловероятен:
Слайд 75ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
Изменение энергии при переходе гидрофильного
Слайд 76Свойства ионных каналов
Селективность
Независимость работы отдельных каналов
Дискретный характер проводимости
Зависимость параметров каналов от
Слайд 77Свойства ионных каналов
1.Селективность – способность пропускать ионы одного типа.
ИК обладают абсолютной
Через катион-селективные каналы проходят различные ионы, но проводимость для основного иона максимальна;
Способность ионного канала пропускать различные ионы называется относительной селективностью и характеризуется рядом селективности. Это соотношение проводимости канала для различных ионов, взятых при одной концентрации. Для основного иона селективность принимается за 1 (для Na-канала ряд селективности:
Na+ : K+ = 1 : 0,05).
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
Слайд 782.Независимость работы отдельных каналов
Прохождение тока через отдельный
Например, К+-каналы могут быть включены или выключены, но ток через Na+-каналы не меняется. Изменение проницаемости ионных каналов меняет мембранный потенциал.
Слайд 793.Дискретный характер проводимости
Проводимость ионного канала
Слайд 80
4.Зависимость параметров каналов от мембранного потенциала
Ионные каналы
Слайд 81ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
В 2003 году Нобелевская премия по химии
Слайд 82ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
Строение потенциал-чувствительного калиевого канала
Слайд 84Потенциал-чувствительный натриевый канал
Канал состоит из четырёх
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
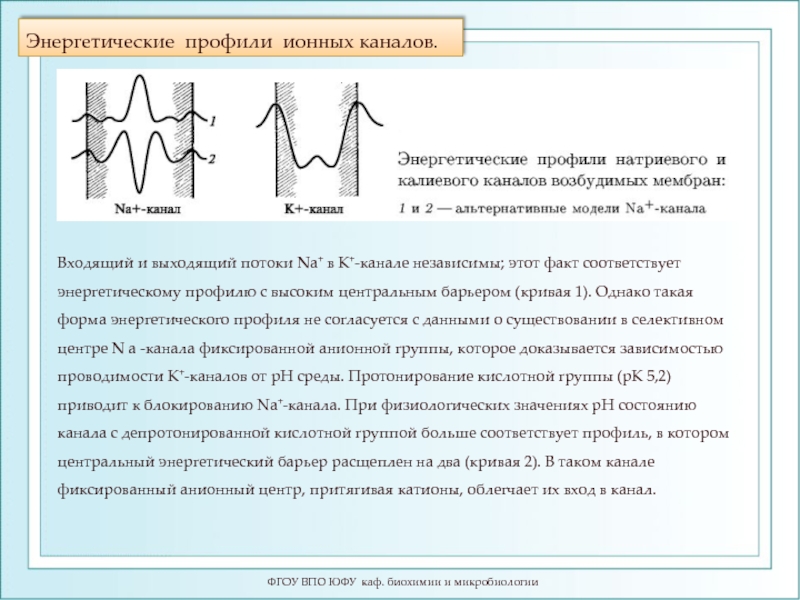
Слайд 87Энергетические профили ионных каналов.
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
Входящий и
Слайд 88ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
Блокатор натриевых каналов тетродотоксин
Рыба фугу —
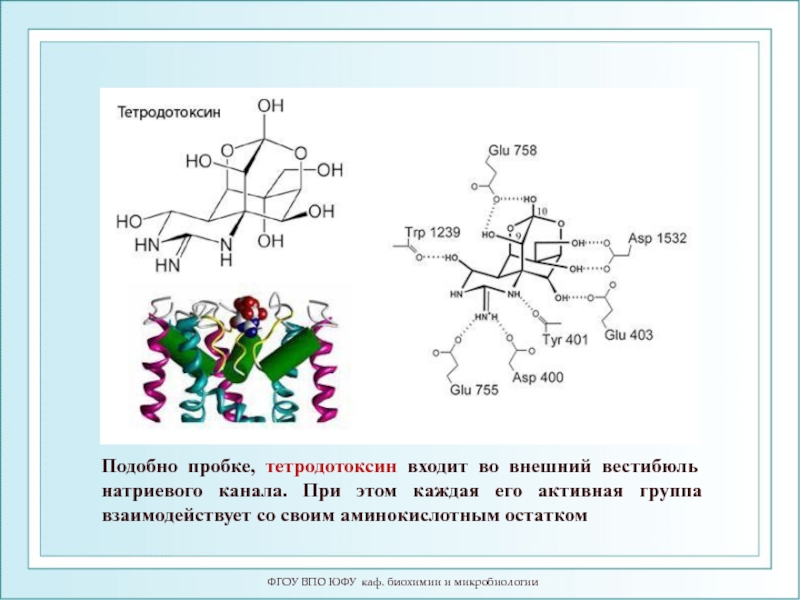
Слайд 89ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
Подобно пробке, тетродотоксин входит во
Слайд 90ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
Хищный брюхоногий моллюск Conus textile и структура
Слайд 91ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
Третий класс соединений, воздействующих на
Молекула батрахотоксина сидит в канале и не дает ему закрыться, пропуская ионы натрия. Стрелкой показан ток ионов
Слайд 92ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
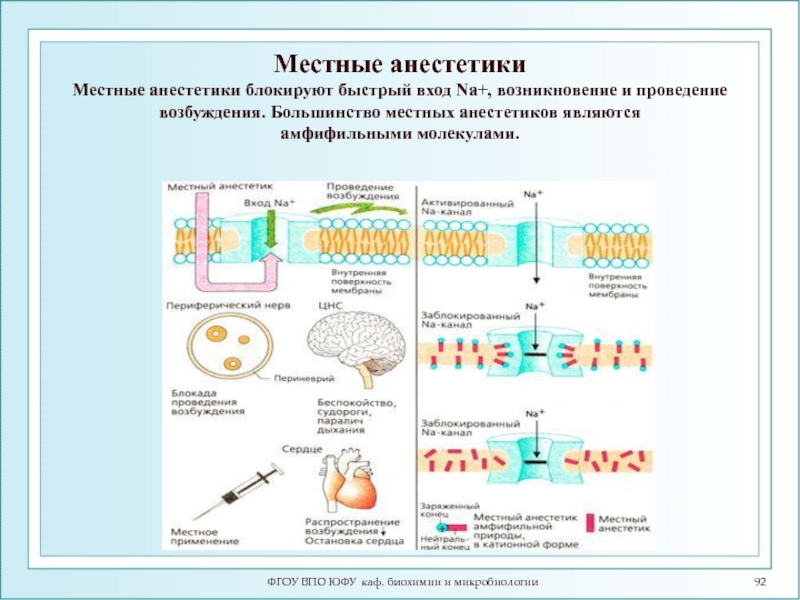
Местные анестетики
Местные анестетики блокируют быстрый
амфифильными молекулами.
Слайд 95ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
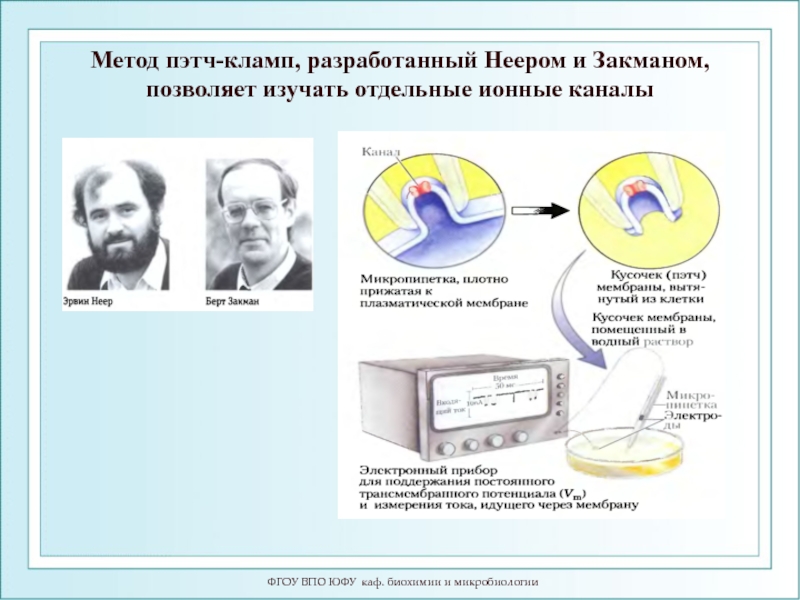
Метод пэтч-кламп, разработанный Неером и
Слайд 96ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
Нобелевская премия по химии 2003
«за открытие водных каналов»
Открытие, сделанное профессором Эгром, — яркий пример роли счастливого случая в науке. Недаром сам нобелевский лауреат любит повторять на своих лекциях: «Всегда относитесь к научной деятельности как к приключению… Мы не знаем, что ждет нас за поворотом, и в этом смысле я, скорее, Гекльберри Финн, чем Альберт Эйнштейн».
Выступление П.Эгра в МГУ в 2013 г.
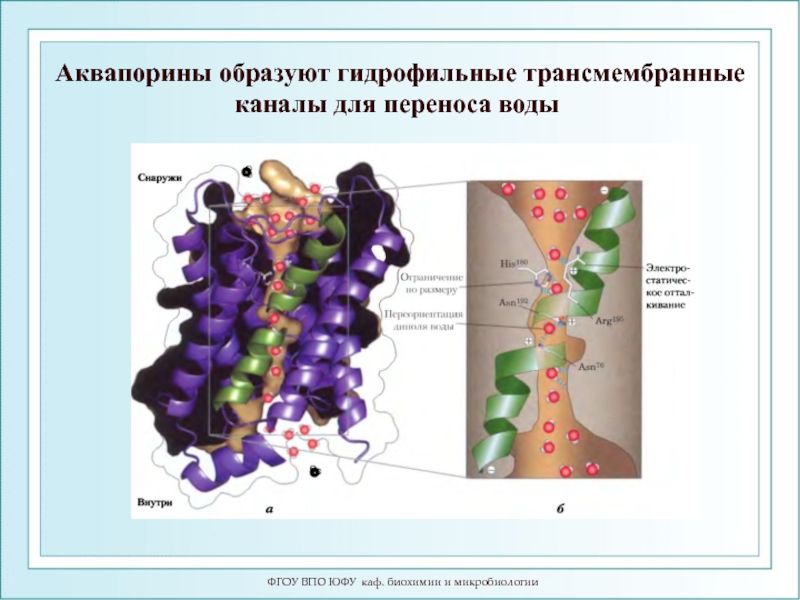
Слайд 97ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
Аквапорины образуют гидрофильные трансмембранные каналы
Слайд 98
Индуцированный ионный транспорт осуществляется ионофорами, которые делятся на 2 группы:
1. Подвижные
2. Каналообразующие агенты (каналоформеры)
Слайд 99ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
Подвижные переносчики.
1. Образование комплекса иона с ионофором на одной стороне мембраны.
2. Перемещение комплекса через мембрану.
3. Освобождение иона на другой стороне.
4. Возвращение ионофора.
Возможны 2 схемы работы переносчика:
1. Малая "карусель", когда ионофор не выходит из мембраны.
2. Большая "карусель", когда ионофор проходит мембрану насквозь, а образование и распад комплекса происходит вне мембраны.
Так, для заряженного комплекса радиусом 1 нм свободная энергия перехода из воды в мембрану составляет около 15 кДж/моль в отличие от энергии свободного иона - 250-300 кДж/моль
Слайд 100ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
Подвижные переносчики. Валиномицин.
Антибиотик валиномицин впервые
структуру этого соединени.
Валиномицин - макроциклическое соединение, состоящее из шести α-аминокислот и шести α-гидроксикислот, соединённых друг с другом попеременно амидными и сложноэфирными связями.
В 1978 году Ю. А. Овчинников и член-корреспондент АН СССР В.Т. Иванов были удостоены Ленинской премии за исследование ионофоров.
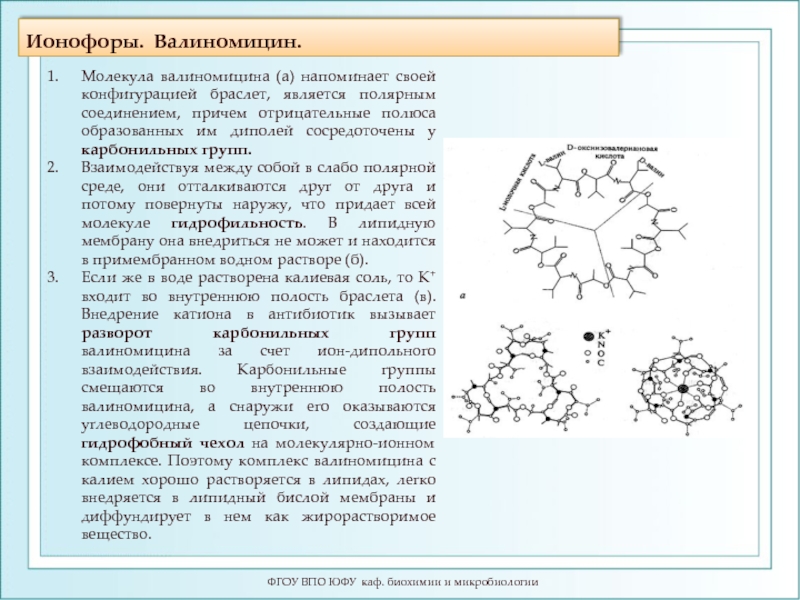
Слайд 101Ионофоры. Валиномицин.
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
Молекула валиномицина (а)
Взаимодействуя между собой в слабо полярной среде, они отталкиваются друг от друга и потому повернуты наружу, что придает всей молекуле гидрофильность. В липидную мембрану она внедриться не может и находится в примембранном водном растворе (б).
Если же в воде растворена калиевая соль, то К+ входит во внутреннюю полость браслета (в). Внедрение катиона в антибиотик вызывает разворот карбонильных групп валиномицина за счет ион-дипольного взаимодействия. Карбонильные группы смещаются во внутреннюю полость валиномицина, а снаружи его оказываются углеводородные цепочки, создающие гидрофобный чехол на молекулярно-ионном комплексе. Поэтому комплекс валиномицина с калием хорошо растворяется в липидах, легко внедряется в липидный бислой мембраны и диффундирует в нем как жирорастворимое вещество.
Слайд 102ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
Кристаллическая структура ионофора - комплекса
Слайд 103Механизм работы валиномицина – малая «карусель»
ФГОУ ВПО ЮФУ каф. биохимии
Молекула валиномицина переносит через мембрану не более 104 ионов/c.
Слайд 104ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
Скульптурная композиция комплекса
К+-валиномицин перед
Слайд 105Индуцированный транспорт ионов при участии различных переносчиков
I - нейтральные ионофоры (валиномицин)
II
III - липофильные разобщители фосфорилирования (перенос протонов)
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
I - нейтральные ионофоры (валиномицин)
II - слабокислые ионофоры (нигерицин- обмен Н+ на К+)
III - липофильные разобщители фосфорилирования (перенос протонов)
Слайд 106Грамицидин – каналообразующий антибиотик
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
1) Грамицидин
2) Молекула грамицидина имеет форму спирали. Такая же форма присуща и димеру. Внутренность спирали гидрофильна и заполнена 5—6 молекулами воды. Катион, движущийся по каналу, проталкивает их подобно поршню.
3) Грамицидиновый канал проводит преимущественно одновалентные катионы, причем проницаемость мембраны для них растет по мере уменьшения гидратного ионного радиуса. Почти не транспортируются анионы, так как внутрь поры «смотрят» отрицательно заряженные группы.
5) Скорость переноса 107 ионов калия за 1 с.
6) Грамицидиновый канал может пребывать либо в открытом, либо в закрытом состоянии, что обусловлено тепловым движением молекул грамицидина. За счет теплового движения концы димера то погружаются в липидную основу, то выходят на обе ее поверхности.
Слайд 107Структура амфипатической α-спирали и расположение спиралей в мембране при формировании гидрофильного
Слайд 108Аламетицин – каналообразующий антибиотик
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
Аламетицин, пептидный
Аламетициновый канал собирается из молекул этого антибиотика как бочонок из дощечек, причем встраивание дополнительного мономера («дощечки») увеличивает периметр поры примерно на 0,66 нм.
Важной особенностью аламетициновых каналов является их зависимость от внешнего электрического поля.
В отсутствие разности потенциалов на липидной мембране молекулы антибиотика распластаны на ее поверхности и не образуют каналов. Создание трансмембранной разности потенциалов приводит к тому, что положительный полюс аламетициновой молекулы оказывается на одной стороне мембраны, а отрицательный (глутаминовый остаток) — на другой.
Слайд 109ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
Проведение потенциала действия в безмиелиновых
Слайд 110ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
Проведение возбуждения в нервных волокнах.
Слайд 111Передача нервного импульса
Выделяют 2 способа повышения скорости передачи нервного импульса :
1.
2.Уменьшения емкости аксолеммы за счет появления миелиновых волокон. Проведение идет скачками от одного перехвата Ранвье до другого и называется сальтаторным.
Обеспечивает экономию энергии:
- Скорость проведения больше (25-140 м/c), чем при непрерывном проведении (0,5-0,7 м/c)
- Потребление кислорода в 200 раз меньше, чем при непрерывном проведении
- Скорость проведения в миелиновом волокне прямо пропорциональна его диаметру, а в безмиелиновом - √ из величины диаметра.
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии













![Облегчённая диффузия.ФГОУ ВПО ЮФУ каф. биохимии и микробиологииI = Imax [C]/Kt + [C], где](/img/tmb/5/412595/561f3da688c96d12fc7f86d51f487717-800x.jpg)