- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Водно-солевой обмен у животных презентация
Содержание
- 1. Водно-солевой обмен у животных
- 2. Организм ~= водный раствор в оболочке
- 3. %С жидкостей тела отличается от внешней
- 4. Задачи по поддержанию постоянной среды организма меняются
- 5. 1. Водная среда 1.1. Масштабы
- 6. Состав морской воды. Кроме перечисленных ионов, морская
- 7. Вариации: в Средиземном море – до
- 8. Типичный состав мягкой, жесткой и материковой соленой
- 9. Природная дождевая вода из-за растворения
- 10. Во внутренних водоемах: Б.
- 11. В прибрежных районах Взаимодействие морской и
- 12. Биологическое значение солоноватых вод (0.05%
- 14. Эвригалинные - стеногалинные
- 15. Чем термин изотоничный (изотонический) отличается от термина
- 16. Пресноводные животные - гиперосмотичные
- 17. 1.3. Водные беспозвоночные
- 18. Концентрация важнейших ионов (в миллимолях на 1
- 19. Если различия слабые – регуляция или нет?
- 20. Регуляция ионов у некоторых морских беспозвоночных. Концентрация
- 21. Животные в пресной и солоноватой воде В
- 22. Соотношение между концентрациями жидкостей в теле и
- 23. Соотношение между концентрациями жидкостей тела и внешней
- 25. Активный транспорт ионов – против градиента %С
- 26. Беспозвоночные, живущие в солоноводной среде:
- 27. Осмотическое давление жидкостей тела артемии в сильно
- 28. Суточный обмен ионов в воде у личинки
- 30. Концентрация важнейших растворенных веществ (в миллимолях на
- 31. Различное решение осмотических проблем разными
- 32. %С Na+ в крови акул = 0.5
- 33. Концентрация растворенных веществ в сыворотке крови амазонского
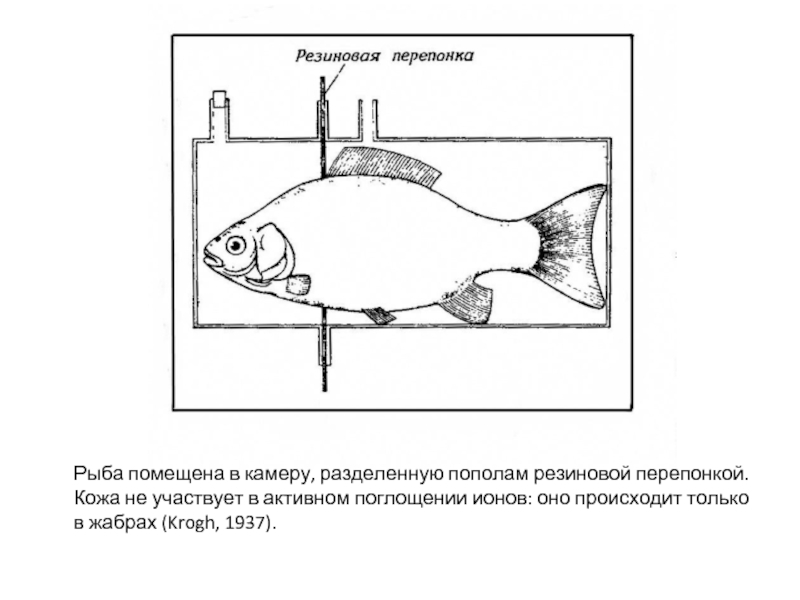
- 34. Рыба помещена в камеру, разделенную пополам резиновой
- 37. Фильтрационно-реабсорбционный принцип работы почки рыб →
- 38. Выход на сушу → выработка адаптаций к
- 39. Концентрация важнейших растворенных веществ (в миллимолях на
Слайд 2Организм ~= водный раствор в оболочке
Этот раствор = среда б/х реакций, среда транспортировки питательных веществ
Объем организма (V) и концентрация (%С) веществ ~= const. Большие отклонения –гибель.
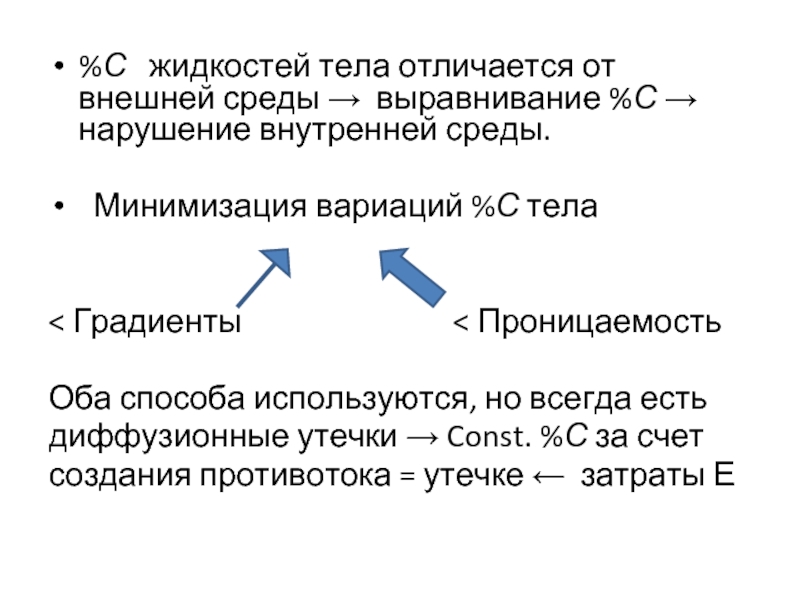
Слайд 3%С жидкостей тела отличается от внешней среды → выравнивание %С
Минимизация вариаций %С тела
< Градиенты < Проницаемость
Оба способа используются, но всегда есть
диффузионные утечки → Const. %С за счет
создания противотока = утечке ← затраты Е
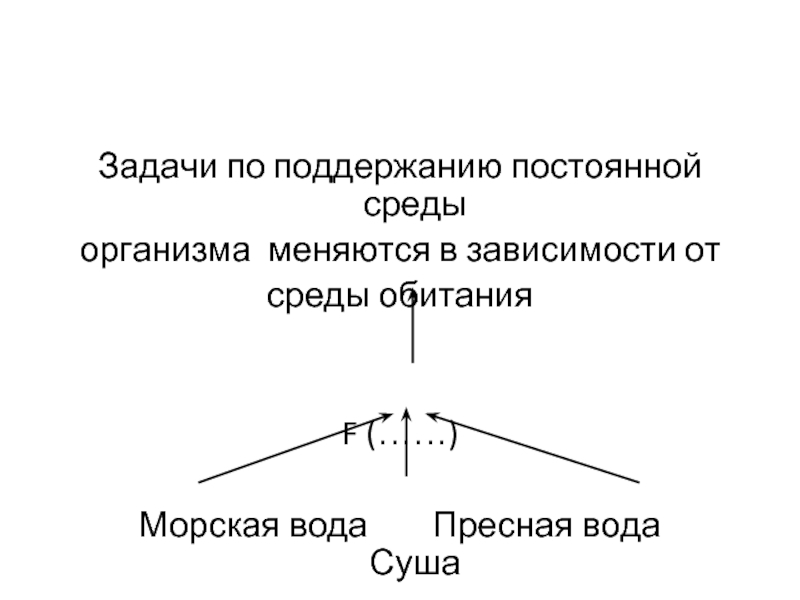
Слайд 4Задачи по поддержанию постоянной среды
организма меняются в зависимости от
среды обитания
F
Морская вода Пресная вода Суша
Слайд 51. Водная среда
1.1. Масштабы и свойства водной среды
71% поверхности
V пресной воды ~ 0.01% (<1% поверхности) от
морской воды.
На суше – жизнь в тонкой пленке.
В воде - в толще до 10 000 м.
Вода: растворенные соли, газы и немного
органических веществ
Морская вода: 3.5% солей (35 г солей в 1 л морской воды)
Основные ионы: Na+ Cl-
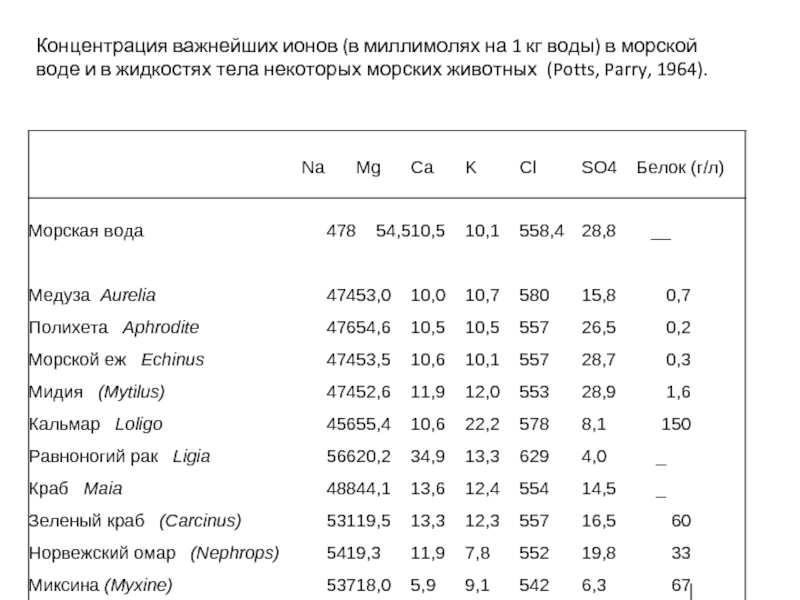
Слайд 6Состав морской воды. Кроме перечисленных ионов, морская вода содержит
небольшие количества
(Potts, Parry,1964)
В термодинамике концентрации вычисляются на 1 кг веса и обозначаются как моляльность
раствора.
Слайд 7Вариации:
в Средиземном море – до 4%, так как испарение >
соотношение ионов const.
Сильная вариация %С в пресных водах.
[Источник солей – брызги океана → частицы соли разносятся токами воздуха].
Состав дождевой воды меняется в зависимости от поверхности, по которой она течет:
Гранит → мягкая вода
Пористый известняк – соли кальция → жесткая вода
→ CV 0.1ммоль/л - 10 ммоль/л + сильная CV %ионов
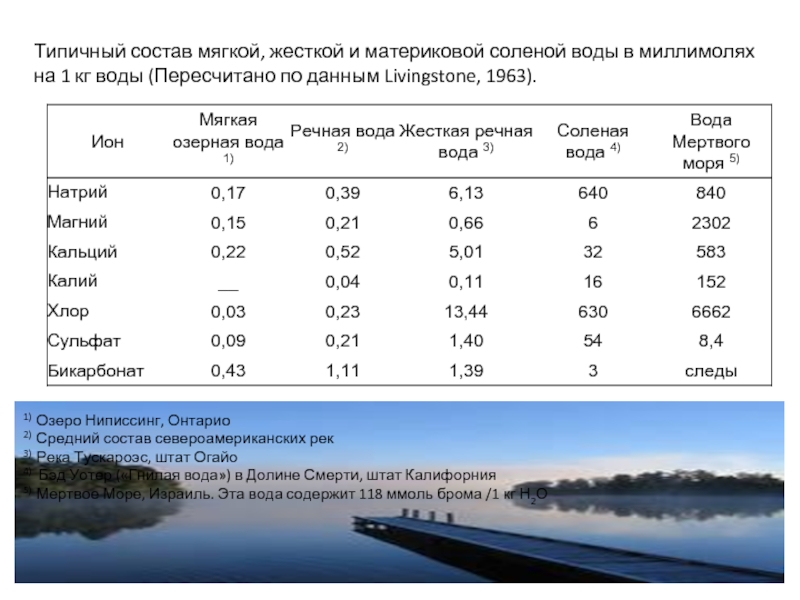
Слайд 8Типичный состав мягкой, жесткой и материковой соленой воды в миллимолях
на 1
1) Озеро Ниписсинг, Онтарио
2) Средний состав североамериканских рек
3) Река Тускароэс, штат Огайо
4) Бэд Уотер («Гнилая вода») в Долине Смерти, штат Калифорния
5) Мертвое Море, Израиль. Эта вода содержит 118 ммоль брома /1 кг Н2О
Слайд 9Природная дождевая вода из-за растворения
атм. СО2 имеет рН
В некоторых районах из-за сгорания ископаемого топлива (сернистый газ образует сильные кислоты) рН = 4.0.
Скандинавия – с подветренной стороны к Центральной Европе → выпадают кислотные дожди.
Основная подстилающая порода гранит + незабуференная вода озер → кислоты не нейтрализуются → падение рН тормозит у рыб поглощение Na → массовая гибель кумжи в озерах.
Слайд 10
Во внутренних водоемах:
Б. Соленое озеро (штат Юта) насыщено NaCl,
который
но много рачка Artemia
Мертвое море (Израиль) – насыщено Mg & Cl + кристаллизуется на берегу СaSO4. Здесь выживают только микроорганизмы.
Особые условия
Слайд 11В прибрежных районах
Взаимодействие морской и пресной воды
солоноватые воды в речных
∆ %С в связи с приливно-отливным циклом.
Довольно замкнутая акватория Балтики → устойчивый градиент от 0.5% на севере до 3% у западных берегов Швеции.
Особые условия
Слайд 12Биологическое значение солоноватых вод
(0.05% - 3%) – барьер для
но в географическом смысле их значение невелико – <1% земной поверхности
Слайд 13
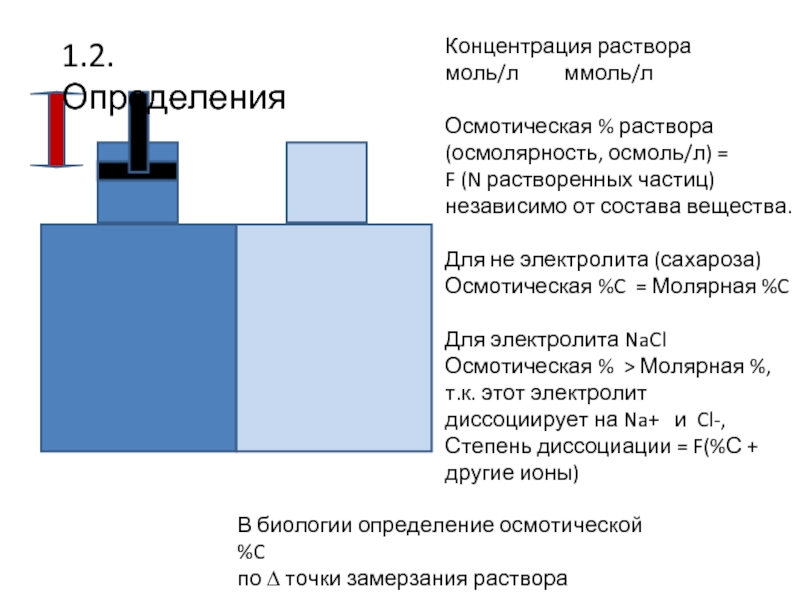
Концентрация раствора
моль/л ммоль/л
Осмотическая % раствора (осмолярность, осмоль/л)
F (N растворенных частиц) независимо от состава вещества.
Для не электролита (сахароза)
Осмотическая %C = Молярная %C
Для электролита NaCl
Осмотическая % > Молярная %,
т.к. этот электролит диссоциирует на Na+ и Cl-,
Степень диссоциации = F(%С + другие ионы)
В биологии определение осмотической %C
по ∆ точки замерзания раствора
1.2. Определения
Слайд 14Эвригалинные - стеногалинные
Пойкилоосмотические – гомойоосмотические
Осмоконформеры – осморегуляторы
Изотоничные
Изоосмотичные - гипоосмотичные – гиперосмотичные
∆ %С среды → ~=∆ %С в теле = осмоконформеры
∆ %С среды → Const. %С в теле = осморегуляторы
Концентрация отдельных ионов животного отличается от
внешней среды даже, если животное изоосмотично
среде. → Ионная регуляция - у всех.
=
Слайд 15Чем термин изотоничный (изотонический) отличается от термина изоосмотический.
Клетка изотонична с данным
Эритроцит в растворе NaCl (150 ммоль/л)
сохраняет размер и форму, а в изоосмотическом
растворе мочевины надувается и лопается.
Мочевина проникает в клетку сквозь мембрану, а
электролиты не выходят из клетки. → Н2О входит в
клетку… Раствор мочевины не изотоничен клетке.
Изоосмотичность – понятие физхимии, а термин
изотоничность описывает поведение клетки
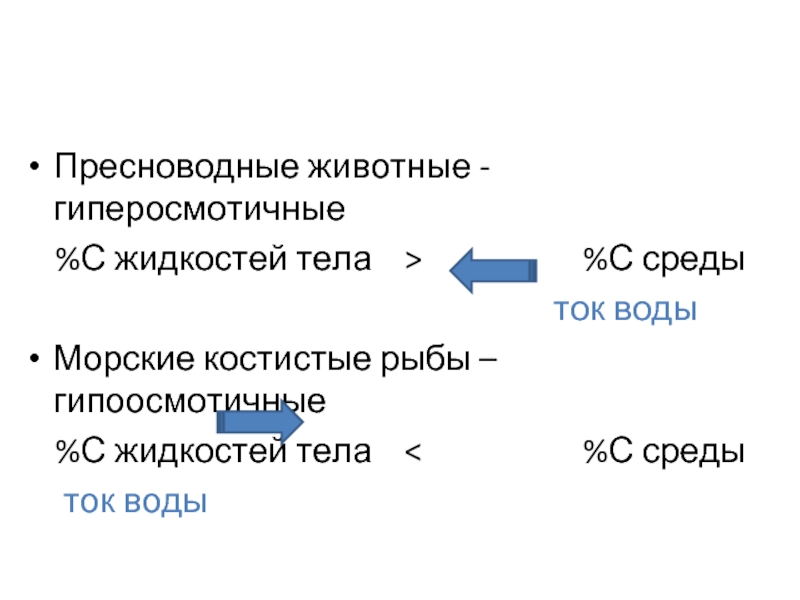
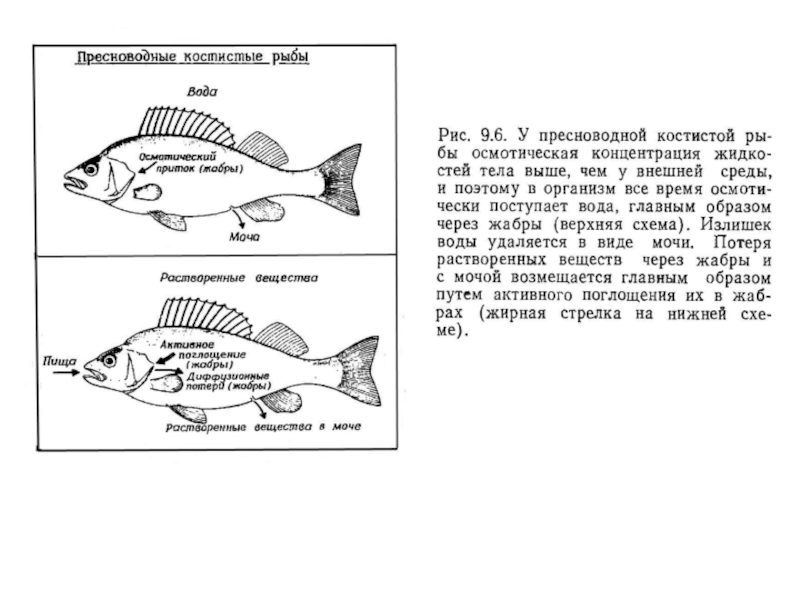
Слайд 16Пресноводные животные - гиперосмотичные
%С жидкостей тела >
ток воды
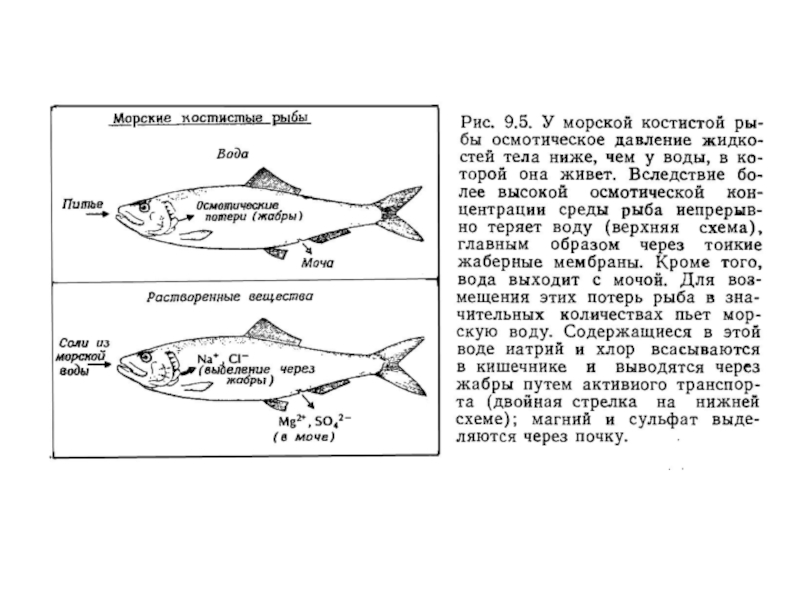
Морские костистые рыбы – гипоосмотичные
%С жидкостей тела < %С среды
ток воды
Слайд 171.3. Водные беспозвоночные
Большинство осмоконформеры – нет
проблем с осмосом.
Регуляция %С ионов.
Непроницаемость условна (жабры, пища) →
Удаление одних ионов
Удержание других ионов
У многих SO42- в 2 раза < , чем в морской воде =
пример активной секреции, а не реабсорбции
Слайд 18Концентрация важнейших ионов (в миллимолях на 1 кг воды) в морской
Слайд 19Если различия слабые – регуляция или нет?
Эффект Доннана -
J. Robertson помещал пробу в полупроницаемый целлофан и помещал мешок в морскую воду. Соли и вода проходят через целлофан, а белки – нет. В состоянии равновесия %С ионов в мешке не равна %С в морской воде. = ДИАЛИЗ.
%С ионов в мешке – опорная величина, а
%С ионов в пробе – в % от этой величины.
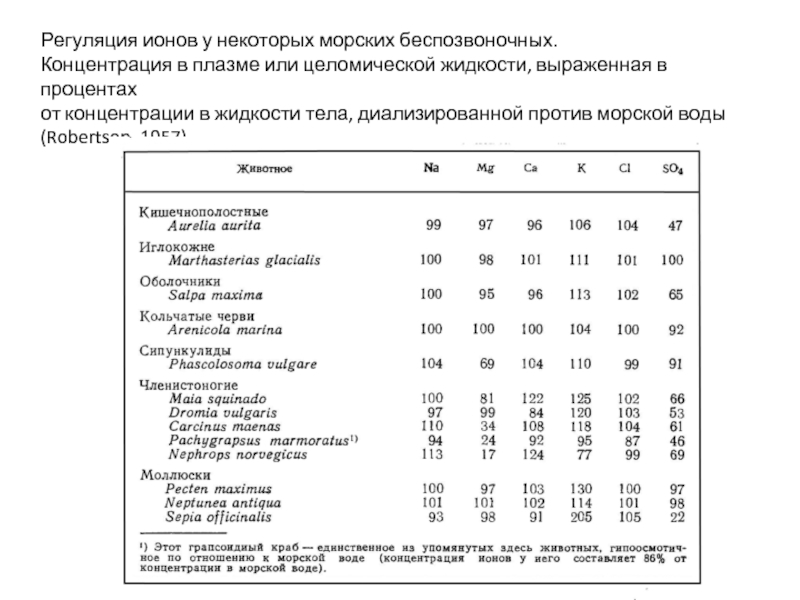
Слайд 20Регуляция ионов у некоторых морских беспозвоночных.
Концентрация в плазме или целомической жидкости,
от концентрации в жидкости тела, диализированной против морской воды
(Robertson, 1957)
Слайд 21Животные в пресной и солоноватой воде
В эксперименте многие морские животные выживали
Осморегуляторы долго остаются гиперосмотическими при падении %С солености в солоноватых водах и в целом лучше выдерживают колебания солености
среды, чем осмоконформеры.
Слайд 22Соотношение между концентрациями жидкостей в теле и во внешней
среде у разных
неразведенной морской воды указана стрелкой. Линия, идущая по диагонали,
соответствует одинаковым концентрациям жидкости тела и среды
(Beadle, 1943).
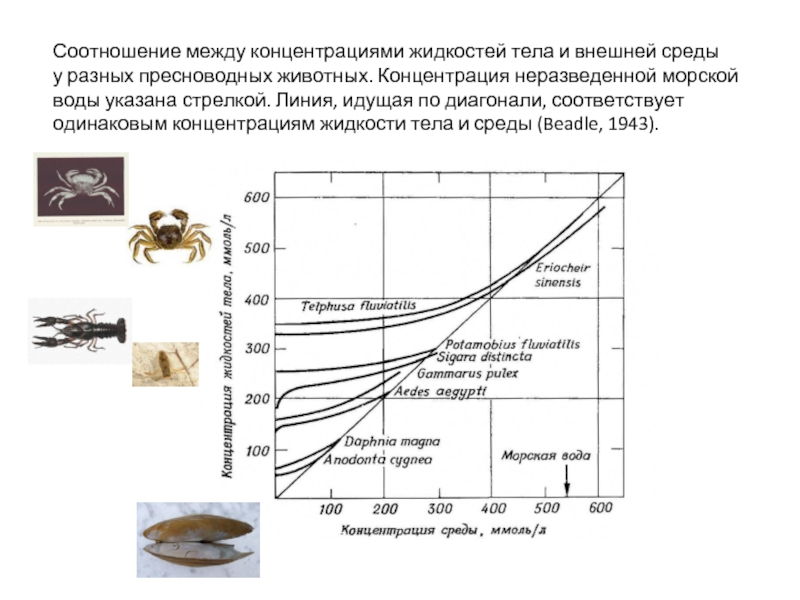
Слайд 23Соотношение между концентрациями жидкостей тела и внешней среды
у разных пресноводных
воды указана стрелкой. Линия, идущая по диагонали, соответствует
одинаковым концентрациям жидкости тела и среды (Beadle, 1943).
Слайд 24
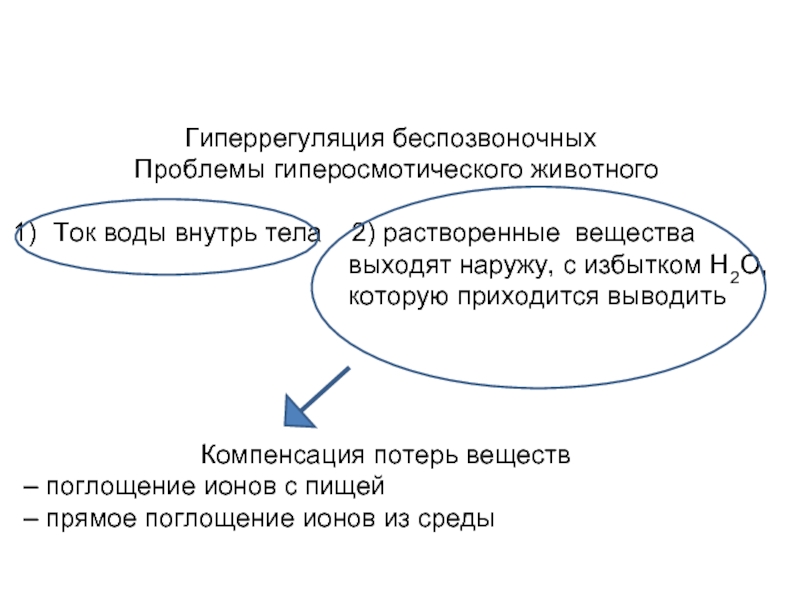
Проблемы гиперосмотического животного
Ток воды внутрь тела 2) растворенные вещества
выходят наружу, с избытком Н2О,
которую приходится выводить
Компенсация потерь веществ
– поглощение ионов с пищей
– прямое поглощение ионов из среды
Слайд 25Активный транспорт ионов – против градиента %С
Эксперимент: речной рак в дистиллированной
воде → потеря солей с 500 до 450 мосмоль/л;
Затем в обычной воде →с 450 до 500 мосмоль/л,
хотя %С = 5 мосмоль/л.
Органы ионного транспорта
У ракообразных 2) У водных личинок
насекомых
это жабры (дыхание это «анальные жабры»
+ транспорт ионов) (только орган ионной регуляции)
Затраты Е ~= 0.3 – 1.3% от MR (вычислены на основе
термодинамики)
Слайд 26Беспозвоночные, живущие в солоноводной среде:
Креветки Palaemonetes и Leander гипотоничны в обычной морской воде ← активная гипорегуляция, что необычно для морских б/п-х.
Внутр. сол. водоемы - огромная % солей – гипорегуляция у рачка Artemia (этот рачок приспособлен к огромному диапазону %С среды: от 3.5г/л (рачок- гиперрегулятор) до 300 г/л (рачок- гипорегулятор).
* * *
У позвоночных гипорегуляция широко распространена
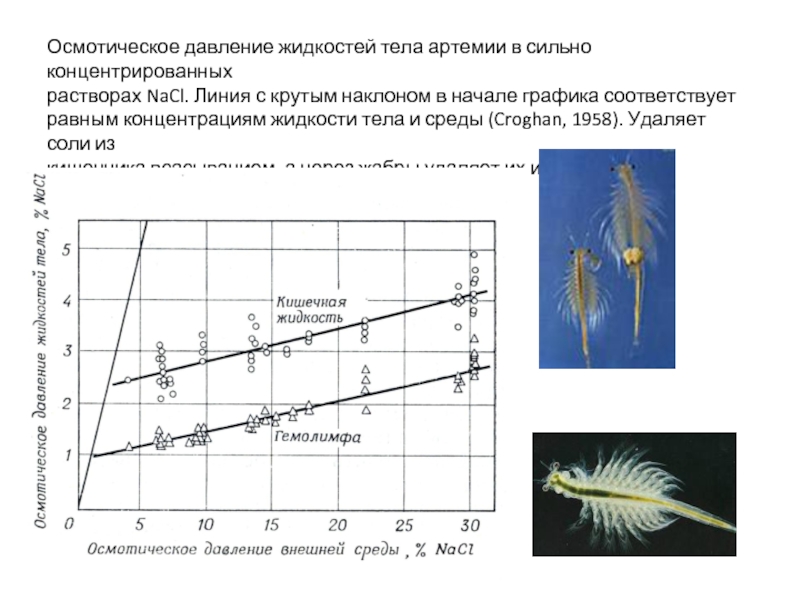
Слайд 27Осмотическое давление жидкостей тела артемии в сильно концентрированных
растворах NaCl. Линия с
равным концентрациям жидкости тела и среды (Croghan, 1958). Удаляет соли из
кишечника всасыванием, а через жабры удаляет их из организма
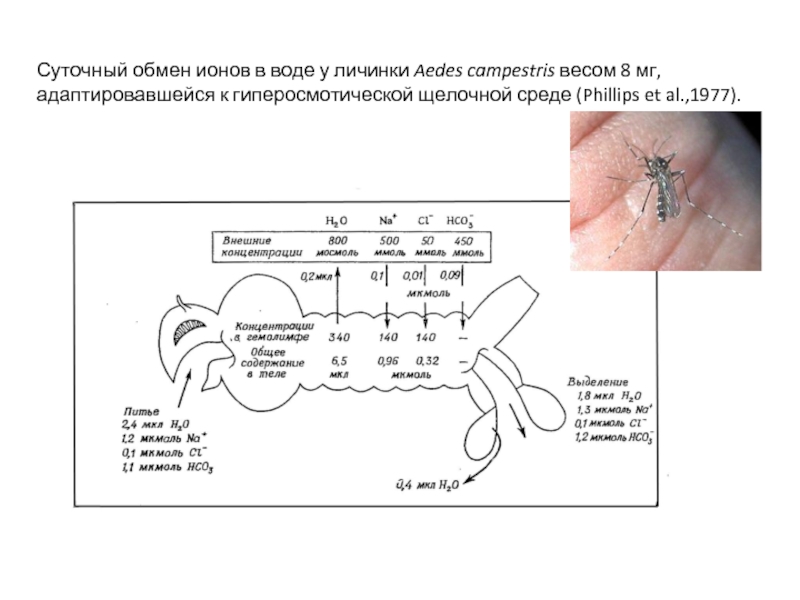
Слайд 28Суточный обмен ионов в воде у личинки Aedes campestris весом 8
адаптировавшейся к гиперосмотической щелочной среде (Phillips et al.,1977).
Слайд 29
Среди морских рыб - 2 группы:
1) Нет проблем с осмосом
2) Проблема утечки воды (гипорегуляторы)
Пресноводные позвоночные: все гиперосмотические (сходны с пресноводными беспозвоночными)
Слайд 30Концентрация важнейших растворенных веществ (в миллимолях
на литр) в морской воде и
Среда Na K Мочевина мосмоль/л
*
*
*
*
*
*
* нет проблем с осмосом
* проблема утечки воды
Слайд 31
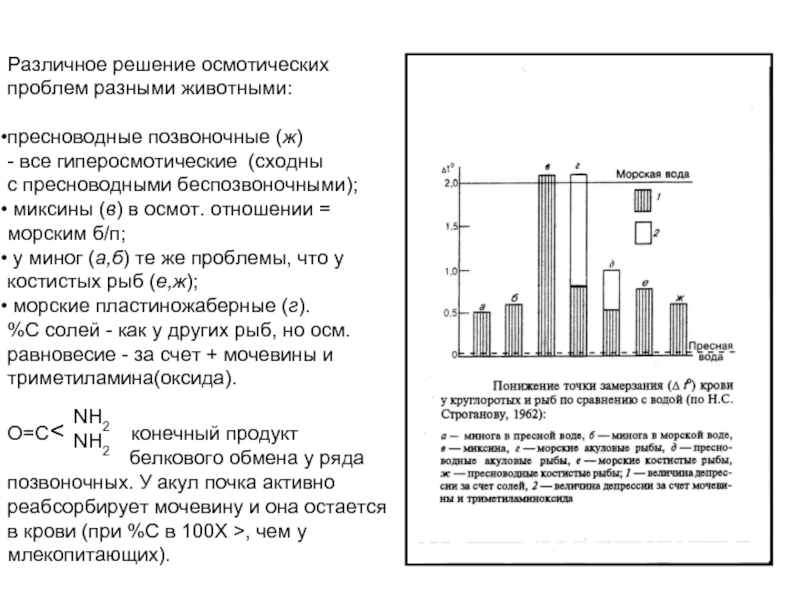
Различное решение осмотических
проблем разными животными:
пресноводные позвоночные (ж)
- все гиперосмотические (сходны
с пресноводными беспозвоночными);
миксины (в) в осмот. отношении =
морским б/п;
у миног (а,б) те же проблемы, что у
костистых рыб (е,ж);
морские пластиножаберные (г).
%С солей - как у других рыб, но осм.
равновесие - за счет + мочевины и
триметиламина(оксида).
O=C< конечный продукт
белкового обмена у ряда
позвоночных. У акул почка активно
реабсорбирует мочевину и она остается
в крови (при %С в 100Х >, чем у
млекопитающих).
NH2
NH2
Слайд 32%С Na+ в крови акул = 0.5 %С Na+ в морской
Na+ диффундирует через жабры + поступает с пищей,
(зато акулы не нуждаются в питье воды - нет проблем с осмосом – не поступает дополнительный Na+).
Он выводится почками и ректальной железой, имеющей проток в прямую кишку.
Осм. %С чуть > %С морской воды → небольшой приток
воды в организм через жабры → эта вода используется для выведения избытка ионов.
Слайд 33Концентрация растворенных веществ в сыворотке крови амазонского ската.
Они примерно такие же,
пластиножаберным, мочевина в в жидкостях его тела практически
отсутствует ( Thorson et al., 1967).
Слайд 34Рыба помещена в камеру, разделенную пополам резиновой перепонкой. Кожа не участвует
Слайд 37
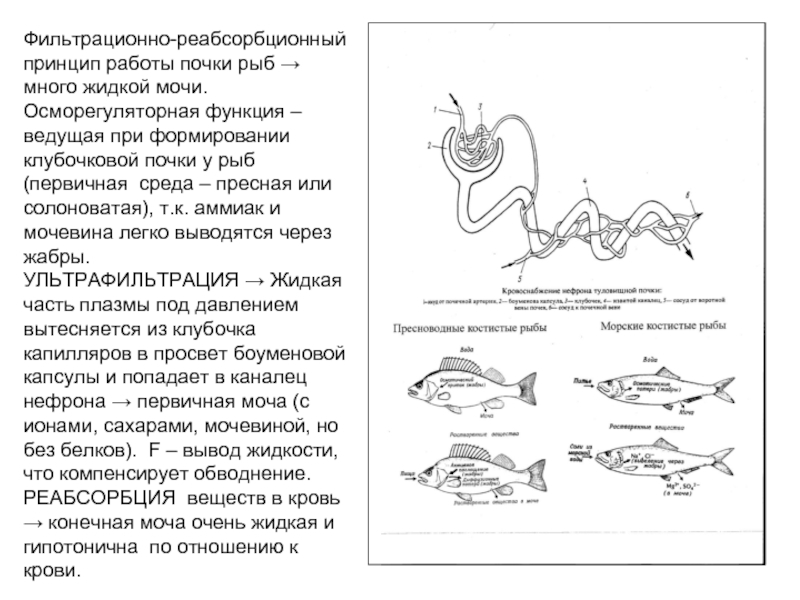
Фильтрационно-реабсорбционный принцип работы почки рыб → много жидкой мочи.
Осморегуляторная функция –
ведущая при формировании клубочковой почки у рыб (первичная среда – пресная или
солоноватая), т.к. аммиак и мочевина легко выводятся через жабры.
УЛЬТРАФИЛЬТРАЦИЯ → Жидкая часть плазмы под давлением вытесняется из клубочка капилляров в просвет боуменовой капсулы и попадает в каналец нефрона → первичная моча (с ионами, сахарами, мочевиной, но без белков). F – вывод жидкости, что компенсирует обводнение. РЕАБСОРБЦИЯ веществ в кровь → конечная моча очень жидкая и гипотонична по отношению к крови.
Слайд 38Выход на сушу → выработка адаптаций к
уменьшению влагопотерь.
Промежуточное положение
с водной средой (+ не у всех ad перешли на легочное
дыхание – см., например, Necturus maculosus).
По осморегуляции амфибии сходны с костистыми рыбами
(выведение жидкой мочи). Потеря солей через
мочу и кожу → активный захват кожей солей из
сильно разведенной среды.
Особое свойство крабоядной лягушки Rana cancrivora
Слайд 39Концентрация важнейших растворенных веществ (в миллимолях
на литр) в морской воде и
Среда Na K Мочевина мосмоль/л
*
*
*
*
*
*
* нет проблем с осмосом
* проблема утечки воды