- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Углеводы. Моносахариды и их производные. (Лекция 5) презентация
Содержание
- 1. Углеводы. Моносахариды и их производные. (Лекция 5)
- 2. ЦЕЛИ ЛЕКЦИИ ОБУЧАЮЩАЯ:
- 3. ПЛАН ЛЕКЦИИ Классификация Моносахариды, строение Химические свойства моносахаридов Производные моносахаридов, строение
- 4. Углеводы входят в состав
- 5. Биологические функции углеводов
- 6. Биологические функции углеводов
- 7. Кератансульфат Хондроитинсульфат Гиалуроновая кислота Связующие белки Сердцевидный
- 8. В состав внеклеточного матрикса также входят гликопротеины
- 9. Полисахарид хитин (C8H13NO5)n (от греч. χιτών: хитон
- 10. Биологические функции углеводов
- 11. Биологические функции углеводов
- 12. Биологические функции углеводов
- 13. Биологические функции углеводов
- 14. Биологические функции углеводов
- 15. Прием легкоферментируемых углеводов (кондитерские изделия,
- 16. Биологические функции углеводов Хорошо, что появилась
- 17. Углеводы входят в состав фарм. препаратов. Медико-биологическое значение темы Моносахариды
- 18. Полисахариды Медико-биологическое значение темы
- 19. Находит применение бактериальная целлюлоза.
- 20. Образование углеводов 6CO2 + 6H2O → C6H12O6
- 21. Elysia chlorotica Elysia chlorotica —
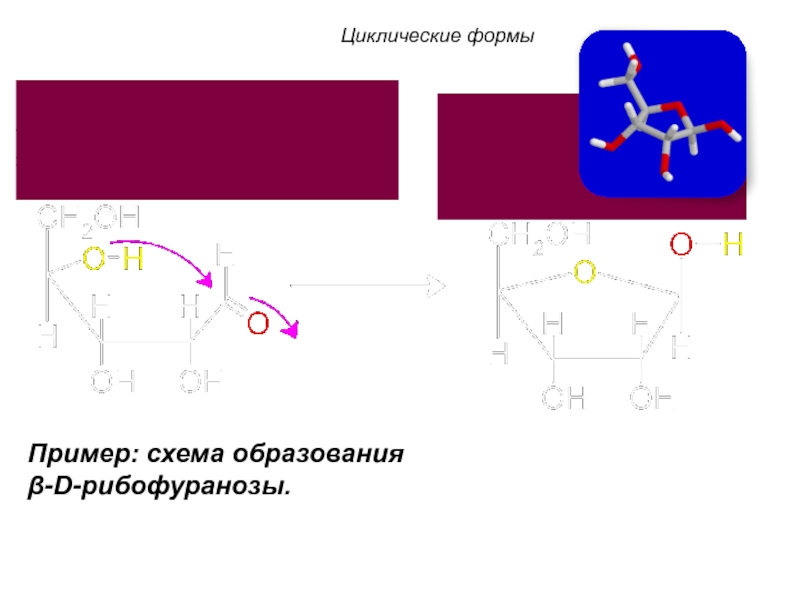
- 22. 2. Углеводы образуются в
- 23. Моносахариды Углеводы Углеводы - гетерофункциональные соединения полигидроксикарбонильного
- 24. Классификация углеводов По способности к гидролизу
- 25. Классификация углеводов
- 26. Классификация углеводов Олигосахариды
- 27. Моносахариды Моносахариды относятся к полигидроксикарбонильным соединениям. Классификация
- 28. Номенклатура
- 30. Стереоизомерия Молекулы моносахаридов имеют несколько
- 31. Энантиомеры – это изомеры, которые относятся друг
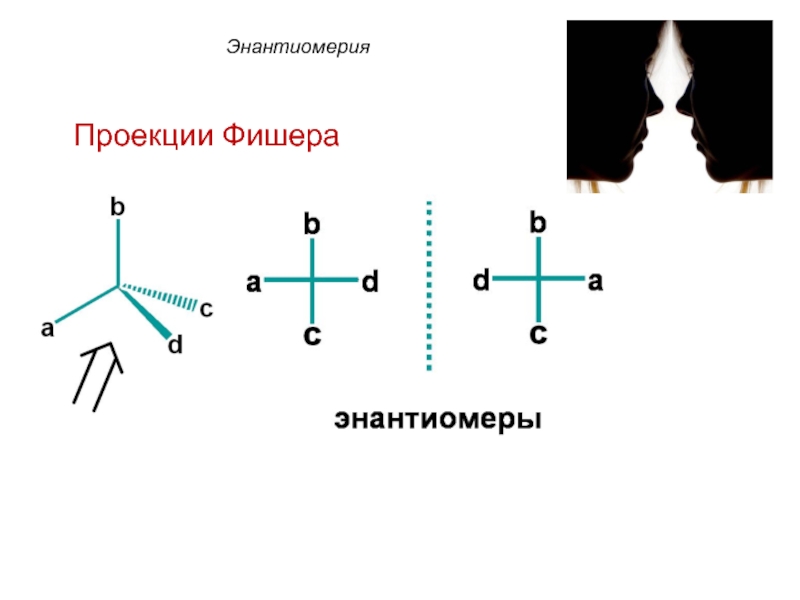
- 32. Энантиомерия Проекции Фишера
- 33. Энантиомерия В зависимости от конфигурации
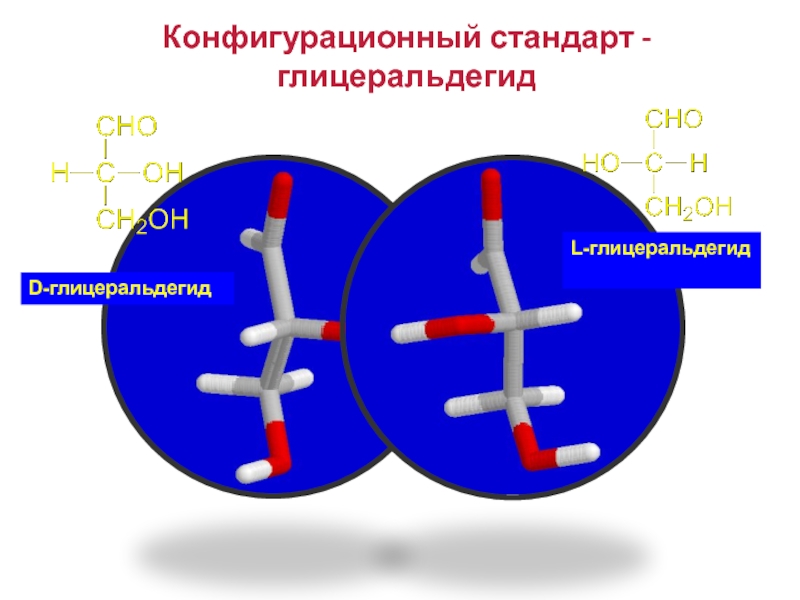
- 34. Конфигурационный стандарт - глицеральдегид D-глицеральдегид L-глицеральдегид
- 36. Энантиомерия Энантиомерам D-ряда
- 38. Энантиомеры обладают одинаковыми физическими и
- 40. σ - Диастереомерия σ-Диастереомерия возникает в молекулах с 2 и более центрами хиральности.
- 41. Число стереоизомеров рассчитывают по формуле
- 43. Альдогексозы D-глюкоза 1. Глюкоза (виноградный
- 44. Альдогексозы Глюкоза Международное наименование: Декстроза (Dextrose) 5%
- 45. Альдогексозы D-галактоза D-галактоза входит в
- 46. Альдогексозы Галактоза (Galactose) – ультразвуковое контрастно-диагностическое средство.
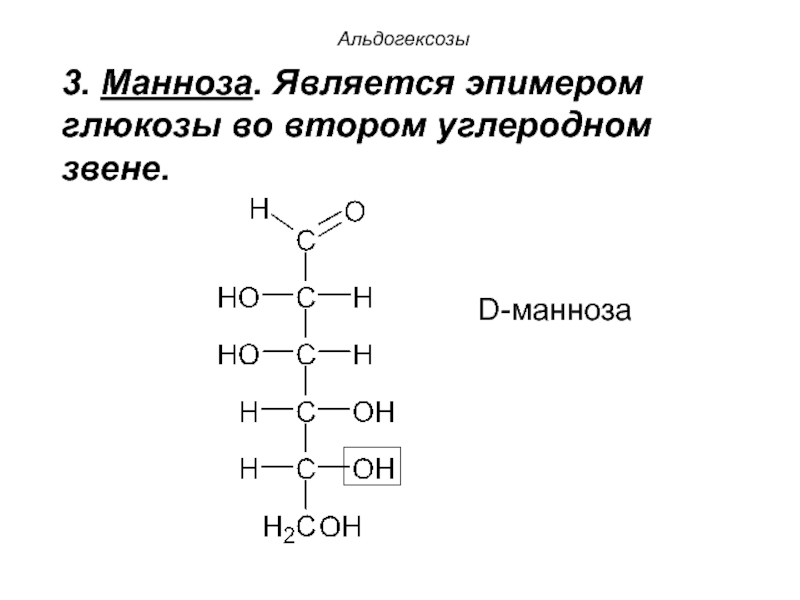
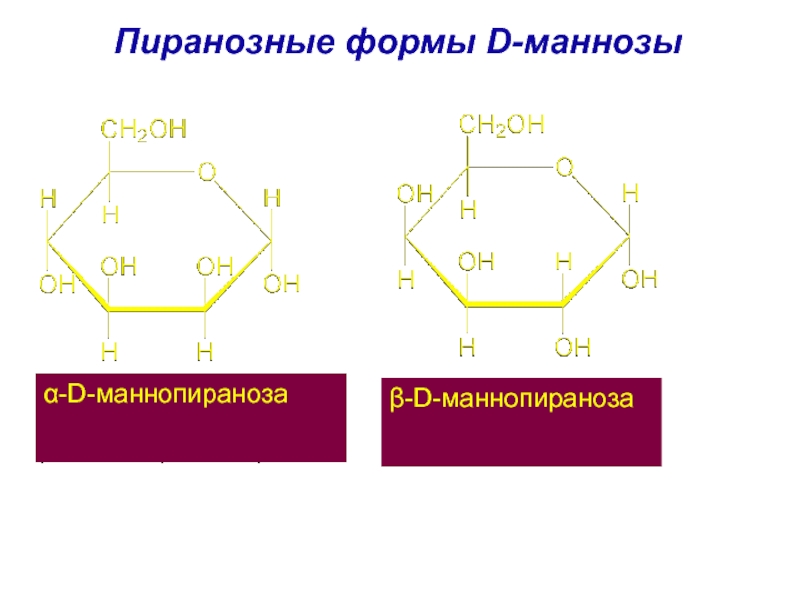
- 47. 3. Манноза. Является эпимером глюкозы во втором углеродном звене. Альдогексозы D-манноза
- 48. Альдопентозы 1.
- 49. D-рибоза D-ксилоза D-дезоксирибоза эпимеры Альдопентозы H
- 50. Кетогексозы D-фруктоза. Содержится в мёде, фруктах,
- 51. Фруктоза - парентеральное средство для регидратации и дезинтоксикации. Кетогексозы
- 52. «Открытие меда» - Пье́ро ди Ко́зимо (1462). (Вустерский «Музей искусств»)
- 53. Циклические формы моносахаридов
- 54. C C C C C C O
- 55. C C C C C C O
- 56. C C C C C C O
- 57. C C C C C C O
- 58. C C C C C C O
- 59. C C C C C C O
- 60. Циклические формы моносахаридов
- 61. β-аномер
- 63. Фуран
- 64. Моносахариды Нумерацию цепи
- 65. α-аномер β-аномер Моносахариды
- 66. Переход линейной формы в циклическую 1. Поворот
- 67. C C C C C C O
- 68. C C C C C C O
- 69. Циклические формы β-форма
- 70. Пример: схема образования β-D-рибофуранозы. Циклические формы
- 71. Моносахариды В растворе моносахариды
- 72. Кольчато-цепная таутомерия
- 73. Фуранозные формы D-рибозы D-рибоза α-D-рибофураноза β-D-рибофураноза
- 74. Пиранозные формы D-маннозы α-D-маннопираноза β-D-маннопираноза
- 75. Фуранозные формы D-фруктозы α-D- фруктофураноза
- 76. Таутомерия Кольчато-цепная таутомерия
- 77. Конформации молекул моносахаридов В реальности
- 79. α-D-маннопираноза
- 80. Физические свойства Моносахариды представляют собой
- 81. Физические свойства
- 82. Сахарин (E954), 500 раз Этоксифенилмочевина (дульцин),
- 83. Белок монеллин из тропического растения Dioscoreophyllum cumminsii в 3000 раз слаще сахарозы. Физические свойства
- 84. Белок тауматин (E957) из тропического растения Thaumacoccus
- 85. Белок миракулин из Synsepalum
- 86. Физические свойства Фрукт Synsepalum dulcificum сам по
- 88. Производные моносахаридов Аминосахара – образуются
- 91. N-ацетил-α-D-глюкозамин 2-ацетамидо-2-дезокси-α-D-глюкопираноза Аминосахара Аминогруппа часто ацилирована остатком
- 92. N-ацетил-D-галактозамин 2-ацетамидо-2-дезокси-D-галактопираноза Аминосахара Аминосахара входят в состав
- 93. Уроновые (сахарные) кислоты
- 94. Моносахариды Уроновые кислоты (от греч.
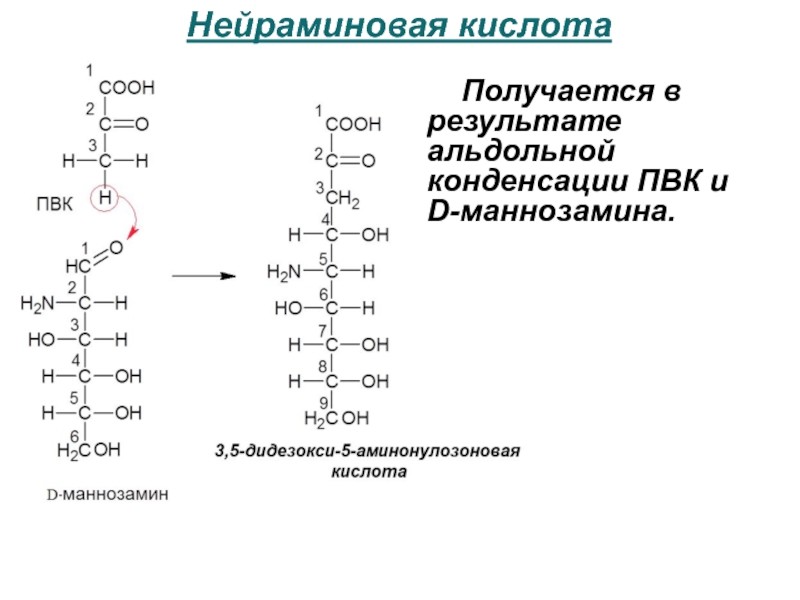
- 95. Нейраминовая кислота Получается в результате альдольной конденсации ПВК и D-маннозамина.
- 96. N-ацетил-D-нейраминовая кислота (сиаловая кислота) Сиаловые кислоты
- 97. Сиаловые кислоты N-ацетил-D-нейраминовая кислота (сиаловая кислота)
- 98. Моносахариды Нейраминовые и сиаловые кислоты
- 99. Химические свойства моносахаридов
- 100. Химические свойства I. Свойства многоатомных спиртов.
- 101. 2. Ацилирование: D-глюкопираноза 1,2,3,4,6-пентаацетал-D-глюкопираноза Химические свойства
- 102. α,D-глюкопираноза 6-фосфат α,D-глюкопиранозы Химические
- 103. II. Свойства альдегидов, 1. Окисление моносахаридов а)
- 104. Химические свойства Качественная реакция с мягкими
- 105. Реакция с Cu(OH)2 называется пробой Троммера и
- 106. б) Гликаровые кислоты образуются при жёстком
- 107. в) Гликуроновые (уроновые) кислоты образуются при окислении
- 108. Гликуроновые (уроновые) кислоты образуются при окислении
- 109. Химические свойства
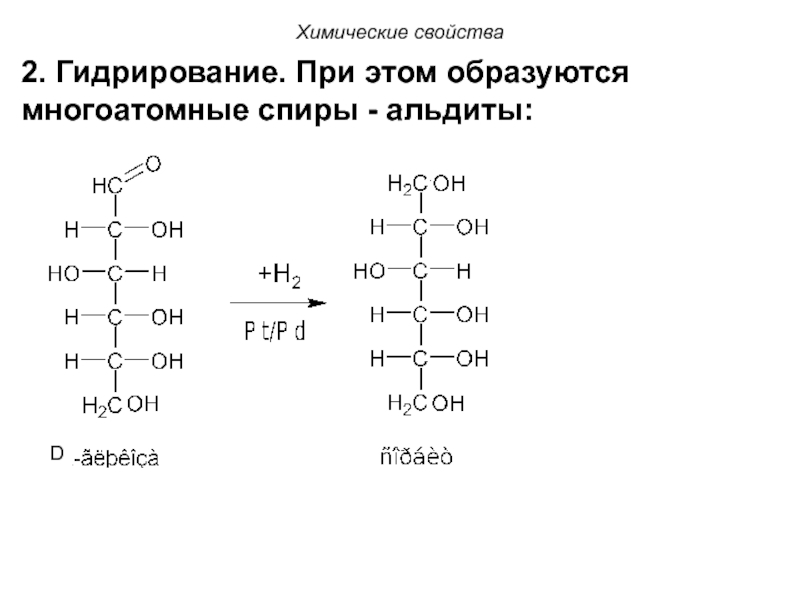
- 110. Химические свойства 2. Гидрирование. При этом образуются многоатомные спиры - альдиты: D
- 111. D-глюкоза образует глицит (сорбит, E420), D-манноза -
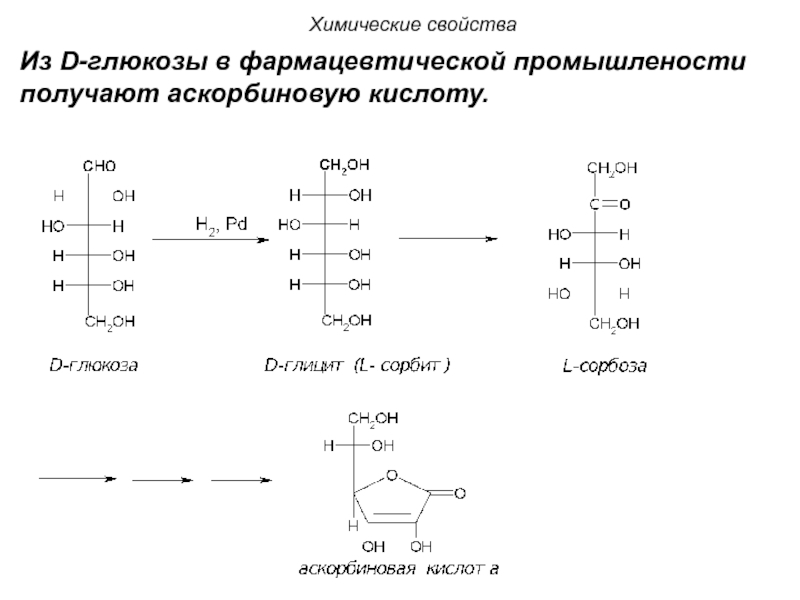
- 112. Химические свойства Из D-глюкозы в фармацевтической промышлености получают аскорбиновую кислоту.
- 113. Аскорбиновая кислота (а – отрицающая частица
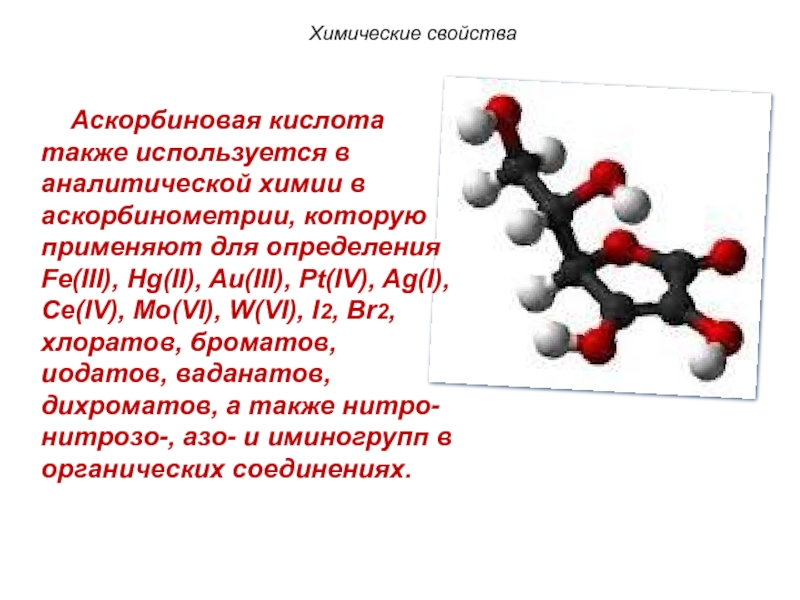
- 114. Аскорбиновая кислота также используется в
- 115. β,D-глюкопираноза Метил-β-D-глюкопиранозид Химические свойства III. Свойства полуацеталей
- 116. IV. Специфические свойства 1. Спиртовое брожение Химические
- 117. 2. Молочнокислое брожение Химические свойства C6H12O6
- 118. Вопросы для самоконтроля Перечислите биологически важные
- 119. СПАСИБО ЗА ВАШЕ ВНИМАНИЕ!
Слайд 1Углеводы. Моносахариды и их производные
ОМСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ
КАФЕДРА ХИМИИ
БИООРГАНИЧЕСКАЯ ХИМИЯ
Лекция 5
Лектор:
профессор, зав. кафедрой химии
Слайд 2 ЦЕЛИ ЛЕКЦИИ
ОБУЧАЮЩАЯ: сформировать знания о строении, номенклатуре
РАЗВИВАЮЩАЯ: расширить кругозор обучающихся на основе интеграции знаний, развить логическое мышление.
ВОСПИТАТЕЛЬНАЯ: содействовать формированию у обучающихся устойчивого интереса к изучению дисциплины.
Слайд 3ПЛАН ЛЕКЦИИ
Классификация
Моносахариды, строение
Химические свойства моносахаридов
Производные моносахаридов, строение
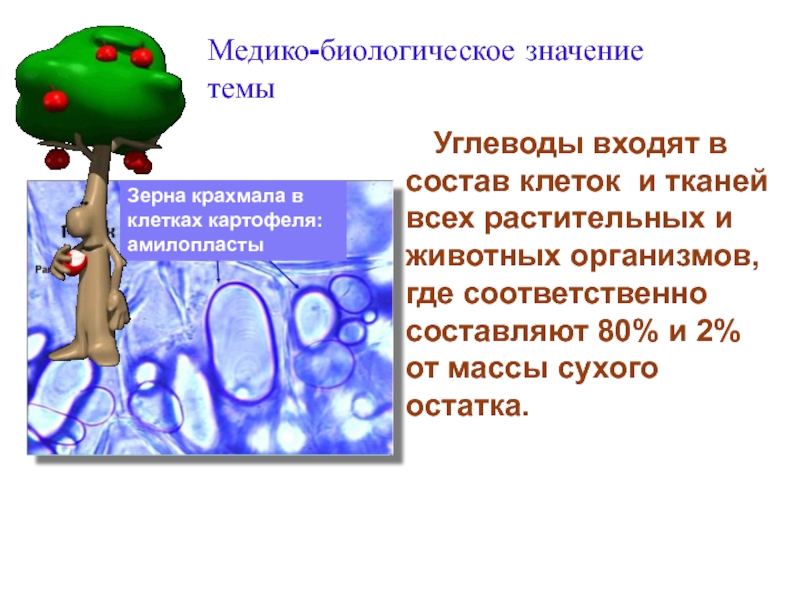
Слайд 4 Углеводы входят в состав клеток и тканей всех
Медико-биологическое значение темы
Зерна крахмала в клетках картофеля: амилопласты
Слайд 5
Биологические функции углеводов
1. Энергетическая. Углеводы –
главный вид
При сгорании 1 моль глюкозы
выделяется 3060 Дж энергии,
которая расходуется в
эндотермических биологических
процессах и частично
аккумулируется в АТФ.
Слайд 6
Биологические функции углеводов
2. Пластическая.
Углеводы являются
Хондроитинсульфат
Снаружи
Внутри
Гепарансульфат
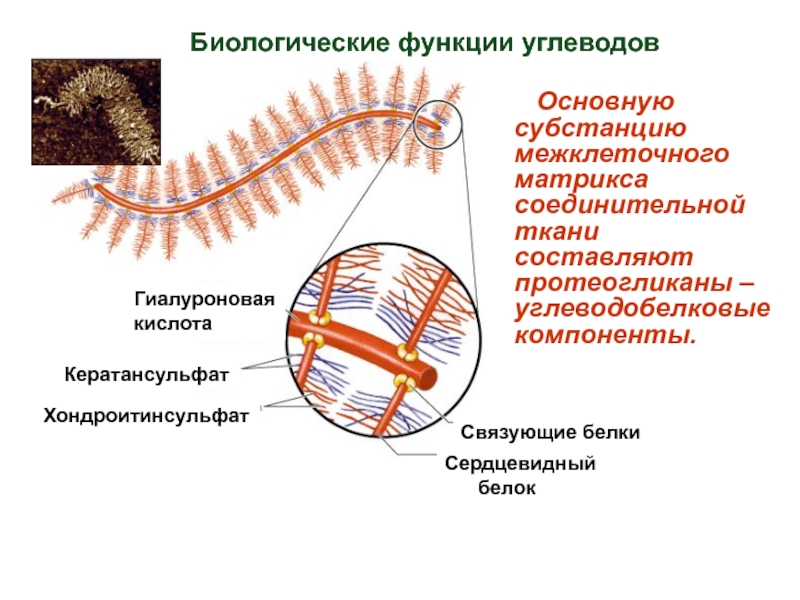
Слайд 7Кератансульфат
Хондроитинсульфат
Гиалуроновая
кислота
Связующие белки
Сердцевидный
белок
Основную субстанцию межклеточного матрикса
Биологические функции углеводов
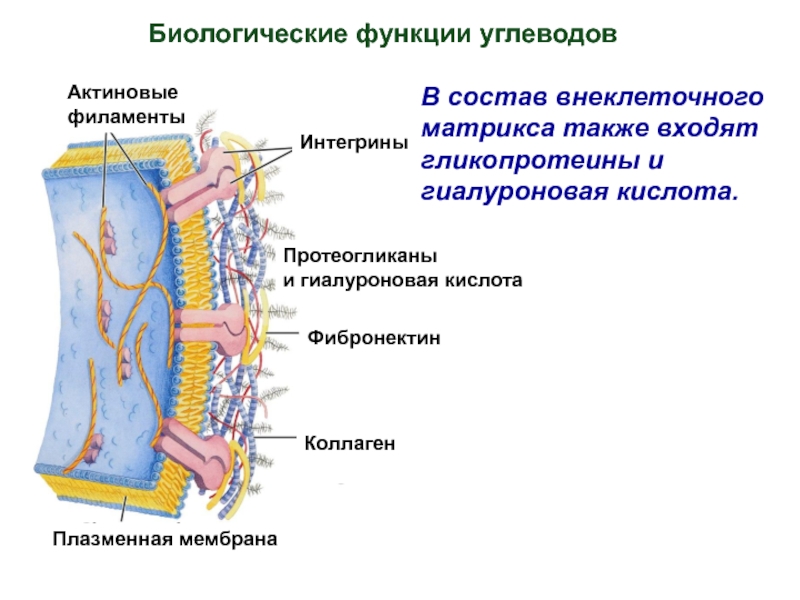
Слайд 8В состав внеклеточного матрикса также входят гликопротеины и гиалуроновая кислота.
Биологические функции
Плазменная мембрана
Протеогликаны
и гиалуроновая кислота
Фибронектин
Интегрины
Коллаген
Актиновые
филаменты
Слайд 9Полисахарид хитин (C8H13NO5)n (от греч. χιτών: хитон — одежда, кожа, оболочка)
Биологические функции углеводов
Слайд 10
Биологические функции углеводов
3. Синтетическая. Углеводы участвуют в синтезе
β2-Гликопротеин I
Слайд 11
Биологические функции углеводов
4. Защитная. Углеводы участвуют в поддержании иммунитета
Тиреотропный гормон
Слайд 12
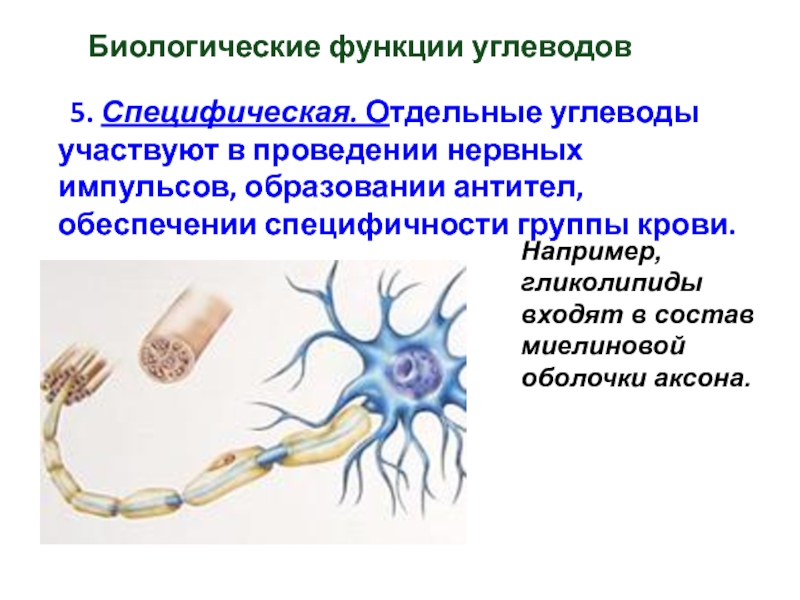
Биологические функции углеводов
5. Специфическая. Отдельные углеводы участвуют в
Например, гликолипиды входят в состав миелиновой оболочки аксона.
Слайд 13
Биологические функции углеводов
6. Регуляторная. Растительная пища содержит
Слайд 14
Биологические функции углеводов
Для оптимального обеспечения организма человека углеводами
Высокоуглеводный рацион питания может привести к ожирению.
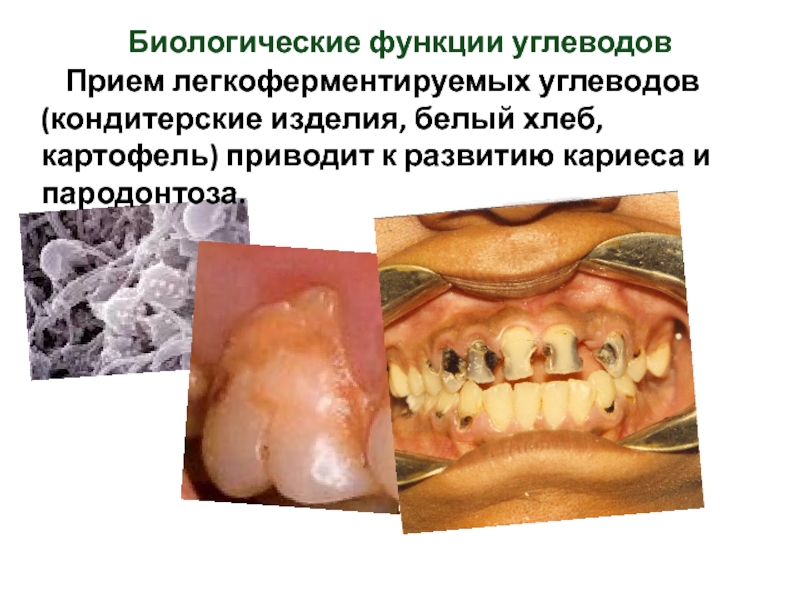
Слайд 15 Прием легкоферментируемых углеводов (кондитерские изделия, белый хлеб, картофель) приводит
Биологические функции углеводов
Слайд 16Биологические функции углеводов
Хорошо, что появилась низкоуглеводная диета. Сейчас никто не хочет
Слайд 19 Находит применение бактериальная целлюлоза.
Чайный гриб – симбиоз дрожжеподобного
гриба Saccharomycodes ludwigii
и бактерий Acetobacter xylinum
Медико-биологическое значение темы
Слайд 20Образование углеводов
6CO2 + 6H2O → C6H12O6 + 6O2
1.
Хлоропласты в клетках листа
Слайд 21Elysia chlorotica
Elysia chlorotica — вид морских слизней, относящийся к
Геном молюска кодирует некоторые белки, необходимые хлоропластам для фотосинтеза.
Образование углеводов
Моллюск использует хлоропласты морской водоросли Vaucheria litorea, которую употребляет в пищу.
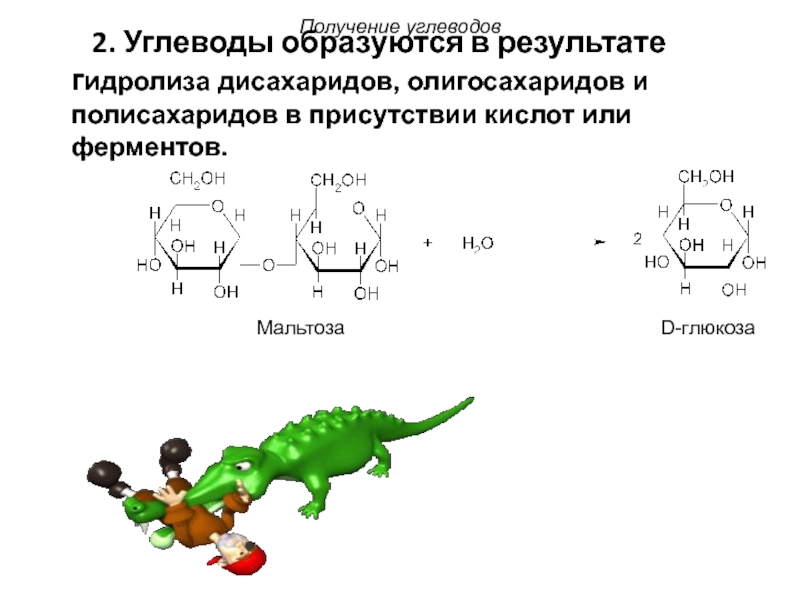
Слайд 22 2. Углеводы образуются в результате гидролиза дисахаридов, олигосахаридов и
Получение углеводов
Мальтоза D-глюкоза
Слайд 23Моносахариды
Углеводы
Углеводы - гетерофункциональные соединения полигидроксикарбонильного ряда и их производные.
Общая формула простых
Cn(H2O)m
Ранее сахара считали гидратированными формами углерода, что объясняет этимологию слова “углевод”.
Англ. Carbohydrate происходит от carbon (углерод) и гидрат (от греч. υδορ – вода).
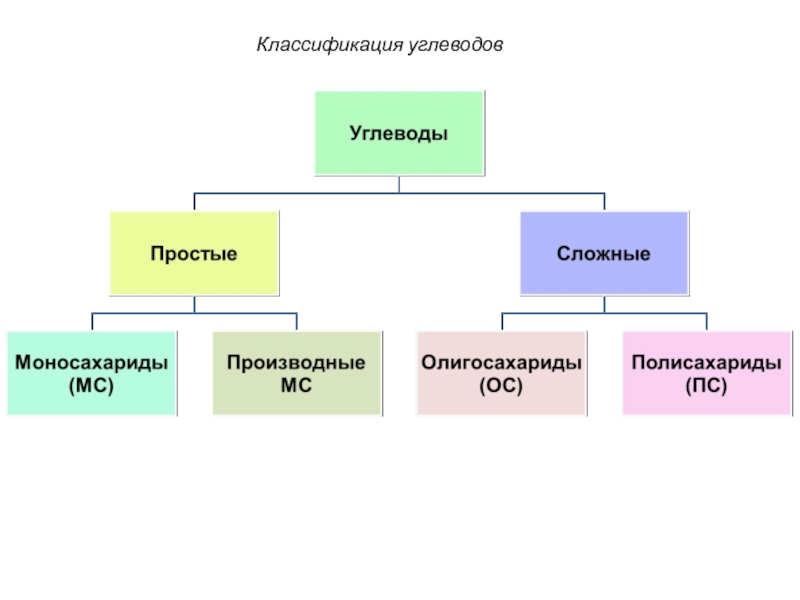
Слайд 24Классификация углеводов
По способности к гидролизу углеводы делятся на 2 класса:
1.
– не подвергаются гидролизу;
2. сложные - гидролизуются с образованием простых углеводов.
Слайд 26Классификация углеводов
Олигосахариды содержат от 2 до 10
Полисахариды подразделяются на:
- гомополисахариды - однородные по составу сложные углеводы;
- гетерополисахариды - сложные углеводы, включающие остатки разных моносахаридов.
Слайд 27Моносахариды
Моносахариды относятся к полигидроксикарбонильным соединениям.
Классификация моносахаридов:
Моносахариды делят по функциональной принадлежности на:
2. кетозы – полигидроксикетоны.
По числу атомов углерода в цепи различают:
1. триозы;
2. тетрозы;
3. пентозы;
4. гексозы;
5. высшие сахара.
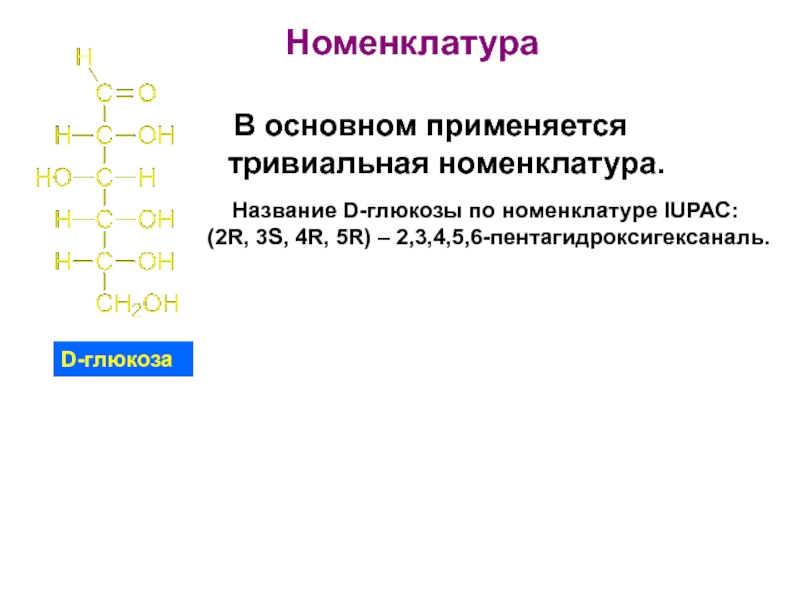
Слайд 28 Номенклатура
Название D-глюкозы
(2R, 3S, 4R, 5R) – 2,3,4,5,6-пентагидроксигексаналь.
D-глюкоза
В основном применяется тривиальная номенклатура.
Слайд 29
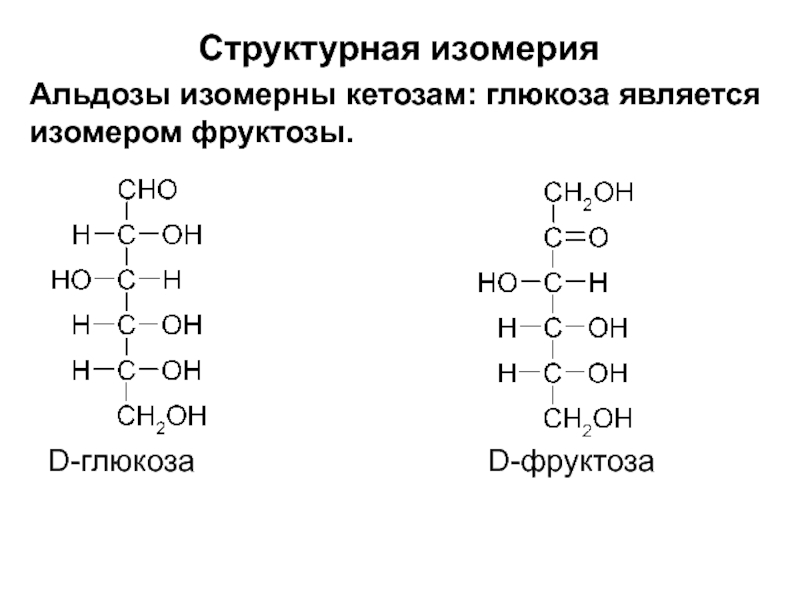
Альдозы изомерны кетозам: глюкоза является изомером фруктозы.
D-глюкоза D-фруктоза
Слайд 30Стереоизомерия
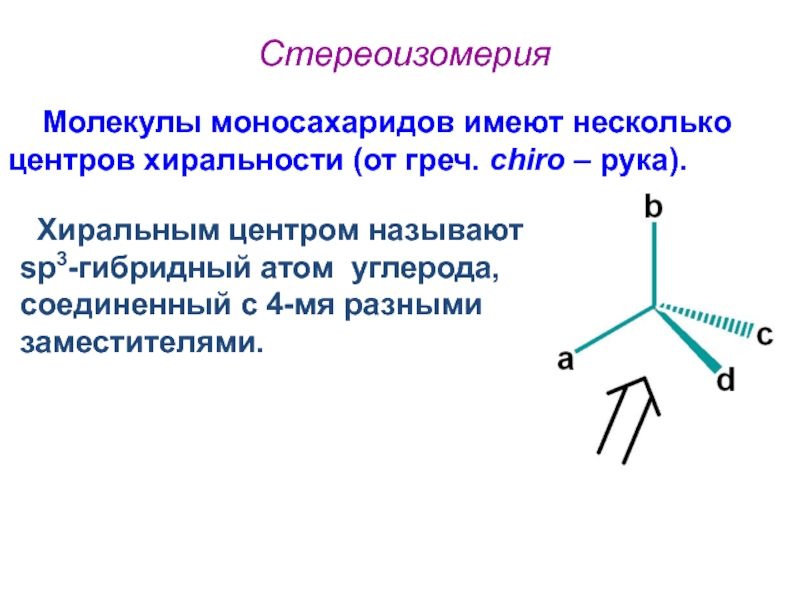
Молекулы моносахаридов имеют несколько центров хиральности (от греч. сhiro
Хиральным центром называют sp3-гибридный атом углерода, соединенный с 4-мя разными заместителями.
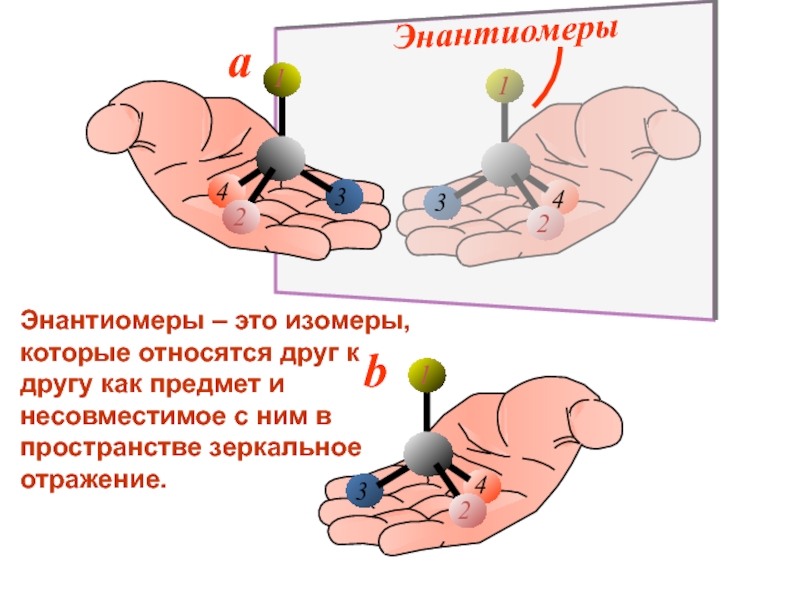
Слайд 31Энантиомеры – это изомеры, которые относятся друг к другу как предмет
Слайд 33Энантиомерия
В зависимости от конфигурации хирального центра различают D- и
В D-форме гидроксильная (-ОН) функциональная группа хирального центра располагается справа от углеродной цепи;
В L-форме – функциональная гидроксильная (-ОН) группа хирального центра располагается слева от углеродной цепи.
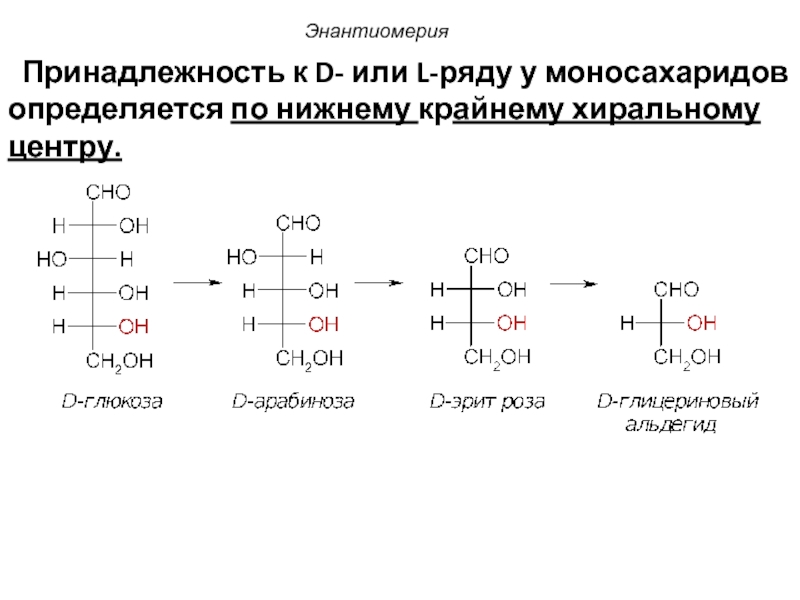
Слайд 35
Принадлежность к D- или L-ряду у моносахаридов определяется по нижнему крайнему хиральному центру.
Слайд 36 Энантиомерия
Энантиомерам D-ряда углеводов соответствует энантиомер L-ряда с
Большинство природных моносахаридов принадлежат D-ряду.
Слайд 38 Энантиомеры обладают одинаковыми физическими и химическими свойствами, но являются
Энантиомерия
Слайд 39
ячейка
Поляриметр
Угол вращения плоскости поляризованного света определяется с помощью поляриметра.
[α]
Энантиомерия
25°C
D
Слайд 41 Число стереоизомеров рассчитывают по формуле Фишера: Z =2n ,
где
σ - Диастереомерия
σ– Диастереомеры имеют разные физические и химические свойства и физиологическое действие.
Слайд 42 Диастереомерия
σ-Диастереомеры
Слайд 43
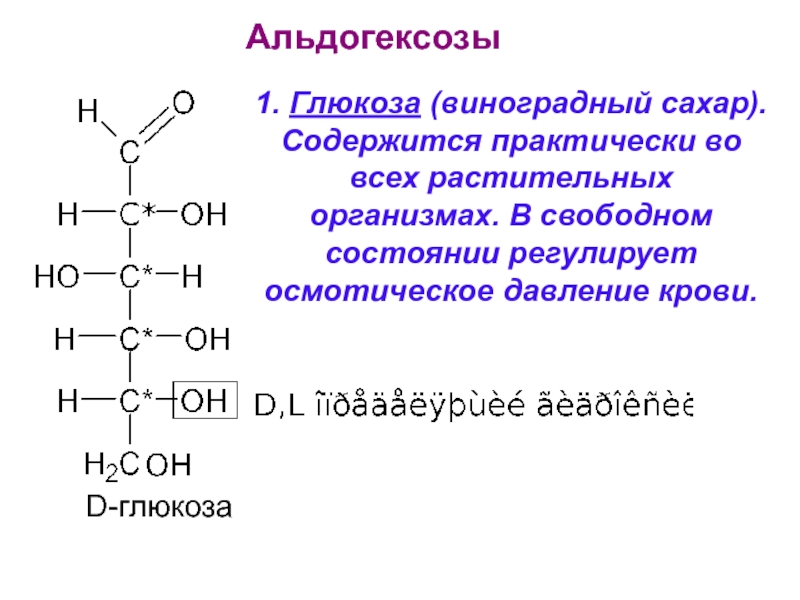
Альдогексозы
D-глюкоза
1. Глюкоза (виноградный сахар). Содержится практически во всех растительных организмах. В
Слайд 44Альдогексозы
Глюкоза
Международное наименование: Декстроза (Dextrose)
5% Раствор глюкозы оказывает дезинтоксикационное, метаболическое действие, является
Гипертонические растворы (10%, 20%, 40%) повышают осмотическое давление крови, улучшают обмен веществ; повышают сократимость миокарда; улучшают антитоксическую функцию печени, расширяют сосуды, увеличивают диурез.
Слайд 45Альдогексозы
D-галактоза
D-галактоза входит в состав лактозы и гликолипидов. В печени
2. Галактоза. Является эпимером глюкозы в четвертом углеродном звене.
Слайд 48
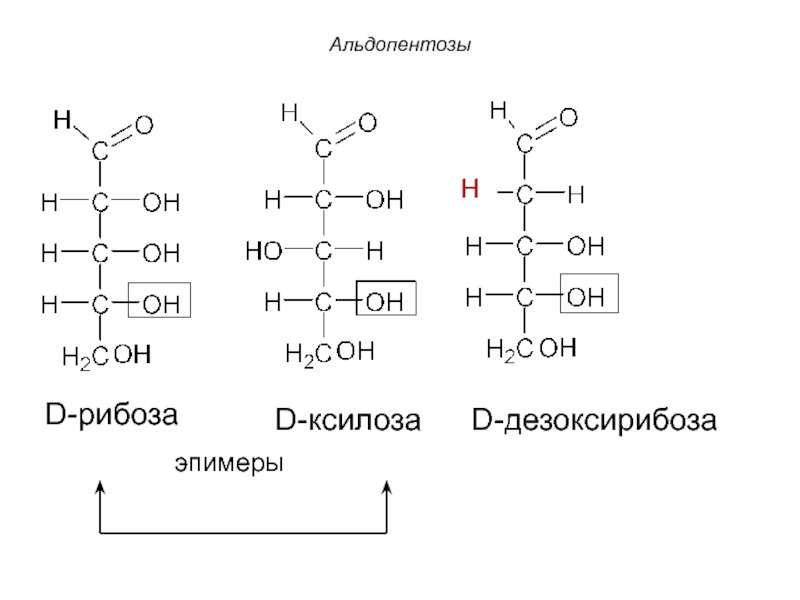
Альдопентозы
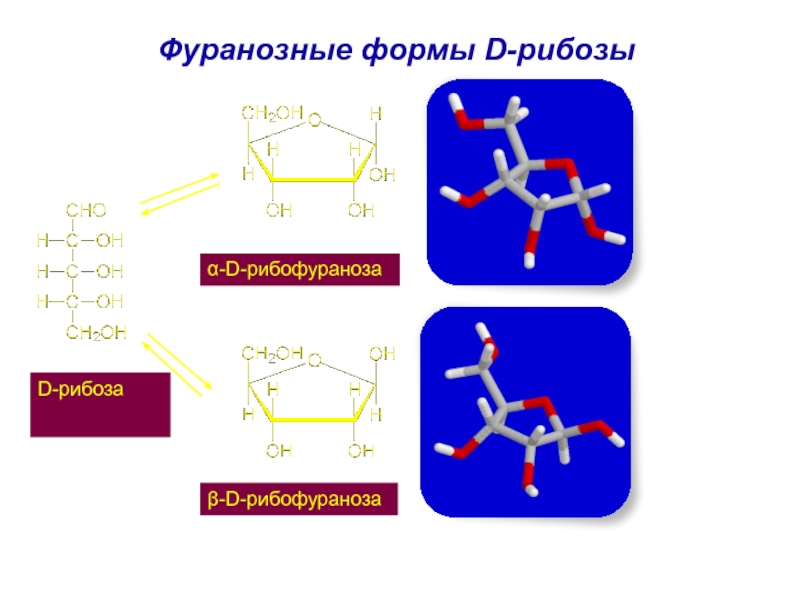
1. D-рибоза. Входит в состав нуклеотидов РНК.
3. Производным рибозы является дезоксисахар –2-дезокси-D-рибоза (дезоксирибоза) - входит в состав ДНК.
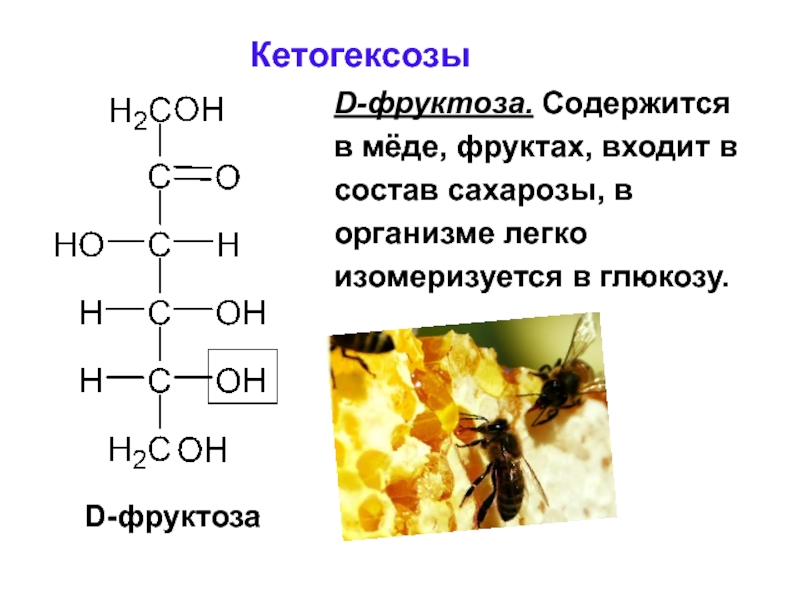
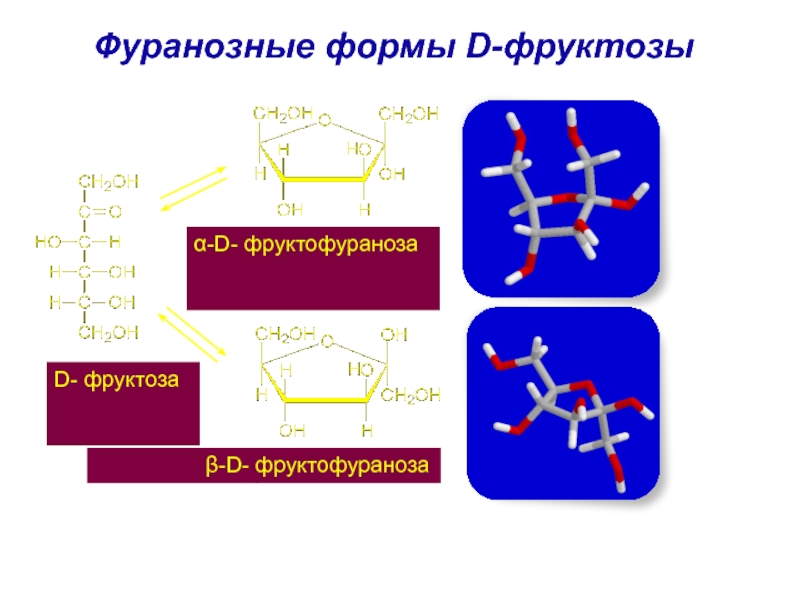
Слайд 50Кетогексозы
D-фруктоза. Содержится
в мёде, фруктах, входит в
состав сахарозы, в
организме
изомеризуется в глюкозу.
D-фруктоза
Слайд 53
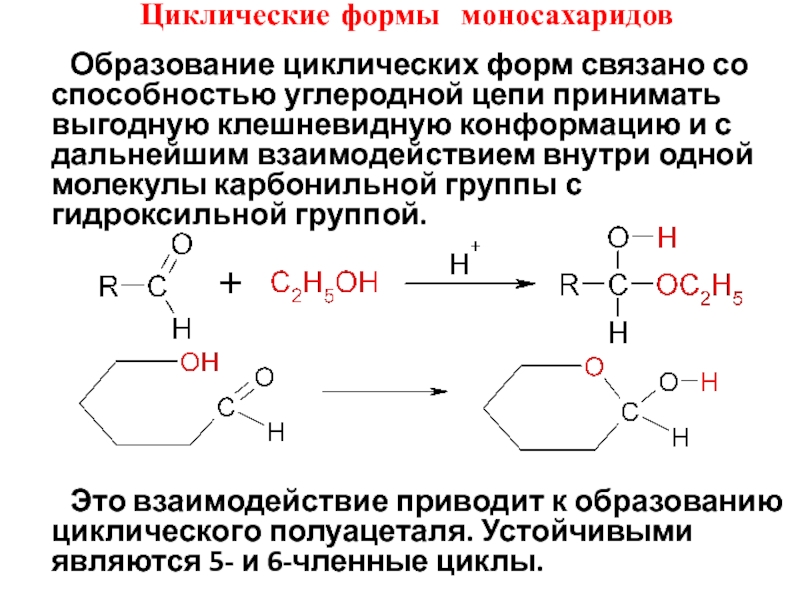
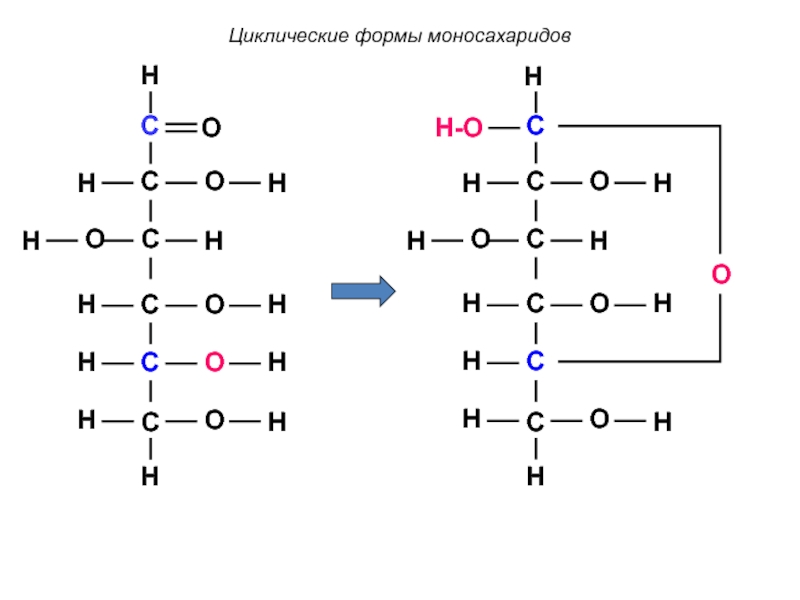
Циклические формы моносахаридов
Образование циклических форм связано со
Это взаимодействие приводит к образованию циклического полуацеталя. Устойчивыми являются 5- и 6-членные циклы.
Слайд 54C
C
C
C
C
C
O
O
O
O
O
O
H
H
H
H
H
H
H
H
H
H
H
H
Пример: образование 6-членных
Циклические формы моносахаридов по Фишеру
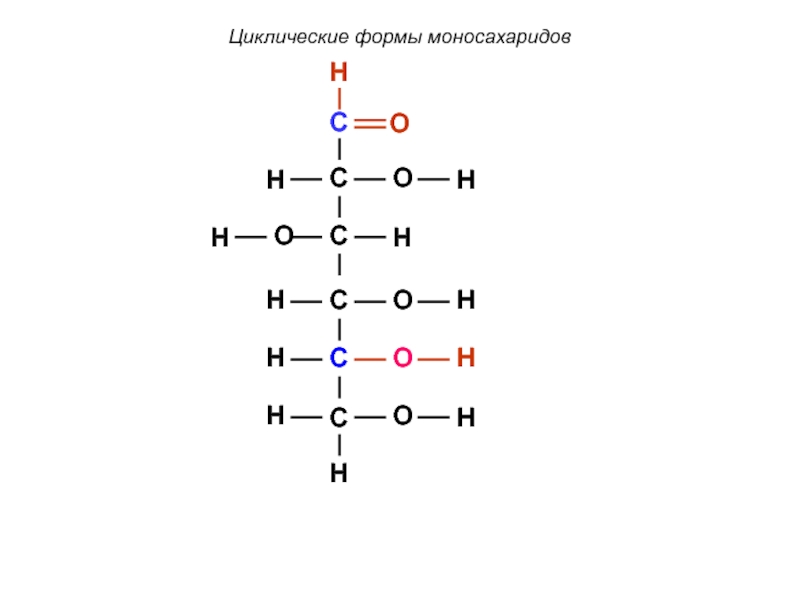
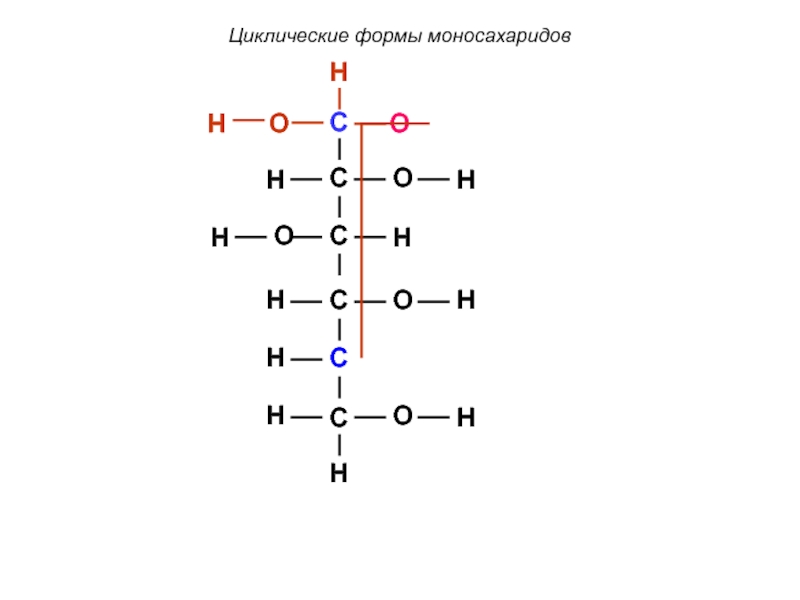
Слайд 60
Циклические формы моносахаридов
В случае образования циклического полуацеталя появляется
Два образующихся σ-диастереомера называются аномерами.
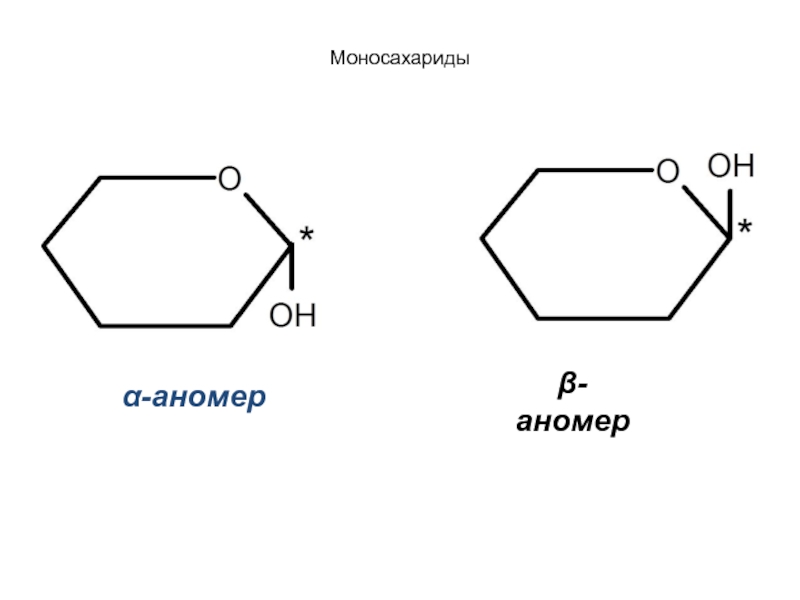
Слайд 61
β-аномер
Циклические формы моносахаридов
Если у циклической формы конфигурация аномерного центра такая же, как у концевого хирального центра, то это α-аномер, если противоположная, то β-аномер.
Образующаяся полуацетальная OH-группа называется гликозидной гидроксигруппой.
Слайд 62
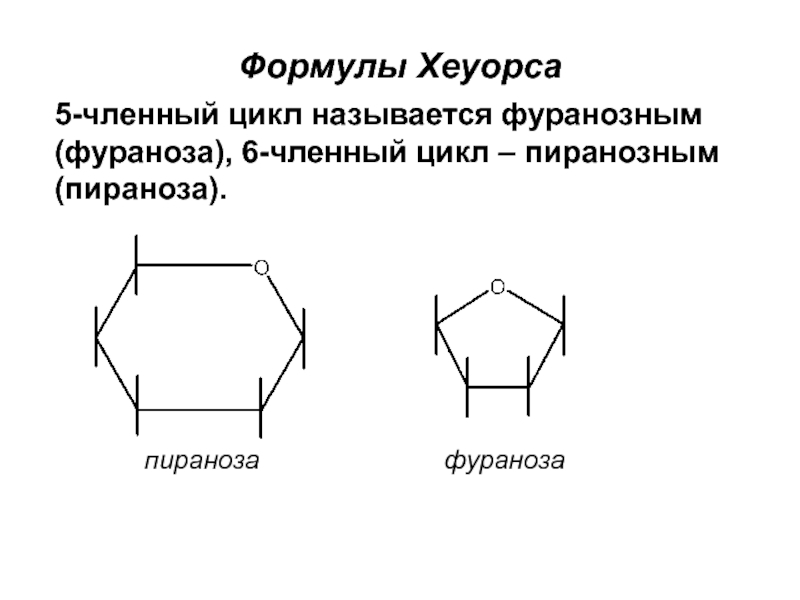
пираноза
Формулы Хеуорса
5-членный цикл называется фуранозным (фураноза), 6-членный цикл – пиранозным (пираноза).
Слайд 63 Фуран
Моносахариды
Названия циклов происходят от названия родственных гетероциклов: фурана и пирана.
В названиях циклических форм наряду с названием моносахарида указывается размер цикла в виде окончания «фураноза» или «пираноза».
Слайд 64Моносахариды
Нумерацию цепи в формулах Хеуорса ведут от
Если полуацетальный гидроксил расположен под плоскостью цикла, то имеем α-аномер.
Если полуацетальный гидроксил расположен над плоскостью цикла - β-аномер.
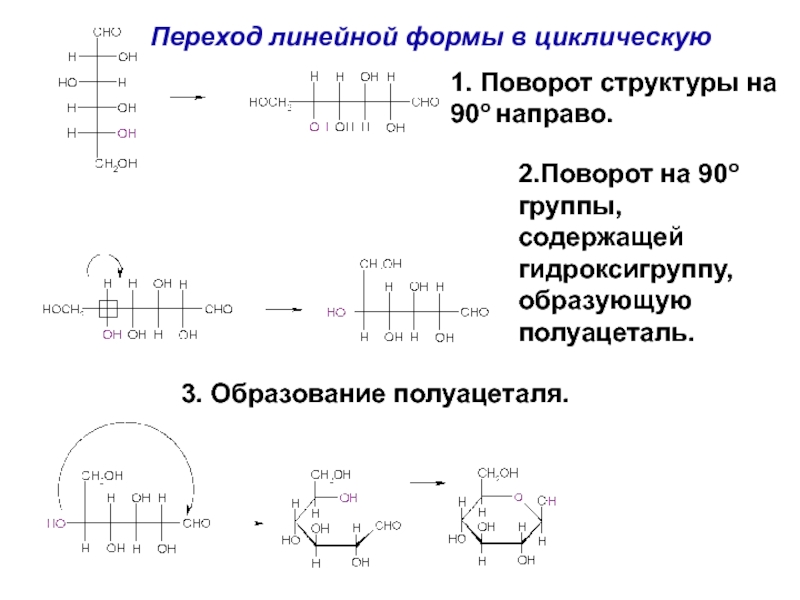
Слайд 66Переход линейной формы в циклическую
1. Поворот структуры на 90o направо.
2.Поворот на
3. Образование полуацеталя.
Слайд 67C
C
C
C
C
C
O
O
O
O
O
H
H
H
H
H
H
H
H
H
H
H
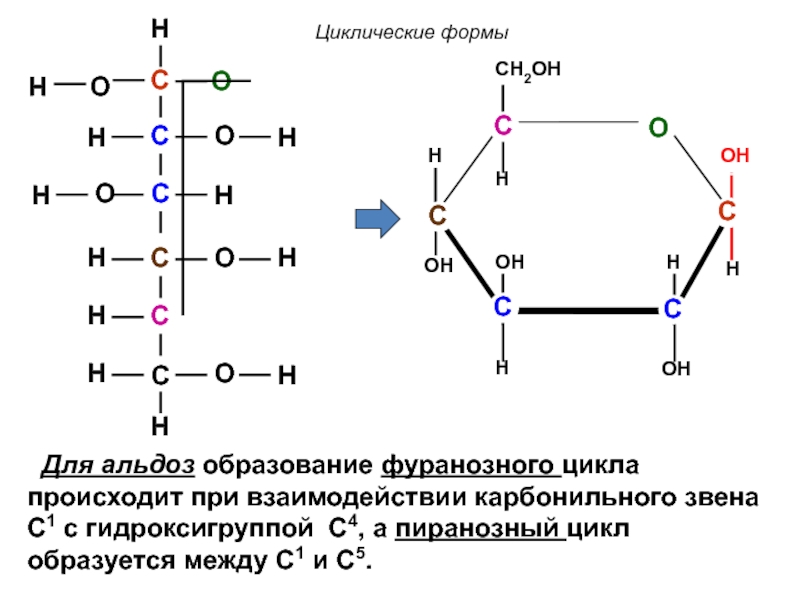
O
Для альдоз образование фуранозного цикла происходит при взаимодействии карбонильного звена
Циклические формы
Слайд 68C
C
C
C
C
C
O
O
O
O
H
H
H
H
H
H
H
H
H
H
O
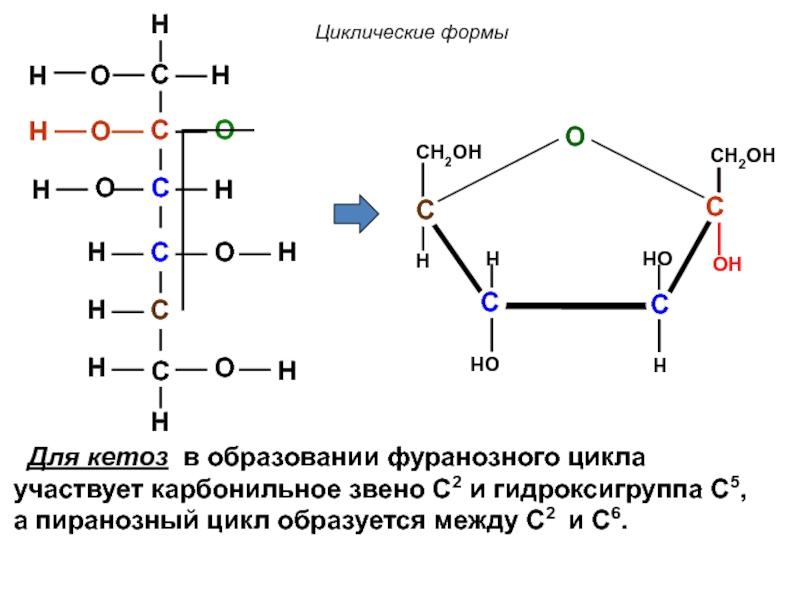
CH2OH
O
H
Для кетоз в образовании фуранозного цикла участвует карбонильное звено С2
Циклические формы
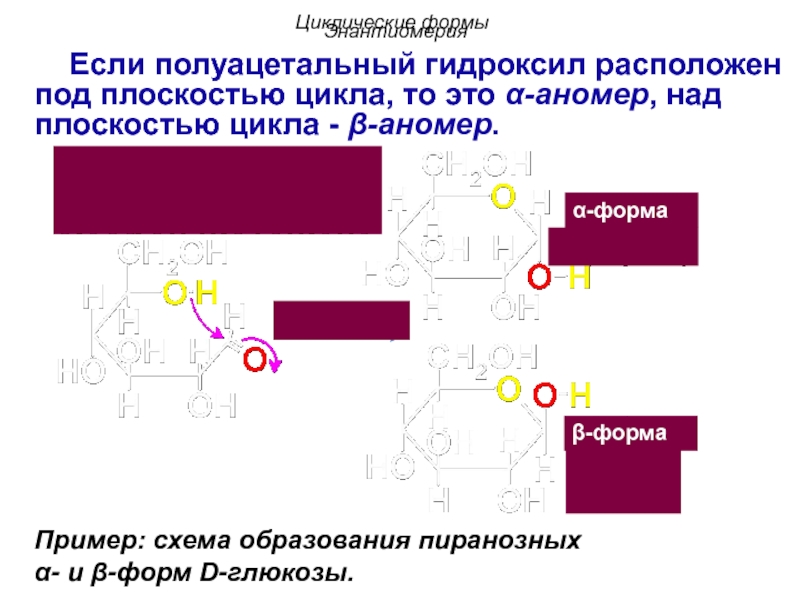
Слайд 69Циклические формы
β-форма
Пример: схема образования пиранозных
Если полуацетальный гидроксил расположен под плоскостью цикла, то это α-аномер, над плоскостью цикла - β-аномер.
Энантиомерия
α-форма
Слайд 71Моносахариды
В растворе моносахариды присутствуют в открытых и циклических
Изомеры, взаимно переходящие друг в друга и находящиеся в состоянии динамического равновесия, называются таутомерами.
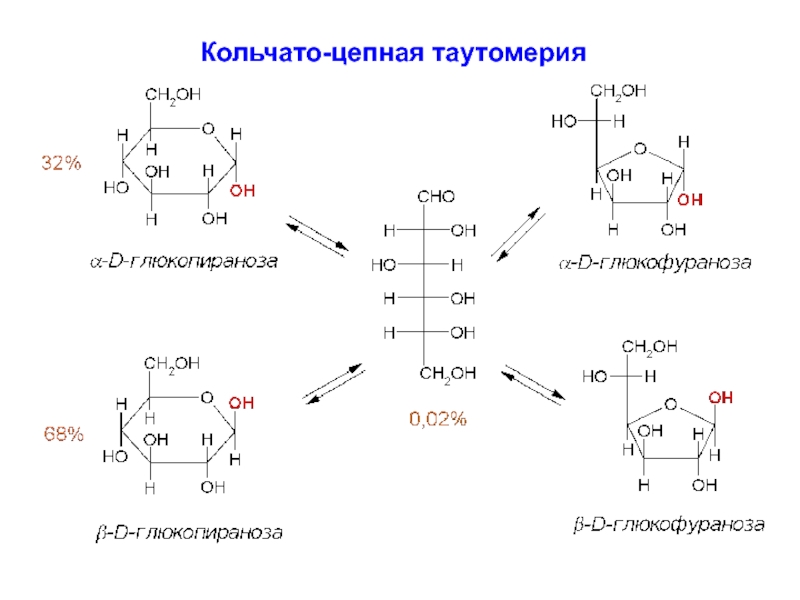
Слайд 76Таутомерия
Кольчато-цепная таутомерия сопровождается закономерным явлением –
Мутаротация (от лат. mutare – изменять, rotatio – вращение) в данном случае - это изменение вращения плоскости поляризации света свежеприготовленными растворами разных аномеров.
Например, a-D-глюкопираноза имеет удельное вращение [a] = +112o, а b-D-глюкопираноза имеет [a] = +19o. При стоянии свежеприготовленных растворов каждого из аномеров удельное вращение изменяется и достигает значения +52,5o, соответствующего равновесию.
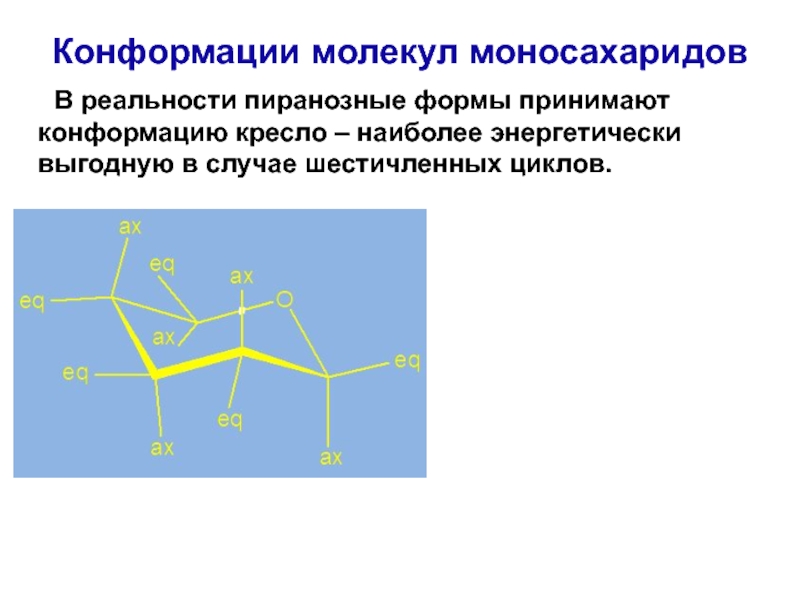
Слайд 77Конформации молекул моносахаридов
В реальности пиранозные формы принимают конформацию кресло
Слайд 78
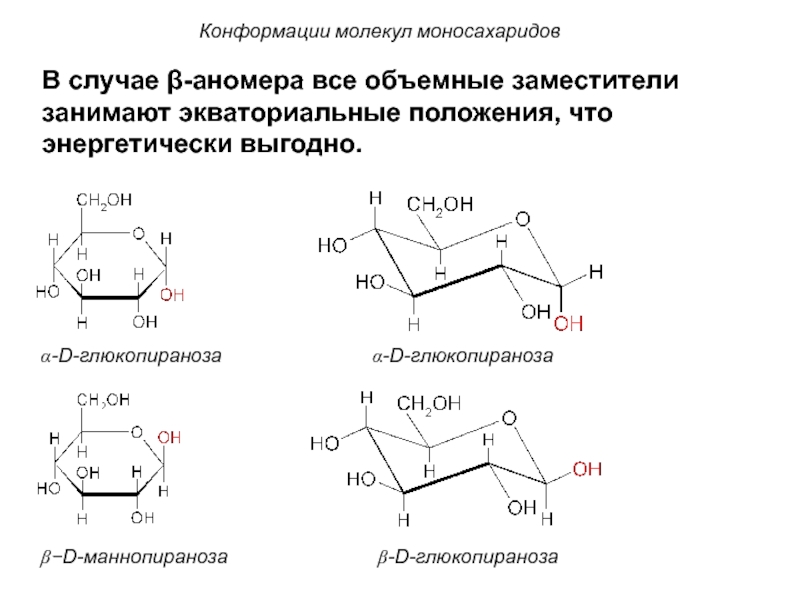
α-D-глюкопираноза α-D-глюкопираноза
β−D-маннопираноза β-D-глюкопираноза
В случае β-аномера все объемные заместители занимают экваториальные положения, что энергетически выгодно.
Слайд 79
α-D-маннопираноза
α-D-галактопираноза β-D-галактопираноза
Конформации молекул моносахаридов
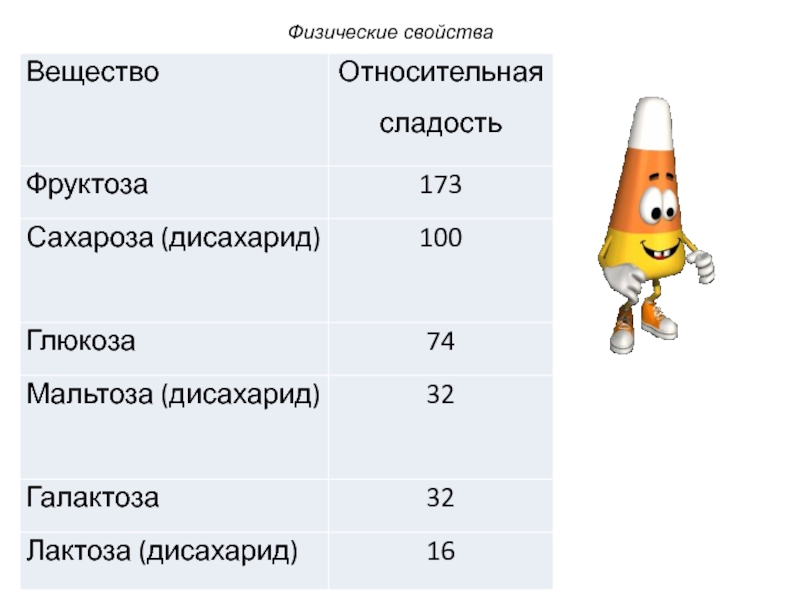
Слайд 80Физические свойства
Моносахариды представляют собой бесцветные кристаллические вещества очень хорошо
Концентрированные растворы сахаров в воде называются сиропами.
Слайд 82
Сахарин (E954), 500 раз
Этоксифенилмочевина (дульцин), 200 раз
Ацесульфам (E950), 200 раз
Аспартам (метиловый
Метилфенхиловый эфир L-аспартиламиномалоновой кислоты, 33000 раз
Сукроновая кислота, 200000 раз.
Физические свойства
Слайд 83Белок монеллин из тропического растения Dioscoreophyllum cumminsii в 3000 раз слаще
Физические свойства
Слайд 84Белок тауматин (E957) из тропического растения Thaumacoccus daniellii слаще сахарозы в
Thaumacoccus daniellii
Физические свойства
Слайд 85 Белок миракулин из Synsepalum dulcificum имеет уникальное свойство
Synsepalum dulcificum
Физические свойства
Слайд 86Физические свойства
Фрукт Synsepalum dulcificum сам по себе не сладкий, но может
Слайд 87
рибоза
Производные моносахаридов
Дезоксисахара - моносахариды, содержащие в молекуле один или несколько атомов водорода вместо гидроксильных групп.
Слайд 88
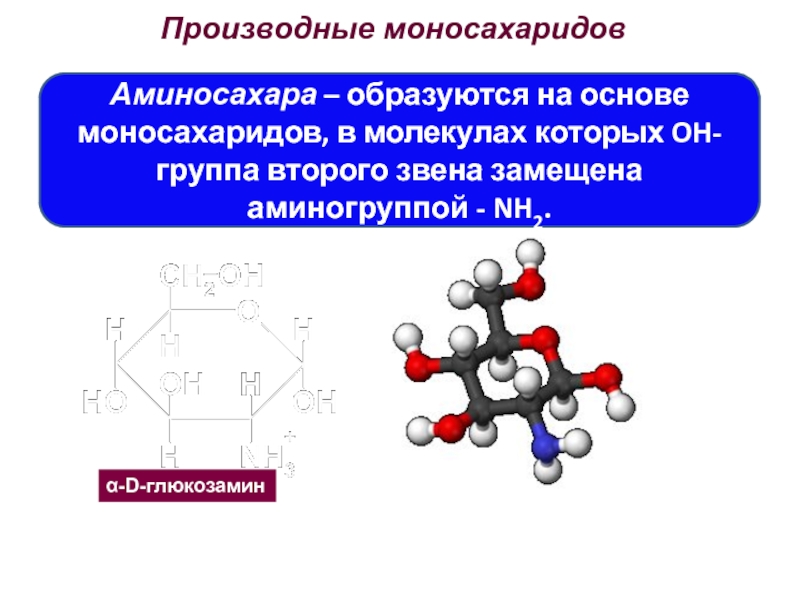
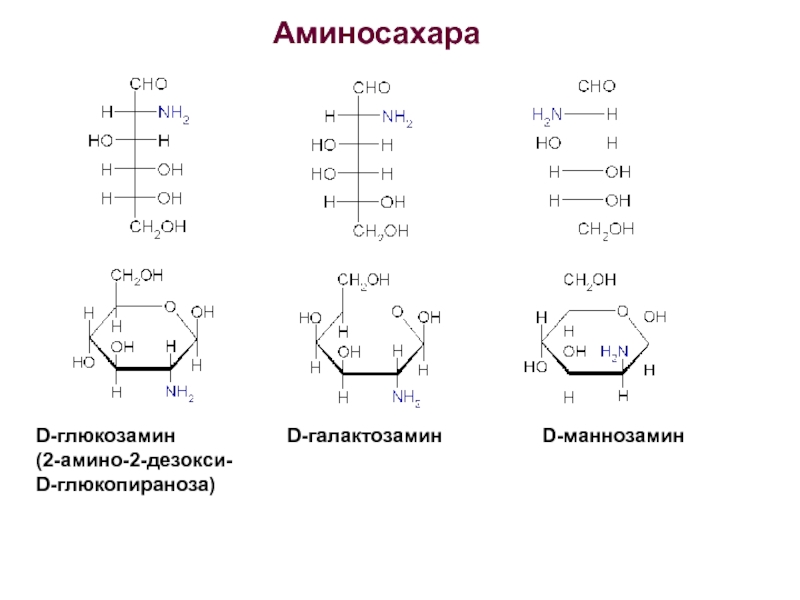
Производные моносахаридов
Аминосахара – образуются на основе моносахаридов, в молекулах которых OH-группа
α-D-глюкозамин
Слайд 90
Глюкозамин применяется в качестве лекарственного средства группы нестероидных противовоспалительных препаратов для восполнения его эндогенного дефицита.
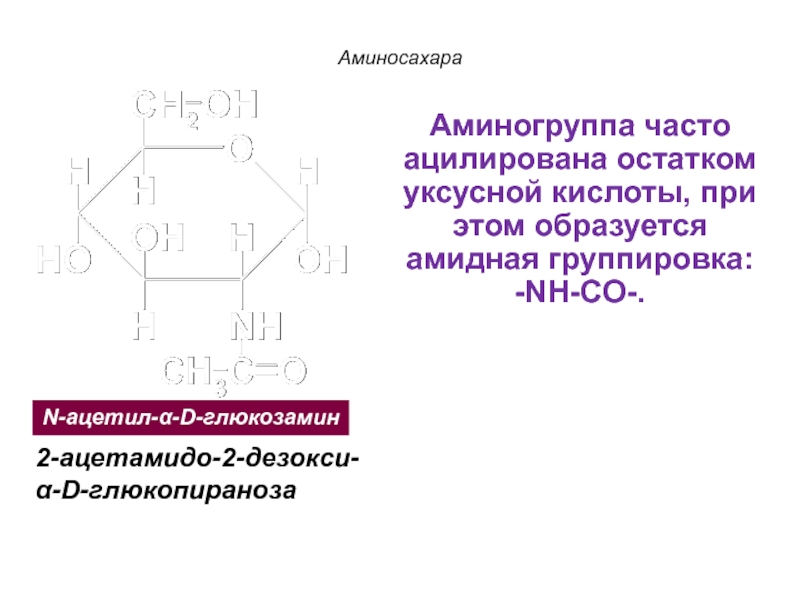
Слайд 91N-ацетил-α-D-глюкозамин
2-ацетамидо-2-дезокси-α-D-глюкопираноза
Аминосахара
Аминогруппа часто ацилирована остатком уксусной кислоты, при этом образуется амидная группировка:
-NH-CO-.
Слайд 92N-ацетил-D-галактозамин
2-ацетамидо-2-дезокси-D-галактопираноза
Аминосахара
Аминосахара входят в состав групповых веществ крови, определяя их специфичность и
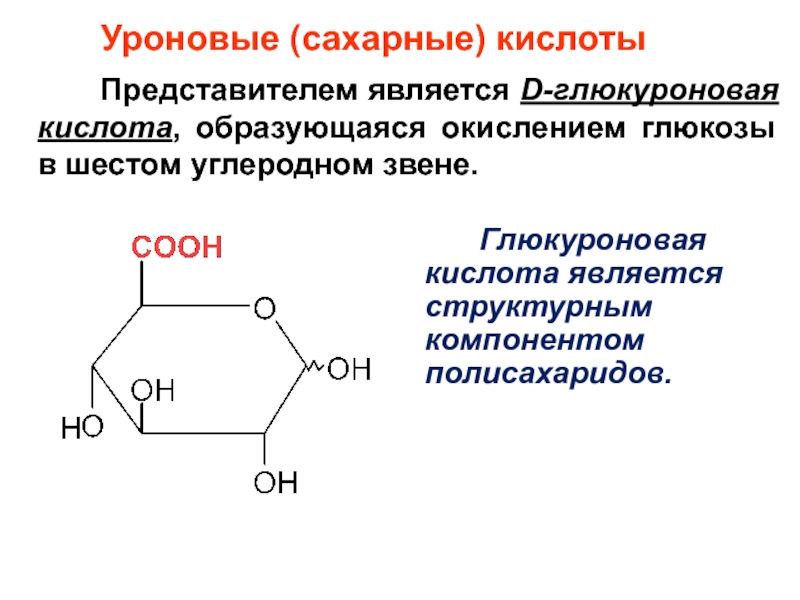
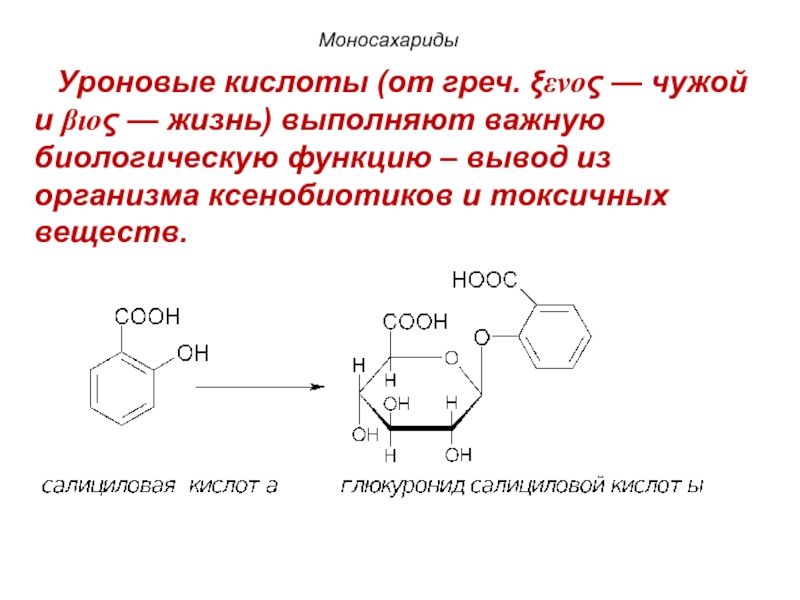
Слайд 93Уроновые (сахарные) кислоты
Представителем является D-глюкуроновая
Глюкуроновая кислота является структурным компонентом полисахаридов.
Слайд 94Моносахариды
Уроновые кислоты (от греч. ξενος — чужой и βιος
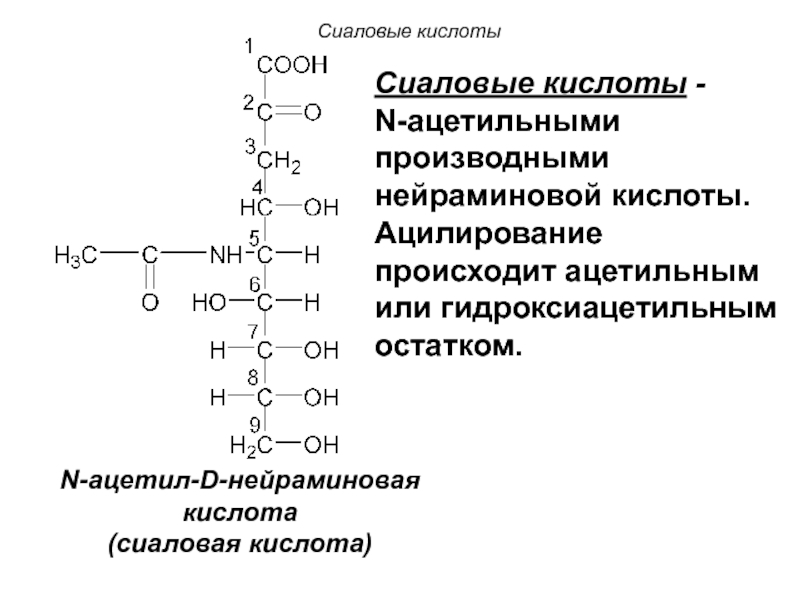
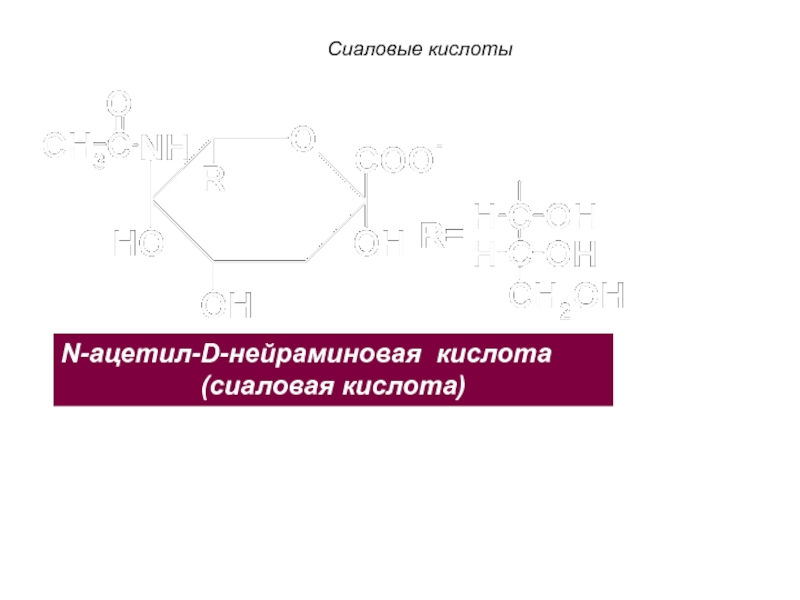
Слайд 96N-ацетил-D-нейраминовая
кислота
(сиаловая кислота)
Сиаловые кислоты
Сиаловые кислоты - N-ацетильными производными
Слайд 98Моносахариды
Нейраминовые и сиаловые кислоты в свободном состоянии содержатся в
Сиаловые кислота
Галактоза
Нейраминидаза
Слайд 99
Химические свойства моносахаридов
Исходя из функционального состава, моносахариды
Слайд 100Химические свойства
I. Свойства многоатомных спиртов.
В результате происходит образование растворимого хелатного комплекса ярко-синего цвета.
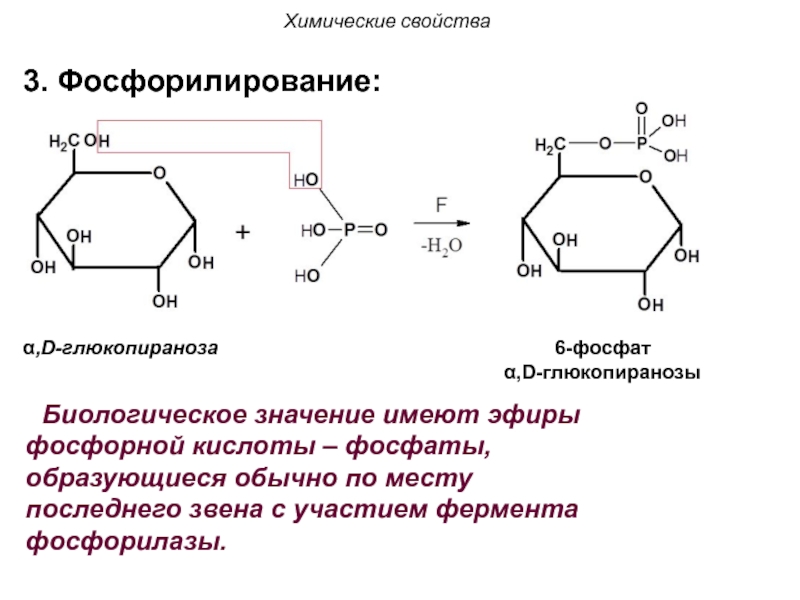
Слайд 102α,D-глюкопираноза
6-фосфат
α,D-глюкопиранозы
Химические свойства
3. Фосфорилирование:
Биологическое значение имеют эфиры фосфорной
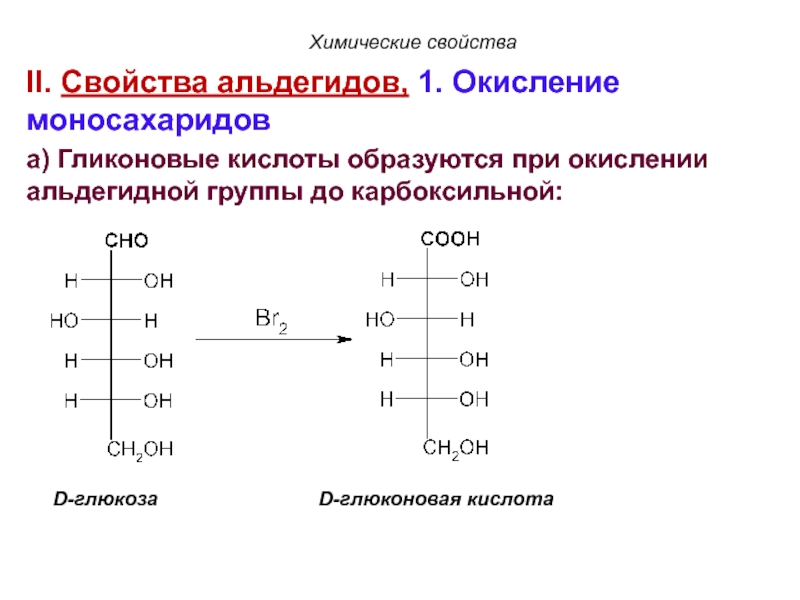
Слайд 103II. Свойства альдегидов, 1. Окисление моносахаридов
а) Гликоновые кислоты образуются при окислении
D-глюкоза D-глюконовая кислота
Химические свойства
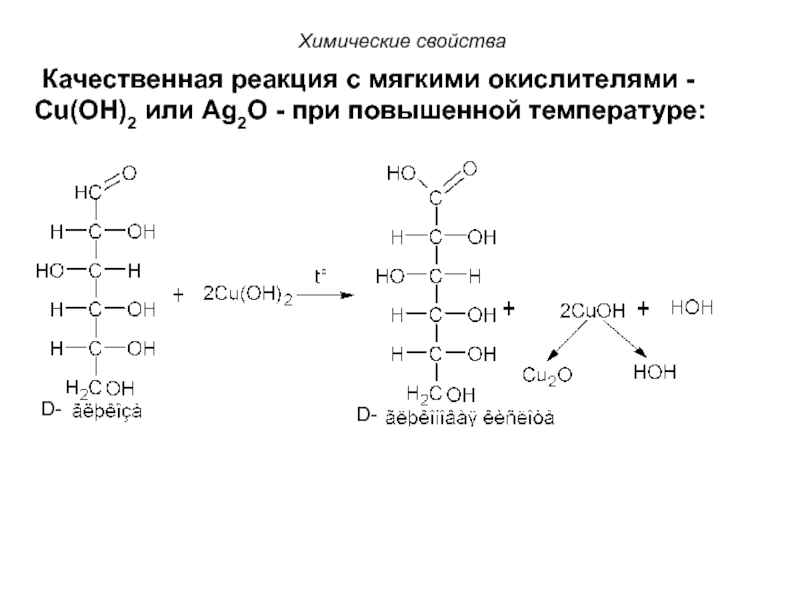
Слайд 104Химические свойства
Качественная реакция с мягкими окислителями - Сu(OH)2 или Ag2O
D-
D-
Слайд 105Реакция с Cu(OH)2 называется пробой Троммера и используется для обнаружения глюкозы
Химические свойства
Слайд 106 б) Гликаровые кислоты образуются при жёстком окислении. При этом окисляется
D-галактоза D-галактаровая кислота
Химические свойства
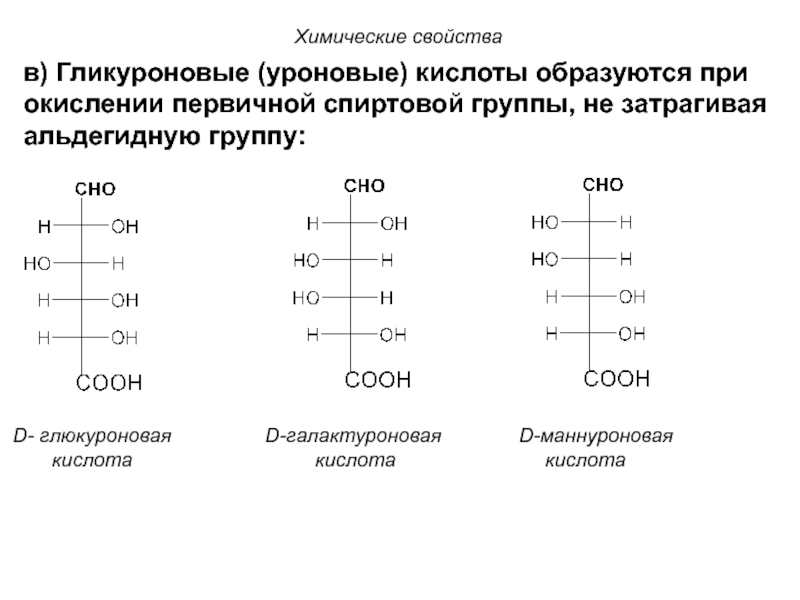
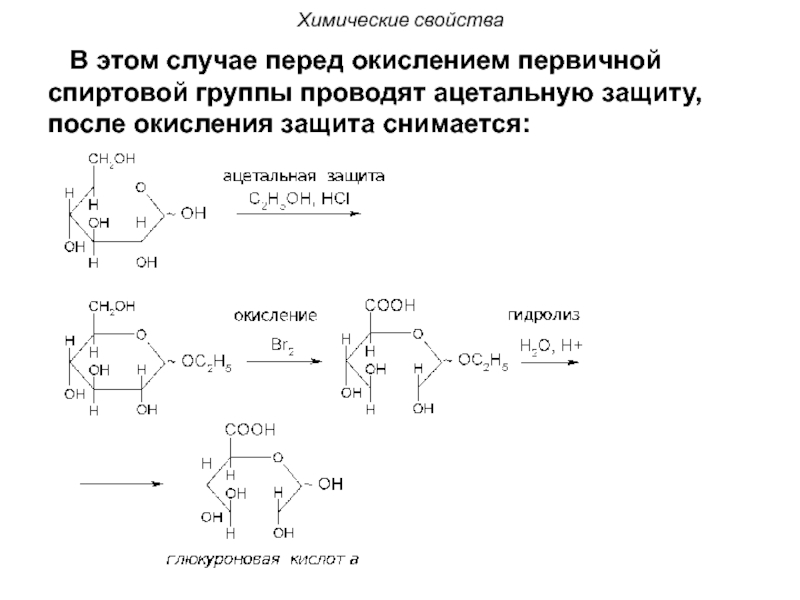
Слайд 107в) Гликуроновые (уроновые) кислоты образуются при окислении первичной спиртовой группы, не
D- глюкуроновая D-галактуроновая D-маннуроновая
кислота кислота кислота
Химические свойства
Слайд 108 Гликуроновые (уроновые) кислоты образуются при окислении первичной спиртовой группы, не
глюкуроновая галактуроновая маннуроновая
кислота кислота кислота
Химические свойства
Слайд 109
Химические свойства
В этом случае перед окислением первичной спиртовой группы
Слайд 111D-глюкоза образует глицит (сорбит, E420), D-манноза - маннит, D-ксилоза - ксилит
Химические свойства
Слайд 112
Химические свойства
Из D-глюкозы в фармацевтической промышлености получают аскорбиновую кислоту.
Слайд 113 Аскорбиновая кислота (а – отрицающая частица и scorbutus – цинга)
Химические свойства
Слайд 114 Аскорбиновая кислота также используется в аналитической химии в аскорбинометрии,
Химические свойства
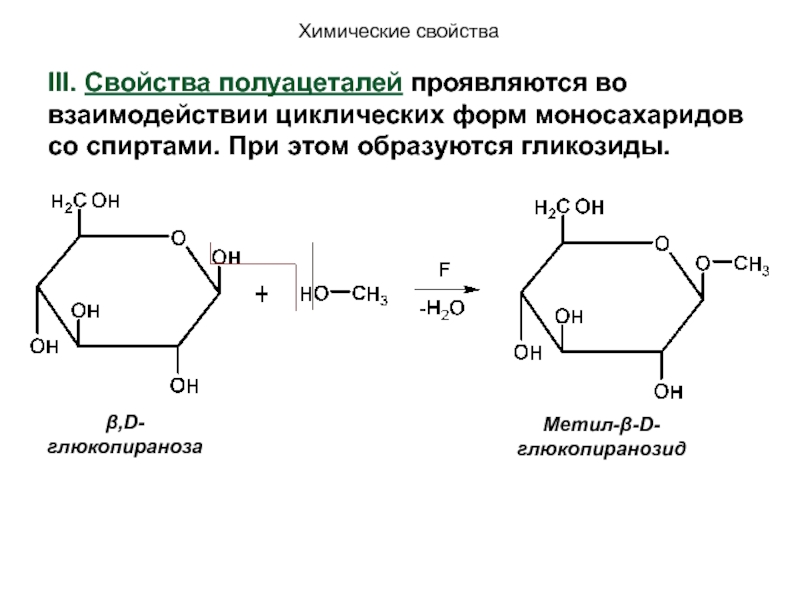
Слайд 115β,D-глюкопираноза
Метил-β-D-глюкопиранозид
Химические свойства
III. Свойства полуацеталей проявляются во взаимодействии циклических форм моносахаридов со
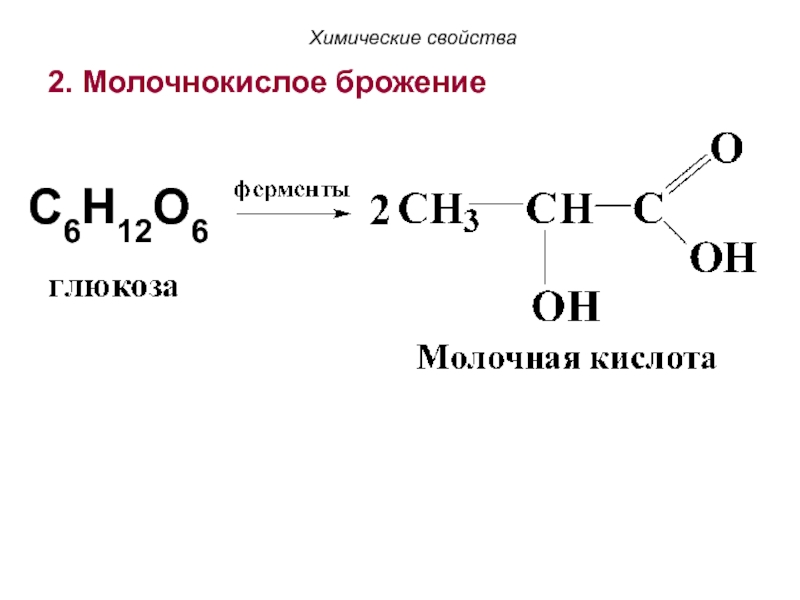
Слайд 116IV. Специфические свойства
1. Спиртовое брожение
Химические свойства
C6H12O6 →
Фермент
дрожжей
Слайд 118Вопросы для самоконтроля
Перечислите биологически важные альдопентозы, альдогексозы и кетогексозы.
Охарактеризуйте кольчато-цепную
Какое явление называют мутаротацией?
Охарактеризуйте химические свойства моносахаридов.
Перечислите биологически важные производные моносахаридов.






















![ячейкаПоляриметр Угол вращения плоскости поляризованного света определяется с помощью поляриметра. [α] - удельное вращениеЭнантиомерия25°CD](/img/tmb/5/450275/c8f78f46c19e3529dc32694212f44bec-800x.jpg)